Questões comentadas ENEM 2011 – Parte 4
Ciências da Natureza e suas Tecnologias
Caro estudante,
Trazemos para você a quarta parte da prova do Exame Nacional do Ensino Médio (ENEM), do
ano de 2011, do grupo “Ciências da Natureza e suas Tecnologias”.
Acompanhe nossos comentários e resoluções!
Bom aprendizado!
QUESTÃO 28
Em um experimento realizado para determinar a densidade da água de um lago, foram utilizados alguns materiais
conforme ilustrado: um dinamômetro D com graduação de 0 N a 50 N e um cubo maciço e homogêneo de 10 cm de
aresta e 3 kg de massa. Inicialmente, foi conferida a calibração do dinamômetro, constatando-se a leitura de 30 N
quando o cubo era preso ao dinamômetro e suspenso no ar. Ao mergulhar o cubo na água do lago, até que metade
do seu volume ficasse submersa, foi registrada a leitura de 24 N no dinamômetro.
2
3
Considerando que a aceleração da gravidade local é de 10 m/s , a densidade da água do lago, em g/cm , é
(A) 0,6.
(B) 1,2.
(C) 1,5.
(D) 2,4.
(E) 4,8.
Comentários
Precisamos representar as forças atuando sobre o bloco, uma vez que o sistema está em equilíbrio. A
força peso do bloco é indicada pelo dinamômetro, quando suspenso no ar com o peso dado, ou seja, 30N,
de cima para baixo. No sentido contrário, de baixo para cima, a mola do dinamômetro exerce uma força de
tração. Se o sistema não estivesse na água, a força de tração seria também de 30N, equilibrando o peso.
Mas, mergulhada na água, há também a força de empuxo atuando no bloco de baixo para cima, que
diminui a tração da mola do dinamômetro. Essa nova força de tração é indicada pelo valor do
dinamômetro, quando o objeto está parcialmente mergulhado, que equivale a 24N.
Ora, se o peso é 30N e a força de tração é 24N, o empuxo está atuando com uma força de 6N.
A questão pede o valor da densidade do líquido.
A força peso do cubo está
representada pela seta verde; a
força de tração da mola, pelo vetor
vermelho; e a força de empuxo, pela
seta azul. Os vetores não estão em
escala na ilustração ao lado.
Sabemos que o empuxo (E) é uma força exercida pelo peso do líquido deslocado pelo sólido que foi
mergulhado.
Como o peso é a massa vezes aceleração da gravidade, temos: E = m . g
E, se massa (m) é igual à densidade (d) multiplicada pelo volume (V), temos:
Assim,
E=d.V.g
d=E/V.g
Como o cubo tem 10cm de aresta e ficou mergulhado apenas pela metade dentro do líquido, seu volume
total corresponde a 1000cm3 (10 . 10 . 10 = 1000), sendo que apenas 500cm3 está submerso.
Mas, como o valor do empuxo está em newtons e o valor da aceleração da gravidade está em m/s 2, é
necessário converter o valor do volume de cm3 para m3. Para isso, precisamos dividir 500 por 1.000.000 ou
o mesmo que multiplicar por 10-6.
Se
d = E / V . g, então:
d = 6 / 500 . 10-6. 10
d = 6 / 5.10-3
d = 1,2. 10-3 kg/m3
Dividindo as unidades obtidas por 1000 para adequar o resultado às respostas, temos:
d = 1,2 g/cm3
Grau de dificuldade – Difícil.
A questão envolve cálculos em sequência, demandando bastante concentração e mais tempo de
resolução.
Resposta
(B) 1,2.
QUESTÃO 29
Uma equipe de cientistas lançará uma expedição ao Titanic para criar um detalhado mapa 3D que “vai tirar,
virtualmente, o Titanic do fundo do mar para o público”. A expedição ao local, a 4 quilômetros de profundidade no
Oceano Atlântico, está sendo apresentada como a mais sofisticada expedição científica ao Titanic. Ela utilizará
tecnologias de imagem e sonar que nunca tinham sido aplicadas ao navio, para obter o mais completo inventário de
seu conteúdo. Esta complementação é necessária em razão das condições do navio, naufragado há um século.
O Estado de São Paulo. Disponível em: http://www.estadao.com.br.
Acesso em: 27 jul. 2010 (adaptado).
No problema apresentado para gerar imagens através de camadas de sedimentos depositados no navio, o sonar é
mais adequado, pois a
(A) propagação da luz na água ocorre a uma velocidade maior que a do som neste meio.
(B) absorção da luz ao longo de uma camada de água é facilitada enquanto a absorção do som não.
(C) refração da luz a uma grande profundidade acontece com uma intensidade menor que a do som.
(D) atenuação da luz nos materiais analisados é distinta da atenuação de som nestes mesmos materiais.
(E) reflexão da luz nas camadas de sedimentos é menos intensa do que a reflexão do som neste material.
Comentários
A luz sofre atenuação pelos sedimentos, logo na primeira camada de areia e outros sedimentos
submarinos depositados no corpo e na estrutura do navio. Em outras palavras, a maior parte das ondas
luminosas não chega até o corpo do navio; ou, quando chegam, poucas são refletidas, pois são
bloqueadas na volta pelos sedimentos.
As ondas sonoras também sofrem atenuação, mas conseguem penetrar mais nos sedimentos, atingindo o
corpo do navio e sofrendo reflexão para detecção pelo sonar e interpretação dos dados pelos
computadores. Os sedimentos também refletem o som, porém os ecos produzidos pelos sedimentos são
captados em instantes diferentes dos ecos produzidos pelo corpo do navio, permitindo distingui-los para
selecionar os dados corretos para a formação da imagem.
Grau de dificuldade – Médio.
O estudante precisa ter conhecimento das propriedades da luz e do som, sabendo compará-las em uma
situação específica, para chegar à resposta correta.
Resposta
(D) atenuação da luz nos materiais analisados é distinta da atenuação de som nestes mesmos materiais.
QUESTÃO 30
Os refrigerantes têm-se tornado cada vez mais o alvo de políticas públicas de saúde. Os de cola apresentam ácido
fosfórico, substância prejudicial à fixação de cálcio, o mineral que é o principal componente da matriz dos dentes. A
cárie é um processo dinâmico de desequilíbrio do processo de desmineralização dentária, perda de minerais em
razão da acidez. Sabe-se que o principal componente do esmalte do dente é um sal denominado hidroxiapatita. O
refrigerante, pela presença da sacarose, faz decrescer o pH do biofilme (placa bacteriana), provocando a
desmineralização do esmalte dentário. Os mecanismos de defesa salivar levam de 20 a 30 minutos para normalizar o
nível do pH, remineralizando o dente. A equação química seguinte representa esse processo:
desmineralização
2+
Ca5(PO4)3OH(s)
3–
–
5 Ca (aq) + 3 PO4 (aq) + OH (aq)
mineralização
GROISMAN, S. Impacto do refrigerante nos dentes é avaliado sem tirá-lo da dieta.
Disponível em: http://www.isaude.net. Acesso em: 1 maio 2010 (adaptado).
Considerando que uma pessoa consuma refrigerantes diariamente, poderá ocorrer um processo de desmineralização
dentária, devido ao aumento da concentração de
–
2+
(A) OH , que reage com os íons Ca , deslocando o equilíbrio para a direita.
–
+
(B) H , que reage com as hidroxilas OH , deslocando o equilíbrio para a direita.
–
2+
(C) OH , que reage com os íons Ca , deslocando o equilíbrio para a esquerda.
–
+
(D) H , que reage com as hidroxilas OH , deslocando o equilíbrio para a esquerda.
2+
–
(E) Ca , que reage com as hidroxilas OH , deslocando o equilíbrio para a esquerda.
Comentários
Essa é uma questão típica de equilíbrio químico, envolvendo deslocamento do equilíbrio por variação da
acidez do meio.
O refrigerante é um líquido aquoso, de pH ácido, pela presença de ácido carbônico (H2CO3), que não foi
mencionado na questão, e ácido fosfórico (H3PO4).
O ácido carbônico tem pouca influência, uma vez que se decompõe rapidamente em gás carbônico e
água:
H2CO3
H2O (l) +
CO2 (g)
No caso do ácido fosfórico, um fornecimento diário de cátions H+ (ou, mais corretamente, H3O+), que
caracterizam os ácidos, promove a reação com os ânions hidróxido (OH-), neutralizando-os:
H+ (aq)
+
OH- (aq)
→
H2O (l)
H3O+ (aq)
+
OH- (aq)
→
H2O (l)
ou
Fazendo diminuir a concentração de ânions hidróxido, a velocidade da reação inversa (mineralização) fica
diminuída, o que acelera relativamente a velocidade da reação direta (desmineralização).
Assim, a ingestão diária de refrigerante provoca a desmineralização do esmalte dos dentes, por
deslocamento do equilíbrio químico para a direita.
Grau de dificuldade – Fácil.
O enunciado da questão já menciona que a causa da desmineralização é a acidez do refrigerante.
Resposta
(B) H+, que reage com as hidroxilas OH–, deslocando o equilíbrio para a direita.
QUESTÃO 31
Diferente do que o senso comum acredita, as lagartas de borboletas não possuem voracidade generalizada. Um
estudo mostrou que as borboletas de asas transparentes da família Ithomiinae, comuns na Floresta Amazônica e na
Mata Atlântica, consomem, sobretudo, plantas da família Solanaceae, a mesma do tomate. Contudo, os ancestrais
dessas borboletas consumiam espécies vegetais da família Apocinaceae, mas a quantidade dessas plantas parece
não ter sido suficiente para garantir o suprimento alimentar dessas borboletas. Dessa forma, as solanáceas tornaramse uma opção de alimento, pois são abundantes na Mata Atlântica e na Floresta Amazônica.
Cores ao vento. Genes e fósseis revelam origem e diversidade de borboletas sul-americanas.
Revista Pesquisa FAPESP. N° 170, 2010 (adaptado).
Nesse texto, a ideia do senso comum é confrontada com os conhecimentos científicos, ao se entender que as larvas
das borboletas Ithomiinae encontradas atualmente na Mata Atlântica e na Floresta Amazônica, apresentam
(A) facilidade em digerir todas as plantas desses locais.
(B) interação com as plantas hospedeiras da família Apocinaceae.
(C) adaptação para se alimentar de todas as plantas desses locais.
(D) voracidade indiscriminada por todas as plantas existentes nesses locais.
(E) especificidade pelas plantas da família Solanaceae existentes nesses locais.
Comentários
Em geral, as pessoas pensam que as lagartas das borboletas comem qualquer tipo de folha; mas, não. Há
uma seletividade, uma preferência para uma espécie específica de vegetais; ou seja, seu tubo digestório é
adaptado àquela espécie vegetal.
A investigação científica dos fósseis indica que, no passado, os ancestrais das borboletas modernas
devoravam outra espécie vegetal. Mas, com o aumento da variabilidade genética dos descendentes,
surgiram indivíduos capazes de digerir plantas de outra espécie, que foram mudando de hábito por essas
espécies vegetais estarem mais disponíveis em maior oferta.
Na atualidade, essas larvas das borboletas de asas transparentes preferem a nova espécie vegetal (da
família Solanaceae), existentes na Mata Atlântica e na Floresta Amazônica. Esse é um caso típico de
seleção natural do tipo direcional.
Grau de dificuldade – Fácil.
As opções falsas são muito óbvias, bastando ao candidato ler a questão cuidadosamente e usar o bom
senso.
Resposta
(E) especificidade pelas plantas da família Solanaceae existentes nesses locais.
QUESTÃO 32
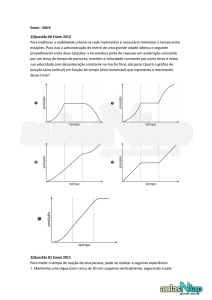
Para medir o tempo de reação de uma pessoa, pode-se realizar a seguinte experiência:
I. Mantenha uma régua (com cerca de 30 cm) suspensa verticalmente, segurando-a pela extremidade superior, de
modo que o zero da régua esteja situado na extremidade inferior.
II. A pessoa deve colocar os dedos de sua mão, em forma de pinça, próximos do zero da régua, sem tocá-la.
III. Sem aviso prévio, a pessoa que estiver segurando a régua deve soltá-la. A outra pessoa deve procurar segurá-la
o mais rapidamente possível e observar a posição onde conseguiu segurar a régua, isto é, a distância que ela
percorre durante a queda.
O quadro seguinte mostra a posição em que três pessoas conseguiram segurar a régua e os respectivos tempos de
reação.
Distância percorrida pela régua Tempo de reação
durante a queda (metro)
(segundo)
0,30
0,24
0,15
0,17
0,10
0,14
Disponívelem :
http: //br.geocities.com. Acessoem :1 fev. 2009.
A distância percorrida pela régua aumenta mais rapidamente que o tempo de reação porque a
(A) energia mecânica da régua aumenta, o que a faz cair mais rápido.
(B) resistência do ar aumenta, o que faz a régua cair com menor velocidade.
(C) aceleração de queda da régua varia, o que provoca um movimento acelerado.
(D) força peso da régua tem valor constante, o que gera um movimento acelerado.
(E) velocidade da régua é constante, o que provoca uma passagem linear de tempo.
Comentários
Essa é uma questão sobre o fenômeno da “queda livre”, ou seja, sobre aceleração, aparentemente
disfarçada em um experimento de velocidade constante. O estudante distraído pode achar que a
velocidade de reflexo das pessoas testadas está diretamente relacionada com a distância em centímetros,
medida diretamente na régua; mas isso só seria verdadeiro, se a velocidade de queda fosse constante.
Desprezando-se o efeito da resistência do ar, a força resultante na régua será o seu peso, que é
constante. Mas o movimento de queda da régua terá aceleração constante - e não velocidade constante.
A distância percorrida pela régua (variação da posição, Δs) é proporcional ao quadrado do tempo de
queda (t); e, por isso, Δs aumenta mais rapidamente do que o tempo (t).
Δs = g .t2 / 2
Ou seja, a velocidade da régua está aumentando durante a queda.
Grau de dificuldade – Médio.
O estudante precisa estar atento para não confundir o movimento acelerado (velocidade variável), que
possui aceleração constante, como é o caso da queda livre.
Resposta
(D) força peso da régua tem valor constante, o que gera um movimento acelerado.
QUESTÃO 33
Um tipo de vaso sanitário que vem substituindo as válvulas de descarga está esquematizado na figura. Ao acionar a
alavanca, toda a água do tanque é escoada e aumenta o nível no vaso, até cobrir o sifão. De acordo com o Teorema
de Stevin, quanto maior a profundidade, maior a pressão. Assim, a água desce levando os rejeitos até o sistema de
esgoto. A válvula da caixa de descarga se fecha e ocorre o seu enchimento. Em relação às válvulas de descarga,
esse tipo de sistema proporciona maior economia de água.
Faça você mesmo. Disponível em: http://www.facavocemesmo.net. Acesso em: 22 jul. 2010.
A característica de funcionamento que garante essa economia é devida
(A) à altura do sifão de água.
(B) ao volume do tanque de água.
(C) à altura do nível de água no vaso.
(D) ao diâmetro do distribuidor de água.
(E) à eficiência da válvula de enchimento do tanque.
Comentários
Quando um vaso sanitário é conectado diretamente à caixa d’água geral da residência (modelo antigo), a
pressão de descida da água dependerá da largura do tubo e da altura da caixa em relação ao vaso. Mas o
usuário pode acionar o botão da descarga por um tempo indeterminado, gastando muita água. Além disso,
as válvulas desse sistema possuem uma ou mais molas, que fazem o botão retornar muito lentamente à
posição original, fechado, gastando ainda mais água.
No modelo apresentado, a pressão é dada pelo volume de água do reservatório, que provoca um
desnivelamento da altura do vaso e do sifão, de acordo com a Lei de Stevin (pressão hidrostática = gH),
segundo a qual a pressão hidrostática da água é proporcional à altura da água, não dependendo da
quantidade (volume) de água que está dentro do vaso. Porém essa pressão depende do volume de água
dentro do reservatório, que, quanto maior, maior o desnível provocado em relação ao nível do sifão.
Mas, como o volume do reservatório (tanque) é fixo, ele é dimensionado de fábrica para causar a pressão
necessária para eliminar os dejetos do vaso, sem o gasto de muita água.
Grau de dificuldade – Médio.
A questão apresenta algumas opções falsas muito óbvias. Porém o enunciado cita o Teorema de Stevin,
que afirma que “quanto maior a profundidade, maior a pressão”, provavelmente para direcionar o
estudante desatento para a alternativa C, que afirma que é a altura do nível da água no vaso que
proporciona mais economia. Mas, como vimos, a altura da água do vaso não aumenta a pressão da
descarga, nem gera mais economia.
Resposta
(B) ao volume do tanque de água.
QUESTÃO 34
Moradores sobreviventes da tragédia que destruiu aproximadamente 60 casas no Morro do Bumba, na Zona Norte de
Niterói (RJ), ainda defendem a hipótese de o deslizamento ter sido causado por uma explosão provocada por gás
metano, visto que esse local foi um lixão entre os anos 1960 e 1980.
Jornal Web. Disponível em: http://www.ojornalweb.com. Acesso em: 12 abr. 2010 (adaptado).
O gás mencionado no texto é produzido
(A) como subproduto da respiração aeróbia bacteriana.
(B) pela degradação anaeróbia de matéria orgânica por bactérias.
(C) como produto da fotossíntese de organismos pluricelulares autotróficos.
(D) pela transformação química do gás carbônico em condições anaeróbias.
(E) pela conversão, por oxidação química, do gás carbônico sob condições aeróbias.
Comentários
O metano (CH4) é um gás formado pela degradação anaeróbica de resíduos orgânicos em geral, pela
ação de bactérias, como é o caso da decomposição do lixo orgânico nos aterros sanitários. Se
considerarmos os rejeitos como de base celulóica, como é o caso do papel e da maioria dos restos de
comida, podemos considerar a reação geral de decomposição anaeróbica pela equação:
(C6H10O5)n
+
nH2O
→
3n CH4 (g)
+
3n CO2 (g)
Quando o metano escapa e entra em contato com o ar atmosférico (oxigênio, O 2) e alguma fonte de calor
inicial, podem acontecer violentas explosões:
CH4 (g)
+
2 O2 (g)
→
CO2 (g)
+
2 H2O
+
calor
Nos aterros sanitários, normalmente, são instalados “suspiros”, que atravessam as várias camadas de lixo
e terra, através dos quais os gases escapam para a atmosfera. Mas, no caso dos lixões, esses suspiros
não existem, podendo ter sido formados bolsões de metano e gás carbônico no subsolo, que, em dado
momento, escapou e explodiu, causando a tragédia. Um erro lamentável das autoridades municipais de
Niterói em permitir a urbanização do local, sem um estudo prévio detalhado do solo e subsolo, ainda mais
conhecendo a antiga utilização do local para lixão.
Grau de dificuldade – Fácil.
A decomposição anaeróbica produzindo metano é amplamente discutida na Química e na Biologia do
Ensino Médio.
Resposta
(B) pela degradação anaeróbia de matéria orgânica por bactérias.
QUESTÃO 35
O peróxido de hidrogênio é comumente utilizado como antisséptico e alvejante. Também pode ser empregado em
trabalhos de restauração de quadros enegrecidos e no clareamento de dentes. Na presença de soluções ácidas de
oxidantes, como o permanganato de potássio, este óxido decompõe-se, conforme a equação a seguir:
5 H2O2 (aq) + 2 KMnO4 (aq) + 3 H2SO4 (aq) 5 O2 (g) + 2 MnSO4 (aq) + K2SO4 (aq) + 8 H2O (l)
ROCHA-FILHO, R. C. R.; SILVA, R. R. Introdução aos Cálculos da Química.
São Paulo: McGraw-Hill, 1992.
De acordo com a estequiometria da reação descrita, a quantidade de permanganato de potássio necessária para
reagir completamente com 20,0 mL de uma solução 0,1 mol/L de peróxido de hidrogênio é igual a
0
(A) 2,0×10 mol.
(B) 2,0×10
–3
(C) 8,0×10
–1
mol.
mol.
–4
(D) 8,0×10 mol.
(E) 5,0×10
–3
mol.
Comentários
De acordo com a equação balanceada, a relação mol/mol das substâncias envolvidas é:
5 mol de H2O2 para 2 mol de KMnO4
Então, primeiramente, precisamos calcular a quantidade em mols de H2O2 na solução:
Molaridade = 0,1 mol/L = número de mols de soluto (n) / volume da solução (V)
Volume da solução = 20mL = 0,02L
M = 0,1 = n / V
0,1mol/L = n / 0,02L
n = 0,002mol = 2.10-3mol
Para calcular a quantidade, em mol, de permanganato de potássio que reage, temos:
5 mol de H2O2 ----------------- 2 mol de KMnO4
2.10-3mol
------------------ x
x = 8.10-4mol de permanganato de potássio.
Grau de dificuldade – Médio.
A questão exige entendimento de concentração e estequiometria de reações, mas oferece a equação
química já balanceada. Além disso, envolve cálculos de concentração de apenas um dos reagentes.
Resposta
(D) 8,0×10–4 mol.
QUESTÃO 36
Segundo dados do Balanço Energético Nacional de 2008, do Ministério das Minas e Energia, a matriz energética
brasileira é composta por hidrelétrica (80%), termelétrica (19,9%) e eólica (0,1%). Nas termelétricas, esse percentual
é dividido conforme o combustível usado, sendo: gás natural (6,6%), biomassa (5,3%), derivados de petróleo (3,3%),
energia nuclear (3,1%) e carvão mineral (1,6%). Com a geração de eletricidade da biomassa, pode-se considerar que
ocorre uma compensação do carbono liberado na queima do material vegetal pela absorção desse elemento no
crescimento das plantas. Entretanto, estudos indicam que as emissões de metano (CH 4) das hidrelétricas podem ser
comparáveis às emissões de CO2 das termelétricas.
MORET, A. S.; FERREIRA, I. A. As hidrelétricas do Rio Madeira e os impactos socioambientais
da eletrificação no Brasil. Revista Ciência Hoje. V. 45, n° 265, 2009 (adaptado).
No Brasil, em termos do impacto das fontes de energia no crescimento do efeito estufa, quanto à emissão de gases,
as hidrelétricas seriam consideradas como uma fonte
(A) limpa de energia, contribuindo para minimizar os efeitos deste fenômeno.
(B) eficaz de energia, tomando-se o percentual de oferta e os benefícios verificados.
(C) limpa de energia, não afetando ou alterando os níveis dos gases do efeito estufa.
(D) poluidora, colaborando com níveis altos de gases de efeito estufa em função de seu potencial de oferta.
(E) alternativa, tomando-se por referência a grande emissão de gases de efeito estufa das demais fontes geradoras.
Comentários
A questão não menciona porque as hidrelétricas emitem metano (CH4). Isso ocorre devido às grandes
áreas alagadas, geralmente florestas, que ficam submersas. Com o tempo, a madeira, as folhas e outros
materiais orgânicos entram em decomposição anaeróbica, produzindo metano e gás carbônico, de acordo
com a equação geral:
(C6H10O5)n
+
nH2O
→
3n CH4 (g)
+
3n CO2 (g)
Essa emissão de gases de efeito estufa pode ser equiparada às emissões de dióxido de carbono pelas
termelétricas, uma vez que o número de hidrelétricas é alto no Brasil, e o número de termelétricas é
pequeno. Logicamente, com o passar do tempo, as áreas alagadas não mais produzirão gases, pois
cessará a matéria orgânica a ser decomposta.
Grau de dificuldade – Médio.
Estamos acostumados a pensar nas hidrelétricas como energia “limpa”, de pouco impacto ambiental, pois
a energia elétrica obtida é derivada exclusivamente da energia potencial gravitacional da água que desce
da represa, através das turbinas, em um desnível natural do rio, onde é construída a barragem.
Considerando esse aspecto, realmente a energia é “limpa”.
Porém, em relação aos efeitos na região alagada pela represa - a morte de grandes populações animais e
vegetais, e a emissão de gases derivados da decomposição - as hidrelétricas são poluidoras. O estudante
pouco informado sobre o tema pode se deixar influenciar pelas afirmativas falsas.
Resposta
(D) poluidora, colaborando com níveis altos de gases de efeito estufa em função de seu potencial de
oferta.