1
SECRETARIA DE ESTADO DA EDUCAÇÃO
SUPERINTENDÊNCIA DA EDUCAÇÃO
UNIVERSIDADE ESTADUAL DE MARINGÁ
PROGRAMA DE DESENVOLVIMENTO EDUCACIONAL
METAIS. UMA PROPOSTA DE ABORDAGEM COM ENFOQUE
CIÊNCIA/TECNOLOGIA/SOCIEDADE
ÁREA: QUÍMICA
PROFESSOR PDE: MARIA APARECIDA DO CARMO PADULLA SOARES
ORIENTADOR: MARCELO PIMENTEL DA SILVEIRA
2008
2
METAIS
Vários são os elementos químicos que fazem parte da constituição
de diferentes materiais utilizados no dia-a-dia. Dentre esses materiais, escolhemos
os metais para estudar nessa unidade. Você já notou se eles são importantes para a
vida, ou para a sobrevivência do homem?
ATIVIDADE 1
Formar grupos de, no máximo, cinco alunos e responder às
questões abaixo:
1) Cite alguns materiais, ou objetos, que você julga ter a presença
de metais na sua composição.
2) Vocês podem citar algum exemplo de metal?
3) Por que esses materiais que vocês citaram, são metais?
4) Que critérios vocês utilizaram para classificar o(s) material(is)
citado(s) como metal(is)?
5) Será que existem algumas propriedades que permitem aos
materiais citados serem classificados como metais?
6) Os metais tiveram papel importante para o desenvolvimento da
sociedade humana? Explique.
7) Seria possível, na atual sociedade, viver sem o uso dos metais?
Continuando a reflexão sobre as questões que envolvem os metais,
propomos que façam os experimentos a seguir. Antes, porém, tentem refletir sobre
as questões abaixo:
1) Por que utilizamos panela de alumínio para cozinhar os
alimentos?
2) Por que o cabo das panelas de alumínio ou de ferro, não é de
metal?
3) Por que panelas de ferro e cobre não são mais utilizadas? Ou, em
quais situações são utilizadas?
3
EXPERIMENTO Nº 01 - Os metais são bons condutores de calor?
MATERIAL
− Uma placa de alumínio
− Uma placa de cobre
− Uma placa de ferro
− Uma placa de zinco
− Pedaços de parafina
− Uma lamparina
− Um relógio
PROCEDIMENTO
1.
Coloque na extremidade da placa de cobre, pedacinhos de
parafina e segure com uma pinça metálica (ou de madeira).
2.
Coloque o extremo da placa de cobre com a parafina sob a
chama da lamparina e anote no quadro 1, o tempo necessário para começar a fundir
(derreter) a parafina.
3.
Repita o mesmo procedimento para os outros materiais:
alumínio, ferro e zinco, tomando o cuidado para utilizar a mesma quantidade de
parafina em todas as placas.
Material
Tempo necessário para começar a fundir (derreter) a
parafina.
Alumínio
Cobre
Zinco
Ferro
Quadro 1 – Resultados do experimento nº 1.
Agora, com base nos seus resultados apresentados no quadro 1,
responda:
1. Os materiais testados são bons condutores de calor?
4
2.
Porque você utilizou a mesma quantidade de parafina em todas
3.
É possível identificar qual foi a placa que melhor conduziu calor?
as placas?
Que critério(s) você utilizou para responder?
4.
Cite exemplos de como o homem utiliza a propriedade que você
5.
Que conclusões, a respeito da condução de calor pelos metais,
verificou.
podem ser tiradas da experiência realizada?
PESQUISA 1
Pesquise sobre a utilização de mantas de alumínio, ou algum
material alternativo, por exemplo, como as embalagens tetraplack® (caixinhas de
leite) na cobertura de casas e construções.
Procure identificar qual o objetivo de se utilizar tal material e qual o
princípio de seu funcionamento.
Discuta se o principio de funcionamento das mesmas pode ser
explicado a partir das propriedades dos metais.
EXPERIMENTO Nº 02 - Os metais são bons condutores de eletricidade?1
Você já pensou sobre quais são os materiais que utilizamos no diaa-dia que conduz corrente elétrica?
Todos os metais podem ser considerados condutores de corrente
elétrica?
MATERIAL
− 1 dispositivo para medir corrente como o ilustrado abaixo.
1
Adaptado de SÃO PAULO. Secretaria de Estado da Educação. Coordenadoria de Estudos e
Normas Pedagógicas. Programa de Educação Continuada (PEC) Construindo SempreAperfeiçoamento de professores. Módulo 3. São Paulo: SE/CENP, 2003. p.13-16.
5
− Pedaços de ferro, de cobre, borracha, alumínio, vidro, zinco, ferro, plástico (PVC,
fórmica, etc.).
− 1 lâmpada (pode ser utilizada de 60W).
Recomendações:
Não
toque
nos
dois
eletrodos
(fios
desencapados)
simultaneamente quando o dispositivo estiver ligado à tomada.
Figura 1 - Aparelho para testar condutibilidade elétrica.
PROCEDIMENTO
1. Enrosque a lâmpada no dispositivo e ligue-o à tomada.
2. Faça as medidas dos materiais listados, colocando os eletrodos do dispositivo
em contato com cada um dos materiais, e observando o resultado.
3. Anote os resultados no quadro abaixo:
Material
Cobre
Borracha
Alumínio
Vidro
Zinco
Plástico
Ferro
Condução de corrente elétrica
6
Quadro 2 – Resultados do experimento nº 2.
A partir dos resultados do experimento, responda:
1. Todos os materiais testados são condutores de corrente
elétrica?
2. Essa propriedade é importante para o homem? Por quê?
3. Por que os cabos de ferramentas metálicas, por exemplo,
alicates e chave de fenda, são encapados com borracha ou plásticos?
4. Faça uma tabela com os materiais testados acima e, classifiqueos como condutores de corrente elétrica ou isolantes.
ATIVIDADE 2
Analise os dados apresentados na tabela 1 e responda:
1. É possível afirmar que todos os metais apresentam pontos de
fusão e de ebulição altos?
2. Isso é comum a todos os metais, ou há exceções?
3. Considerando a temperatura ambiente como 25 oC, qual deve
ser o estado físico do mercúrio? Ele pode ser considerado um metal?
4. Qual(is) dos metais indicados na tabela 1, você não conhece ou
não sabia que era um metal?
Tabela 1 – Alguns metais e seus pontos de fusão e de ebulição.
Metal
Ponto de fusão (ºC)
Ponto de ebulição (ºC)
Ferro
1538
2862
Alumínio
660
2520
Zinco
420
907
Cobre
1084
2563
Chumbo
327,5
1750
Ouro
1064
2857
Sódio
97,8
883
Potássio
63
759
Estanho
232
2603
Mercúrio
-39
3575
Gálio
30
2205
7
PROPRIEDADES DOS METAIS E SUAS APLICAÇÕES
PARA VOCÊ PENSAR!
1) A partir dos resultados dos experimentos 1 e 2, e das discussões
sobre os mesmos, é possível afirmar que os metais podem ser caracterizados
somente pelas propriedades de conduzir corrente elétrica e calor?
2) Você conhece outras propriedades dos metais? Quais?
A partir das discussões realizadas até o momento, podemos
perceber que os materiais metálicos são amplamente utilizados em nossa sociedade
graças às suas propriedades físicas e químicas. Algumas dessas propriedades,
apresentadas no quadro 3, embora em diferentes graus, são comuns a todos eles.
Propriedades
Observações
Brilho característico
Se polidos, os metais refletem muito bem a luz
Alta condutibilidade térmica e elétrica
Prata e ouro são os metais que apresentam os
maiores valores de condutibilidade elétrica
Altos pontos de fusão e de ebulição
Embora haja exceções, como mercúrio, PF = -39 ºC;
gálio, PF = 30 º C; e potássio, PF = 63 ºC), como
discutido na atividade 2. Devido a essa propriedade
e também à boa condutividade térmica, alguns
metais são utilizados em panelas e radiadores de
automóveis.
Maleabilidade
Metais são muito maleáveis, ou seja, são fáceis de
transformarem-se em lâminas. O metal mais
maleável é o ouro
Ductibilidade
Metais também são muito dúcteis, isto é, são fáceis
de transformarem-se em fios. O ouro é também o
mais dúctil dos metais
Quadro 3 – Propriedades dos metais.
8
Do ponto de vista tecnológico, a dureza e a densidade também são
propriedades importantes. O ferro e o alumínio são classificados como metais duros.
O magnésio, o alumínio e o titânio são considerados metais com densidades baixas,
isto é, com densidade inferior a 5 g/cm3. A escolha do metal mais apropriado para a
confecção de um objeto dependerá muito do conjunto de propriedades que ele
apresenta, além de outros fatores como o econômico e o ambiental.
O quadro 4, apresenta algumas das aplicações e características de
determinados metais.
Metal
Al (alumínio)
Pb (chumbo)
Cu (cobre)
Sn (estanho)
Fe (ferro)
Hg (mercúrio)
Zn (zinco)
Aplicações-importância
Fabricação de panelas, esquadrias,
folhas, tubos, aviação, automóveis, etc.
Fogos de artifício
Proteção contra radiações.
Bateria de automóveis e tubos de
canalização.
Ligas fusíveis, soldas e munição.
Formação do bronze (com estanho), do
latão (com o zinco) e cunhagem de
moedas (com o níquel).
Fabricação de arames, fios, panelas,
etc.
Formação do bronze (com o cobre),
latas (folhas de Flandres) e presente em
soldas e moedas.
Esquadrias, ferramentas, pregos, etc.
Principal constituinte do aço.
Fabricação
de
barômetros
e
termômetros.
Formação de amálgamas, lâmpadas a
vapor e sensores elétricos.
Formação de latão.
Fabricação de pilhas secas, calhas,
telhas e peças de automóveis.
Refrigeração de reatores atômicos.
Iluminação (lâmpada a vapor de sódio)
Características
Metal
mais
abundante.
Quando pulverizado, de fácil
explosão e ignição.
Metal com muito brilho, baixa
dureza e baixa tenacidade.
Condutor
de
eletricidade.
calor
e
Resistente à corrosão.
Elemento atraído pelo ímã
Metal líquido a 25ºC.
Usado em revestimento de
outros metais para proteção
da oxidação.
Na (sódio)
Reação violenta com a água.
Não encontrado na forma de
minérios, pois a maioria reage
com a água.
Ag (prata)
Talheres, espelhos, jóias, moedas, Bom condutor de calor e
medalhas, etc.
eletricidade.
Au (ouro)
Moedas, jóias, circuitos eletrônicos.
Metal muito maleável, dúctil e
também muito valorizado.
Ni (níquel)
Fabricação de moedas.
Atração pelo ímã, alta dureza,
Niquelação (proteção de metais).
resistência à oxidação.
Mg (magnésio)
Formação de ligas:motores, aeronaves Quando aquecido inflama
e rodas.
com chama intensa.
Fogos de artifício e sinalização.
Fabricação de flash descartável.
Quadro 4 - Propriedades e usos de alguns metais.
Fonte: Ferreira (1998, p. 15).
9
LIGAS METÁLICAS
Até o momento, já foi possível estudar um pouco sobre os metais
por meio de vários exemplos, seus usos e propriedades. No sentido de ampliar os
conhecimentos sobre esses materiais, responda as questões a seguir:
1. Vocês conhecem, ou já ouviram falar, de um material chamado
bronze?
2. O bronze pode ser considerado um metal? Por quê?
3. Vocês conhecem aço e aço inox? Existem diferenças entre
esses materiais? Quais?
4. O que vocês acham que é o latão? E ouro 18 quilates? O que
seria o ouro branco?
5. Como vocês poderiam verificar se os materiais indicados são
metais?
EXPERIMENTO Nº 3 – Pesquisa de ligas metálicas
MATERIAL
− Uma amostra de bronze (objeto de decoração, chave, etc.)
− Uma amostra de latão (objeto de decoração)
− Uma amostra de aço inoxidável (por exemplo, talher)
− Uma peça de ouro (anel, pulseira, brinco, etc.)
− Um pedaço de solda elétrica
− Estanho
− Chumbo
− Tripé
− Bico de Bunsen
− Tela de Amianto
− 03 cadinhos
− Proveta de 100 mL
10
Obs.: trabalhar com amostras pequenas, para facilitar a determinação do volume
através do deslocamento de água na proveta.
PROCEDIMENTO
Parte I – Condução de calor e corrente elétrica
1.
Repetir o procedimento dos experimentos 1 e 2 para as
amostras de bronze, latão, aço inoxidável, ouro e solda elétrica.
2.
Organizar os dados obtidos em quadros, da mesma forma
sugerida nos experimentos 1 e 2, e depois responder as questões:
I. Os materiais testados são condutores de calor?
II. Os materiais testados conduzem a corrente elétrica?
III. Esses materiais e os metais apresentam o mesmo comportamento com relação
à condução de calor e de corrente elétrica?
IV. Podemos diferenciar os metais de uma liga metálica, utilizando a condução de
calor e eletricidade?
Parte II - Ponto de fusão
1.
Coloque, separadamente, pequenas quantidades iguais de solda
e de seus componentes (estanho e chumbo), em um cadinho.
2.
Coloque os cadinhos sobre a tela de amianto que está em cima
3.
Em seguida, utilizando o bico de Bunsen, aqueça por igual e
de um tripé.
simultaneamente as três amostras. Observe a ordem de fusão e responda:
I. Os pontos de fusão do metal puro e de sua liga são os mesmos?
II. Qual foi a ordem em que os materiais se fundiram?
III. Faça uma pesquisa sobre os valores corretos do ponto de fusão para a solda e
compare com os valores para os metais que a constituem, para isso consulte a
tabela 1.
11
IV. O ponto de fusão pode ser uma propriedade utilizada para diferenciar os metais
puros de uma liga metálica? Por que?
Parte III – Densidade
1.
Pese a amostra da liga de bronze e anote a sua massa.
2.
Em seguida, coloque 70 mL de água na proveta de 100 mL,
mergulhe cuidadosamente (para não quebrar o fundo da proveta), a liga na mesma e
anote o novo volume observado na proveta.
3.
A partir dos resultados obtidos, é possível saber o qual é o
volume da amostra da liga de bronze? Explique.
4.
Repita o procedimento para as outras amostras de liga metálica.
5.
Sabendo que a propriedade densidade pode ser representada
matematicamente pela relação massa/volume, então, é possível calcular o valor da
densidade pela relação: d = m/V. Com os dados obtidos no experimento, preencha o
quadro abaixo:
Materiais
Massa(g)
Volume(mL)
d(g/mL)
Bronze
Latão
Aço inoxidável
Ouro
Solda
Quadro 5 – Resultados do experimento nº 3 – Parte III.
PESQUISA 2
Faça uma pesquisa sobre as ligas metálicas utilizadas no
experimento, e para cada uma delas, procure identificar: a composição; a densidade
e a densidade dos metais que as constituem. Após obter os dados, responda:
1) Se os valores obtidos experimentalmente forem diferentes, como
explicar o resultado?
2) O valor de densidade da liga é igual a dos metais? Por quê?
3) A densidade pode ser uma propriedade utilizada para diferenciar
os metais de uma liga metálica? Por quê?
12
Muitos dos materiais utilizados pelo homem, não são metais, mas
sim, misturas de diversos metais, podendo conter também elementos não-metálicos.
Assim, a maioria dos materiais metálicos usados em nosso cotidiano são, na
realidade, ligas metálicas. Isso acontece porque, quando puros, os metais não
apresentam as propriedades físicas adequadas às exigidas pela indústria.
Ligas metálicas são misturas sólidas de dois ou mais elementos
em que a totalidade, ou pelo menos a maioria, é de elementos metálicos.
A liga metálica é preparada misturando-se dois ou mais metais em
forma líquida e, depois, deixando-os esfriar e solidificar. As propriedades das ligas
dependem dos metais que as constituem e das porcentagens em que cada um entra
na sua composição. Pequenas variações nas proporções dos constituintes podem
afetar muito as propriedades desejadas. O quadro 6 apresenta a composição, as
propriedades e o uso de algumas ligas.
13
Liga
Aço
Aço Inox
Duralumínio
Solda
elétrica
Níquelcrômio
Elementos
Constituintes
Fe
(ferro),
C
(carbono) e traços
de Si (silício), S
(enxofre)
e
P
(fósforo).
Aço comum, Cr
(crômio)
e
Ni
(níquel)
Al (alumínio); Cu
(cobre);
Mn
(manganês);
Mg
(magnésio)
Propriedades
Aplicações
Branco acinzentado
PF = 1300 ºC
Densidade=7,7g/cm3
Fabricação de ligas.
Várias aplicações.
Inoxidável.
aparência.
Boa Talheres, utensílios de
cozinha, decoração.
Baixa densidade
Peças de aviões e
automóveis.
Para
hidroaviões,
outros
elementos fazem parte
como Ce e Zr, que
impedem o ataque pela
água do mar.
Solda
de
contatos
elétricos
baixa Fios
de
resistência
elétrica.
Pb (chumbo) e Sn Baixo PF
(estanho)
Ni (níquel) e Cr PF elevado,
(crômio)
condutividade
elétrica
Ouro
18 Au
(ouro);
Ag Dureza,
inércia Joalheria.
quilates
(prata); Cu (cobre) química,
boa
aparência
Ouro
Au;
Ag;
Pd Dureza,
inércia Joalheria.
Branco
(paládio)
química,
boa
aparência
Bronze
Cu e Sn (estanho) Facilmente moldado Engrenagens,
decoração.
Latão
Cu e Zn (zinco)
Flexível,
boa Tubos,
torneiras,
aparência
decorações.
Amálgama
Composição
Facilmente moldada, Odontologia.
variada:
Hg( relativa
inércia
mercúrio),
Cd química.
(cádmio), Sn, Ag e
Cu
Amálgama
Hg e Zn
Oxida-se apenas em Pilhas elétricas.
de zinco
um circuito elétrico
fechado.
Quadro 6 - Composição e uso de algumas ligas metálicas.
Fonte: Ferreira (1998, p.16).
14
ATIVIDADE 3
O quadro 6 apresenta algumas ligas e suas aplicações. Essas foram
desenvolvidas pelo homem ao longo do tempo, conforme os conhecimentos
adquiridos sobre os metais foram se ampliando. Nesse sentido, vamos refletir um
pouco sobre o desenvolvimento de algumas das descobertas do homem na nossa
sociedade atual?
Procure entrevistar pessoas mais velhas, da sua família ou
conhecidos, e busque informações como:
a) De que material eram feitas às bicicletas antigamente? E
atualmente?
b) Quais são as principais diferenças identificadas? Comparando
com as atuais, elas eram mais pesadas? Por quê?
c) E com relação aos ferros de passar roupa, como eles eram?
d) Do que os ferros de passar roupa são feitos atualmente?
e) Na opinião deles, quais as vantagens (ou desvantagens) que as
atuais bicicletas e ferros de passar roupa têm em relação aos mais antigos?
Toda a análise das propriedades dos metais e das ligas metálicas,
explicam a larga utilização desses materiais pelo homem e a importância que eles
exercem na sociedade desde a Antigüidade. Assim, o estudo dos metais permite
compreendermos aspectos importantes de como nossa sociedade foi evoluindo ao
longo do tempo.
Para aprofundarmos essas discussões, faça a leitura do texto a
seguir.
15
Texto 1
HISTÓRIA DOS METAIS
Por volta de 6000 anos antes de Cristo, o homem já conhecia os metais.
Na realidade, os povos da Idade da Pedra Polida (Neolítico), (que não conheciam técnicas
de metalurgia), usaram acidentalmente os metais nativos, especialmente o cobre, e
posteriormente outros metais, como o ouro e a prata, pois ao procurar pedras para fazer
armas e utensílios, eles encontravam, às vezes, pedaços desses metais.
Desde o Período Neolítico, as civilizações desenvolvem-se por meio de
diferentes culturas, caracterizadas por um conjunto de técnicas fundamentais. O uso do
cobre, depois do bronze, em seguida do ferro e do aço vão se definindo pouco a pouco na
evolução destas culturas.
Provavelmente, o cobre tenha sido descoberto por acaso, em meio a
alguma fogueira feita sobre pedras que continham o minério. É possível que algum
observador neolítico tenha notado o metal, obtido a partir do calor do fogo, reproduzindo o
processo, mais tarde, propositalmente. No início, o cobre era utilizado na forma pura, que
era dúctil demais para a fabricação de instrumentos e armas úteis. A seguir, provavelmente
por acaso, segue-se a descoberta de que, ao adicionar ao cobre pequena proporção de
estanho, forma-se uma liga mais dura do que o cobre puro. Era a descoberta do bronze, que
possibilitou ao homem modelar novos e melhores utensílios. Inicia-se a chamada Idade do
Bronze, período compreendido entre 3500 a.C. a 1200 a.C..Essa época é contemporânea
dos sumérios, egípcios, cretenses e os habitantes de um conjunto de ilhas localizadas na
Grécia.
Cerca de 2.000 anos após a descoberta do cobre e do bronze, o ferro
também passou a ser usado, provavelmente com os hititas, mas só teve grande difusão no
primeiro milênio antes de Cristo, devido ao seu largo emprego na fabricação de armas. O
homem passa a viver a denominada Idade do Ferro, quando as ferramentas e armas
passaram a ser feitas principalmente de ferro ou aço. Tanto o ferro quanto o aço foram
obtidos em 1.000 a.C., através da queima do carvão vegetal com o minério de ferro.
Assim, é possível percebemos que os metais ocupam um papel
fundamental na história da humanidade. A análise dos variados tipos de objetos fabricados
com metais e ligas metálicas é um dos meios de se identificar o grau de desenvolvimento de
uma civilização.
16
ATIVIDADE 4
1. Por que o desenvolvimento da civilização humana esteve tão
relacionado ao uso de metais?
2. Converse com seu professor de história e faça uma pesquisa
sobre o uso dos metais nas civilizações antigas.
Pelo que foi discutido, percebemos que os metais são muito
importantes para o homem e para o desenvolvimento da civilização. Assim,
consideramos relevante refletir sobre algumas questões:
1. Onde os metais são encontrados?
2. Quando encontrados, eles já estão prontos para o uso?
3. Todos os países têm os metais de que necessitam?
4. As reservas minerais de metais são fontes renováveis?
5. A extração desses metais provoca impactos ambientais?
FONTE DE EXTRAÇÃO DOS METAIS
Minerais - Minérios – Metais
Em geral os metais não são encontrados no subsolo “prontos para o
uso”, mas sim fazendo parte da composição de minerais denominados “minérios”.
Normalmente se faz confusão entre as palavras mineral, minério e metal. Saber a
diferença entre elas é fundamental para o entendimento deste estudo.
Recursos Minerais
Os
recursos
minerais
incluem
as
substâncias
inorgânicas
encontradas na crosta terrestre. Os agregados naturais de minerais são chamados
de rochas. Todavia, é comum chamar uma rocha de mineral. Muitas rochas
17
apresentam interesse econômico, pois a partir delas podem-se obter substâncias
que servirão de matéria-prima para as indústrias. Essas rochas são denominadas
minérios.
Minérios: fonte de metais
Minérios são minerais dos quais são extraídos, com vantagem
econômica, uma ou mais substâncias de interesse industrial.
Todos os metais que utilizamos são retirados de minérios presentes
nas rochas que contêm minerais em quantidades economicamente viáveis de
extração. Do ponto de vista químico, os minerais são compostos formados por pelo
menos um metal e um outro elemento, como por exemplo, a cassiterita, que é um
óxido de estanho, de fórmula SnO2.
Do ponto de vista econômico, três são os fatores que influem no
valor de um metal e na sua importância econômica: as suas propriedades físicas e
químicas, o custo de sua produção e a sua quantidade na natureza. No entanto, não
é somente a quantidade um dos fatores preponderantes, ou seja, uma grande
quantidade de metal existente na natureza não determina sozinha, um baixo preço.
O alumínio, apesar de ser o metal mais abundante da crosta terrestre, não é o mais
barato, pois o custo da sua produção é bem elevado.
Os minérios não estão homogeneamente distribuídos na crosta
terrestre. Encontram-se concentrados em determinadas regiões do planeta,
conforme indicam os estudos geológicos sobre a Terra. Como conseqüência, alguns
países são ricos em determinados minérios, e outros totalmente dependentes da
importação. Por exemplo, a África do Sul e o Brasil são grandes produtores de ouro
e de ferro, já o Japão precisa comprar muitos metais para o seu consumo.
Devido à importância que os metais apresentam para a sociedade,
muitos pesquisadores defendem que uma análise sobre o consumo dos mesmos
pode ser uma forma de avaliar o grau de desenvolvimento de um país. Os países
desenvolvidos consomem muito mais metal do que os países emergentes, mesmo
que não possuam as maiores reservas minerais. Assim, por exemplo, o consumo per
capita por ano de cobre nos Estados Unidos é de aproximadamente 8 kg, enquanto
18
que na Índia é de 0,1 kg. A população em 2002, dos EUA era de aproximadamente
281 milhões de pessoas, e a da Índia é de aproximadamente 1 bilhão.
Atualmente, muitas jazidas de minérios estão se esgotando. É o que
vem acontecendo com as reservas de ferro, chumbo, crômio, manganês, níquel,
zinco, ouro, platina e prata. Tem sido cada vez mais difícil encontrar novas jazidas,
e, geralmente, elas apresentam pequena porcentagem de minério na rocha.
Os países que mais consomem metais necessitam importar a maior
parte deles. Os Estados Unidos importam manganês, estanho, cobalto, crômio e
mercúrio, entre outros. A Alemanha importa cobre, manganês, chumbo, zinco e
mercúrio. O Japão depende totalmente da importação de minério de ferro, crômio,
níquel, cobalto, molibdênio, estanho e muitos outros.
O homem, no futuro, vai enfrentar a escassez de minérios e,
portanto, de metais, ou seja, nós não teremos, para sempre, a possibilidade de
retirar da natureza esse precioso material. Portanto, torna-se cada vez mais
necessário evitar perdas por corrosão e praticar intensamente a reciclagem dos
metais, ao lado da substituição por outros materiais.
PARA PENSAR E DEBATER
1. É possível substituir o uso dos metais por outros materiais?
2. Identifique materiais metálicos do seu dia-a-dia que estão sendo
substituídos por outros materiais e relacione as vantagens e desvantagens dessa
substituição.
3. As reservas minerais de metais são fontes não renováveis.
Proponha medidas para evitar o desperdício dos materiais e evitar a exaustão das
reservas.
ATIVIDADE 5
Essa pesquisa tem por finalidade ampliar o estudo dos metais e as
possibilidades de obtenção dos mesmos. Ao final, cada grupo deverá compor um
mural e fazer uma apresentação oral sobre a pesquisa.
19
Orientações:
Parte I
1. Pesquisar sobre as fontes de obtenção dos metais (nome do
minério, ocorrência) apresentando as informações em um quadro, como o exemplo a
seguir:
Metal
Alumínio (Al)
Principal
Principal composto
Ocorrências importantes
minério
do minério
(reservas de minério)
bauxita
Óxido de alumínio
Guiné, Austrália, Brasil
hidratado, Al2O3.H2O
Chumbo (Pb)
Cobre (Cu)
Estanho (Sn)
Ferro (Fe)
Manganês (Mn)
Titânio (Ti)
Zinco (Zn)
Mercúrio (Hg)
Cromo (Cr)
Ouro (Au)
Prata (Ag)
Platina (Pt)
Fonte: Beltran; Ciscato (1991, p.214).
2. Identificar quais são as principais jazidas de minérios do Brasil e
localizá-las no mapa. Procure identificar também, os grandes projetos minerais
implantados no Brasil a partir da década de 1970.
3. A partir da discussão e análise do mapa, formar um grupo de
estudos sobre a exploração mineral no Brasil.
4. Cada grupo deverá escolher um minério e realizar a parte II da
pesquisa. O grupo escolhe o(s) minério(s) a abordar.
20
Parte II
O trabalho escrito deve abordar (ou responder) pelo menos quatro
questões relativas ao(s) minério(s) e a(s) área(s) escolhida(s). Por exemplo:
a. Qual o principal minério explorado na(s) área(s) abordada(s) e quais as
características geológicas que explicam sua ocorrência?
b. Quais os agentes econômicos (empresas nacionais ou estrangeiras) envolvidos
no processo de exploração e comercialização do(s) minério(s) abordado(s) e, se for
o caso, como se realiza o escoamento do produto para as regiões consumidoras
(nacionais ou internacionais)?
c. O processamento do minério é feito no Brasil, ou o mesmo é exportado na forma
bruta? Qual seriam as principais etapas do processamento químico para obtenção
do metal a partir do minério extraído?
d. Há ocorrência de algum impacto social ou ambiental na área de estudo?
No mural devem constar fotografias, ilustrações diversas, mapas e
gráficos selecionados em revistas, jornais e outras publicações, além de notas
explicativas das ilustrações. Os mesmos serão afixados na sala de aula com uma
pequena apresentação de cada grupo a respeito dos resultados obtidos (ADAS,
2000).
A EXTRAÇÃO DOS METAIS
Existem várias técnicas para extrair os metais que ocorrem
combinados, agrupadas sob o nome de metalurgia. O processo metalúrgico de
extração de metais consiste em reduzir minérios a metais, que são substâncias
simples. Particularmente, as técnicas de obtenção do ferro constituem a siderurgia.
Metalurgia e Siderurgia: transformando minérios em metais
Na superfície da Terra encontramos os minerais, que são
substâncias que foram formadas ao longo de milhares de anos pela natureza.
21
Conforme já vimos, grande parte dos minerais contém metais em sua composição e,
dependendo da composição química e da abundância do mineral, é possível extrair
esses metais.
A composição da crosta terrestre é aproximadamente a que
apresentamos na tabela 2:
Tabela 2 - Composição da crosta terrestre.
Elemento
% em massa
O
46,6
Si
27,7
Al
8,1
Fe
5,0
Ca
3,6
Na
2,8
K
2,6
Mg
2,1
Todos os demais
1,5
Fonte: Romeiro (1997, p.5)
Por meio de uma análise da tabela 2, é possível observar que o
alumínio é o metal mais abundante na crosta terrestre. Já o ferro, por sua vez,
apesar de ser o metal mais utilizado pelo homem representa 5% da constituição da
crosta terrestre.
Siderurgia – Metalurgia do Ferro
A siderurgia é o ramo da metalurgia que trata especificamente do
beneficiamento do ferro, sendo a produção de aço sua principal atividade. O ferro é
extraído de minérios encontrados em jazidas minerais, sob a forma de óxidos,
carbonatos e sulfetos, conforme exemplos apresentados no quadro 7.
22
Substância
Óxidos
Fe3O4
Fe2O3
Fe2O3.H2O
Carbonatos
FeCO3
Sulfetos
FeS
Nome Mineralógico
Percentual de Ferro
Magnetita
Hematita
Limonita
45 a 70 %
50 a 70 %
20 a 60 %
Siderita
30 a 45 %
Pirita
Extração para obtenção de aço não é viável
devido à presença de enxofre, prejudicial ao
aço.
Quadro 7 - Ocorrência do ferro na natureza.
Fonte: Romeiro (1997, p.8)
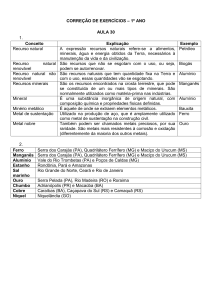
Pelo quadro acima, verificamos que o principal minério de ferro
encontrado no Brasil é a hematita com 50 a 70% de ferro, o que corresponde a 8%
das reservas mundiais. No Brasil, as maiores jazidas de ferro encontram-se em
Minas Gerais (Quadrilátero Ferrífero), Mato Grosso do Sul (Maciço de Urucum) e
Pará (Serra do Carajás).
ATIVIDADE 6: Leia a poesia: A Montanha Pulverizada de Carlos Drummond de Andrade
e procure responder as questões a seguir:
1) Em que época ela foi escrita?
2) De que lugar de Minas Gerais o autor está falando? A qual montanha o autor se refere?
3) Esse local ainda fornece minério de ferro?
4) É possível perceber na poesia uma preocupação do autor com a problemática ambiental?
Sabemos que os metais são encontrados na natureza na forma de
substâncias compostas, os chamados minérios. Mas, os materiais metálicos são, em
geral, substâncias simples, isto é, eles são constituídos por átomos de um único
elemento químico. Dessa forma, ainda temos uma questão importante para
responder:
Como se podem obter os materiais metálicos a partir de substâncias compostas?
Para compreendermos esses processos, será necessário estudar as
reações de oxidação e redução.
23
OXIDAÇÃO E REDUÇÃO
EXPERIMENTO Nº 4 – Queima da palha de aço
MATERIAL
− Vidro de relógio
− Balança
− Palha de aço (tipo bombril)
PROCEDIMENTO
1. Colocar a palha de aço sobre o vidro de relógio e anotar a massa
do conjunto.
2. Queimar toda a palha de aço encostando a chama de um palito
de fósforo. Se ainda restarem pedaços não queimados, atear fogo novamente.
3. Espere esfriar e pese novamente o conjunto.
Análise dos resultados
I. A massa do conjunto pesado permaneceu a mesma antes e depois do
experimento?
II. O que representa a diferença de massa observada?
III. Sabendo que a palha de aço é composta do metal ferro (Fe), como você
representaria a equação química que representa a queima?
Texto 2
A teoria do flogístico
Explicar o fenômeno da combustão é uma preocupação antiga dos
homens. A teoria do flogístico, criada pelo cientista alemão Georg Ernest Stahl (1660-1734)
em 1697, se preocupou com a explicação desse fenômeno. De acordo com essa teoria,
algumas espécies de matéria, tais como o enxofre, o carvão, os óleos vegetais, a madeira,
24
os metais, continham flogístico – um “espírito” que lhes dava a propriedade de serem
combustíveis. O flogístico seria, portanto, um princípio comum inflamável presente apenas
nos materiais combustíveis. Utilizando essa idéia, Stahl explicou o fenômeno da combustão,
a transformação dos metais em óxidos (oxidação) e a transformação dos óxidos em metais
(redução), processos que interessavam muito aos químicos, por causa do progresso
crescente da metalurgia durante o século XVII, que viria a culminar, no século XVIII, com a
Revolução Industrial.
Como a teoria do flogístico explicava a combustão dos metais?
Para compreendermos a explicação dada por essa teoria para a
combustão, precisamos entender que hoje, a combustão de um metal é explicada pela sua
reação com o oxigênio, formando o seu óxido.
Metal + oxigênio
à
óxido do metal
Obs.: o óxido é um composto formado pelo metal e o oxigênio.
Portanto, o óxido é um composto e o metal se combina com o oxigênio
para formá-lo. Já, pela teoria do flogístico, seria o contrário, ou seja, o metal seria o
composto e não o óxido. O óxido se combinaria com o flogístico para formar o metal.
óxido do metal + flogístico à metal
e, ao ser queimado, o metal liberaria o flogístico:
Metal à óxido do metal + flogístico
É freqüente a afirmação de que a teoria do flogístico desapareceu
rapidamente porque teria sido incapaz de explicar aspectos quantitativos das reações.
Como explicar o aumento de peso dos metais após a combustão? Como o metal poderia
desprender o flogístico para o ar dando origem a um produto de peso superior? Alguns
adeptos desta teoria chegaram a admitir que o flogístico tivesse peso negativo.
Essa dificuldade em explicar o aumento de massa na combustão dos
metais, abriu espaço para os trabalhos de Lavoisier que, primeiro criou uma nova teoria da
combustão, contrária àquela de Stahl e depois colocou a massa como uma informação
25
pertinente nas transformações químicas, inaugurando definitivamente a era da química
como uma ciência quantitativa.
Entendendo que o oxigênio é um participante importante nas
reações de combustão, as mesmas podem ser interpretadas como um processo que
envolve ganho de oxigênio. Para compreender melhor, vamos analisar a reação de
combustão do ferro, a partir da queima da palhinha de aço.
a) combustão do ferro:
2 Fe(s)
+
(ferro)
O2(g)
?á
(oxigênio do ar)
2 FeO(s)
óxido de ferro II
O ferro (Fe) ganhou oxigênio.
b) combustão completa do carvão:
C(s)
+
(carvão)
O2(g)
?á
(oxigênio)
CO2(g)
(gás carbônico)
O carbono (C) ganhou oxigênio.
c) a queima do enxofre, processo responsável pela formação da chuva ácida:
S(s)
(enxofre)
+
O2(g)
?á
(oxigênio)
SO2(g)
(dióxido de enxofre)
O Enxofre (S) ganhou oxigênio.
Analise agora, o que acontece neste outro experimento, quando a
palhinha de aço é exposta ao ar e á água.
26
EXPERIMENTO Nº 5 – Formação de ferrugem.2
MATERIAL
− 3 tubos de ensaio iguais
− 1 bastão de vidro
− 3 placas de Petri
− Esponja de aço
PROCEDIMENTO
Ensaio I
1.
Umedeça um tubo de ensaio com água e coloque dentro, uma
pequena mecha de esponja de aço (na forma de bolinha).
2.
Com o auxílio do bastão de vidro, distribua-a até que ocupe
cerca de 1/3 do comprimento do tubo.
3.
Coloque água em uma placa de Petri de maneira a preenchê-la.
4.
Inverta o tubo de ensaio, mantendo-o nessa posição e coloque-o
na placa de Petri.
Ensaio II
1. Coloque um tubo, vazio e invertido, numa placa de Petri
contendo água.
Ensaio III
1. Repita (sem umedecer a palhinha de aço) o procedimento
indicado para o ensaio I, agora com uma placa de Petri vazia.
2
Adaptado de GEPEQ. Interações e Transformações I: Elaborando Conceitos sobre
Transformações Químicas. São Paulo: Edusp, 2005. p. 157-161.
27
2. Utilize o quadro 8 para registrar as características (início e fim)
dos sistemas.
3. Deixe os tubos de ensaio, sem tocar, até a próxima aula, quando
serão registradas as observações referentes ao estado final dos sistemas.
Figura 2 - Ensaios I, II e III, respectivamente.
Ensaio
Estado inicial
Estado final
I
II
III
Quadro 8 – Características dos sistemas analisados.
Analisando os dados registrados no experimento, responda às
seguintes questões:
I. Foi observada alteração na esponja de aço utilizada no ensaio I? E no ensaio
III?
28
II. O que ocorreu com o nível da água no ensaio I e no ensaio II? Tente explicar o
que observou.
III. Levando em conta suas respostas às questões 1 e 2, que materiais terão
interagido dando origem à ferrugem?
IV. Levando em conta que a ferrugem é constituída, em grande parte, por óxido de
ferro (III) hidratado (Fe2O3. n H2O – n significa que o número de partículas de
água é variável), e lembrando que, no experimento, o tubo foi inicialmente
umedecido, escreva a equação que representa a formação da ferrugem.
Dessa forma, o processo de enferrujamento do ferro exposto ao ar
úmido, pode ser representado pela equação química:
4 Fe(s)
(ferro)
+
3 O2(g)
(oxigênio)
+
x H2O
(água)
?á
2 Fe2O3. xH2O(s)
(óxido de ferro)
Nesse processo, também podemos dizer que o ferro (Fe) ganhou
oxigênio.
No enferrujamento, bem como em todos os exemplos aqui
analisados, observamos que houve ganho de oxigênio na formação dos produtos
das transformações químicas. O processo de ganho de oxigênio em uma
transformação química é denominado oxidação.
Assim, ao observamos os produtos dessas transformações,
verificamos que a oxidação está relacionada à oxigenação, ou seja, ao ganho de
oxigênio. Historicamente, as reações de oxidação receberam esse nome porque
designavam as reações que envolviam a combinação entre o oxigênio e outro
elemento.
Da mesma forma que ocorre o processo de oxidação, ou seja, ganho
de oxigênio, pode ocorrer a perda de oxigênio nas transformações químicas. A esse
processo é dado o nome de redução.
No século XVIII, por exemplo, era muito comum obter o óxido de
mercúrio a partir do aquecimento do mercúrio e regenerá-lo a partir da sua
decomposição térmica (hoje entendida dessa forma). É importante lembrar que,
29
naquela época, os modelos explicativos para esse processo ainda estavam em
construção e não eram os mesmos que utilizamos atualmente.
d)
2 HgO(s)
2 Hg(l)
?á
(óxido de mercúrio)
+
O2(g)
(mercúrio)
(oxigênio)
Nesse processo, podemos dizer que o óxido de mercúrio perde
oxigênio – processo de redução.
Nos exemplos discutidos até o momento, oxidação e redução
parecem
processos
independentes.
No
entanto,
os
mesmos
ocorrem
simultaneamente, como é possível analisar por meio do processo de produção do
ferro a partir do óxido de ferro, exemplificado a seguir:
e)
2 Fe2O3(s)
(óxido de ferro)
+
3C(s)
(carvão)
?á
4 Fe(s)
(ferro)
+
3CO2(g)
(dióxido de carbono)
2Fe2O3(s) à 4 Fe(s): processo de redução, ou seja, perda de oxigênio.
3C(s)
à 3CO2(g): processo de oxidação, ou seja, ganho de oxigênio.
Dessa forma, os processos de oxidação e redução ocorrem ao
mesmo tempo e, enquanto uma espécie perde oxigênio, a outra espécie,
necessariamente, ganha oxigênio. Oxidação e redução são, portanto, fenômenos
simultâneos.
A espécie que sofre redução está provocando a oxidação da outra
espécie e, por esse motivo, é chamada de agente oxidante ou, simplesmente,
oxidante.
30
A espécie que sofre oxidação está provocando a redução de outra
espécie, e por esse motivo, é chamada de agente redutor ou, simplesmente,
redutor.
ATIVIDADE 7
Discuta se é possível visualizar a ocorrência conjunta de oxidação
(ganho de oxigênio) e redução (perda de oxigênio), em cada uma das
transformações químicas representadas por meio das equações químicas 1 e 2:
1) K2Cr2O7(s)
+
dicromato de potássio
2) FeCl2(s)
cloreto de ferro II
KOH(s)
?á
hidróxido de potássio
+
Cl2(g)
?á
gás cloro
K2CrO4(s)
cromato de potássio
+
H2O(l)
água
FeCl3(s)
cloreto de ferro III
No exemplo 1 da atividade acima, é possível verificar que, nem
sempre, conseguimos visualizar, por meio de uma equação química a ocorrência
simultânea do ganho e perda de oxigênio.
Também, existem casos em que está envolvida a perda e o ganho
de outros elementos, como é o caso do exemplo 2, que não apresenta oxigênio na
equação.
Nesse sentido, é preciso buscar idéias (modelos explicativos) mais
amplas sobre os conceitos de oxidação e redução, de forma a ampliar a capacidade
de explicar os diferentes fenômenos. No entanto, cabe salientar que isso será feito
em outros momentos dos seus estudos em química.
31
REVENDO O PROCESSO SIDERÚRGICO: UMA NOVA EXPLICAÇÃO.
Já vimos que o ferro não se encontra livre na natureza. Assim, é
necessário utilizar um agente redutor para obtê-lo a partir de seus minérios. O
monóxido de carbono (CO) é o agente redutor geralmente empregado.
Nesse sentido, é necessário utilizar o carvão (C) como matéria prima
para a produção do monóxido de carbono.
A seguir, são apresentadas as principais reações químicas que
ocorrem no interior do alto-forno:
1) Produção de energia e formação de monóxido de carbono (CO):
2C(s)
+
Carvão
O2(g)
Oxigênio do ar
2 CO(g)
?á
+
energia (calor)
monóxido de carbono
Analisando a reação 1, podemos afirmar que o carbono (C) está
ganhando oxigênio e, portanto, sofrendo oxidação.
Nesse caso, a combustão do carvão tem dupla finalidade: fornecer o
calor necessário e, ao mesmo tempo, produzir o monóxido de carbono que vai
provocar a redução do minério.
2) Entendendo o processo de redução do ferro (que faz parte da
constituição do minério):
O ferro, que se encontra nos minérios, deve ser reduzido a ferro
metálico. O monóxido de carbono vai atuar como agente redutor. Trata-se de um
processo complexo e, do ponto de vista de nosso estudo, a reação mais importante
é a representada pela equação global abaixo.
Essa equação representa o que é observado no início do processo e
na saída do alto forno. No entanto, como já foi discutido anteriormente, nesse trajeto,
ocorrem várias etapas:
32
2 Fe2O3(s) +
minério de ferro
6 C(s) + 3 O2(g)
carvão
4 Fe(s)
?á
gás oxigênio
+
ferro (metal)
6 CO2(g) +
dióxido de carbono
energia
luz e calor
Na reação acima, o minério de ferro está perdendo oxigênio e,
portanto, sofrendo redução, ou seja, sendo reduzido a ferro metálico. Por sua vez, o
carvão está ganhando oxigênio e sendo oxidado a gás carbônico.
Como a temperatura na região inferior do alto-forno é muito superior
ao ponto de fusão do metal impuro, este funde, escorrendo para a parte inferior,
onde é recolhido.
Esse ferro, que sai do alto-forno, chama-se ferro-gusa ou ferro-
fundido (mesmo depois de solidificado mantém esse nome). Contém cerca de 5 %
de carbono, sendo, por esse motivo, muito quebradiço.
O ferro gusa passa então por um processo de purificação, onde
pode conter em sua composição até cerca de 0,2 % de carbono, recebendo o nome
de ferro doce. O ferro com até cerca de 1,5 % de carbono é chamado de aço e
trata-se da liga metálica mais usada pela nossa civilização.
O resíduo dessa produção, rico em calcário, sílica e outras
impurezas, chamado escória, serve de matéria-prima para a fabricação de cimento.
3) Reação da escória:
I-
CaCO3(s)
?á
Carbonato de cálcio
II -
CaO(s)
CaO(s)
+
óxido de cálcio
+
óxido de cálcio
SiO2(s)
óxido de silício (ganga)
CO2(g)
dióxido de carbono
?á
CaSiO3(s)
silicato de cálcio (escória)
Algumas reflexões sobre a exploração dos recursos minerais
Sabemos que é inevitável a exploração de recursos minerais, pois a
sociedade industrial depende deles. Por outro lado, sabemos também que não se
pode permitir que a exploração mineral devaste o meio-ambiente. É preciso refletir
sobre esse problema, pois não podemos encarar a exploração dos recursos
minerais, como uma atividade desprovida de conseqüências ambientais, sociais,
políticas e econômicas.
33
PARA VOCÊ PENSAR!
1. Você conhece o Projeto Carajás?
2. A Companhia Vale do Rio Doce, que mudou recentemente seu
nome para Vale, é uma das empresas responsáveis pela extração e comercialização
de minérios no Brasil. Essa companhia, que era estatal, foi privatizada no governo
do presidente Fernando Henrique Cardoso. Essa privatização foi uma boa opção
para o governo brasileiro?
3. Você
acompanhou
a
discussão
do
plebiscito
sobre
a
privatização da Companhia Vale do Rio Doce?
4. O que o poeta Carlos Drummond de Andrade, quis dizer com o
seguinte pensamento: “Carajás é a saída ou o fundo do poço? Quem me explica
isso em língua fácil e troco miúdo?”
34
REFERÊNCIAS
ADAS, Melhen. Panorama Geográfico do Brasil: contradições, impasses e desafios
socioespaciais. São Paulo: Editora Moderna, 2000.
BELTRAN, N.O.; CISCATO, C.A.M. Química: Coleção Magistério 2º Grau – Série
Formação Geral. São Paulo: Cortez Editora, 1991.
CANTO, Eduardo Leite do. Minerais, minérios, metais: de onde vêm? para onde
vão? São Paulo: Moderna, 1996.
FERREIRA, M. Ligações Químicas: uma abordagem centrada no cotidiano.
Disponível em:
< http://www.iq.ufrgs.br/aeq/html/publicacoes/matdid/livros/pdf/ligacoes.pdf>. Acesso
em: 22 nov. 2007.
GEPEQ. Interações e Transformações I: Elaborando Conceitos sobre
Transformações Químicas. São Paulo: Edusp, 2005.
ROMEIRO, S. B. B. Química na Siderurgia. Disponível em:
http://www.iq.ufrgs.br/aeq/html/publicacoes/matdid/livros/pdf/siderurgia.pdf. Acesso
em: 25 nov. 2007.
SANTOS, W.L.P., MÓL, G.S. e outros. Química & Sociedade. São Paulo: Nova
Geração, 2005.
SÃO PAULO. Secretaria de Estado da Educação. Coordenadoria de Estudos e
Normas Pedagógicas. Proposta Curricular para o ensino de química: 2º grau. 2 ed.
São Paulo: SE/CENP, 1988.