Metabolismo e Endocrinologia
12 de Abril de 2006
Nomenclatura dos principais dissacáridos
Grupo 3
Os monossacarídos são os açúcares mais simples, de fórmula estrutural (CH 2O)n. Esse
"n" pode variar de 3 a 7 (trioses, tetroses, pentoses, hexoses e heptoses), sendo os mais
importantes as pentoses e hexoses.
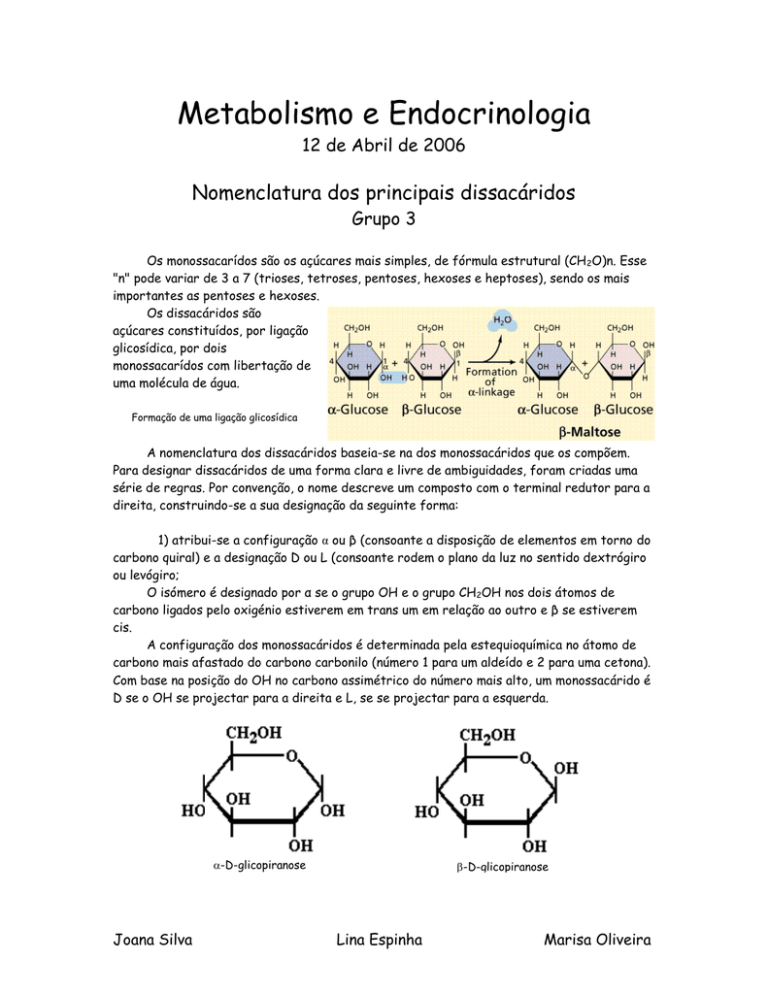
Os dissacáridos são
açúcares constituídos, por ligação
glicosídica, por dois
monossacarídos com libertação de
uma molécula de água.
Formação de uma ligação glicosídica
A nomenclatura dos dissacáridos baseia-se na dos monossacáridos que os compõem.
Para designar dissacáridos de uma forma clara e livre de ambiguidades, foram criadas uma
série de regras. Por convenção, o nome descreve um composto com o terminal redutor para a
direita, construindo-se a sua designação da seguinte forma:
1) atribui-se a configuração α ou β (consoante a disposição de elementos em torno do
carbono quiral) e a designação D ou L (consoante rodem o plano da luz no sentido dextrógiro
ou levógiro;
O isómero é designado por α se o grupo OH e o grupo CH 2OH nos dois átomos de
carbono ligados pelo oxigénio estiverem em trans um em relação ao outro e β se estiverem
cis.
A configuração dos monossacáridos é determinada pela estequioquímica no átomo de
carbono mais afastado do carbono carbonilo (número 1 para um aldeído e 2 para uma cetona).
Com base na posição do OH no carbono assimétrico do número mais alto, um monossacárido é
D se o OH se projectar para a direita e L, se se projectar para a esquerda.
-D-glicopiranose
Joana Silva
-D-glicopiranose
Lina Espinha
Marisa Oliveira
2) dá-se nome ao resíduo redutor, isto é, estabelece-se a distinção entre estruturas:
os monossacáridos de cinco e seis carbonos formam hemiacetais ciclicos ou hemicetais em
solução. Origina-se um novo carbono assimétrico de modo que duas formas isométricas são
possíveis: estruturas em anel de cinco membros (furanose) e de seis membros (piranose)
sendo a segunda a mais frequente.
3) indicam-se, entre parentêses, os dois átomos de carbono unidos pela ligação
glicosidica, com uma seta a ligar os dois números;
4) dá-se o nome ao segundo resíduo.
Os principais dissacáridos são a maltose, a sacarose e a lactose:
A maltose contém dois resíduos de D-glicose unidos por ligações glicosídicas entre o C1 (carbono anomérico) de um resíduo de glicose e o C-4 de outro. Ainda que o carbono
anomérico envolvido na ligação glicosídica não está disponível para reagir com os iões de
cobre ou ferro, a maltose é um açúcar redutor pois o carbono anomérico do segundo resíduo
de glicose está livre e pode ser oxidado.
Maltose:
glicose+glicose
Nomenclatura:
-D-glicopiranosil-(1->4)- -D-glicopiranose
Ou abreviadamente
−D−Glcp−(14)−ou −D−Glcp
A lactose contém um resíduo de D-galactose e um resíduo de D-glicose e ocorre
principalmente no leite, estando a galactose unida a glicose por uma ligação glicosídica do
tipo b1,4. O carbono anomérico do resíduo de glicose está disponível para oxidação e assim a
lactose é um açúcar redutor. A hidrólise da lactose em galactose e glicose é catalisada pela
enzima lactase.
Lactose: galactose+glicose
Nomenclatura:
-D-galactopiranosil-(1->4)- -D-glicopiranose
Ou abreviadamente
−D−Galp−(14)−−D−Glcp
Joana Silva
Lina Espinha
Marisa Oliveira
A sacarose é obtida comercialmente da cana-de-açúcar ou beterraba. Os dois
átomos de carbono anoméricos da glicose e frutose estão envolvidos na ligação
glicosídica, do tipo a(1-2), sendo portanto a sacarose um açúcar não redutor.
Sacarose: glicose+frutose
Nomenclatura:
-D-glicopiranosil-(12)--D-frutofuranósido
Ou abreviadamente
−D−Glcp−(12)−−D−Fruf
Joana Silva
Lina Espinha
Marisa Oliveira












