INSTRUÇÕES DE USO
HEMAGEN®VIRGO
SARAMPO (MEASLES) - IgG - Imunofluorescência
Cat. No. 903100 - 96 testes (12x8)
USO DO PRODUTO
O teste de Sarampo (Measles) - IgG VIRGO por imunofluorescência indireta
é usado para a detecção e titulação dos anticorpos IgG do vírus do sarampo
no soro humano.
RESUMO, EXPLICAÇÃO E PRINCÍPIO DO TESTE
Desde a introdução da vacina do vírus do sarampo em 1963, os Estados
Unidos tem aumentado o programa efetivo de imunização resultando uma
essencial eliminação do sarampo como uma das mais freqüentes doenças
infantis. Porém, tem sido reportado uma mudança persistente na
suscetibilidade da população de adultos jovens como um resultado da falha
da vacina ou falta de vacinação1.
Nos casos de sarampo, a severidade da doença e a taxa de mortalidade são
mais altas em adultos2.
Deste modo, a sorologia tem se tornado de importância crescente como uma
ferramenta para determinar o estado imune, particularmente daquela
população de adulto jovem.
Além disso, a ligação entre a infecção por sarampo e o parto prematuro ou
aborto espontâneo torna importante a pesquisa da suscetibilidade em
mulheres grávidas3.
Apesar do sarampo ter sido reconhecido como uma doença há mais de dois
mil anos, uma descrição de sua epidemiologia apareceu primeiro em um
jornal por Panum em 1849. Em seu estudo de uma epidemia nas Ilhas Faroe,
Panum observou que o sarampo teve um período de incubação de duas
semanas e era contagiosa, mas que a imunidade vitalícia seguiu a infecção
primária4. Mais de 100 anos mais tarde, em 1963, a primeira vacina de
sarampo vivo foi licenciada nos USA. O desenvolvimento da vacina foi
possível pela descoberta de Enders e Peebles, em 1954, que descobriu que o
vírus crescia com sucesso in vitro em sistema de cultura de tecido5. O
sucesso da vacina é evidente pela queda da incidência anual de infecção de
sarampo de 500.000 a menos de 3000 casos reportados por ano.
SARAMPO IFA
1
Classificado como um paramixovirus, o sarampo produz uma infecção
respiratória altamente contagiosa. A doença é propagada durante a fase
prodrômica através do contato direto com as secreções respiratórias em
forma de gotículas.
Em adição ao sarampo, várias outras doenças têm sido associadas mas não
ligadas às causas do vírus do sarampo. Esta lista inclui panencefalites
esclerosante subaguda (PES)6, lupus eritematoso sistêmico (LES)7 e
esclerose múltipla (EM)8. Pacientes com PES, uma doença neurológica
degenerativa crônica, tem documentado altos títulos de anticorpos ao vírus
do sarampo. Porém, para LES e EM há menos elevação pronunciada, mas
estatisticamente significativa nos títulos de anticorpo. A significância ou o
papel da infecção por sarampo nestes estágios de doença é desconhecido até
agora.
Uma vez que a presença do anticorpo IgG circulante para o vírus do
sarampo é indicativo de infecção prévia ou vacinação, a pesquisa da
soropositividade em mulheres grávidas, jovens adultos e outros pacientes de
alto risco é uma ferramenta valiosa para o seu estado imune.
O kit de Sarampo IF VIRGO fabricado pela Hemagen Divisão VIRGO
fornece todos os reagentes necessários para uma rápida determinação do
anticorpo do Sarampo no soro humano. O substrato antigênico, soro
controle, conjugado FITC, tampão, meio de montagem e instruções de uso
estão inclusos no kit.
Princípio do Teste
O ensaio de anticorpos fluorescente VIRGO utiliza o método indireto de
impregnação de anticorpo fluorescente, descrito pela primeira vez por
Weller e Coons em 19549. O procedimento é realizado em dois passos de
reações básicas. No passo um, o soro humano a ser testado entra em contato
com o substrato antigênico. O anticorpo, se presente no soro teste, irá ligar
ao antígeno, formando um complexo antígeno-anticorpo. Se o soro a ser
testado não contém anticorpo a este antígeno particular, não é formado
nenhum complexo e todos os componentes do soro são removidos no passo
de lavagem. O segundo passo envolve a adição de um anticorpo anti-humano
marcado com fluoresceína aos poços de teste. Se o complexo antígenoanticorpo específico é formado no passo um, o anticorpo marcado com
fluoresceína irá ligar à metade do anticorpo do complexo no passo dois.
Uma reação positiva, verde-maçã fluorescente brilhante, pode ser vista com
a ajuda de um microscópio de fluorescência.
Princípio do teste de Anticorpo Fluorescente Indireto.
SARAMPO IFA
2
Passo 1
Antígeno (Substrato)
na lâmina
Antígeno-Anticorpo
+
Anticorpo específico
=
Complexo
Passo 2
Anticorpo-Antígeno
Fluorescência
+
Anticorpo anti-humano marcado
=
com Fluoresceína
MATERIAIS FORNECIDOS
Quantidade de teste
96 Testes
12 (8 poços)
01 frasco
01 frasco
01 frasco
03 pacotes
01 frasco
02 pacotes
Lâminas infectadas com Sarampo (cepa de Edmonston) e
infectadas fixadas.
Frasco de Controle Positivo contendo soro humano liofilizado.
Frasco de Controle Negativo contendo soro humano liofilizado.
Conjugado FITC contendo IgG inativado de cabra anti-humano (
e pesada) liofilizado com contra-corante.
*Tampão Fosfato (PBS) em pó, com pH 7,4 +/- 0,2.
*Contendo 2 ml de Glicerol tamponado.
*Contendo 5 mata-borrões cada.
* Estes componentes podem ser trocados entre diferentes lotes.
MATERIAIS REQUERIDOS MAS NÃO FORNECIDOS
Tubos de testes e estantes para fazer as diluições.
Pipetas para a preparação das diluições.
Lamínulas de 22 x 50 mm, No.1 de espessura.
Câmara úmida.
Agitador magnético de placa (opcional).
Travessa de coloração e estante com suporte de lâmina.
SARAMPO IFA
3
Microscópio de fluorescência. Referir ao manual de instrução do
fabricante para que o sistema de filtro dê ótimos resultados para o FITC
(Comprimento de excitação máxima = 490 nm. Comprimento de emissão
média = 520 nm).
Estes materiais podem ser obtidos nas lojas e/ou empresas que vendem
produtos e acessórios para laboratório.
ARMAZENAMENTO E ESTABILIDADE
1. Armazenar o kit de 2º a 8oC. O pó de PBS e o Glicerol Tamponado
podem ser armazenados de 2º a 30 oC se desejado. O kit de teste pode ser
usado até a data de expiração escrita no lado externo da caixa.
2. Após a hidratação: O Controle Positivo, Controle Negativo, e
Conjugado FITC deverão ser armazenados de 2º a 8 oC, ou divididos em
alíquotas e armazenados a - 20 oC ou menos se não for usado dentro de
uma semana.
NOTA: Foram tomadas precauções na fabricação deste produto para
proteger os reagentes de contaminação. Após a reconstituição, deverá ser
tomado cuidado para proteger os reagentes deste kit de contaminação. Se
for mantida uma temperatura constante de armazenamento, os reagentes
e substratos deverão ser estáveis até o período de vencimento do kit.
CUIDADOS E PRECAUÇÕES
1. Este kit é somente para uso diagnóstico in vitro.
2. Manusear todas as amostras do ensaio, lâminas, controles positivo e
negativo como se fossem capazes de transmitir agentes infecciosos.
Todos os componentes de sangue humano do kit foram testados por
métodos aprovados pelo FDA e apresentou-se negativo para antígeno de
superfície da hepatite B (HBsAg) e para anticorpos ao vírus tipo 1 da
imunodeficiência humana HIV-1. Como nenhum método pode oferecer
completa segurança de que os vírus do HIV, hepatite B e outros agentes
infecciosos estão ausentes, as amostras e os reagentes do kit deverão ser
manuseados no Nível 2 de Biossegurança, como recomendado para
qualquer soro humano ou amostra de sangue potencialmente
infeccioso.10,11
3. Os substratos antigênicos são fixados em acetona.
4. Não pipetar com a boca.
SARAMPO IFA
4
5. Não fumar, comer, ou beber em áreas onde as amostras ou reagentes do
kit são manuseadas.
6. Todos os materiais usados neste ensaio, incluindo reagentes, amostras e
materiais de limpeza deverão ser descartados de uma maneira que irá
inativar os agentes infecciosos.
7. Não usar o kit ou os reagentes individuais além das suas datas de
expiração marcadas.
8. Os componentes do kit foram testados como uma unidade. Não trocar os
componentes de outras fontes ou de diferentes lotes, exceto quando
anotado.
9. Proteger o conjugado de exposição prolongada de luz.
COLETA, ARMAZENAMENTO E MANUSEIO DA AMOSTRA
1. As amostras de soro podem ser armazenadas à temperatura ambiente até
24 horas. Por um período mais longo, podem ser armazenados de 2 a 8 oC
(por até 3 dias), ou congelados a
- 20 oC ou menos. Colocar a 37 oC
até que a amostra seja descongelada. Remover e misturar bem antes do
uso. Não é recomendado o autodegelo. Evitar ciclos múltiplos de
congelamentos e descongelamentos12.
2. A ótima execução do kit de Sarampo IgG VIRGO IF depende do uso de
amostras de soro frescas. As amostras deverão ser colhidas
assepticamente. A separação rápida do coágulo previne a hemólise do
soro13.
3. Para melhores resultados, deverá ser colhida uma nova amostra se
houver a presença de contaminação bacteriana ou lípides. Se não for
obtida uma nova amostra, é requerida uma filtração (0,45µ) ou
centrifugação (aproximadamente 3000 x G por 10 minutos).
4. O excesso de lípides no soro teste pode produzir uma reação de
“filmagem”. Os lípides “fixam” não especificamente no vidro e são
extremamente difíceis de remover. A experiência irá habilitar o técnico a
diferenciar esta reação de “filme” da reação específica.
5. Ocasionalmente, as amostras podem conter certas enzimas proteolíticas
que atacam e digerem o substrato. Isto é devido especialmente a amostras
contaminadas com microorganismos. Tais amostras podem ser aquecidas
a 56 oC por 30 minutos. Se isto não ocasionar a redução da atividade
enzimática, deverá ser obtida uma outra amostra de paciente.
PROCEDIMENTO DO TESTE
A - PREPARAÇÃO DOS REAGENTES
SARAMPO IFA
5
Deixar todos os reagentes e lâminas atingirem a temperatura ambiente
por 15 a 30 minutos antes do uso.
1. Lâminas e Glicerol: Prontos para o uso.
2. PBS: Dissolver o conteúdo de um pacote em 1 litro de água destilada ou
deionizada. Fechar o recipiente para prevenir contaminação ou
evaporação.
3. Controles: Reidratar com 0,5 ml do PBS. Os controles estão agora a
uma diluição de 1:8. Aliquotar e armazenar a -20 oC.
4. Conjugado: Reidratar com 2,0 ml de PBS. Armazenar de 2º - 8oC ou
aliquotar e armazenar a -20 oC.
B - PROCEDIMENTO
As amostras podem conter agentes infecciosos, portanto deverão ser
manuseadas com cuidado.
Para obter ótimos resultados NÃO deixar os poços do substrato
secarem enquanto executa o teste.
1. Remover as lâminas e os reagentes requeridos do refrigerador e deixe-os
atingir a temperatura ambiente (15 a 30 minutos).
2. Remova as lâminas da embalagem apenas antes do uso e rotule.
3. Reidrate os controles para preparar a diluição de 1:8. Estes são agora
representativos de padrões de fluorescência positivo e negativo típico.
4. Dilua as amostras com PBS a diluições de 1:8 ou prepare diluições
seriadas para a determinação quantitativa.
5. É necessário testar 1 Controle Positivo, 1 Controle Negativo e um
Controle de Tampão PBS para cada bateria de lâminas testadas.
6. Cobrir cada poço com uma amostra diluída ou controles
(aproximadamente 10-20 µl por
poço).
7. Incubar em uma câmara úmida a 37º +/- 2oC por 30 minutos.
8. Enxaguar as lâminas rapidamente com um leve jato de PBS. Não jogar
direto nos poços.
9. Enxaguar as lâminas completamente por 7 minutos em uma travessa de
coloração do PBS.
Trocar o tampão e
lavar uma vez mais por 8 minutos. Manusear as lâminas levemente. É
necessária uma leve agitação do tampão para a lavagem eficiente da
lâmina.
SARAMPO IFA
6
10.Secar o lado pintado da lâmina com o mata-borrão fornecido. Não deixar
os poços secarem
antes da adição do
conjugado.
11.Cobrir cada poço com uma gota (~ 10 µl) do Conjugado FITC.
12.Incubar em uma câmara úmida a 37º +/- 2oC por 30 minutos. Proteger da
luz intensa.
13.Repetir os passos 8 e 9. Secar o lado pintado da lâmina com o mataborrão, não deixar os
poços secarem antes
da adição do glicerol.
14. Colocar uma pequena gota do Glicerol Tamponado em cada poço e
cobrir com uma lamínula.
15. Para melhores resultados, as lâminas deverão ser lidas imediatamente em
um aumento de 200-500 X. Alternativamente, as lâminas podem ser lidas
dentro de 24 horas. Porém, elas deverão ser armazenadas de 2º - 8oC no
escuro, e seladas para prevenir a secagem do fluido de montagem.
C - CRITÉRIO PARA A GRADUAÇÃO DA INTENSIDADE DE
FLUORESCÊNCIA
4+
3+
2+
1+
forma, mas legível.
0
discretamente visível.
Fluorescência verde-maçã brilhante.
Fluorescência verde-maçã luminoso.
Fluorescência verde-maçã claro distinguível.
Fluorescência verde-maçã escuro, mudando a
Nenhuma
fluorescência
ou
fluorescência
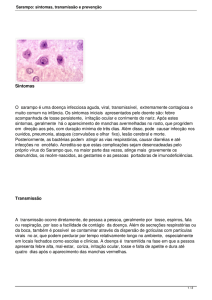
D - GUIA PARA CARACTERIZAR A FLUORESCÊNCIA
Fluorescência associada ao Sarampo.
Uma reação de anticorpo de Sarampo positiva é identificada pela presença
de fluorescência luminosa no citoplasma de células infectadas.
Como um controle adicional, as células não-infectadas são misturadas com
as células infectadas. Cada campo de fonte alta deve conter células que não
exibem nenhuma fluorescência específica. Estas células não infectadas
“negativas” deverão exibir coloração vermelha ou laranja do citoplasma com
um núcleo preto-esverdeado a preto.
Fluorescência Não-Específica
SARAMPO IFA
7
Toda a célula exibe fluorescência verde-maçã positiva, no núcleo,
citoplasma ou ambas. Uma reação produzida por um estado de doença não
relacionada ou em conjunto com uma infecção por Sarampo, por exemplo,
anticorpo antinuclear ou anticorpo antimitocondrial deverá ser
considerado.14,15
Nenhuma Fluorescência
Ausência de fluorescência ou menos que 1+ no citoplasma de células
infectadas.
Nota: Nas determinações quantitativas, o título de ponto final é a diluição
mais alta que apresenta uma fluorescência de 1+ nas inclusões.
ORIENTAÇÕES SOBRE OS PROCEDIMENTOS DE LEITURA
ESPECIFICAÇÕES DO MICROSCÓPIO
Os sistemas de comparação de filtro são mostrados abaixo:
Fluorescência da luz transmitida:
Fonte de Luz
Vapor de Mercúrio
200W
50W
Tungstenio Halogenio
50W
100W
Fluorescência da luz incidente:
Fonte de Luz
Vapor de mercúrio
200W
100W
50W
Tungstenio Halogenio
SARAMPO IFA
Filtro de Excitação
KP490 + BG 38
(4 mm) ou BG 12 (4 mm) +
BG 38 (4 mm)
KP 490 + BG 38
(4 mm)
Filtro de Barreira
KP510, K530
KP510, K515, K530
Raio dicroico
Filtro de Excitação
de espelho dividido
KP500 + BG 38 (4 mm) ou
TK510
BG 23 (4 mm) para a
supressão vermelha mais
forte. Filtro de canto de 450
nm, 480 nm para banda de
excitação estreita, supressão
da série de auto-fluorescência.
KP500 + BG 38 (4 mm)
TK510
8
50W
100W
INTERPRETAÇÃO DOS RESULTADOS
Resultados
Significado
Pesquisa
Nenhuma
Fluorescência
ou
intensidade
fluorescência < 1 + a diluição de 1:8.
de Nenhum anticorpo IgG de
detectável. Tais indivíduos são p
serem não infectados, entretanto,
a uma infecção primária de saramp
Fluorescência > 1 + a diluição 1:8 ou maior em uma Positivo pela IF para os anticorpos
única amostra de soro.
do Sarampo. Tais indivíduos são p
ser imunes à infecção de sara
diagnostica infecção recente ou co
amostra de soro pareada.
Para confirmar infecção aguda, são requeridas amostras pareadas. A
primeira amostra (aguda) deverá ser colhida logo após os sinais clínicos da
infecção. A segunda amostra (convalescente) deverá ser colhida dentro de
10-14 dias da primeira. Ambas as amostras devem ser testadas ao mesmo
tempo usando o mesmo lote de reagentes.
Soros Pareados
Diferença de uma diluição no título ponto final dos
soros pareados colhidos com intervalo de 10 a 14
dias.
Nenhuma evidência de infecção rece
Aumento no título de 4 diluições ou mais nos títulos
de ponto final dos soros pareados colhidos com
intervalo de 10 a 14 dias.
Diagnóstico de infecção recente ou c
LIMITAÇÕES DO PROCEDIMENTO
SARAMPO IFA
9
1. O procedimento do teste de Sarampo IgG IF VIRGO e a interpretação
dos resultados dos testes devem ser seguidos à risca para obtenção de
resultados de testes confiáveis.
2. A falta de um aumento significativo no título de anticorpos não exclui a
possibilidade de infecção por Sarampo.
3. Quando medir os níveis de anticorpos IgG, os resultados positivos em
neonatos deverão ser interpretados com cuidado uma vez que o anticorpo
materno é transferido passivamente da mãe para o feto antes do
nascimento. Os ensaios de IgM são geralmente indicadores mais úteis de
infecção em crianças abaixo de seis meses.
4. Os resultados deste teste deverão ser interpretados juntamente com
outros achados clínicos e procedimentos diagnósticos.
CONTROLE DE QUALIDADE
1. Os Soros Controle são representativos de reações positivas e negativas.
Na diluição de pesquisa, o Controle Positivo representa uma forte reação
(3+ - 4+). Se a intensidade de fluorescência do Controle Positivo for
menor que a faixa aceitável, o teste é inválido e deverá ser repetido.
2. Cada lote do Controle Positivo deve ser titulado em uma diluição ponto
final. O título ponto final deverá estar dentro de +/- duas diluições seriais
de duplo passo do título do Controle Positivo reportado na nota de
diluição do kit de Sarampo IgG por IF VIRGO. Se os resultados obtidos
estiverem fora da faixa, o teste é inválido e deverá ser repetido.
3. Na diluição de pesquisa, o Controle Negativo não deverá apresentar uma
fluorescência verde-maçã. Se for observada uma fluorescência verdemaçã, o teste é inválido e deverá ser repetido.
4. Os resultados do Controle de Qualidade foram obtidos em um
microscópio equipado Nikon® por epiiluminação com uma lâmpada
ARC de mercúrio de 50W HBO, sistema de filtro B para FITC e uma
objetiva seca de 40X (NA 0,65). Diferenças na reatividade de ponto final
e intensidade de fluorescência pode ser afetado pelo tipo e condição de
fluorescência do equipamento usado (ver especificações do
Microscópio).
CARACTERÍSTICAS DO DESEMPENHO
O teste de Sarampo de IF foi avaliado pela comparação com dois testes, FC
e HAI, correntemente usado para a detecção dos anticorpos do virus de
sarampo.
SARAMPO IFA
10
As amostras foram colhidas aleatoriamente de uma população de crianças de
idade escolar. Estes soros foram colhidos pelo Bureau of Laboratories para
estudar os níveis de anticorpo para o vírus de sarampo em uma população
previamente imunizada.
As amostras colhidas foram testadas no procedimento de IF. Os resultados
obtidos foram expressos como “títulos de ponto final” nas amostras reativas,
por exemplo, a mais alta diluição que reativamente foi discernível (1+ de
reatividade). Os resultados obtidos foram subseqüentemente comparados
com os resultados obtidos nas alíquotas das amostras testadas pelos
métodos de FC e HAI do Bureau of Laboratories. Os resultados obtidos
estão nas Tabela 1 e 2.
Tabela 1: Resultados dos ensaios de IF e HAI para o anticorpo do vírus
de sarampo
No. da Amostra
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
Títulos de Ponto Final
IF
128
256
32
128
128
128
128
64
64
128
64
256
64
128
64
256
32
128
256
128
128
256
SARAMPO IFA
11
HAI
80
160
10
40
80
80
80
20
20
40
40
160
10
40
20
160
10
80
160
40
80
80
23
24
25
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42
43
44
45
46
47
48
49
50
8
256
64
<8
256
512
64
256
32
32
256
256
32
256
128
128
128
256
128
128
128
128
128
64
128
64
<8
256
10
160
40
10
80
320
160
160
20
40
160
160
10
160
20
10
80
160
40
80
80
40
40
40
40
20
10
120
Tabela 2: Resultados dos ensaios de IF e FC para o anticorpo do vírus
de sarampo
No. da Amostra
1
SARAMPO IFA
Títulos de Ponto Final
IF
FC
128
16
12
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
31
32
33
34
35
36
37
38
39
SARAMPO IFA
32
128
128
256
8
64
256
32
8
128
64
64
256
64
16
128
64
128
64
512
128
512
256
256
32
32
8
512
256
32
32
256
<8
256
256
512
QNS
128
<8
16
16
32
<8
8
32
8
<8
8
16
8
32
8
<8
8
16
8
16
32
16
32
16
16
<8
8
<8
32
16
8
<8
16
<8
32
32
32
QNS
16
13
40
41
42
43
44
45
46
47
48
49
50
256
128
128
512
128
32
<8
64
QNS
32
256
32
32
16
32
16
8
<8
16
QNS
8
16
REFERÊNCIAS BIBLIOGRÁFICAS
1. Frank, JA et al. 1985 Major Impediments to Measles Elimination: The
Modern Epidemiology of an Ancient Disease. AJDC (American Journal
of Disease of Children), 139:881-888.
2. Measles Surveillance Report No. ll. 1977-1981. Atlanta.
3. Kempe, CH, and VA Fulginite. 1965. The Pathogenesis of Measles Virus
Infection. Arch Gesamte Virusforsch, 16:103-l28.
4. Panum, P. 1989. Observations Made During the Epidemic of Measles on
the Faroe Islands in the Year 1846. Med. Classics, 3:829-886.
5. Enders, JR, and TC Peebles. 1954. Propagation in Tissue Cultures of
Cytopathogenic Agents from Patients with Measles. Proc. Soc. Exp.
Biol. Med., 86:277-286. 6. Connolly, JH et al. 1967. Measles-virus
Antibody and Antigen in Subacute Sclerosing Panencephalitis. Lancet,
1:542- 546.
6. Tannenbaum, M et al. Electron Microscopic Virus-like Material in
Systematic Lupus Erythematosus: With Prelimi-nary lmmunologic
Observations on Presence of Measles Antigen. J. Urol., 105:615-619.
7. Adams, JM, and DT lmagawa. 1962. Measles Antibodies in Multiple
Sclerosis. Proc Exp Biol. Med., ll1:562-566.
8. Weller, TH and AH Coons. 1954. Fluorescent antibody studies with
agent of varicella and herpes zoster propagated in vitro. Proc. Soc. Exp.
Biol. Med., 86:789-794.
9. NCCLS Doc M29-P. 1988. Protection of laboratory workers from
infectious disease transmitted by blood and tissue, Proposed guideline.
National Committee for Clinical Laboratory Standards. Villanova, PA.
SARAMPO IFA
14
10. CDC/NIH Manual. 1988. Biosafety in Microbiological and Biomedical
Laboratories, 2nd Ed. pp 12-16.
11. NCCLS Doc Hi 8-T. 1984. Procedures for the Handling and Processing
of Blood Specimens. National Committee for Clinical Laboratory
Standards. Villanova, PA.
12. NCCLS Doc H3-A2. 1984. Procedures for the Collection of Diagnostic
Blood Specimens by Venipuncture, 2nd Edition: Approved Standard.
National Committee for Clinical Laboratory Standards. Villanova, PA.
13. Holborow, EJ, DM Weir and GD Johnson. 1957. A Serum factor in
lupus erythematosus with affinity for tissue nuclei. Br. Med. J., I1:732734.
14. Berg PA, I Roitt, D Doniach, and HM Cooper. 1969. Mitochondrial
antibodies in primary biliary cirrhosis. IV. Significance of membrane
structure for the complement fixing antigen. lmmunol., 17:281-293.
RESUMO DO KIT DE SARAMPO(MEASLES) IgG HEMAGEN
VIRGO
IMPORTANTE: É recomendado que se esteja familiarizado com o
procedimento detalhado nas instruções de uso antes de usar este
resumo.
Cobrir os poços com as diluições de 1:8 das amostras e controles. Para a
determinação quantitativa, preparar diluições seriadas de duas etapas.
Incube as lâminas em câmara úmida a 37 +/- 2oC por 30 minutos.
Enxaguar as lâminas rapidamente com PBS. Lavar por 15 minutos, trocando
o tampão 1 vez. Enxugar as lâminas.
Cobrir cada poço com o conjugado FITC.
Incubar as lâminas em uma câmara úmida à 37 +/- 2oC por 30 minutos.
SARAMPO IFA
15
Repetir o passo de lavagem descrito acima.
Colocar uma pequena gota do Glicerol Tamponado em cada poço e cobrir
com uma lamínula.
Ler as lâminas imediatamente de 200-500X de aumento em um microscópio
de fluorescência
TERMO DE GARANTIA
Este kit como um todo tem garantia de troca, desde que esteja dentro do
prazo de validade e seja comprovado pela Assessoria Científica da
HEMAGEN DIAGNÓSTICOS de que não houve falhas técnicas na
execução, manuseio do teste e na conservação do produto.
IMPORTADO E DISTRIBUÍDO POR:
HEMAGEN DIAGNÓSTICOS COM. IMP. EXP. LTDA.
Rua Doutor Diogo de Faria, 109 – Vila Clementino
São Paulo - SP - CEP 04037-000
Fone: (011) 3819-5222 Fax: (011)3816-7623
CGC: 64.002.686/0001-32
Resp. Técnico: Dhália Gutemberg CRF 07.183 - SP
FABRICADO POR:
HEMAGEN DIAGNOSTICS, INC.
VIRGO® PRODUCTS DIVISION
Columbia, Maryland 21045 - USA
Fone: (800) 436-2436 ou 617-890-3748.
SERVIÇO DE ATENDIMENTO AO CLIENTE
SARAMPO IFA
16
Quaisquer dúvidas técnicas, no manuseio deste kit ou no seu procedimento
entrar em contato com a ASSESSORIA CIENTÍFICA DA HEMAGEN
DIAGNÓSTICOS, que estará sempre à disposição para auxiliar quando
ocorrerem dificuldades na utilização de seus produtos. Contate a
HEMAGEN através do endereço do importador acima :
DATA DA REVISÃO DAS INSTRUÇÕES DE USO
Documento Revisado em: - Março de 2014.
SARAMPO IFA
17