Sou na areia um pequeníssimo grão
Sou da exaurível vida
O derradeiro grão de solidão
(autor desconhecido)
Poucos meses passados
da Revolução do 25 de
Abril, pelas oito horas
da manhã do dia 23
de Dezembro de 1974,
nasci, no lugar da Sr.ª
da Luz na freguesia de
Arcozelo, a terceira de
quatro
filhos
Fernandes
de
da
José
Costa
Brito e de Maria de
Lurdes Veiga da Silva.
(…) A mim coube-me o nome de Sandra Sofia Silva
da Costa Brito.
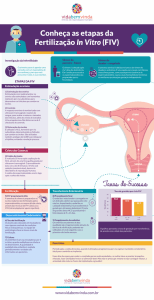
Fecundação In Vitro (FIV)
Consiste na união do óvulo com o espermatozóide em
laboratório in vitro, com o objectivo de obter um número
de embriões para transferir para o útero materno.
O Pai da Fertilização in vitro
Robert G. Edwards nasceu em 1925 em Manchester, no Reino Unido, e está
ligado à Universidade de Cambridge, no mesmo país. Depois do serviço militar
na segunda Guerra Mundial, estudou Biologia na Universidade de Gales e na
Universidade de Edimburgo, onde completou em 1955 o seu doutoramento com
uma tese sobre o desenvolvimento embrionário em ratinhos. Em 1958 integrou o
“National Institute for Medical Research”, em Londres, onde se dedicou à
fertilização em humanos. A partir de 1963 passou a trabalhar em Cambridge,
primeiro na universidade e depois na clínica Bourn Hall, o primeiro centro
mundial de bebés-proveta, que fundou com Patrick Steptoe, o ginecologista que
foi sempre o seu braço direito nestas investigações.
“A sua descoberta permitiu tratar a infertilidade, uma condição médica que afecta
uma larga proporção da humanidade, incluindo mais de dez por cento dos casais
de todo o mundo”, explicou a academia sueca, em comunicado. Foi ainda na
década de 1950 que Edwards percebeu que a fertilização in vitro poderia ser o
caminho para o tratamento da infertilidade, trabalhando, desde aí, em
experiências com óvulos e culturas de células. Um empenho que veio a colher
frutos a 25 de Julho de 1978, dia em que nasceu o primeiro “bebé-proveta”. Nos
anos seguintes, Edwards e os seus colaboradores refinaram as técnicas
necessárias e partilharam-nas com médicos do mundo inteiro.
De acordo com dados avançados pela Assembleia Nobel, até ao momento, o
investigador já foi pai de quatro milhões de bebés, muitos dos quais já são
adultos e até pais. “Uma nova era da Medicina emergiu, com Robert Edwards a
liderar o processo desde as descobertas mais fundamentais às mais correntes (...)
O seu contributo representa um marco no desenvolvimento da Medicina
moderna”. Para a descoberta de Edwards em muito contribuíram outros cientistas
que concluíram com sucesso as experiências com maturação de ovócitos de
mamíferos, nomeadamente ratinhos e coelhos, em tubos de ensaio.
Edwards percebeu, contudo, que nos humanos os ciclos são muito diferentes,
comparativamente com animais como os coelhos, conseguindo clarificar como se
processa a maturação, que hormonas a regulam e em que condição é possível
haver fertilização. Conseguiu fertilizar um óvulo in vitro, pela primeira vez, em
1969, mas este não se subdividiu. Partiu para uma nova fase: recolher óvulos já
amadurecidos nos ovários através de uma técnica chamada laparoscopia e que
gerou grande polémica na época, a par com os diversos debates éticos e
religiosos que lançou sobre recriar vida em laboratório.
25 de Julho de 1978 foi um sábado muito especial para o casal Leslie e John
Brown, de Bristol, no Sul de Inglaterra. Mas também foi um sábado especial para
muitos casais em todo o mundo, que estavam, até aí, impossibilitados de ter
filhos naturalmente. Leslie preparava-se para ser a mãe do primeiro bebé-proveta
de sempre, uma menina, chamada Louise Brown.
“Comecei a fazer estudos com tecido ovárico humano recolhido em cirurgias.
Mas tinha de conseguir fertilizar os ovócitos no laboratório”, contou Edwards,
em 2003, aquando da celebração dos 25 anos da sua invenção. As primeiras
experiências de Pincus e Saunders, com coelhos, tinham mostrado que bastavam
12 horas para o amadurecimento e fertilização dos ovócitos no tubo de ensaio.
Ter acreditado que esses resultados poderiam aplicar-se a células humanas
custou-lhe vários desgostos. Até que chegou o dia: "Decidi então esperar 25
horas por três ovócitos que me restavam. De repente, foi a alegria. Agora havia
esperança para a fertilização in vitro".
O primeiro bebé
Louise Brown da Inglaterra foi o
primeiro bebé nascido via FIV, em
1978. No mesmo ano, na Índia, outro
bebé nasceu pelo mesmo processo.
Logo, começaram a chamar a essas
crianças de "bebés proveta". Marcou
o início de uma era de extraordinário
progresso
tratamento
no
entendimento
dos
e
problemas
relacionados à fertilidade humana.
Em 1981, nasceu o primeiro bebé de
tubo de ensaio e o número continuou
a aumentar a cada ano. De acordo
com os Centros de Controle de Doenças, mais de 48 mil nasceram em 2003 por
meio de TRA (99% via FIV).
Originalmente a fertilização in vitro seguida de transferência de embriões (FIVTE) foi proposta para o tratamento dos casos de infertilidade tubária, ou seja,
para aquelas pacientes em que as trompas estavam ausentes ou irreparavelmente
obstruídas. O aprimoramento das técnicas de FIV ampliou as suas indicações e
permitiu o seu uso para o tratamento da infertilidade de outras etiologias.
A fertilização in vitro, muitas vezes denominada "bebé proveta", deve-se ao facto
da fecundação do óvulo pelo espermatozóide ocorrer fora do corpo, em
laboratório, ou seja, in vitro. Os embriões resultantes da fertilização in vitro são
transferidos para o útero aproximadamente 72 horas após a captação de óvulos.
Esta técnica, desenvolvida num laboratório de última geração, é utilizada quando
os tratamentos prévios fracassaram, como a Inseminação Artificial. É a solução
para problemas de esterilidade derivados do factor masculino e do factor tubário trompas de Falópio obstruídas - entre outros.
A inseminação dos óvulos pode ser realizada mediante a técnica de FIV
convencional ou da Injecção Intracitoplasmática de Espermatozóides (ICSI), esta
última indicada em casos de factor de infertilidade masculino grave, nos
fracassos de fecundação anteriores com FIV, nos fracassos nos tratamentos
prévios de Inseminação Artificial, ou em situações nas quais dispomos de um
número limitado de óvulos.
O caminho da fertilidade
é longo e difícil,
repleto de obstáculos, mas também de muita esperança. É
um caminho que é percorrido por cada vez mais casais,
estimando-se actualmente que entre 15 a 20 por cento da
população sofra desta doença.
Muitos, sofrem, provavelmente em silêncio, a crer nos dados que apontam para
que em Portugal se façam 250 ciclos de tratamento de Procriação Medicamente
Assistida (PMA) por milhões de habitantes, uma média quatro vezes e meia
inferior à da União Europeia.
Recentemente foi anunciada a compartição a 100 por cento dos chamados
tratamentos de primeira linha (inseminação artificial e estimulação ovárica) e do
primeiro ciclo de tratamentos de segunda linha (fertilização in vitro e
microinjecção intracitoplasmática de espermatozóide) realizados em clínicas
privadas, tendo como objectivo beneficiar muitos dos casais inférteis.
Infertilidade
São casais com dificuldade em
conceber sendo que a infertilidade se define, segundo a
OMS, quando a gravidez não é alcançada ao fim de um
ano consecutivo de relações sexuais sem contracepção.
São muitos os factores que influenciam a
fertilidade.
Na mulher, tudo começa a nível do cérebro, com a glândula pituitária a enviar
todos os meses um sinal para que os ovários preparem um oócito para a
ovulação. Essa preparação dá-se por influência de duas hormonas, que estimulam
os ovários. E a fertilização acontece se entretanto um espermatozóide alcançar o
oócito. Se esta união se concretiza, o ovo movimenta-se em direcção ao útero,
onde se desenvolve a gravidez.
No que ao homem diz respeito, muito pode acontecer no processo de fertilização,
mediante o qual um espermatozóide alcança um ovo e fecunda. Antes de mais é
preciso que haja espermatozóides em quantidade suficiente, que possuam a forma
e a dimensão adequadas e que se movimentem na direcção certa. E é preciso que
haja sémen suficiente para transportar os espermatozóides.
A fertilidade não é um dado adquirido, nela podendo interferir tanto factores
femininos como masculinos, numa relação equilibrada. Casos há em que as
causas têm dupla origem e outros em que não são detectadas razões concretas.
Pelo lado feminino
Pelo lado masculino
Um (longo) caminho a dois
Quando o desejo de constituir família
esbarra na incapacidade de conceber,
emergem naturalmente múltiplos e
potentes sentimentos. Mas é importante
que, nesse tumulto de emoções, o casal
encontre o caminho que o conduza à
ajuda médica.
Uma vez perante um especialista,
ambos os membros do casal são sujeitos
a uma série de exames de modo a identificar a causa da infertilidade. Existem
testes específicos para determinar a infertilidade masculina e a feminina, ainda
que, com frequência, haja uma combinação de factores a influenciar a dificuldade
em conceber e não uma causa única. Além de que, nalguns casos, a infertilidade
fica por explicar.
O tratamento depende da causa, da duração da infertilidade e de muitos outros
factores, sendo que há causas que não são passíveis de correcção. Estão, no
entanto, disponíveis vários métodos que permitem a uma mulher engravidar e
que passam por restaurar a fertilidade ou por uma das diversas técnicas de
reprodução medicamente assistida. Restaurar a fertilidade implica na maior parte
dos factores uma maior frequência das relações sexuais para, assim, aumentar as
probabilidades de concepção: é que os espermatozóides podem sobreviver no
corpo da mulher por 72 horas e um óvulo pode ser fertilizado nas 24 horas
seguintes à ovulação, tratando-se de criar o máximo de oportunidades para que
esse encontro seja bem sucedido.
Para
as
desordens
mulheres
com
ovulatórias,
a
primeira linha de tratamento
implica o uso de medicamentos
específicos
ovulação.
para
São,
regular
no
a
entanto,
fármacos a que está associado o
risco de nascimentos múltiplos.
Quanto
à
infertilidade
por
obstrução das trompas pode ser
ultrapassada com recurso à cirurgia, sendo a laparoscopia uma das técnicas para
reparar os bloqueios e lesões. Mais difícil a tratar é a infertilidade devida a
endometriose: a terapia ovulatória é uma das alternativas, a par da fertilização in
vitro, mediante a qual o óvulo e o espermatozóide são unidos em laboratório e só
depois transferidos para o útero. A fertilização in vitro é, uma das técnicas
pioneiras da chamada reprodução medicamente assistida. Mas há outras como a
injecção citoplasmática, que consiste numa técnica microscópica da implantação
directa de um único espermatozóide num óvulo.
Estas são as técnicas que resultam melhor em mulheres com um útero saudável,
que respondam bem aos medicamentos da fertilidade e que ovulem naturalmente.
Porém, há complicações possíveis como é o caso de gravidez múltipla ou
hiperestimulação dos ovários. Quanto às causas da infertilidade masculina, a sua
identificação e consequente tratamento envolve um conjunto de testes que visam,
antes de mais, avaliar a condição física, para despiste de doenças que tem ou já
teve, medicamentos que toma habitualmente e hábitos sexuais. Depois, é feita
uma análise ao sémen, de modo a aferir da quantidade e qualidade dos
espermatozóides. Permite ainda detectar eventuais infecções. Uma análise ao
sangue pode também ser necessária, com o objectivo de medir os níveis de
testosterona.
2 células
4 células
8 células
Mórula
Blastocisto
Porém, há intervenções mais especificas, dirigidas à quantidade e/ou qualidade
do esperma. A alternativa pode ainda residir em medicamentos utilizados para
aumentar a quantidade do esperma, ainda que não influenciem a sua quantidade
ou mobilidade. Nos homens com esperma normal, mas escasso, os índices de
gravidez melhoram com a inseminação artificial, em que é aproveitada a primeira
porção do sémen ejaculado, mais rica em espermatozóides. A fertilização in vitro
e a transferência de gâmetas também são eficazes em determinados tipos de
infertilidade masculina.
Em Portugal, são cada vez mais os bebés que a Ciência traz ao mundo. Muitos
passos se deram desde que, em 1986, nasceu o primeiro filho da reprodução
medicamente assistida no nosso país, é hoje jogador profissional do Sporting
Clube
de
Portugal,
avançado,
Carlos
Saleiro.
O procedimento é composto por várias fases
Avaliação personalizada
É feito um diagnóstico personalizado para uma melhor escolha do tratamento
para cada problema de infertilidade. Para tal, os pacientes são examinados
relativamente aos seus antecedentes familiares, ao índice de massa corporal, à
reserva ovarina, etc.
(Estimulação dos ovários)
Estimulação dos ovários
Este procedimento é necessário
para aumentar as possibilidades
de êxito, já que de forma natural,
a mulher só produz um folículo e
portanto, um óvulo – por cada
ciclo menstrual. Este tratamento
consiste na estimulação do ovário
para que este produza mais
óvulos, que assim, de forma
natural, se possa obter um maior número de embriões. O tratamento demora entre
12 e 20 dias, em função do protocolo utilizado e da velocidade de resposta de
cada paciente. Durante o mesmo serão realizadas várias eco grafias - umas 3 ou 4
– e se determinará o estradiol no sangue, para comprovar que o crescimento e a
evolução dos folículos encontram-se dentro da normalidade.
Punção folicular
Quando é evidenciado através de eco grafia que os folículos alcançaram a
dimensão adequada é considerado que encontram-se disponíveis um número
adequado de óvulos, programando-se a punção folicular 36 horas depois da
administração de uma injecção de hCG, que induz a maturação ovarina final. A
punção é realizada em internamento e sob anestesia, com o objectivo de que a
paciente não sinta nenhum tipo de incómodo durante o procedimento, cuja
duração é de aproximadamente 10-15 minutos.
Inseminação dos óvulos
Uma vez na posse dos óvulos depois da realização da punção folicular, e dos
espermatozóides, que normalmente são obtidos a partir da recolha de uma
amostra de esperma por parte do elemento masculino, procede-se à inseminação
dos óvulos. Este processo pode ser realizado através da FIV convencional, que
consiste na colocação de um óvulo na placa de cultivo rodeado por
espermatozóides, ou através da ICSI, que consiste na introdução de um
espermatozóide vivo dentro do ovário, mediante a punção do mesmo, com a
ajuda de uma pipeta.
Cultivo embrionário em laboratório
Os embriões resultantes são observados
no laboratório dia após dia, e são
classificados de acordo com a sua
morfologia e capacidade de divisão.
Alguns
embriões
podem
chegar
a
bloquear o seu desenvolvimento, e serão
excluídos
por
serem
considerados
inviáveis.
Transferência embrionária
Consiste
na
introdução
dos
melhores
embriões da corte no interior do útero
materno, com a ajuda de uma cânula
especialmente concebida para o efeito. O
procedimento é realizado em internamento,
apesar de neste caso não ser necessário
administrar uma anestesia, já que é um
processo rápido e indolor.
Vitrificação dos restantes embriões
Uma vez realizada a transferência embrionária, é
realizada a vitrificação dos restantes embriões de boa
qualidade, com o objectivo de poderem ser transferidos
num ciclo posterior, sem necessidade de estimulação
dos ovários. A nova técnica de congelação rápida ou de
vitrificação realizada na IVI, assegura resultados
esperançosos, já que os embriões não são afectados pela mesma, e que a taxa de
gestação não diminui – conforme ocorria com a congelação lenta ou
convencional – relativamente à taxa obtida com os embriões em fresco.
Teste de gravidez
Aproximadamente
2
semanas
após
a
transferência embrionária, a paciente deve
realizar um teste sanguíneo de beta-hCG,
para confirmar se conseguiu engravidar e
para quantificar a hormona de gravidez no
sangue. Se a prova for positiva, deve
realizar uma eco grafia vaginal uma semana
mais tarde, com o objectivo de visualizar o
saco gestacional.
Riscos
Durante a retirada do óvulo, o risco depende
do processo. A aspiração trans-vaginal por eco
grafia tem um risco pequeno de sangramento e
infecção e, às vezes, prejudica as estruturas
que estão ao redor, como o intestino e a
bexiga. Os riscos associados à laparoscopia
são
dificuldade
de
respirar,
infecção
pulmonar, lesões nervosas e reacções alérgicas
a medicações (o que pode acontecer com
qualquer cirurgia em que é necessária uma
anestesia.
Quando mais de um embrião é transferido, existe o risco de gravidez múltipla.
Um casal infértil pode ouvir isso como uma boa notícia, mas a presença de mais
de um embrião aumenta o risco aos embriões e à mãe. O risco mais comum é o
parto prematuro. Os bebés podem desenvolver complicações após o nascimento
ou nascer cedo demais para conseguir sobreviver. Cerca de 5% das gravidezes
por Fertilização in vitro são atópicas, o que significa que o óvulo fertilizado se
desenvolveu fora do útero, geralmente nas trompas de Falópio. Essa
complicação, infelizmente, requer a eliminação imediata do feto.
Técnica promete revolucionar a fertilização in vitro
Investigadores britânicos estão a desenvolver uma nova técnica de fertilização in
vitro, ainda em fase de testes, que poderá triplicar as hipóteses de uma mulher
conseguir engravidar após inseminação artificial, diminuindo “drasticamente” o
número de abortos espontâneos no início da gestação.
Actualmente, aos 40 anos, uma mulher têm dez por cento de probabilidade de
engravidar a cada ciclo de fertilização in vitro. Através desta técnica em
desenvolvimento, as hipóteses ascenderiam aos 30 por cento, enquanto em
mulheres de 30 anos passariam de 30 a 40 por cento para entre 70 e 80 por cento.
Esta técnica permite aos médicos testarem o embrião por alterações nos
cromossomas, responsáveis por 70 por cento dos abortos espontâneos nos
primeiros três meses de gestação. Assim, o embrião mais “saudável” é escolhido
antes da implantação, diminuindo os riscos de complicações.
Até ao momento, o novo procedimento foi testado em três mulheres entre os 35 e
os 40 anos, que deverão dar à luz no final de Dezembro.
Simon Fishel, coordenador do projecto, acredita que esta técnica representa “um
incrível avanço que, em breve, fará uma grande diferença na vida de milhares
de mulheres”.
No processo de fertilização in vitro, o embrião chega a um estado em que é
denominado por blastocisto, no quinto dia de existência, em que costuma ser
implantado no útero. Nesta fase, o embrião é constituído por duas partes. Uma
delas é formada pelas células que vão dar origem ao bebé e a outra são as células
que se vão tornar em placenta. Agora, com a nova técnica, é possível fazer uma
“pequena biopsia” das células da placenta sem se afectar as do feto.
Nesta análise, diz Fishel, é possível ver todos os cromossomas antes da
transferência do embrião para o útero, pelo que o seu implante torna-se menos
arriscado e mais eficiente. “Acredito que haverá uma revolução na fertilização
in vitro nos próximos meses”.
Trabalho realizado por: Sandra Sofia Brito