QUÍMICA QUÂNTICA E
ESPECTROSCOPIA
Igor Khmelinskii, FCT, DQBF
Modulo IV, ano lectivo 2007-2008
Unidades
a0
2
Unidades derivadas
3
Prefixos SI
4
Unidades de uso comum
5
T1
Dinâmica de sistemas
microscópicos
Cap. 9
Peter Atkins, Julio de Paula
Physical Chemistry for Life Sciences
Recursos (Living Graphs):
http://www.oup.com/uk/orc/bin/9780199280957/01stud
ent/graphs/ch09/
Princípios de teoria quântica
Física clássica
1. Uma partícula desloca-se pela trajectória,
tendo um valor definido da posição e do
momento linear em cada instante
2. Qualquer tipo de movimento pode ser
excitado até um estado de uma energia
arbitrária
3. As ondas e as partículas são conceitos
distintos
7
Dualidade onda-partícula
•
•
•
•
Radiações: c = ln; c = 3 108 m/s
E = nhn; n = 0, 1, 2, …
Fotões
Efeito fotoeléctrico
8
Dualidade onda-partícula
• Relação de de Broglie
h
l
p
p (2mEc ) ;
Exemplo: c.d.o. dos
electrões num
microscópio
DU=15,0 kV
Ec eV ;
p (2meV ) ;
e 1,602 10 19 C;
m 9,1110 31 kg;
h 6,626 10 34 Js;
l 1,00 10 11 m
9
Equação de Schrödinger
• A função de onde para
uma partícula em
movimento livre é sen(x)
• A função de onda de uma
partícula que oscila a
x2
volta de um ponto, é e
• A função de onda para
um electrão no átomo de
hidrogénio é e r
2 d 2
V E
2
2m dx
h
1,054 10 34 Js
2
10
Equação de Schrödinger
• Restrições: condições na fronteira
• Apenas certas soluções são aceitáveis
apenas certos valores de energia são
aceitáveis
• Interpretação da f.d.o. (Max Born): A
probabilidade de encontrar a partícula numa
região do espaço é dada por
δV
2
11
Exemplo
A f.d.o. do electrão do átomo H no
estado fundamental é
proporcional à
Calcular as probabilidades
relativas de encontrar o
electrão num pequeno volume,
localizado: a) junto do núcleo;
b) a distância a0 do núcleo
a) r = 0; Prob. 1,0;
b) r = a0; Prob. e-2 = 0,14
e
r / a0
Prob. 2δV
12
Princípio de incerteza
• Uma onda com um c.d.o. constante, f.d.o.
= sin (2x/l), corresponde a uma
partícula com momento linear p = h / l
• Uma f.d.o. de uma partícula localizada
pode ser obtida por sobreposição de
várias f.d.o. sinusoidais.
• Relação quantitativa: DpDx ≥ / 2
Dp p
2
p
2 1/ 2
13
Princípio de incerteza
• Variáveis complementares: x e px, y e py,
etc.
Exemplo: Velocidades são conhecidos até
1,0 mm s-1; calcular incertezas de posição:
a) electrão, m = 9,109 10-31 kg (58 m);
b) E. coli, m = 1 pg (5,3 10-14 m)
14
Aplicações de teoria quântica
• Partícula em caixa
Condições na fronteira:
f.d.o. = 0 em 0 e L
l 2L / n
nx
n N sin
, n 1,2,...
L
N (2 / L)1/ 2
h
nh
p
, n 1,2,...; E p 2 / 2m
l 2L
n2h2
En
, n 1,2,...
2
8mL
15
Partícula em caixa
16
Partícula em caixa
17
Partícula em caixa
h2
• Energia do ponto zero (n = 1): E1
8mL2
• Quanto maior o sistema, menos importantes são
os efeitos de quantização
• Maior a massa da partícula, menos importantes
são os efeitos de quantização
(n 1) h
nh
DE En 1 En
2
2
8mL
8mL
h2
(2n 1)
, n 1,2,...
2
8mL
2
2
2
2
18
Partícula em caixa
19
Estrutura electrónica de b-caroteno
• 10 ligações simples e 11 duplas, conjugação;
ligação C-C: 140 pm;
• Partícula em caixa: L = 21140 pm = 2,9410-10m
• Um electrão por cada C anda livremente; são
ocupados todos os níveis até n=11
20
Estrutura electrónica de b-caroteno
• Transição electrónica, de menor energia,
com absorção/emissão da luz: E11E12
• DE = E12 - E11 = 1,60 10-19 J
• DE = hn
• n = 2,41 1014 s-1
• Experimental: n = 6,03 1014 s-1
(l = 497 nm)
21
T2
Tunelamento
• Penetração em zonas
classicamente
proibidas
• Barreira alta e larga
T 16 (1 )e 2L
2m(V E )
1/ 2
E / V ; L largura
22
Tunelamento
23
Microscópio com varrimento
da sonda
• A corrente varia
exponencialmente
com a distância
24
Átomos de Cs sobre uma
superfície de Ga
25
ADN por STM
26
AFM – microscopia de força
atómica
Suporte
27
AFM – plasmidas de ADN
28
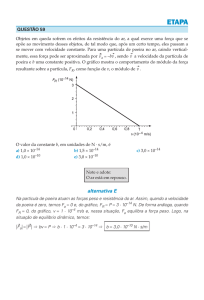
Forças medidas por MFA
Força entre 2 electrões
que distam 2 nm?
q1q2
V
40 r
0 8,854 10 12 C 2 J 1m 1
e 1,602 10 19 C
F dV / dr
F
e2
40 r
2
5,8 10
11
N
29
Rotação
• Momento angular J:
J = pr (p = mv)
30
Partícula no anel
• Energia:
• Momento de inércia
p2
J z2
E
; E
2m
2mr 2
I mr 2
2
z
J
E
2I
• (de Broglie)
J z pr
hr
l
31
Partícula no anel
• Condição periódica
na fronteira:
2r
l
n
n 0,1,...
2
nh
2
2 2
(hr / l )
n
2
En
2I
2I
2I
n 0,1,2,...
32
Partícula no anel
• Expressão final
2
ml 2
Eml
2I
ml 0, 1, 2, ...
• Estados degenerados para |ml| > 0
• Momento angular quantizado:
hr
hr
J z pr
ml ml 0, 1, 2, ...
l 2r / ml
33
Partícula no anel
34
Partícula no anel
• Funções de onda
35
Estrutura electrónica de
fenilalanina
36
Estrutura electrónica de
fenilalanina: partícula no anel
• Anel, raio 140 pm
• 6 electrões no sistema conjugado
• ml = 0, +1, -1 são preenchidos com 2 electrões
cada
DE E 2 E1 3,1110 19 J
DE
n
4,69 1014 Hz
h
15
Exper. : n 1,15 10 Hz; l 260 nm
37
Partícula na esfera
• Duas condições
cíclicas 2 números
quânticos
38
Partícula na esfera
2
J2
E l (l 1)
l 0, 1, 2, ...; E
2I
2I
1/ 2
J l (l 1) l 0, 1, 2, ...
• l – número quântico do momento angular orbital
• ml – número quântico magnético
J z ml
ml l, l 1, ..., l 1, l
39
Partícula na esfera
40
Vibrações: oscilador harmónico
• F = - kx – lei de Hooke
• V(x) = kx2/2 – energia
potencial
41
Vibrações: oscilador harmónico
E ( 1 / 2)hn
0, 1, 2, ...
1/ 2
1 k
n
2 m
número quântico vibracion al
42
Vibração na ligação peptídica N-H
• É o átomo H que se
desloca (aproximação)
• N-H: k = 300 N m-1
• 1H: mH=1,6710-27 kg
• n = 6,75 1013 Hz
(Infravermelhos)
• E = hn = 4,47 10-20 J
43
Vibrações: oscilador harmónico
44
Oscilador harmónico
45
T3
Energias permitidas de átomos
tipo hidrogénio
• Núcleo: carga +Ze;
electrão: -e
• Energia potencial:
Ze 2
V
40 r
Z2
En A 2
n
me 4
A
32 2 02 2
me mN
m
me mN
n 1, 2, ...
46
Energias permitidas de átomos tipo
hidrogénio
• n – número quântico
principal
• m – massa efectiva
E1 AZ 2
IH
me e 4
32 2 02 2
2,179 1018 J 13,59 eV
• Energia de ionização I
• E.I. do He?
47
Orbitais atómicas
• 3 condições na fronteira:
– As f.d.o. não podem ser infinitas
– Devem repetir-se dando uma volta equatorial
– Devem repetir-se dando uma volta polar
• 3 números quânticos
– n = 1, 2, … – principal
– l = 0, 1, 2, …, n-1 – momento angular orbital
– ml = l, l - 1, l - 2, …, -l – magnético
• ml = +1, ml = - 2 etc.
48
Orbitais atómicas
• n 1 2
K L
• l
0
s
1
p
3 4 …
M N
2
d
3 …
f
• Número de orbitais:
s p d f
1 3 5 7
49
Forma das orbitais atómicas
50
Forma das orbitais atómicas
• Factorização
n ,l ,m Yl ,m ( , ) Rn ,l (r )
l
l
• F.d.o. radial: R(r)
• F.d.o. angular Y(,)
51
Probabilidade radial
• Probabilidade de
encontrar o electrão
entre r e r +dr :
P(r ) 4r
2
2
P(r) - Função de
distribuição radial
• Superfície de fronteira
52
F.d.o. radiais
53
Superfícies de fronteira
54
Superfícies de fronteira
55
Estrutura de átomos
polielectrónicos
• Aproximação orbital:
(1) (2)...
He :
8 2 ( r1 r2 ) / a0
(1) (2) 3 e
a0
• É uma aproximação, pois despreza:
– Os electrões repelem-se
– A presença dos outros electrões altera a carga
nuclear efectiva
56
Spin electrónico
• Número quântico de
spin, s
Valor: s = ½
• Dois estados:
ms = + ½ e ms = ½
aeb
57
Spin electrónico
• Princípio de exclusão de Pauli:
Um orbital pode ser ocupado pelo máximo
de 2 electrões, sendo 2, têm os seus spins
emparelhados.
58
Penetração e blindagem
• Definem forma geral da
tabela periódica e
propriedades físicas e
químicas dos elementos
• Um electrão a distância r
fica afectado pelos outros
que são dentro da esfera
de raio r : carga do
núcleo aparente Zeffe;
blindagem da carga
nuclear.
59
Penetração e blindagem
• Um electrão s tem
uma penetração
maior que um
electrão p, etc.
• Energias: s < p < d < f
60
Princípio de Aufbau
1.
2.
3.
4.
1s 2s 2p 3s 3p 4s 3d 4p 5s
4d 5p 6s …
Cada orbital pode acomodar
até 2 electrões.
Electrões ocupam orbitais
diferentes da subcamada
antes de ocupar duplamente
qualquer uma delas.
No estado fundamental, o
átomo assume uma
configuração com um
número maior de electrões
desemparelhados.
61
Casos especiais
• Repulsão entre os
electrões em 3d é
maior que em 4s
Sc: [Ar]3d14s2 mas não
[Ar]3d3 ou [Ar]3d24s1
Geral: [Ar]3dn4s2
Excepções:
Cr: [Ar]3d54s1
Cu: [Ar]3d104s1
62
Configurações de catiões e aniões
• Catiões: ordem de remoção de electrões:
– p de valência
– s de valência
– d de valência
• Aniões: continua a preencher até um gas
nobre
63
Raios atómicos
Grupos principais
64
Raios atómicos
Contracção lantanídea
65
Raios iónicos
66
Papel do Zn2+ em bioquímica
• Ácido Lewis: Espécie com défice de
electrões (catião metálico)
• Base de Lewis: Espécie com par isolado
(H2O)
• Zn2+: grande valor de Zeff/rion
• Anidrase carbónica (pH do sangue):
CO2 + H2O HCO3- + H+
67
Papel do Zn2+ em bioquímica
68
Energia de ionização
• Definição
E(g) E+(g) + e-(g)
E+(g) E2+(g) + e-(g)
etc.
I1 = E(E+) - E(E)
I2 = E(E2+) - E(E+)
69
Energia de ionização
70
Energia de ionização, I1
71
Afinidade electrónica
• Definição
E(g) + e-(g) E-(g)
Eea = E(E) - E(E-)
72
Afinidade electrónica
73