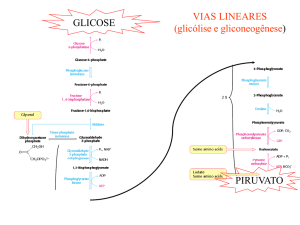
O Ciclo do Ácido Cítrico
(Ciclo dos ácidos tricarboxílicos ou Ciclo de Krebs)
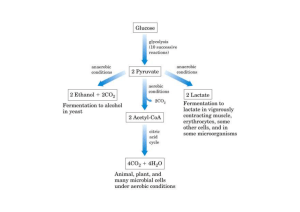
Para a maioria das células eucarióticas e
muitas bactérias, vivendo em condições
aeróbicas, a glicólise não é mais que o 1o
estágio da oxidação completa da glicose.
O piruvato formado na glicólise não é
reduzido nem a lactato nem a etanol, em
vez disso ele é oxidado a CO2 e H2O. Essa
fase aeróbica do catabolismo é chamada
de respiração, que em um sentido
microscópico se refere aos processos
moleculares que envolvem o consumo de
O2 e a formação de CO2 pelas células.
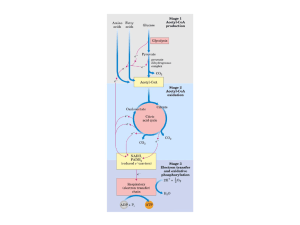
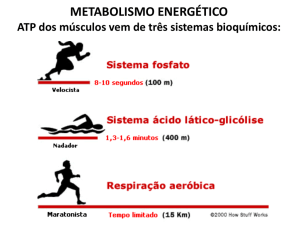
A respiração celular ocorre em três estágios:
1. Oxidação dos
compostos orgânicos
2.
Oxidação
do acetilCoA
3. Fosforilação
oxidativa
A produção de acetato
Nos organismos aeróbicos, a glicose e outros açúcares,
ácidos graxos e a maioria dos aminoácidos são oxidados
a CO2 e H2O. Entretanto, para entrar no ciclo do ácido
cítrico, seus esqueletos carbônicos precisam ser degradados
até o grupo acetil do acetil-CoA, a forma na qual o ciclo
recebe a maior parte de seu combustível. O piruvato é
oxidado para liberar acetil-CoA e CO2 por um complexo de
3 enzimas: o complexo da piruvato desidrogenase,
localizado na mitocôndria das células eucarióticas
e no citosol das procarióticas.
O piruvato é
transportado do
citosol para o interior
da mitocôndria
através de uma
proteína
transportadora
(simporte de
piruvato-H+)
Descarboxilação oxidativa: um processo irreversível de
oxidação no qual o grupo carboxila é removido do
piruvato na forma de uma molécula de CO2 e os 2
carbonos remanescentes tornam-se o grupo acetil do
acetil-CoA.
Cede um íon
hidreto com seus 2
elétrons para a
cadeia respiratória
A reação global catalisada pelo complexo da piruvato desidrogenase.
O complexo da piruvato desidrogenase requer
5 coenzimas ou cofatores:
Tiamina pirofosfato (TPP)
FAD
NAD
Coenzima A
Lipoato
Descarboxilação do
piruvato até
acetaldeído
Transportadores de elétrons
O grupo reativo tiol é
crítico para o seu papel
como transportadora
de grupos acila
(tioésteres)
O complexo da piruvato desidrogenase possui 3
enzimas distintas:
Piruvato
desidrogenase (E1)
S
Diidrolipoil
transacetilase (E2)
Diidrolipoil
desidrogenase (E3)
S
FAD
TPP
E1
E2
E3
Deve estar na
dieta
BERIBÉRI
A tiamina (vitamina B1) não é sintetizada nem armazenada
em quantidades significativas pelos tecidos da maioria dos
vertebrados.
BERIBÉRI
Deficiência de
tiamina
Doença que resulta da deficiência dietética
de tiamina caracterizada pela perda parcial
de funções neurais. Dor, paralisia e atrofia
dos membros inferiores, falência cardíaca
e edema fazem parte do quadro.
Incapacidade
de oxidar o
piruvato
Cérebro: obtém toda a
sua energia pela
oxidação aeróbica da
glicose
Populações que se alimentam de arroz branco (polido) ou indivíduos que
ingerem grandes quantidades de bebidas alcoólicas.
Reações do Ciclo do Ácido Cítrico
Em cada volta
entra um grupo
acetil (acetil-CoA) e
saem
duas
moléculas de CO2.
Uma molécula de
oxalacetato
é
empregada
para
formar citrato, mas
após uma série de
reações
esta
molécula
é
regenerada. Quatro
dos oito passos
são oxidações e a
energia liberada é
conservada
na
forma de NADH e
FADH2.
O Ciclo do Ácido Cítrico possui oito passos
Formação do citrato
É reciclada para formar
outra molécula de acetilCoA na descarboxilação
de outra molécula de
piruvato
Formação do isocitrato via cis-aconitato
É um ácido
tricarboxílico
que não se
dissocia do
sítio ativo
desidratação
hidratação
Oxidação do isocitrato à -cetoglutarato
e CO2
Descarboxilaçã
o oxidativa
Oxidação do -cetoglutarato a succinilCarreador do
CoA e CO2
grupo succinil
Descarboxilaçã
o oxidativa
A energia de oxidação do -cetoglutarato é conservada pela
formação de uma ligação tioéster do succinil-CoA. O complexo da
-cetoglutarato desidrogenase é muito semelhante ao complexo da
piruvato desidrogenase.
Conversão do succinil-CoA em succinato
Tem uma energia livre de hidrólise de
sua ligação tioéster forte e negativa.
A energia liberada no rompimento
desta ligação é empregada para
dirigir a síntese de ATP ou GTP.
GDP + ATP
GTP + ADP
Nucleosídeo
difosfato quinase
O resultado final da atividade de
qualquer isoenzima da succinil-CoA
sintetase é a conservação de energia na
forma de ATP.
Oxidação do succinato a fumarato
Nos eucariotos, a succinato desidrogenase
está
firmemente
ligada
à
membrana
mitocondrial interna; nos procariotos ela é
ligada a membrana plasmática. É a única
enzima do ciclo do ácido cítrico ligada à
membrana.
O malonato, um análogo do succinato, é um
potente inibidor competitivo da succinato
desidrogenase, logo é um bloqueador do ciclo
do ácido cítrico.
Hidratação do fumarato para produzir
malato
Esta enzima é altamente estereoespecífica;
ela catalisa a hidratação da dupla ligação
trans do fumarato, porém não é capaz
de agir no maleato (isômero cis do fumarato)
Na direção inversa, a fumarase é igualmente
estereoespecífica: o D-malato não é um
substrato.
A oxidação do malato a oxaloacetato
O equilíbrio desta reação está muito deslocado para a esquerda
sob as condições termodinâmicas padrão. Entretanto, nas células
intactas, o oxaloacetato é continuamente removido pela reação da
citrato sintase que é altamente exergônica. Isso conserva a
concentração de oxaloacetato na célula em valores extremamente
pequenos (10-6M), deslocando a reação na direção de formação de
oxaloacetato.
Produtos de uma volta do ciclo do ácido cítrico
Os 2 átomos de C que aparecem
com CO2 não são os mesmos 2C
que entraram no ciclo na forma de
grupo acetil; são necessárias
várias voltas no ciclo para que
isso aconteça.
Cada volta do ciclo
do ácido cítrico
produz três NADH
e um FADH2, bem
como um GTP (ou
um ATP). Dois CO2
são produzidos nas
reações
de
descarboxilação
oxidativa.
A estequiometria da redução das coenzimas e da formação de ATP
na oxidação aeróbica de uma molécula de glicose por meio da via
glicolítica seguida da reação da piruvato desidrogenase, do ciclo do
ácido cítrico e da fosforilaçao oxidativa.
Cada NADH
= 2,5 ATP
Cada FADH2
= 1,5 ATP