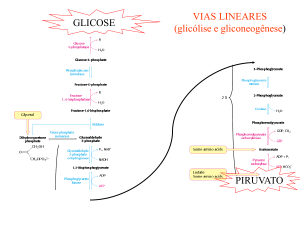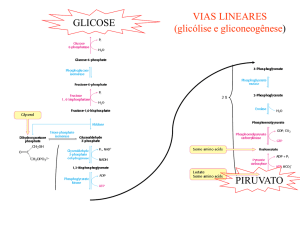
GLICOSE
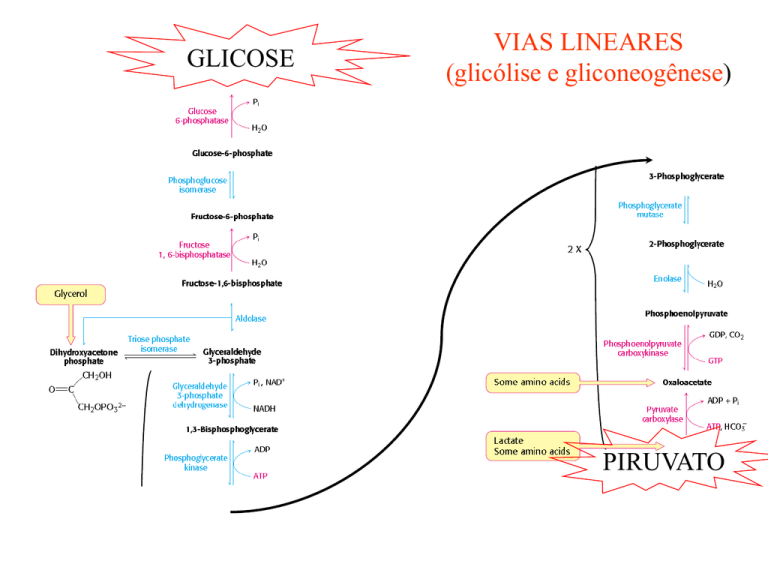
VIAS LINEARES
(glicólise e gliconeogênese)
PIRUVATO
VIA CIRCULAR
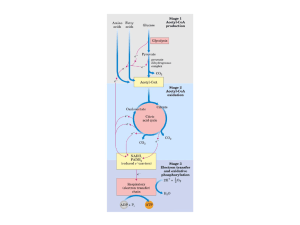
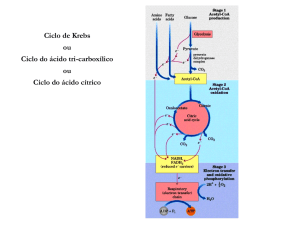
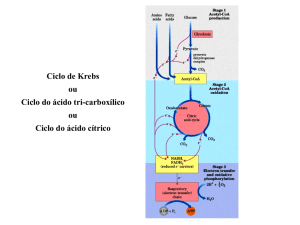
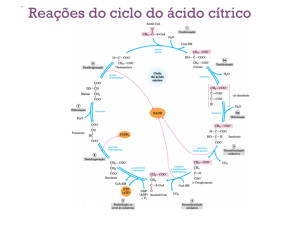
Ciclo do ácido cítrico ou ciclo de Krebs
representa o estágio final da oxidação
de fontes de energia metabólica
(carbohidratos, ácidos graxos e
aminoácidos)
= rota central de recuperação de energia
a partir de vários combustiveis meta-bólicos
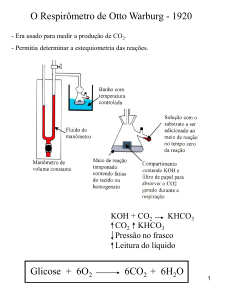
O manômetro de Otto Warburg - 1920
- Era usado para medir a produção de CO2.
- Permitia determinar a estequiometria das reações.
Coloca o
substrato
Tecido
Meio de cultura
Fluido
com cor
Papel de filtro
com KOH
KOH + CO2
KHCO3
CO2 KHCO3
Pressão no frasco
Leitura do líquido
Glicose + 6O2
6CO2 + 6H2O
Os experimentos de Hans Krebs
- Observando os dados disponíveis na época Krebs destaca os trabalhos de Thumberg entre 1906 e 1920
usando tecidos musculares. Ele testou a oxidação de cerca de 60 substâncias orgânicas e descobriu que a
forma ionizada de vários ácidos como o lactato (1 carboxila), succinato, fumarato, malato (2 carboxilas),
eram rapidamente oxidadas.
- Krebs então testa outros ácidos dicarboxílicos. Em 1935 descobre que um deles, o α-cetoglutarato, com
5 carbonos, assim como nos experimentos de Szent-Györgyi, aceleravam a produção de CO2 e não eram
consumidos na reação.
50
piruvato +
CO2
40
30
piruvato
20
10
0
0
5
10
tempo
15
20
lactato
succinato
malato
fumarato
-
Em 1937 Krebs testa ácidos tricarboxílicos como citrato, isocitrato e aconitato, agora com 6
carbonos, e observa que a produção de CO2 também era estimulada e esses intermediários não eram
consumidos.
50
piruvato
CO2
40
30
piruvato
20
10
0
0
5
10
tempo
15
20
+
citrato
isocitrato
aconitato
- Segundo Krebs, outra contribuição significativa para suas descobertas veio
dos estudos de Martius e Knoop, em 1937, que elucidaram a transformação
oxidativa de citrato até α-cetoglutarato.
Em 1936, Carl Martius e Franz Knoop demonstraram que o citrato pode ser formado de
modo não-enzimático a partir do oxaloacetato e do piruvato
- Krebs observou nos trabalhos de Shiffield em 1937 que a formação de
citrato (C6) ocorria rapidamente após a adição de oxaloacetato (C4) em
diversos tecidos. Concluiu então que a formação desse composto de 6
carbonos poderia se originar da ligação de um produto de 4 carbonos
(oxaloacetato) mais dois carbonos vindos provavelmente da degradação
da glicose.
- Juntando as seguintes informações:
1- ácidos di e tri carboxílicos aceleravam a formação de CO2 em diversos
tecidos mas não eram consumidos na reação.
2- algum composto de 2 carbonos vindo provavelmente da glicólise se
combinava com oxaloacetato e formava um composto de 6 carbonos
(citrato) que iniciava uma via de interconversão, Krebs conclui e postula
um modelo que ele chamou de “Ciclo do Ácido Cítrico” ou dos “Ácidos
Tricarboxílicos”.
Krebs então postula que:
“O piruvato, ou um derivado vindo da glicólise (acetato), se condensa
com o oxaloacetato e forma citrato. Por uma sequência de reações que
envolvem cis-aconitato, isocitrato, α-cetoglutarato, succinato, fumarato,
malato e oxaloacetato como intermediários, um ácido acético é oxidado e
o oxaloacetato necessário para a reação inicial de condensação é
regenerado. Isso explica a ação catalítica dos ácidos di e tricarboxílicos
(de 4,5 e6 carbonos), bem como a capacidade que esses ácidos possuem
de se oxidar nos tecidos que oxidam carboidratos.”
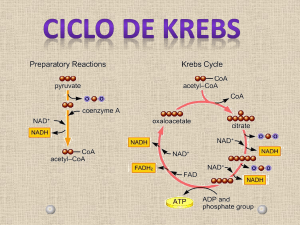
Ciclo do ácido cítrico ou ciclo de krebs
Os experimentos de Fritz Lipmann
- Naquela época já se sabia que a Coenzima A estava envolvida em reações
de transferência de carbono e que ela era derivado do ácido pantotênico,
uma vitamina pertencente ao complexo B (vit. B5).
- A coenzima A é uma molécula ubíqua nos tecidos
Ac. Pantotênico = Vit. B5
- A síntese de citrato aumenta na presença de CoA
- Lipmann demonstra que o consumo de O2 é aumentado na presença de CoA quando se fornece
glicose-fosfato para leveduras
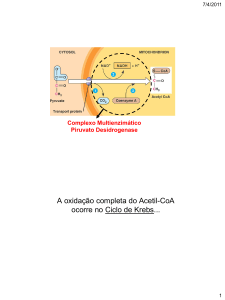
O complexo Piruvato
Desidrogenase
Complexo multienzimático: grupos de enzimas associadas de modo nãoTrês tipos de enzimas em cópias múltiplas: E1, E2, E3
covalente que catalisam duas ou mais reações seqüencias em uma rota
Ex: piruvato desidrogenase de E. coli contém 60 s-u
metabólica (aumento a velocidade das reações, canalização dos
proteícas
intermediários minimizando as reações secundárias, controle coordenado
Descarboxilação oxidativa
Complexo piruvato desidrogenase:
E1= piruvato desidrogenase (24 s-u)
E2= dihidrolipoil transacetilase (24 s-u)
E3= dihidrolipoil desidrogenase (12 s-u)
E. coli diâmetro de ~300 Å > ribossoma
4 vitaminas são necessárias para formação de Acetil-CoA
Ácido
nicotínico =
Vitamina B3
Riboflavina =
Vitamina B2
lipoamida
tiamina =
Vitamina B1
Falta de vitamina B1 – tiamina – causa uma doença conhecia por beriberi
Hidroxietil-TPP
Lipoamido = ac. Lipóico ligado
A um resíduo lisina
Acetil- dihidropoliamido
Transesterificação e produção
da AcetilCoA
dihidropoliamido
Regeneração do lipoamido
O complexo piruvato desidrogenase pode ser inibido pela reação
do grupo lipoamido com compostos que contêm arsênico
E1= piruvato desidrogenase
Piruvato + TPP
Hidroxietil-TPP + CO2
E2= dihidrolipoil transacetilase
Hidroxietil-TPP + lipoil-lisina oxidada
TPP + Acetil tioester da lipoil-lisina reduzida
Acetil tioester da lipoil-lisina reduzida + CoA
E2= dihidrolipoil transacetilase
Acetil-CoA + lipoil lisina reduzida
E3= dihidrolipoil desidrogenase: restauração do complexo PDH ao seu estado inicial
(regeneração da lipoamida oxidada e produção de FADH2)
Regulação do complexo PDC
• Inibida quando [ATP/ADP], [NADH/NAD+] e [acetilCoA/CoA]
• Inibida por ácido graxos de cadeia longa (mod. alostérica)
• Por modificação covalente de E1 (mamíferos):
- piruvato desidrogenase cinase fosforila E1
inativa o PDC (ATP é um ativador alost. desta cinase)
- piruvato desidrogenase fosfatase : reativa o PDC
A insulina reverte essa inativação ativando a PD fosfatase promovendo
Complexo multienzimático: grupo de enzimas associadas de modo
a síntese de acetil-CoA
não-covalente que catalisam duas ou mais reações sequenciais em
uma rota metabólica.
Vantagens:
-velocidade das reções limitada pela difusão do substrato entre os sítios ativos
-canalização dos intermediários metabólicos evitando reações secundárias
-contrôle coordenado das reações no complexo mutienzimático
As Reações do Ciclo de Krebs
Piruvato
NAD+
Mitocôndria
NADH
CO2
CoA-SH
1° Reação:
2° Reação:
3° Reação:
Ocorre a primeira descarboxilação oxidativa com liberação com conservação de energia na forma de NADH
4° Reação:
Sintase: reação de condensação sem nucleosídeo trifosfato (ATP, GTP...) ou outra origem de energia
Importância da ligação tioester
Citrato sintase
Oxaloacetato (em amarelo) é o primeiro substrato a se
ligar, e promove uma mudança conformacional,
criando um sítio de ligação para o segundo substrato, o Acetil-CoA
(em vermelho um análogo da Acetil-CoA)
= reação cinética seqüencial ordenada
Aconitase contêm um grupo ferro-enxofre 4Fe-4S
O CO2 eliminado vem do OAA não do acetil-CoA
Perda do grupo carboxila na forma de CO2 e En. de oxidação conservada na ligação tioéster
5° Reação:
6° Reação:
Ocorre conservação de energia na forma de FAD reduzido.
A succinato desidrogenase é a única enzima do TCA que está ligada à matriz mitocondrial
7° Reação:
8° Reação:
En. livre de hidrólise da ligação tioéster do succinil-CoA forte e negativa (-36 kJ/mol)
Sintetase: reação de condensação com uso de nucleosídeos trifosfato
= anidro fosfato de alta energia
Fosforilação ao nível do substrato
(diferente das fosforilação oxidativa)
Catalise a desidrogenação estereoespecífica do succinato em fumarato
Malonato= inibidor competitivo
Etapa final do ciclo com regeneração do oxaloacetato
Saldo final – Cada molécula de Acetil-CoA que entra no ciclo gera:
•3 NADH
•1 FADH2
•1 GTP ou ATP
Componentes do TCA são importantes intermediários anabólicos
Reações anapleróticas repõem os intermediários
O catabolismo de proteínas gera diversos intermediários do TCA
Reações anapleróticas repõem intermediários metabólicos importantes para o TCA
Regulação do Ciclo de Krebs
No músculo cardáco o flúxo de metabólitos no TCA é proporcinal a taxa de
consumo de oxigênio :
3 níveis de regulação:
Piruvato carboxilase
-Disponibilidade de Substrao
-Inibição por acumulo de Produto
-Inibição competitiva retroativa
pelos intermediários
Velocidades da glicólise e do CK
são reguladas de maneira
integrada (NADH, ATP, Citrato)
Diabetes e formação dos corpos cetónicos...