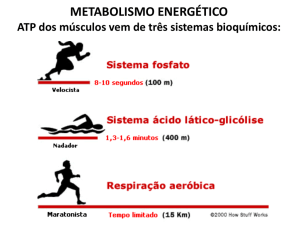
ENERGIA E METABOLISMO
O que é energia?
O estado da energia: potencial e cinética.
O estudo da energia – a termodinâmica
O que é bioenergética?
O fluxo de energia nos seres vivos
A) Energia potencial
B) Energia cinética
Energia potencial e cinética. A) Objetos que têm a capacidade de se moverem
mas não estão se movendo possuem energia potencial. A energia necessária
para levar a bola ao topo da colina fica armazenada como energia potencial;
B) Objetos em movimento possuem energia cinética. A energia armazenada é
liberada como energia cinética a medida que a bola desce a colina.
A ENERGIA NOS SISTEMAS VIVOS
A energia vem do sol – atingem a Terra 40 milhões de bilhões de calorias
por segundo
Fotossíntese – armazena energia em forma potencial nas ligações químicas
A energia contida nessas ligações pode ser transferida para novas ligações
através de reações de óxido-redução.
Uma reação de óxido redução. As células utilizam substâncias como o NAD+ para as
reações de óxido-redução. Elétrons energéticos são freqüentemente pareados com um
próton em um átomo de hidrogênio. Moléculas que ganham esse elétron são reduzidas
e as que perdem são oxidadas. NAD+ oxida moléculas ricas em energia reduzindo-se
ao ganhar seus hidrogênios. O NADH pode então reduzir outras moléculas cedendolhes o hidrogênio.
Reação Redox. Oxidação é a perda de um elétron; redução é o ganho de um elétron.
Neste exemplo, as cargas das moléculas A e B são mostradas em pequenos círculos
acima da figura. A molécula A perde energia quando perde um elétron, enquanto que a
molécula B ganha energia quando ganha um elétron.
AS LEIS DA TERMODINÂMICA
Todas as transformações de energia no Universo são regidas pelas leis
da termodinâmica
I – A energia total do Universo é constante, portanto, ela só pode ser
transformada de uma forma para outra, não pode ser nem criada nem
destruída.
II – A disordem (entropia) no Universo está sempre aumentando. A energia
só se transforma espontaneamente de uma energia de “alta qualidade”
para de “baixa qualidade”, ou seja, de uma forma mais ordenada para
uma menos ordenada.
ENERGIA LIVRE
Energia nas ligações químicas. A) em uma reação endergônica, o produto da
reação contém mais energia do que os reagentes; B) Em uma reação
exergônica, os produtos contém menos energia do que os reagentes, sendo o
excesso de energia liberado.
ENERGIA DE ATIVAÇÃO
Energia de ativação e catálise. a) Reações exergônicas não necessariamente ocorrem
rapidamente, pois necessitam energia para desestabilizar as ligações químicas. Essa
energia extra é chamada de energia de ativação para a reação; b) Catálise acelera
reações específicas diminuindo a energia de ativação necessária para iniciar a reação.
ENZIMAS
Anidrase carbônica – enzima que cataliza a transformação de CO2 em ácido
carbônico no sangue. Esta é uma reação exergônica mas que precisa de uma
alta energia de ativação. A enzima acelera a reação em 10 milhões de vezes.
Cerca de 70% do CO2 transportado pelo sangue é na forma de íon bicarbonato.
COMO AGEM AS ENZIMAS
Como a enzima lisosima funciona. a) um sulco na lisosima encaixa-se com a forma
de um polissacarídio que forma a parede celular de uma bactéria; b) ao se
encaixar o polissacarídio induz a enzima a alterar sua forma e se ajustar mais
precisamente. Esse ajuste faz com que um ácido glutâmico da enzima se encaixe
entre duas ligações de açúcares. O ácido sequestra um elétron da ligação e a
molécula quebra.
O ciclo catalítico de uma enzima.
ENZIMAS PODEM TER MUITAS FORMAS
A enzima piruvato desidrogenase. A enzima (modelo a) que facilita a oxidação do
piruvato é uma das mais complexas enzimas conhecidas – ela tem 60
subunidades, muitas das quais podem ser vistas na fotografia eletrõnica (b) com
aumento de 200.000X.
Diversos fatores afetam a atividade
enzimática. As enzimas são sensíveis
ao meio onde estão. A atividade das
enzimas são influenciadas
principalmente pela temperatura (a) e
pelo pH (b).
Co-fatores. Como a enzima pode ser inibida. a) inibição competitiva, o
inibidor interfere com o sítio ativo; b) inibição não competitiva, o inibidor se
liga a um outro sítio que modifica a conformação do sítio ativo.
Estrutura química da nicotinamida
adenina dinucleotídio (NAD+). Esse
cofator chave é composto de dois
nucleotídeos, NMP e AMP, ligados
cabeça com cabeça.
O que é o ATP? a) O modelo e
b) o diagrama da estrutura
mostra que tal como o NAD+,
o ATP tem um núcleo de AMP.
No ATP o grupo reativo
adicionado ao final do grupo
fosfato do AMP não é um
outro nucleotídeo mas uma
cadeia adicional de 2 grupos
fosfato. As ligações que
conectam esses dois grupos
fosfato um ao outro e ao AMP
são as ligações que
armazenam energia.
Os caminhos bioquímicos: as unidades organizacionais do
metabolismo
O total das reações químicas de um organismo é chamado de
metabolismo – as reações que gastam energia para fazer ou transformar
ligações químicas são chamadas de anabólicas, e as que obtém energia
quando as ligações são rompidas são as catabólicas.
Existem milhares de enzimas envolvidas no metabolismo. Muitas ocorrem
em uma seqüência que recebe o nome de “caminho metabólico” ou “via
metabólica”, muitas vezes em um local específico da célula.
Uma via metabólica. O
substrato original é
modificado por uma enzima
1; este é então reconhecido
por uma enzima 2 que o
transforma novamente para
ser reconhecido por uma
enzima 3. O processo segue
até o produto final.
Como as vias metabólicas são reguladas? Mecanismos de retroalimentação
(feedback).
A Evolução do Metabolismo
Degradação – a forma mais primitiva;
Glicólise – o segundo maior evento na evolução;
Fotossíntese anaeróbica;
Fixação do Nitrogênio;
Fotossíntese formadora de oxigênio;
Respiração aeróbica
Os heterótrofos dependem da energia das ligações
químicas do alimento que ingerem para fornecer
energia para seus processos vitais.
Respiração celular
Aeróbica e anaeróbica
Adenosina trifosfato ou ATP é a “moeda” da célula
As células usam ATP para todas suas atividades que requerem trabalho e
para reações endergônicas.
Estrutura da molécula de ATP. O ATP é composto por uma base orgânica e uma
cadeia de fosfatos. Note que as regiões carregadas da cadeia do fosfato estão
próximas umas das outras. Essas cargas tendem a se repelir umas às outras,
dando às ligações que as mantém unidas uma energia potencial de transferência
particularmente alta.
Como o ATP dirige uma reação endergônica. Em muitos casos, um grupo fosfato
do ATP se quebra e ativa uma proteína, que cataliza uma reação endergônica.
O processo de fermentação alcóolica
e com formação do ácido lático.
Na glicólise anaeróbia 2 ATPs são usados
para fosforilar a glicose. Nas cinco
primeiras reações a molécula de glicose é
convertida a G3P. Nas cinco reações
seguintes o G3P é convertido a piruvato. Na
presença de oxigênio este é conduzido ao
ciclo de Krebs, e na respiração aeróbia
forma-se ácido lático que pode ser
posteriormente oxidado.
Durante o processo são gastos dois
ATPs e formados quatro, com um ganho
de 2 ATPs. (São formados também dois
NADH que originam 4 ATPs)
Catabolismo da Glicose
Fosforilação ao nível do substrato – Algumas moléculas como o fosfoenolpiruvato
possuem um fosfato de alta energia, que pode ser transferido para o ADP,
enzimáticamente.
A respiração aeróbia:
na respiração aeróbia a célula obtém energia da molécula de
glicose em uma seqüência de quatro vias principais: glicólise, oxidação do piruvato, o ciclo
de Krebs e a cadeia de transporte de elétrons. O oxigênio é o receptor final do oxigênio. Na
respiração anaeróbia os elétrons são transferidos para outros compostos orgânicos.
Esse diagrama mostra como o ATP é formado quando os elétrons são transferidos
de um nível de energia para outro. Em vez de liberar a energia de uma vez, os
elétrons caem gradativamente, liberando energia a cada queda para os receptores
mais eletronegativos.
A cadeia de transporte de elétrons. Elétrons de alta energia das moléculas
catabolizadas são transportados (setas vermelhas) por carregadores de elétrons móveis
(as ubiquinonas e os citocromos c) ao longo de uma cadeia de proteínas de membrana.
Três proteínas usam partes da energia dos elétrons para bombear prótons fora da
matriz da mitocôndria para o espaço entre membrana. Os elétrons são finalmente
doados para o oxigênio que se transforma em água.
Quimiosmose – NADH transporta elétrons de alta energia para as bombas de
prótons que usam essa energia para enviar os prótons para fora da matriz da
mitocôndria. A concentração dos prótons no espaço entre as membranas aumenta,
induzindo-os a retornarem para a matriz. Muitos dos prótons passam através de
canais que acoplam sua re-entrada à produção de ATP.
Formação do ATP durante o ciclo de Krebs e a cadeia de transporte de elétrons.
O processo se inicia com o piruvato, produto da glicólise, e termina com a
síntese do ATP.
Ganho total teórico de ATP – a energia armazenada no ATP representa mais da
metade da energia contida nas ligações químicas da glicose.
Controle do catabolismo da
glicose. Os níveis relativos de
ADP e ATP controlam a via
catabólica em dois pontos
principais, na glicólise e no
ciclo de Krebs.
Todos os eucariontes
e muitos procariontes
extraem energia das
moléculas orgânicas
oxidando-as. Primeiro
estas são quebradas
em seus constituintes.
A segunda etapa é a
respiração aeróbica
ou oxidativa que extrai
energia primeiramente
na forma de elétrons
de alta energia e
produz água e gás
carbônico.
Uréia
glutamato
-cetoglutarato
Desaminação. Depois que as proteínas são quebradas em aminoácidos, o
grupo amina é removido do aminoácido para formas moléculas que participam
na glicólise e no ciclo de Krebs. Por exemplo, o aminoácido glutamato, ao
perder seu grupo amina, transforma-se em -cetoglutarato, uma molécula do
ciclo de Krebs.
Eficiência metabólica e tamanha das tramas tróficas