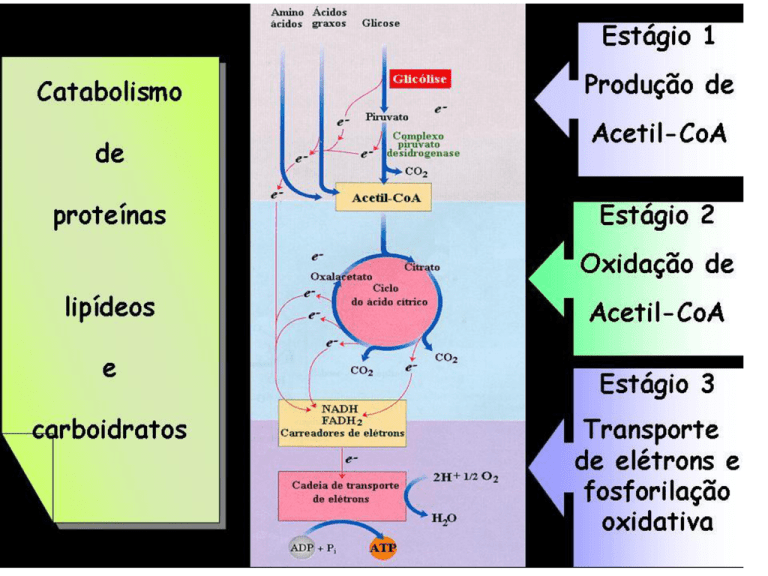
Oxidação das coenzimas
reduzidas
• A energia total inicialmente disponível
na molécula de glicose foi utilizada para
produção de pequena quantidade de ATP
(2 ATP na glicólise e 1 GTP no ciclo de
Krebs).
• A maior parte da energia é conservada
na forma de coenzimas reduzidas
(NADH e FADH2)
Oxidação das coenzimas
reduzidas
•
As coenzimas reduzidas devem ser
reoxidadas por duas razões:
1. Voltar a participar das vias oxidativas
na forma de coenzimas oxidadas
2. É a partir da oxidação destas
coenzimas que a energia nelas
conservada pode ser aproveitada para
sintetizar ATP.
Cadeia de Transporte de elétrons
• A estratégia adotada pela célula é
transformar a energia armazenada nas
coenzimas em um gradiente de prótons
na mitocôndria e utilizar este gradiente
para sintetizar ATP.
FOSFORILAÇÃO OXIDATIVA DO ADP
4H+
2H+
4H+
H+
H+
H+
½ O2 H 2 O
SuccinatoFumarato
NADH
ADP + Pi
NAD+
3H+
ATP
H+ H+
H+
H+
CADEIA DE TRANSPORTE DE ELÉTRONS E
FOSFORILAÇÃO OXIDATIVA
Bactéria aeróbica
Seletividade da membrana interna da mitocôndria
Membrana externa:
livremente permeável a
pequenas moléculas e
íons
Membrana interna:
seletiva – impermeável a
íons e pequenas
moléculas
Matriz mitocondrial:
contém enzimas do
ciclo do ácido
cítrico, proteínas
da cadeia
respiratória,
enzimas da
oxidação de ácido
graxos e
aminoácidos
Os elétrons são transportados por
quatro complexos
• A oxidação das coenzimas reduzidas pela
cadeia transportadora de elétrons
processa-se na membrana interna da
mitocôndria.
• Estes transportadores agrupam-se em 4
complexos, designados complexos I, II, III,
IV.
Complexos protéicos da
cadeia de transporte de elétrons
Complexo
Massa
(kDa)
Número de
subunidades
Grupos
prostéticos
I NADH desidrogenase 850
42 (14)
FMN, Fe-S
II Succinato
desidrogenase
5
FAD, Fe-S
III
250
Ubiquinona:citocromo c
oxidoredutase
11
Hemes, Fe-S
Citocromo c
13
1
Heme
IV Citocromo oxidase
160
13 (3-4)
Hemes, CuA, CuB
140
O complexo I oxida o NADH, transferindo
seus elétrons para a coenzima Q
• Este
complexo também é chamado NADHcoenzima Q redutase
• Possui
FMN
e
centros
ferro-enxofre.
A flavina mononucleotídeo (FMN) é um derivado
da riboflavina capaz de receber 2 prótons e dois
elétrons, passando à forma reduzida FMNH2
O
doador
de
elétrons
é
o
NADH.
Complexo I
Centros ferro-enxofre
Formados
por íons
de ferro e
enxofre
Transportam
apenas
elétrons. Não
transportam
prótons
Isto faz com
que os prótons
sejam
excluídos,
sendo
transportados
da membrana
interna para o
espaço inter
membranas
Complexo II
• Chamado de succinato-coenzima Q redutase
• É uma segunda porta de entrada dos elétrons
na cadeia respiratória
• A succinato desidrogenase do ciclo de Krebs faz
parte deste complexo.
Complexo II
• Os elétrons são transferidos do succinato
para o FAD, que se reduz a FADH2.
• São então repassados para centros ferroenxofre e então para citocromos b560.
• Não é uma proteína transmembrana: não
ocorre extrusão de prótons. Os prótons,
que não são carregados pelos centro-ferro
enxofre e citocromo são devolvidos à
matriz mitocondrial.
Citocromos:
Transportadores
de elétrons
A coenzima Q é o ponto de convergência
dos elétrons provenientes do complexo I e
complexo II
• A coenzima Q é uma quinona com uma
longa cadeia lateral constituídas por
cadeias isoprênicas.
• Recebe dois prótons e dois elétrons
passando à forma reduzida QH2
COENZIMA Q:
POSSUI
CARACTERÍSTICAS
HIDROFÓBICAS QUE
PERMITEM SUA
MOBILIDADE NA
MEMBRANA LIPÍDICA
Complexo III
• Coenzima Q-citocromo c redutase.
• Possui dois citocromos b, centro Fe-S e
citocromo c.
• Participa com a extrusão de 4 prótons
para o espaço intermebranas.
Citocromo c
• É uma proteína pequena situada na face
externa membrana interna da mitocôndria.
• Conecta os complexos III e IV.
Estrutura secundária do citocromo b
bH
Matriz mitocondrial
bL
Citocromo c
Fe+3 + 1e- <-> Fe2+
Complexo IV
• Transfere elétrons para o oxigênio.
• É chamado de citocromo c oxidase.
• Contém dois citocromos do tipo a e dois íons cobre,
que transportam elétrons alterando seus estados de
oxidação de +2 para +1.
• Participa da transferência de 4 elétrons para a
molécula de oxigênio, que se liga a dois prótons,
formando água.
• O complexo IV também participa da extrusão de 2
prótons para o espaço intermembrana.
Cadeia transportadora de elétrons
A retirada de prótons da matriz mitocondrial
contribui para o estabelecimento do gradiente de
prótons.
GRADIENTE DE PRÓTONS
Fosforilção oxidativa
• A energia do transporte de elétrons é convertida
em uma força próton motriz.
• Teoria quimiosmótica: o transporte de elétrons é
utilizado para bombardear prótons para o
espaço intermembranas.
• A membrana interna da mitocôndria é
impermeável à prótons. Isto gera uma diferença
na concentração de prótons dentro e fora da
matriz mitocondrial. Adicionalmente a face
voltada para a matriz fica mais negativa e a
diferença de carga elétrica gera um potencial de
membrana.
Força próton-motriz
• O gradiente eletroquímico formado é
chamado de força próton-motriz.
• Constituída por dois componentes: O
gradiente de pH e o gradiente elétrico.
• O retorno dos prótons para o interior da
mitocôndria é um processo espontâneo, a
favor do gradiente eletroquímico.
• Este retorno libera energia.
A síntese de ATP
• Como a membrana interna é impermeável
a prótons, estes só podem voltar à matriz
e desfazer o gradiente através de sítios
específicos na membrana interna,
constituídos pelo complexo sintetizador de
ATP: a ATP sintase.
A ATP sintase
Compreende
dois
componentes:
F1: contém os
sítios de síntese
de ATP
Fo: contém o
canal através do
qual os prótons
retornam à
matriz.
Matriz
O ATP é
sintetizado
quando os
prótons
retornam à
matriz
mitocondrial.
Espaço
intermembranas
As três subunidades da ATPsintase podem assumir
três diferentes conformações
Estrutura do complexo F1 deduzida por
cristalografia e estudos bioquímicos
FOSFORILAÇÃO OXIDATIVA DO ADP
2H+
4H+
4H+
H+
H+
H+
½ O2 H 2 O
SuccinatoFumarato
NADH
ADP + Pi
NAD+
3H+
ATP
Potencial
químico
pH
( alcalino interior)
Síntese de ATP
dirigida pela
força prótonmotriz
Potencial
elétrico
( negativo interior)
H+ H+
H+
H+
Estequiometria da síntese de ATP
Adenina nucleotídeo e Pi translocase: 1H+
ADP + Pi + 3H+p ATP + H2O + 3H+n
NADH O2 = 10H+/2e-
10H+/4H+ = 2,5 ATP
Succinato (FADH2) O2 = 6H+/2e-
6H+/4H+ = 1,5 ATP
Produção de ATP na oxidação completa de glicose
Processo
Produto
ATP final
Glicólise
2 NADH (citosólico)
5
2 ATP
2
Oxidação do piruvato (2
por glicose)
2 NADH (mitocondrial)
5
Oxidação de acetil-CoA
no ciclo de Krebs
6 NADH (mitocondrial)
15
(2 por glicose)
2 FADH2
3
2 ATP ou GTP
2
Produção total por glicose
32












