Profª Eleonora – Slide de aula
Cadeia de Transporte de Elétrons
e
Fosforilação Oxidativa
Profª Eleonora – Slide de aula
Cadeia de Transporte de Elétrons ou Cadeia Respiratória
Os transportadores de elétrons sempre funcionam em uma seqüência determinada
Os potenciais redox-padrão dos
componentes da cadeia são
sucessivamente mais positivos quando
se encaminham em direção ao oxigênio.
Os elétrons tendem a fluir dos sistemas
eletronegativos para os eletropositivos,
levando a uma diminuição da energia livre.
Cada membro da cadeia é específico
para um dado doador e para um dado
receptor de elétrons.
O NADH pode transferir seus elétrons
para a NADH redutase, mas não os
transfere diretamente para a ubiquinona
ou para o citocromo.
Complexos bem estruturados do
sistema transportador de elétrons
foram isolados da membrana
mitocondrial interna.
Profª Eleonora – Slide de aula
Esquema dos complexos transportadores de elétrons da Cadeia Respiratória
A cadeia respiratória consiste de uma seqüência de reações redox pela qual os elétrons
são transferidos das coenzimas reduzidas (NADH ou FADH2) para o oxigênio.
Complexo
Complexo II == NADH-Ubiquinona
NADH-Ubiquinona Redutase;
Redutase; Complexo
Complexo II
II == Succinato-Ubiquinona
Succinato-Ubiquinona Redutase;
Redutase;
Complexo
III
=
Ubiquinol-Citocromo
C
Redutase;
Complexo
IV
=
Citocromo
Oxidase
Complexo III = Ubiquinol-Citocromo C Redutase; Complexo IV = Citocromo Oxidase
Profª Eleonora – Slide de aula
Fluxo de elétrons e prótons na cadeia respiratória
Profª Eleonora – Slide de aula
Complexos transportadores de elétrons
Isolados como conjuntos funcionais
Profª Eleonora – Slide de aula
Esquema do transporte de elétrons
Succinato
Fumarato
Complexo II
FAD
NADH
NAD+
FADH2
FMN
Fe-Sred
CoQ
Fe-Sred
CiT. c1oxid
CiT. cred
CiT. aoxid
Cu (I)
CiT. a3oxid
H2O
FMNH2
Fe-Soxid
CoQH2
Fe-Soxid
CiT. c1red
CiT. coxid
CiT. ared
Cu (II)
CiT. a3red
½ O2
Complexo I
Ciclo Q
Cit. b
Complexo III
Complexo IV
Os co-fatores reduzidos (NADH e FADH2) podem transferir seus elétrons para substratos
específicos da cadeia de transporte de elétrons, a seguir, os elétrons são transferidos
sucessivamente para outro substrato.
Deste modo, parte da energia liberada na oxidação do primeiro substrato pode ser utilizada para
impulsionar a redução de um segundo substrato.
Profª Eleonora – Slide de aula
FOSFORILAÇÃO OXIDATIVA
Os componentes da cadeia de transporte de elétrons estão organizados em ordem
crescente de potenciais de oxido-redução, desde as coenzimas reduzidas até o oxigênio.
As transferências de elétrons de um componente para o seguinte constituem reações de
óxido-redução que se processam sempre com liberação de energia, que é aproveitada
para a síntese de ATP.
O processo chamado fosforilação oxidativa se refere à fosforilação do ADP em ATP
utilizando a energia liberada por essas reações de óxido-redução.
Teoria quimiosmótica
(proposta por Mitchell)
A energia livre do transporte de
elétrons é conservada pelo
bombeamento de H+ da matriz
mitocondrial para o espaço
intermembrana.
Esta translocação de prótons cria um
gradiente de concentração de H+ e de
carga elétrica através da membrana
mitocondrial interna.
O potencial eletroquímico desse
gradiente é aproveitado para a
síntese de ATP.
Profª Eleonora – Slide de aula
Potencial redox de alguns
sistemas biológicos
A partir destes valores
é possível calcular, não
só a variação de
potencial de uma reação
de oxidação-redução,
como a variação de
energia livre que
acompanha essa
transformação.
Oxidante
Redutor
n
E0’ (V)
Ácido Succínico + CO2
Ácido α-cetoglutárico
2
- 0,67
Ferredoxina (oxidada)
Ferredoxina (reduzida)
1
- 0,43
2 H+
H2
2
- 0,42
Ácido α-cetoglutárico
Ácido isocítrico
2
- 0,38
NAD+ (NADP+)
NADH+H+ (NADPH+H+)
2
- 0,32
Ácido lipóico (oxidado)
Ácido lipóico (reduzido)
2
- 0,29
FAD
FADH2
2
- 0,22
Acetaldeído
Etanol
2
- 0,20
Ácido pirúvico
Ácido láctico
2
- 0,19
Ácido oxaloacético
Ácido málico
2
- 0,17
FMN
FMNH2
2
- 0,12
Ácido fumárico
Ácido succínico
2
+ 0,03
Citocromo b (+3)
Citocromo b (+2)
1
+ 0,04
Coenzima Q
Coenzima QH2
2
+ 0,10
Citocromo c1 (+3)
Citocromo c1 (+2)
1
+ 0,22
Citocromo c (+3)
Citocromo c (+2)
1
+ 0,25
Citocromos a/a3 (+3)
Citocromos a/a3 (+2)
1
+ 0,28
O2
H2O
2
+ 0,81
Observação: Em Bioquímica, as formas reduzidas (AH2) e oxidadas (A) do substrato têm nomes diferentes.
Por exemplo, a forma oxidada do ácido succínico (ou succinato) é o ácido fumárico (ou fumarato).
Profª Eleonora – Slide de aula
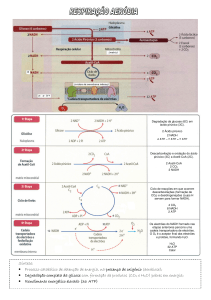
Etapas da Cadeia Respiratória que Permitem a Fosforilação do ADP em ATP
A designação fosforilação oxidativa resulta da possibilidade de conjugação entre oxirredução e
fosforilação de ADP a ATP.
Como a formação de ATP a partir de ADP + Pi necessita de cerca de 7,5 kcal, poder-se-ia
concluir que cada etapa da cadeia respiratória na qual a energia liberada fosse superior a 7,5
kcal permitiria a síntese de 1 ATP. De fato, não é essa, exatamente, a estequiometria do
processo. Mas são, sem dúvida, essas etapas que geram energia para a síntese do ATP.
∆E0’
∆G0’ (**)
(volt)
(kcal/mol NADH)
NADH + H+ + FMN → NAD+ + FMNH2
0,20 (1)
- 9,2 (2)
FMNH2 + Q → FMN + QH2
+ 0,22
- 10,2 (*)
QH2 + cit b (+3) → Q + cit b (+2)
- 0,06
+ 2,8
cit b (+2) + cit c1 (+3) → cit b (+3) + cit c1 (+2)
+ 0,18
- 8,3 (*)
cit c1 (+2) + cit c (+3) → cit c1 (+3) + cit c (+2)
+ 0,03
- 1,4
cit c (+2) + cit a/a3 (+3) → cit c (+3) + cit a/a3 (+2)
+ 0,03
- 1,4
cit a/a3 (+2) + 1/2 O2 + 2 H → cit a/a3 (+3) + H2O
+ 0,53
- 24,5 (*)
+ 1,13
- 52,2
Reações
Obtêm-se fazendo E0’ (FMN/FMNH2) – E0’ (NAD+/NADH) = - 0,12 – (- 0,32) V
Coenzima Q (Q) é móvel. Do NADH à Q pode-se contar como uma única etapa.
No caso do aceptor ser o FAD esta primeira etapa é “saltada”.
(*) Etapas capazes de gerar ATP
(**) Variação de energia livre: ∆G0’ = - n F ∆E0’ Onde: n = 2; F = equivalente energético do Faraday
(23,06 kcal.volt-1. mol-1); ∆E0’ = diferença entre o potencial de oxirredução de dois sistemas
(1)
(2)
Profª Eleonora – Slide de aula
Modelo Quimiosmótico para Mitocôndria
A teoria quimiosmótica, para explicar o mecanismo de fosforilação oxidativa e o seu impacto no
campo de bioenergética, rendeu a Peter Mitchell o prêmio Nobel em 1978.
Profª Eleonora – Slide de aula
Transporte de elétrons acoplado a fosforilação oxidativa
Estrutura da ATP sintase
Quando o co-fator (NADH ou FADH2) é oxidado por transferir seus elétrons ao O2, a energia livre é
recuperada e utilizada para impulsionar a formação de ATP.
O ATP formado é exportado da mitocôndria e fornece a energia necessária para o metabolismo celular
Profª Eleonora – Slide de aula
Acoplamento da produção de ATP ao transporte de elétrons
As reações de oxidação que liberam energia originam o bombeamento de prótons e,
consequentemente, o gradiente de pH pela membrana mitocondrial interna.
Além do gradiente de pH há uma diferença de voltagem pela membrana, formada pelas
diferenças de concentração de íons nos lados interno e externo. A energia do potencial
eletroquímico (queda de voltagem) pela membrana é convertida em energia química
armazenada pelo ATP no processo de acoplamento.
Um termo chamado razão P/O é usado para indicar o acoplamento da produção de ATP ao
transporte de elétrons.
A razão P/O fornece o número de moles de Pi (ADP + Pi → ATP) consumidos, para cada
mol de átomos de oxigênio (½ O2 + 2 H+ + 2 e- → H2O) consumidos na reação .
O oxigênio é o aceptor final de elétrons do NADH e ½ mol de moléculas de O2 (um mol de
átomos de oxigênio) é reduzido para cada mol de NADH oxidado.
A razão P/O determinada experimentalmente é 2,5 quando o NADH é o substrato
oxidado. A razão P/O é 1,5 quando FADH2 é o substrato oxidado (valor experimental).
Observação: até recentemente, os bioquímicos utilizavam os valores integrais de 3 e 2 para as
razões P/O por oxidação de NADH e FADH2, respectivamente.
O consenso de números não-inteiros utilizados aqui destaca a complexidade do transporte de
elétrons, da fosforilação oxidativa e da maneira como os dois estão acoplados.
Profª Eleonora – Slide de aula
Inibidores da Cadeia Respiratória
Rotenona: Extremamente tóxico. Extraído de plantas e usado como veneno, pelos índios
na Amazônia.
Bloqueia o transporte de elétrons entre NADH e Ubiquinona
Antimicina A: Antibiótico tóxico.
Bloqueia o transporte de elétrons entre Ubiquinona e Citocromo C
Cianeto
Bloqueia a redução do O2 pelo Citocromo aa3
Esquema da cadeia respiratória e os pontos de bloqueio no transporte de elétrons
NADH
NADH →
→ [FMN-FeS]
[FMN-FeS] →
→Q
Q→
→ [b
[b FeS
FeS CC11]] →
→ CC →
→ aa
aa33
Rotenona
Rotenona
Antimicina
Antimicina A
A
½
½O
O22
H
H22O
O
Cianeto
Cianeto
Monóxido
Monóxido de
de carbono
carbono
Ácido
Ácido sulfúrico
sulfúrico
Profª Eleonora – Slide de aula
Agentes Desacopladores
Permitem que o transporte de elétrons ocorra na mitocôndria
Impedem a fosforilação oxidativa do ADP em ATP
Desacoplam a ligação essencial entre o transporte de elétrons e a síntese do ATP
Exemplo: 2,4-Dinitrofenol





![RESPIRAÇÃO CELULAR - cursinho [Modo de Compatibilidade]](http://s1.studylibpt.com/store/data/006022270_1-d7809a9e0b738c97fd21dbd36ad9456f-300x300.png)