Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
1
EXERCÍCIOS DE APROFUNDAMENTO:
01) (UEL-PR) X é uma substância gasosa nas condições ambientes. Quando liquefeita, praticamente não
conduz corrente elétrica, porém forma solução aquosa que conduz bem a eletricidade. Uma fórmula
provável para X é:
a)
b)
c)
d)
e)
KBr.
HCl.
Ar.
N2.
O3.
02) (FCB-ARARAS-SP) Após a ionização de um ácido em água, observou-se que o número de moléculas
ionizadas era o quádruplo do número de moléculas não-ionizadas. Com base nessa observação, a
porcentagem de ionização do referido ácido era:
a)
b)
c)
d)
e)
25%.
40%.
70%.
75%.
80%.
03) Adicionando 500 moléculas de HCl à água, quantas estarão ionizadas sabendo-se que o grau de
ionização é 0,9?
a)
b)
c)
d)
e)
500.
450.
360.
50.
400.
04) O grau de ionização do HCN é 0,00008. Quantas moléculas de HCN devem ser adicionadas à água que
encontremos 160 ionizadas?
a)
b)
c)
d)
e)
2000000.
200000.
20000.
2000.
200.
05) (Covest-98) Considere a figura abaixo:
e as seguintes possibilidades para o líquido existente no interior do copo:
(I) H2O
(II) H2O + glicose
(III) H2O + sal de cozinha
Qual alternativa que melhor descreve a condição da lâmpada?
a)
b)
c)
d)
e)
Acesa em II e apagada nas demais.
Apagada em I e acesa nas demais.
Apagada em I e II.
Acesa em I, II e III.
Acesa em I e apagada nas demais.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
2
06) Qual das substâncias abaixo provoca um brilho mais intenso na lâmpada, se adicionada à água?
a)
b)
c)
d)
e)
HCN
NH3
HClO4
CH3COOH
C6H6
07) O fato de uma solução permitir a passagem da corrente elétrica nos permite concluir que o soluto:
a)
b)
c)
d)
e)
também conduz a corrente elétrica quando puro.
tem todas as suas moléculas ionizadas.
é iônico.
é molecular.
pode ser iônico ou molecular.
08) Duas substâncias que, em solução aquosa, apresentam íons são:
a)
b)
c)
d)
e)
cloreto de sódio (NaCl) e álcool etílico (C2H6O).
sacarose (C12H22O11) e álcool etílico (C2H6O).
sacarose (C12H22O11) e ácido sulfúrico (H2SO4).
ácido sulfúrico (H2SO4) e cloreto de sódio (NaCl).
sacarose (C12H22O11) e cloreto de sódio (NaCl).
09) Dos seguintes sólidos:
I.
II.
III.
IV.
glicose (C6H12O6).
dióxido de silício (SiO2).
óxido de magnésio (MgO).
acetato de sódio (H3CCOO-Na+).
Conduzem corrente elétrica no estado de fusão.
a)
b)
c)
d)
e)
I e II.
I e III.
II e III.
II e IV.
III e IV.
10) Observe a figura. Ela representa um circuito elétrico.O béquer contém água pura, à qual adiciona-se
uma das seguintes substâncias: KOH(s), C6H6(l), HCl(g), Fe(s), NaCl(s)
Após essa adição, a lâmpada pode ou não acender. Indique quantas dessas substâncias fariam a
lâmpada acender?
a)
b)
c)
d)
e)
5.
4.
3.
2.
1.
11) O ácido clorídrico puro (HCl) é um composto que conduz muito mal a eletricidade. A água pura (H2O) é
um composto que também conduz muito mal a eletricidade; no entanto, ao dissolvermos o ácido na
água, formamos uma solução que conduz muito bem a eletricidade, o que se deve à:
a)
b)
c)
d)
e)
dissociação da água em H+ e OH – .
ionização do HCl, formando H3O+ e Cl –.
transferência de elétrons da água para o HCl.
transferência de elétrons do HCl para a água.
reação de neutralização do H+ da água com o Cl – do HCl.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
3
12) (FGV-SP) Alguns compostos, quando solubilizados em água, geram uma solução aquosa que conduz
corrente elétrica. Dos compostos abaixo:
I. Na2SO4.
II. O2.
III. C12H22O11.
IV. KNO3.
V. CH3COOH.
VI. NaCl.
Formam-se solução aquosa que conduz eletricidade:
a)
b)
c)
d)
e)
apenas I, IV e VI.
apenas I, IV, V e VI.
apenas I e VI.
apenas VI.
Todos.
ÁCIDOS DE ARRHENIUS
13) Dentre as espécies químicas, citadas, é classificado como ácido de Arrhenius:
a)
b)
c)
d)
e)
Na2CO3
KOH
Na2O
HCl
LiH
14) (Esal-MG) Uma solução aquosa de H3PO4 é ácida devido à presença de:
a)
b)
c)
d)
e)
água.
hidrogênio.
fósforo.
hidrônio.
fosfato.
15) Admitindo-se 100% de ionização para o ácido clorídrico em solução aquosa, pode-se afirmar que essa
solução não contém a espécie:
a)
b)
c)
d)
e)
HCl.
OH – .
H3O+.
H2O.
Cl – .
16) Ao dissociar em água destilada o ácido ortofosfórico (H3PO4), resultam como cátion e ânion:
a)
b)
c)
d)
e)
3–
3 H+(aq) e PO4 (aq).
+
–
PO4 (aq) e 3 H (aq).
3+
+
PO4 (aq) e H (aq).
2 H+(aq) e PO42 – (aq).
+
2–
3 H (aq) e HPO4 (aq).
17) Qual das substâncias a seguir apresenta sabor azedo quando em solução aquosa?
a)
b)
c)
d)
e)
Na2S.
NaCl.
CaO.
HCl.
NaOH.
18) Todas as substâncias azedas estimulam a secreção salivar, mesmo sem serem ingeridas. Esse é o
principal motivo de se utilizar vinagre ou limão na preparação de saladas, pois o aumento da secreção
salivar facilita a ingestão. No vinagre e no limão aparecem substâncias pertencentes à função:
a)
b)
c)
d)
e)
base ou hidróxido.
sal.
óxido.
aldeído.
ácido.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
4
19) Identifique a alternativa que apresenta somente diácidos:
a)
b)
c)
d)
e)
H2S, H2SO4, H3PO4, H3PO3.
HCN, H2S, H3PO4, H3PO3.
H2S, H2SO4, H2CO3, H3PO3.
HCl, H2S, H2SO4, H3PO3.
H2SO4, H2SO3, HNO3, H3PO2.
20) (MACKENZIE-SP) Alguns moluscos, para defender-se dos predadores, liberam um diácido, cuja fórmula
é:
a) NaOH.
b) K2O.
c) Li2CO3.
d) H2SO4.
e) H3PO4.
21) UVA-CE) Os ácidos HClO4, H2MnO4, H3PO3, H4Sb2O7, quanto ao número de hidrogênios ionizáveis,
podem ser classificados em:
a)
b)
c)
d)
e)
monoácido, diácido, triácido, tetrácido.
monoácido, diácido, triácido, triácido.
monoácido, diácido, diácido, tetrácido.
monoácido, monoácido, diácido, triácido.
monoácido, monoácido, triácido, tetrácido.
–2
22) Na ionização total de um ácido, obtém-se íons HPO3 e hidroxônio. Para a fórmula do ácido e para o
número total de íons hidroxônio temos, respectivamente:
a)
b)
c)
d)
e)
H3PO3 e 2.
H3PO3 e 1.
HPO3 e 2.
H3PO4 e 2.
H3PO3 e 3.
23) Considere uma substância cuja fórmula é H3PO4. Essa substância é composta por:
a)
b)
c)
d)
e)
dois elementos.
três elementos.
oito elementos.
quatro elementos.
doze elementos.
24) O ácido que corresponde à classificação monoácido, oxiácido e forte é:
a)
b)
c)
d)
e)
HNO3.
HCl.
H2SO4.
HCNO.
H3PO4.
25) Entre os oxiácidos H2SO3, H3BO3, HClO3 e HMnO4, a ordem crescente de força ácida para esses
compostos é:
a)
b)
c)
d)
e)
H2SO3, HClO3, H3BO3, HMnO4.
HClO3, HMnO4, H2SO3, H3BO3.
H3BO3, HClO3, H2SO3, HMnO4.
H3BO3, H2SO3, HClO3, HMnO4.
HMnO4, HClO3, H3BO3, H2SO3.
26) O vinagre tem caráter ácido, pois nele encontraremos predominantemente:
a)
b)
c)
d)
e)
ácido sulfúrico.
ácido carbônico.
ácido nítrico.
ácido sulfônico.
ácido acético.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
5
27) Sejam os produtos:
I . água de bateria.
II. água mineral com gás.
III. ácido muriático.
Os ácidos presentes nesses produtos são, respectivamente:
a)
b)
c)
d)
e)
HCl, H2CO3, H2SO4.
H3PO4, H2SO4, HCl.
H2SO4, H3PO4, HCl.
HCl, H2CO3, HF.
H2SO4, H2CO3, HCl.
28) O HCl, quanto ao n.º de hidrogênios ácidos, elementos químicos, presença do carbono, presença do
oxigênio e estado físico, classifica-se, respectivamente, como:
a)
b)
c)
d)
e)
monoácido, ternário, inorgânico, oxiácido, líquido.
monoácido, binário, inorgânico, hidrácido, gasoso.
biácido, binário, inorgânico, oxiácido, gasoso.
biácido, ternário, orgânico, hidrácido, gasoso.
monoácido, binário, orgânico, hidrácido, líquido.
29) Considerando-se, exclusivamente, a diferença entre o número de oxigênios e o número de hidrogênios
ionizáveis, em cada ácido, indique o par a seguir em que o ácido à esquerda é mais forte que o ácido à
direita.
a)
b)
c)
d)
e)
H3BO3 e HNO3.
HClO4 e H2SO4.
HClO e HClO4.
H3PO4 e HNO3.
H3PO2 e HNO3.
30) O esquema a seguir mostra a aparelhagem que pode ser utilizada para testar a força dos ácidos. Em
qual das soluções, todas com mesma concentração e temperatura, a lâmpada apresenta maior brilho?
a) HF.
b) H2S.
c) H3PO4.
d) H4SiO4.
e) HNO3.
31) Um dos compostos responsável pela chuva ácida é o HNO3, o qual pode-se dizer que:
a)
b)
c)
d)
e)
chama-se ácido nitroso.
é um triácido.
é um ácido moderado.
possui grau de ionização maior que 50%.
denomina-se óxido de nitrogênio.
32) Considere os seguintes ácidos, com seus respectivos graus de ionização, a 18°C e usos:
I.
II.
III.
IV.
H3PO4 (27%), usado na preparação de fertilizantes e como acidulante em bebidas e refrigerantes.
–2
H2S (7,6 x 10 %), usado como redutor.
HClO4 (97%), usado na medicina, em análises químicas e como catalisador em explosivos.
– 3
HCN (8,0 x 10 %), usado na fabricação de plásticos, corantes e fumigantes para orquídeas e
poda de árvores.
Podemos afirmar que é correto:
a)
b)
c)
d)
e)
HClO4 e HCN são triácidos.
H3PO4 e H2S são hidrácidos.
H3PO4 é considerado um ácido semiforte.
H2S é um ácido ternário.
O HCN é o mais forte de todos os ácidos citados.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
6
33)(UFPE) Vinagre caseiro é essencialmente uma solução de ácido acético a 4% em água. Esta solução
diferentemente de água pura, conduz eletricidade razoavelmente bem. O vinagre pode ilustrar idéias
importantes, tais como:
0
1
2
3
4
0
1
2
3
4
Substâncias covalentes nunca dão origem a íons.
O ácido acético pode dar origem a íons.
O ácido acético não interage quimicamente com a água.
A água é uma substância covalente e o ácido acético é um composto iônico.
A água e o ácido acético são substâncias polares
CURIOSIDADE
Ácido, bactérias e úlceras
Durante muitos anos acreditou-se que as úlceras eram causadas pelo excesso de ácido
clorídrico no estômago. Esse excesso de acidez teria, como causas, o consumo de alimentos
condimentados, de bebidas alcoólicas e de antiinflamatórios, como aspirina; o stress; o hábito de
fumar.
No entanto, em 1980, o médico australiano Barry J. Marshall provou que a maior parte das
úlceras era causada por uma espécie de bactéria que vive na mucosa gástrica, denominada
Heliocbacter pylori. Essa bactéria, e não o excesso de ácido, é que corrói as paredes do estômago.
Estudos posteriores não só confirmaram a descoberta do Dr. Marshall como relacionaram essa
bactéria ao câncer do estômago.
Com a descoberta, o tratamento de úlceras passou a ser feito com antibióticos e não mais com
dietas, da ingestão de antiácidos e de medicamentos que controlam a produção do ácido clorídrico.
34) Considere o seguinte composto:
O
H
O
P
O
H
H
Assinale (V) se a afirmativa for verdadeira e (F) se for falsa.
O composto apresenta três hidrogênios ionizáveis.
O composto apresenta quatro ligações covalentes normais e uma dativa.
O composto é um diácido.
O composto pertence a uma função orgânica.
A seqüência correta, de cima para baixo, é:
a)
b)
c)
d)
e)
V, V, V, F.
F, F, V, F.
F, V, F, V.
V, F, F, V.
V, F, F, F.
35) (CEESU – 2003) Durante a digestão de alimentos no estômago, ocorre a fundamental precipitação de
um determinado composto químico.
Identifique o composto.
a)
b)
c)
d)
e)
bicarbonato de sódio.
hidróxido de alumínio.
ácido clorídrico.
monóxido de carbono.
ácido sulfúrico.
36) (UFPE) Ácido perclórico (HClO4) é um ácido forte. Quais as espécies químicas presentes, em maior
concentração, em uma solução aquosa deste ácido?
a)
b)
c)
d)
e)
+
–
H e ClO4 .
HClO4 e H+.
–
HClO4 e OH .
+
–
H , Cl e O2.
OH –, Cl – 1 e O2.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
7
37) A fórmula do ácido perclórico é:
a)
b)
c)
d)
e)
HCl.
HClO.
HClO2.
HClO3.
HClO4.
38) (FEI-SP) Os nomes dos ácidos oxigenados abaixo são, respectivamente:
HNO2 (aq), HClO3 (aq), H2SO3 (aq), H3PO4 (aq)
a)
b)
c)
d)
e)
nitroso, clórico, sulfuroso, fosfórico.
nítrico, clorídrico, sulfúrico, fosfórico.
nítrico, hipocloroso, sulfuroso, fosforoso.
nitroso, perclórico, sulfúrico, fosfórico.
nítrico, cloroso, sulfídrico, hipofosforoso.
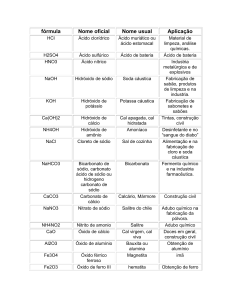
39)(PUC-MG) A tabela apresenta algumas características e aplicações de alguns ácidos:
Nome do ácido
Aplicações e características
Ácido muriático
Limpeza doméstica
Ácido fosfórico
Ácido sulfúrico
Ácido nítrico
Usado como acidulante
Desidratante, solução de bateria
explosivos
As fórmulas dos ácidos da tabela são, respectivamente:
a)
b)
c)
d)
e)
HCl, H3PO4, H2SO4, HNO3.
HClO, H3PO3, H2SO4, HNO2.
HCl, H3PO3, H2SO4, HNO2.
HClO2, H4P2O7, H2SO3, HNO2.
HClO, H3PO4, H2SO3, HNO3.
40) (Mackenzie-SP) Certo informe publicitário alerta para o fato de que, se o indivíduo tem azia ou pirose
com grande freqüência, deve procurar um médico, pois pode estar ocorrendo refluxo gastroesofágico,
isto é, o retorno do conteúdo ácido estômago. A fórmula e o nome do ácido que, nesse caso, provoca
queimação no estômago, a rouquidão e mesmo dor toráxica são:
a)
b)
c)
d)
e)
HCl e ácido clórico.
HClO2 e ácido cloroso.
HClO3 e ácido clórico.
HClO3 e ácido clorídrico.
HCl e ácido clorídrico.
41) O ácido cianídrico é o gás de ação venenosa mais rápida que se conhece; uma concentração de
0,3 mg/L de ar é imediatamente mortal. É o gás usado nos estados americanos do norte que adotam a
pena de morte por câmara de gás. A primeira vítima foi seu descobridor, Carl Withelm Scheele, que
morreu ao deixar cair um vidro contendo solução de ácido cianídrico, cuja fórmula molecular é:
a)
b)
c)
d)
e)
HCOOH.
HCN.
HCNS
HCNO.
H4Fe(CN)6.
42) (UNIV.BRÁS CUBAS-SP) No laboratório de uma escola, encontrou-se um frasco antigo com rótulo
parcialmente destruído. Apenas a palavra ácido estava legível. O líquido apresentava coloração
avermelhada e, depois de algumas análises feitas pelos alunos, constatou-se a presença de NO2. No
rótulo, deveria estar identificado o ácido:
a)
b)
c)
d)
e)
nítrico.
fosfórico.
clorídrico.
sulfúrico.
carbônico.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
8
43) (CEESU – 2003) Os gases e fuligens, que resultam de atividades humanas, interferem no processo de
formação das nuvens que resultam...
a)
b)
c)
d)
e)
na manutenção da composição de grupos de átomos.
em fonte de energia própria.
em chuvas ácidas.
no processo de evapotranspiração.
tempestades.
BASES
44) Qual das substâncias abaixo pode ser considerada base de Arrhenius?
a)
b)
c)
d)
e)
CH3COOH.
HCl.
KOH.
H2SO4.
CH3OH.
45)(Osec-SP) Uma base forte deve ter o grupo OH – ligado a um:
a)
b)
c)
d)
e)
elemento muito eletropositivo.
elemento muito eletronegativo.
semimetal.
metal que forneça 3 elétrons.
ametal.
46) Sabor adstringente é o que percebemos quando comemos uma banana verde (não-madura). Que
substância a seguir teria sabor adstringente?
a)
b)
c)
d)
e)
CH3COOH.
NaCl.
Al(OH)3.
C12H22O11.
H3PO4.
47) (FAEE-GO) O hidróxido de magnésio, Mg(OH)2, que é um componente do “leite de magnésia”, é:
a)
b)
c)
d)
e)
um ácido de Arrhenius.
uma base de Arrhenius.
um sal.
um óxido.
um hidreto.
48) Um médico atendeu a um paciente com dores abdominais originadas de uma patologia denominada
úlcera péptica duodenal. Para tratamento desse paciente, o médico prescreveu um medicamento que
contém um hidróxido metálico classificado como uma base fraca. Esse metal pertence, de acordo com a
tabela de classificação periódica, ao seguinte grupo da:
a)
b)
c)
d)
e)
I A.
III A.
IV A.
II A.
zero.
49) A formação do hidróxido de alumínio, Al(OH)3, resultante da reação de um sal desse metal com uma
base pode ser representada por:
a)
b)
c)
d)
e)
Al +
Al 2+
3+
Al
Al 4+
Al 5+
+
+
+
+
+
OH 1 Al(OH).
2 OH 1- Al(OH)2.
13 OH
Al(OH)3.
4 OH 1- Al(OH)4.
5 OH 1- Al(OH)5.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
9
50) (PUC-MG) A dissolução de uma certa substância em água é representada pela equação abaixo:
M(OH) 3 ( s )
H2O
M 3+
+ 3 OH (aq)
( aq )
Pode representar a dissolução de:
a)
b)
c)
d)
e)
amônia.
hidróxido de cálcio.
hidróxido de sódio.
hidróxido de alumínio.
brometo de hidrogênio.
51) (MACKENZIE-SP) A base, que na dissociação iônica total produz um número de hidroxilas, por mol,
igual ao número de cátions obtidos na ionização total do ácido sulfúrico, é:
a)
b)
c)
d)
e)
Mg(OH)2.
NaOH.
NH4OH.
Al(OH)3.
Pb(OH)4.
52) O gás contido em um cilindro metálico, após a abertura da válvula do cilindro, foi borbulhado em água
contendo o indicador fenolftaleína. Obteve-se solução acentuadamente avermelhada. O gás em
questão poderá ser:
a)
b)
c)
d)
e)
amônia.
dióxido de carbono.
dióxido de enxofre.
cloreto de hidrogênio.
nitrogênio.
53) Entre as bases dadas a seguir, indique quais são praticamente insolúveis em água:
I) KOH; II) Mg(OH)2 ; III) NaOH; IV) Al(OH)3; V) Fe(OH)2; VI) LiOH
a)
b)
c)
d)
e)
V e VI.
IV e V.
II, III, IV.
II, IV, V.
I, III, VI.
54) Assinale a alternativa que apresenta dois produtos caseiros com propriedades alcalinas:
a)
b)
c)
d)
e)
detergente e vinagre.
sal e coalhada.
leite de magnésia e sabão.
bicarbonato e açúcar.
coca – cola e água de cal.
55) De uma certa substância, faz-se às afirmações a seguir:
I.
Reage com ácido, dando sal e água.
II. Em presença de água, sofre dissociação iônica parcial.
III. Em solução aquosa, torna a fenolftaleína vermelha.
A substância que se enquadra nas propriedades dadas é:
a)
b)
c)
d)
e)
BaSO4.
CH4.
Mg(OH)2.
SO3.
HCl.
56) (UEPG-PR) Com relação às propriedades das bases de Arrhenius, é incorreto afirmar:
a) O hidróxido de amônio é uma base não-metálica, bastante solúvel em água.
b) Os metais alcalinos formam monobases com alto grau de dissociação.
c) As bases formadas pelos metais alcalinos terrosos são fracas, visto que são moleculares por
natureza.
d) Os hidróxidos dos metais alcalinos terrosos são pouco solúveis em água.
e) Uma base é tanto mais forte quanto maior for o seu grau de ionização.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
10
57) Em relação às bases de Arrhenius:
0
1
2
3
4
0
1
2
3
4
Sofrem ionização em meio aquoso.
Possuem o hidróxido, OH – , como único ânion.
As bases fortes possuem acentuado caráter iônico.
Sofrem dissociação em meio aquoso.
Possuem sabor adstringente característico.
58) (UPE-2005-Q1) Qual das afirmativas abaixo se aplica ao hidróxido de amônio?
a) É uma base forte, solúvel em água destilada e bem estável em temperaturas altas.
b) É uma base fraca, pouco solúvel em água destilada, mas muito estável em função da atração
1+
1elétrica entre os íons NH4 e OH .
c) A molécula do hidróxido de amônio é fortemente polar, tem geometria tetraédrica, com a oxidrila
ocupando o centro do tetraedro.
d) Na prática, quando se fala do grau de ionização do hidróxido de amônio, refere-se, portanto, ao
grau de ionização do NH3.
e) É a única base da química inorgânica que, dissolvida em água, origina um meio neutro em função
da volatilidade da amônia.
Comentários: Não existe hidróxido de amônio, e sim amônia em solução aquosa, formando uma base
fraca.
59) O hidróxido de sódio é um sólido iônico branco, altamente higroscópico. Sendo uma base muito forte,
possui efeito altamente corrosivo sobre a pele.
A fórmula química do hidróxido de sódio é __________ e, quanto à força podemos classifica-la como
uma base _________ . Respectivamente, podemos completar corretamente a afirmação acima com:
a)
b)
c)
d)
e)
a) HCl ; forte.
NaOH ; moderada.
NaOH ; fraca.
NaOH ; forte
HCl ; fraca.
60) (Mackenzie-SP)
Força e solubilidade de bases em água
Bases dos metais
alcalinos
Fortes e solúveis
Bases dos metais
alcalinos terrosos
Fortes e parcialmente solúveis,
esceto a de magnésio, que é fraca
Demais bases
Fracas e praticamente insolúveis
Para desentupir um cano de cozinha e para combater a acidez estomacal, necessita-se
respectivamente, de uma base forte e solúvel e de uma base fraca e parcialmente solúvel.
Consultando a tabela acima, conclui-se que as fórmulas dessas bases podem ser:
a)
b)
c)
d)
e)
Ba(OH)2 e Fe(OH)3.
Al(OH)3 e NaOH.
KOH e Ba(OH)2.
Cu(OH)2 e Mg(OH)3.
NaOH e Mg(OH)2.
61) Sobre o hidróxido ferroso [Fe(OH)2 ] pode-se afirmar que:
a)
b)
c)
d)
e)
É uma base de Arrhenius fraca e praticamente insolúvel em água.
É uma tribase.
Sofre ionização libertando três íons hidrônio.
Reage com o ácido sulfuroso produzindo o sulfato ferroso.
Tem grau de ionização maior que 90%.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
11
62) Considere a ionização total do ácido fosfórico (H3PO4):
H3PO4 3 H 1+ + PO4 3-
Identifique a alternativa que apresenta uma base que, na sua dissociação total, produz o mesmo
número de íons, por fórmula, que o ácido fosfórico:
a)
b)
c)
d)
e)
hidróxido de sódio.
hidróxido de cálcio.
hidróxido de prata.
hidróxido de alumínio.
hidróxido de bário.
63) (UNIUBE-MG) Na natureza não são encontradas jazidas de ácido sulfúrico, ácido nítrico, ácido
clorídrico, soda cáustica, cal extinta etc. Todos são fabricados industrialmente.
As fórmulas das substâncias mencionadas no texto são, respectivamente:
a)
b)
c)
d)
e)
H2SO3, HNO3, HClO2, Ca(OH)2, CaO.
H2SO4, HNO2, HClO4, NaOH, Ca(OH)2.
H2SO4, HNO2, HCl, Ca(OH)2, CaO.
H2SO3, HNO2, HClO4, NaOH, CaO.
H2SO4, HNO3, HCl, NaOH, Ca(OH)2.
64) “O progresso está fazendo com que o meio ambiente fique cada fez mais poluído, o que nos leva a
refletir até que ponto isto nos trás benefícios. Observando a figura podemos constatar que os óxidos
provenientes de fabricas e escapamentos dos automóveis formam com a água os compostos H2SO4 e
HNO3, que caem como chuva ácida. Estes ácidos presentes no ar e na chuva prejudicam as pessoas,
envenenando lagos, matando plantas e animais aquáticos”.
Uma possível forma de diminuir a acidez no solo e nos lagos seria a adição de uma substância
capaz de anular as características do H2SO4 e do HNO3, ou seja, uma substância básica. Entre as
espécies abaixo, qual substância tem propriedades básicas ou alcalinas?
a)
b)
c)
d)
e)
NaCl.
H2O.
HCl.
SO3.
NaOH.
65) O ácido clorídrico é muito usado industrialmente na manufatura de corantes. Com o nome de ácido
muriático ele é largamente empregado na limpeza em geral, não podendo ser utilizado, no entanto, em
pisos de mármore, os quais são constituídos de carbonato de cálcio. Se por acidente um pouco de
ácido muriático cair sobre um piso de mármore, entre os produtos citados abaixo, normalmente
encontrados em qualquer residência, o mais indicado para se espalhar sobre o local será:
a)
b)
c)
d)
e)
vinagre.
suco de limão.
sal de cozinha.
suco de tomate.
amoníaco.
66) (FMU-SP) A neutralização total de um mol de hidróxido de magnésio consome um mol de...
a)
b)
c)
d)
e)
ácido clorídrico.
ácido sulfúrico.
hidróxido de sódio.
hidróxido de cálcio.
hidróxido de alumínio.
67) (Mackenzie-SP) Observe as fórmulas do sulfato de amônio [(NH4)2SO4] e do hidróxido de potássio
(KOH) e assinale a alternativa que apresenta a fórmula do hidróxido de amônio, substância presente em
alguns produtos de limpeza.
a)
b)
c)
d)
e)
NH4+.
(NH4)2OH.
NH4(OH)2.
NH4OH.
NH4(OH)4.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
12
68) (Mackenzie-SP) O suco gástrico necessário à digestão contém ácido clorídrico que, em excesso, pode
provocar “dor de estômago”. Neutraliza-se esse ácido, sem risco, ingerindo-se:
a)
b)
c)
d)
e)
solução aquosa de base forte, NaOH.
solução aquosa de cloreto de sódio, NaCl.
suspensão de base fraca, Al(OH)3.
somente água.
solução concentrada de ácido clorídrico, HCl.
69) (PUC-MG) Urtiga é o nome genérico dado a diversas plantas da família das Urticácias, cujas folhas são
cobertas de pêlos finos, os quais liberam ácido fórmico (H2CO2) que, em contato com a pele, produz
uma irritação.
Dos produtos de uso doméstico abaixo, o que você utilizaria para diminuir essa irritação é:
a)
b)
c)
d)
e)
vinagre.
sal de cozinha.
óleo.
coalhada.
leite de magnésia.
70) (FEI-SP) Num recipiente contendo uma substância A, foram adicionadas gotas de fenolftaleína, dando
uma coloração rósea. Adicionando-se uma substância B em A, a solução apresenta-se incolor. Com
base nessas informações podemos afirmar que:
a)
b)
c)
d)
e)
A e B são bases.
A é um ácido e B é uma base.
A é uma base e B é um ácido.
A e B são ácidos.
A e B são bases.
71) Aos frascos A, B e C, contendo soluções aquosas incolores de substâncias diferentes, foram
adicionadas gotas de fenolftaleína. Observou-se que só o frasco A passou a apresentar coloração
rósea. Identifique a alternativa que indica substâncias que podem estar presentes em B e C.
a)
b)
c)
d)
e)
NaOH e NaCl.
H2SO4 e HCl.
NaOH e Ca(OH)2.
H2SO4 e NaOH.
NaCl e Mg(OH)2.
72) (Unisinos-RS) Um aluno, trabalhando no laboratório de sua escola, deixou cair uma certa quantidade de
solução alcoólica de fenolftaleína sobre o balcão que estava sendo limpo com sapólio. O local onde caiu
a fenolftaleína adquiriu, quase que imediatamente, uma coloração violácea. Esse aluno, observando a
mancha violácea, concluiu que:
a)
b)
c)
d)
e)
o sapólio deve ser um meio ácido.
o sapólio de deve ser um meio alcalino.
o sapólio deve ser um meio neutro.
o sapólio tem características de um sal.
a fenolftaleína removeu o sapólio do local.
73) (UEPI) O sangue do diabo é um líquido vermelho que logo se descora ao ser aspergido sobre um tecido
branco. Para prepará-lo, adiciona-se NH4OH em água, contendo algumas gotas de fenolftaleína. A cor
desaparece porque:
a)
b)
c)
d)
e)
o tecido branco reage com a solução formando o ácido amoníaco.
a fenolftaleína evapora.
a fenolftaleína reage rapidamente com o NH4OH.
o NH3 logo evapora.
a solução é assim denominada devido à sua alta viscosidade.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
13
74) (UPE-2007 – Q1) Um aluno preparou uma solução, colocando em um erlenmeyer 20,0 mL de álcool
etílico, cinco gotas de azul de bromotimol e uma gota de solução de hidróxido de sódio 1,0 mol/L. A
solução resultante apresentou uma coloração azulada. O aluno, invocando poderes mágicos, solicitou a
um colega de turma que pronunciasse perto da boca do erlenmeyer que continha a solução a seguinte
frase: “Muda de cor solução”. Após pronunciar várias vezes essa frase, a solução mudou sua coloração
de azul para verde, para a glória do aluno mágico.
Assinale a alternativa verdadeira.
a) Não podemos duvidar dos poderes sobrenaturais que certas pessoas exercem sobre as soluções.
b) Essa solução, de algum modo inexplicável, obedeceu ao comando do aluno.
c) A reação química entre o álcool etílico e o azul de bromotimol é a responsável pela mudança de
coloração.
d) A neutralização do hidróxido de sódio pelo ácido carbônico, que se forma na solução, é a
responsável pela mudança de coloração da solução.
e) O ar exalado pelo aluno, que é rico em oxigênio atômico, oxida o álcool etílico, produzindo um ácido
que neutraliza o hidróxido de sódio, ocasionando a mudança de coloração da solução.
SAL
75) Na reação de neutralização total do ácido sulfídrico com o hidróxido de potássio, há formação de sal e
água. A fórmula e o nome correto deste sal são, respectivamente:
a) K2SO4 e sulfato de potássio.
b) K2SO3 e sulfito de potássio.
c) KS e sulfeto de potássio.
d) K2S e sulfato de potássio.
e) K2S e sulfeto de potássio.
76) Quando se reage uma fórmula de hidróxido de potássio com uma fórmula de ácido sulfúrico, obtém-se:
a) 2 fórmulas de sulfato de potássio.
b) 1 fórmula de hidrogeno - sulfato de potássio.
c) 0,5 fórmula de hidrogeno - sulfato de potássio.
d) 1 fórmula de persulfato de potássio.
e) 1 fórmula de sulfato de potássio.
77) Na neutralização parcial de um monoácido por uma dibase, resultam moléculas de água em número de:
a) 1.
b) 2.
c) 3.
d) 4.
e) 5.
78) Os produtos de neutralização parcial do ácido bromídrico (HCl) pelo hidróxido ferroso [Fe(OH)2] são:
a) FeBr2 + H2O.
b) FeBr2 + 2 H2O.
c) FeBr3 + 3 H2O.
d) FeOHBr + H2O.
e) FeOHBr + 2 H2O.
79) Sobre a reação equacionada abaixo, assinale a alternativa incorreta:
a)
b)
c)
d)
e)
2 NaOH + H2SO4 Na2SO4 + 2 H2O
Ocorre neutralização das propriedades do ácido e da base.
Há a formação de um sal neutro.
É chamada reação de ionização.
Um dos reagentes é o hidróxido de sódio.
A soma dos coeficientes do balanceamento nesta equação é igual a 6.
80) Ao participar de uma festa, você pode comer e beber em demasia, apresentando sinais de má digestão
ou azia. Para combater a acidez, ocasionada pelo excesso de ácido clorídrico no estômago, seria bom
ingerir uma colher de leite de magnésia, que irá reagir com esse ácido.
A equação que representa a reação é:
a)
b)
c)
d)
e)
Mg(OH)2 + 2 HClO Mg(ClO)2 + 2 H2O.
Mg(OH)2 + 2 HCl MgCl2 + 2 H2O.
Mg(OH)2 + 2 HClO3 Mg(ClO3)2 + 2 H2O.
Mn(OH)2 + 2 HClO2 Mn(ClO2)2 + 2 H2O.
Mn(OH)2 + 2 HCl MnCl2 + 2 H2O.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
14
81) Um caminhão transportando ácido sulfúrico capotou, derramando o ácido na estrada. O ácido foi
totalmente neutralizado por uma solução aquosa de hidróxido de sódio. Essa neutralização pode ser
corretamente representada pelas equações abaixo.
H2SO4 + 2 NaOH X + 2 H2O
H2SO4 + NaOH Y + H2O
As substâncias X e Y são, respectivamente:
a)
b)
c)
d)
e)
Na2SO4 e NaHSO4.
NaHSO4 e Na2SO4.
Na2SO3 e Na2SO4.
Na2SO4 e NaHSO3.
NaHSO3 e Na2SO4.
82) Duas fórmulas de um ácido X exigem na reação de neutralização total três de uma base Y. o ácido X e a
base Y podem ser, respectivamente:
a)
b)
c)
d)
e)
ácido carbônico e hidróxido de sódio.
ácido carbônico e hidróxido de cálcio.
ácido sulfúrico e hidróxido de alumínio.
ácido nítrico e hidróxido de alumínio.
ácido fosfórico e hidróxido de magnésio.
83) O coral nada mais é que um pequeno animal marinho, que vive em colônias, geralmente em mares de
temperatura mais amena, como as regiões tropicais e subtropicais. Enquanto está vivo, esse organismo
secreta à sua volta um esqueleto de carbonato de cálcio, substância extraída da água do mar. Após a
sua morte, novas colônias desenvolvem-se sobre essa estrutura rígida, formando, com o tempo,
paredões calcáreos que chamamos de recife.o processo todo, obviamente, demora milhares de anos.
a) O carbonato de cálcio é um sal duplo quanto ao ânion.
b) Em um laboratório poderíamos obter o carbonato de cálcio pela reação de neutralização total entre
o ácido carbônico e o hidróxido de cálcio.
c) A fórmula do carbonato de cálcio é Ca2CO3.
d) O carbonato de cálcio é um composto molecular.
e) A solubilidade do carbonato de cálcio na água aumenta diminui com a temperatura.
84) Determinados tipos de fermentos químicos, quando umedecidos, liberam gás carbônico pela reação:
2 NaHCO3 + Ca(H2PO4)2 Na2HPO4 + CaHPO4 + 2 CO2 + 2 H2O
Os componentes desses fermentos são classificados como:
a)
b)
c)
d)
e)
sais ácidos.
sais básicos.
oxiácidos.
hidrácidos.
bases inorgânicas.
85) Associe corretamente, de cima para baixo, os itens a seguir:
I
II
III
IV
Na2B4O7. 10 H2O
Mg(OH)Cl
NaKSO4
NaHCO3
sal básico.
sal duplo.
sal ácido.
sal hidratado.
A associação correta é:
a)
b)
c)
d)
e)
I, III, IV, II.
II, IV, III, I.
I, II, III, IV.
II, III, IV, I.
II, III, I, IV.
86)(UFLA-MG) O composto CuSO4 . 5 H2O é utilizado na agricultura como fungicida. Este composto é:
a)
b)
c)
d)
e)
um sal anidro.
uma base fraca.
um sal hidratado.
uma solução aquosa.
uma base forte.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
15
87) Os compostos abaixo são, respectivamente:
AgNO3
a)
b)
c)
d)
e)
NH4OH
HClO4
ácido, base, sal.
base, sal, base.
sal, base, ácido.
ácido, sal, ácido.
sal, base, base.
88) O mármore é, basicamente, formado de carbonato de cálcio (CaCO3) e, quando extremamente puro,
apresenta a cor branco-neve. É o caso do mármore carrara usado por Michelangelo em suas
esculturas. A função química a que pertence o carbonato de cálcio é:
a) base.
b) sal.
c) ácido.
d) óxido ácido.
e) óxido básico.
89) O salitre do Chile, NaNO3, utilizado como fertilizante pertence à função:
a)
b)
c)
d)
e)
sal.
base.
ácido.
óxido ácido.
óxido básico.
90) Os nomes dos compostos NaHSO3 e Fe3(PO4)2 são, respectivamente:
a)
b)
c)
d)
e)
sulfato de sódio e fosfato de ferro III.
sulfito de sódio e fosfito ferroso.
di-hidrogenossulfato de sódio e fosfato de ferro III.
sulfeto de sódio e fosfito de férrico.
hidrogenossulfito de sódio e fosfato de ferro II.
91) As fórmulas do carbonato de sódio e do nitrato de amônio são, respectivamente, Na2CO3 e NH4NO3.
Sendo assim, a fórmula do carbonato de amônio é:
a) (NH3)HCO3.
b) (NH3)2CO3.
c) NH4CO3.
d) (NH4)HCO3.
e) (NH4)2CO3.
92) Um elemento metálico M forma um sulfato de fórmula MSO4. A fórmula de seu fosfato será:
a) M3(PO4)2.
b) M2PO4.
c) M2(PO4)3.
d) MPO4.
e) M(PO4)2.
93) O líquido de Dakin, utilizado como anti-séptico, é uma solução diluída de NaCl, ou seja:
a) perclorato de sódio.
b) hipoclorito de sódio.
c) cloreto de sódio.
d) clorato de sódio.
e) clorito de sódio.
94) No processo de produção de sal refinado, a lavagem do sal marinho provoca a perda do iodo natural,
sendo necessário, depois, acrescenta-lo na forma de iodeto de potássio. Outra perda significativa é a
de íons magnésio, presentes no sal marinho na forma de cloreto de magnésio e sulfato de magnésio.
Durante este processo são também adicionados alvejantes, como o carbonato de sódio. As fórmulas
representativas das substâncias destacadas no texto anterior são, respectivamente:
a) KI, MgCl, MgSO4 e NaCO3.
b) K2I, MgCl2, Mg2SO4 e Na2CO3.
c) K2I, Mg2Cl, MgSO4 e Na(CO3)2.
d) KI, MgCl2, MgSO4 e Na2CO3.
e) KI2, Mg2Cl, Mg(SO4)2 e Na3CO3.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
2+
www.auladequimica.cjb.net
16
–
95) (UNOPAR-PR) Os íons Hg e Cl compõem o cloreto de mercúrio, sal empregado na preparação de
fungicidas e inseticidas, cuja fórmula é:
a) HgCl.
b) HgCl2.
c) HgCl3.
d) Hg2Cl.
e) Hg2Cl3.
96) Os nomes corretos das substâncias de fórmulas NaHCO3 e NH4NO3, são respectivamente:
a)
b)
c)
d)
e)
carbonato de sódio e nitrato de amônio.
bicarbonato de sódio e nitrato de amônio.
carbonato ácido de sódio e nitrito de amônio.
carbeto de sódio e nitrito de amônio.
bicarbonato de sódio e nitreto de amônio.
97) (PUC-RS) Algumas substâncias, como as apresentadas na tabela a seguir, fazem parte do nosso
cotidiano, tendo as mais diversas aplicações.
Substância
1 – carbonato de amônio
2 – sulfato de bário
3 – nitrato de potássio
4 – fluoreto de sódio
Aplicação
expectorante
contraste de radiografia
diurético
aditivo em cremes dentais
A seqüência que apresenta, respectivamente, a fórmula química das substâncias 1, 2, 3 e 4 encontra-se
na alternativa...
a)
b)
c)
d)
e)
NH3CO3 – BaSO4 – KNO2 – NaF.
(NH4)2CO3 – BaSO3 – KNO3 – NaFO3.
NH3CO3 – BaS – KNO4 – NaF.
(NH4)2CO3 – BaSO4 – KNO3 – NaF.
NH2CO2 – Ba2S3 – K3N – NaFO4.
98) Quantos elementos químicos compõem o sulfeto cúprico pentaidratado?
a) 7.
b) 6.
c) 5.
d) 4.
e) 3.
99) Hidroxiapatita, mineral presente em ossos e dentes, é constituída por íons cálcio, íons fosfato (PO43– ) e
íons hidróxido. A sua fórmula química pode ser representada por Cax(PO4)3(OH). O valor de “x” nessa
fórmula é:
a)
b)
c)
d)
e)
1.
2.
3.
4.
5.
100)Considere o composto XY(SO4)2 . 12 H2O. Sabendo que o íon sulfato é bivalente negativo e que X e Y
são metais de diferentes famílias, identifique a alternativa que completa a fórmula de maneira
adequada:
a) Na e Ca.
b) K e Na.
c) Ca e Ba.
d) Na e Ba.
e) K e Al.
101)Os desagradáveis odores de transpiração são provocados por alguns ácidos carboxílicos presentes no
suor. O composto a seguir que pode ser utilizado para eliminar esse odor é:
a)
b)
c)
d)
e)
leite de magnésia (hidróxido de magnésio).
vinagre (solução diluída de ácido acético).
sal de cozinha (cloreto de sódio).
açúcar (glicose).
água.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
17
102)O creme dental é básico, porque:
a) produz dentes mais brancos.
b) a saliva é ácida.
c) tem gosto melhor.
d) se fosse ácido, iria corroer o tubo (bisnaga).
e) produz mais espuma.
103)(LA SALLE – RS) Ao reagirmos hidróxido de magnésio com ácido clorídrico haverá formação de um sal
e água. Considerando que não houve reagente em excesso, o nome do sal e os coeficientes da reação
serão:
a) hidroxi-cloreto de magnésio; 1, 1, 1, 1.
b) magnésia bisurada; 2, 1, 2, 1.
c) cloridrato de magnésio; 1, 2, 1, 2.
d) cloreto de magnésio; 1, 2, 1, 2.
e) clorato de magnésio; 2, 1, 2, 1.
104)(Covest-98) Em uma solução de sulfato de sódio, qual das espécies abaixo é mais abundante?
a) Na+
–2
b) SO3
c) Na2SO4
d) SO2
e) H2SO4
Reação : Na2SO4 → 2 Na+ + 1SO4-2
105)(UPE-2004-Q2) O “celobar”, medicamento à base de sulfato de bário, provocou, este ano, mais de duas
dezenas de mortes, pois constatou-se a presença de impurezas em quantidades incompatíveis com a
vida humana em sua composição.
Em relação ao sulfato de bário, pode-se afirmar que é:
a) usado como antigripal, pois age eficientemente inibindo a oxigenação das células e
conseqüentemente extinguindo os vírus da gripe.
b) usado como laxante intestinal, por se tratar de um sal perfeitamente solúvel em água.
c) usado como contraste, quando se pretendo submeter pacientes à radiografia do aparelho
digestivos.
d) um poderoso diurético, por se tratar de um sal hidratado que tem ação direta sobre os rins,
hidratando-os.
e) usado no combate à azia, pois sendo um sal de hidrólise alcalina neutraliza a acidez estomacal.
ÓXIDOS
106)Quando o oxigênio se combina com um elemento para formar um composto, a espécie resultante é
chamada:
a)
b)
c)
d)
e)
ácido.
sal.
oxigênio molecular.
óxido.
oxalato.
107)(CEESU – 2003)A cal viva é um material muito usado por pedreiros, pintores e agricultores,
representada pela fórmula CaO. Verifique que função está representada.
a)
b)
c)
d)
e)
Ácido.
Base.
Sal.
Hidreto metálico.
Óxido.
108)Colocando um óxido básico em presença de um ácido, obteremos como produto:
a)
b)
c)
d)
e)
uma base.
um sal.
uma base e um sal.
uma base e água.
um sal e água.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
18
Cristal ou vidro?
O vidro cristal e o vidro comum têm uma estrutura molecular de desenho praticamente idêntico: a
diferença está nos elementos químicos que compõem essa estrutura, afirmar Oscar Peitl Filho, professor de
engenharia de materiais da Universidade Federal de São Carlos.Também conhecido como vidro de cal-soda
ou soda-cal, o vidro comum é feito de areia (sílica), soda (óxido de sódio), cal (óxido de cálcio) e óxido de
alumínio. Já na composição do vidro cristal entra apenas a sílica e o óxido de chumbo, substância que dá
mais brilho e maior peso ao produto.
109)Observando o texto acima, podemos afirmar que:
a)
b)
c)
d)
e)
o óxido de sódio tem fórmula NaO.
o óxido de cálcio é um óxido ácido ou anidrido.
a fórmula do óxido de alumínio é Al2O3.
todos os óxidos presentes no vidro comum ou vidro cristal são óxidos ácidos.
o óxido de chumbo é um óxido molecular.
110)O óxido de magnésio (MgO) precisa ser substituído por um óxido que apresenta propriedades químicas
semelhantes e mesma proporção em átomos. Entre os óxidos a seguir, qual você escolheria?
a) FeO.
b) CaO.
c) Na2O.
d) CO.
e) NO2.
111)Quando o solo é excessivamente ácido, agricultores procuram diminuir a acidez por meio da adição de
substâncias com propriedades alcalinas. Com essa finalidade, um dos produtos utilizados é o:
a)
b)
c)
d)
e)
NaCl.
CaO.
Na2SO4.
NH4NO3.
KClO4.
112)(Covest-90) Os produtos de uma reação de combustão são CO2(g) e vapor de água. Podemos identificar
o desprendimento do CO2 através de:
a)
b)
c)
d)
e)
queima de CO2(g) com o oxigênio.
recolhimento do CO2(g) numa solução de água de cal [Ca(OH)2].
odor característico do CO2(g).
coloração característica do CO2(g).
aumento da temperatura observado durante a reação de combustão.
113)(MACKENZIE-SP) O ferro é um dos elementos mais abundantes na crosta terrestre. Em Carajás, o
principal minério de ferro é a hematita, substância óxido de ferro III, cuja fórmula è:
a) FeO.
b) Fe3O.
c) FeO3.
d) Fe2O3.
e) Fe3O2.
114)(MACKENZIE-SP) Em recipientes fechados e amplos, o gás carbônico em excesso pode ser retirado
pela sua reação com o hidróxido de lítio, produzindo carbonato de lítio e água. A equação que
apresenta as fórmulas das substâncias e o balanceamento corretos é:
a) CO2 + LiOH Li2CO3 + H2O.CO2 + Li2O Li2CO3 .
b) CO2 + 2 LiOH Li2CO3 + H2O.
c) CO2 + Li2OH LiCO3 + H2O.
d) CO2 + Li(OH)2 Li(CO3)2 + H2O.
115)A alternativa que apresenta os anidridos correspondentes aos ácidos H2SO3, H2CO3, H2SiO3, HClO4 é:
a)
b)
c)
d)
e)
SO2, CO2, SiO2, ClO4
SO3, CO2, SiO2, ClO4
SO3, CO2, SiO2, Cl2O5
SO2, CO, SiO2, Cl2O3
SO2, CO2, SiO2, Cl2O7
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
19
116)Certo gás incolor não reage com oxigênio e é solúvel em água, formando uma solução ácida. Este gás
pode ser:
a) H2.
b) NH3.
c) CH4.
d) SO3.
e) C2H2.
117)(Mackenzie-SP) Com cerca de 40 km de profundidade, a crosta terrestre contém principalmente óxido
de silício e óxido de alumínio. Sabendo-se que o número de oxidação do silício é + 4 e do alumínio é
+ 3, as fórmulas desses óxidos são:
a)
b)
c)
d)
e)
SiO2 e Al2O3.
SiO2 e Al2O.
SiO3 e AlO.
SiO4 e AlO3.
Si2O e Al2O3.
118)(FAC. DA CIDADE-RJ)
UM PRODUTO IMPRESCINDÍVEL NO DIA-A-DIA
NO BRASIL,
MERCADO DE GASES É ESTIMADO EM US$ 200 MILHÕES
O mercado do gás X muito mais próximo da realidade do brasileiro do que se imagina: o gás X está
presente no dia-a-dia da população. Basta dizer que os principais consumidores do produto são nada
menos que as industrias de refrigerantes e cervejas, que utilizam o gás no seu processo de produção.
Também é usado como matéria prima para extintores de incêndio e gelo seco.
O nome do gás X que preenche corretamente a matéria transcrita é:
a) argônio.
b) ozônio.
c) carbônico.
d) sulfídrico.
e) hidrogênio.
119)(UPE-2006-Q1) A reação álcali-agregado, apontada como causa de desabamento de alguns edifícios,
consiste, de forma simples, na reação, envolvendo agregados reativos (vidro, granito, etc) com a
solução concentrada de álcalis gerada pela hidratação do cimento. O produto da reação é um gel, que
absorve água e incha, gerando fissuras e deterioração do concreto. O hidróxido de cálcio é um dos
componentes da reação com grande influência na formação e expansão do gel.
Qual das substâncias abaixo age, quimicamente, no sentido de inibir ou minimizar a tão temida reação
álcali-agregado?
a) Na2O
b) CaO
c) NaOH
d) CO2
e) KOH
120)(Fuvest-SP)
A) Na forma sólida é conhecido como gelo - seco, e é considerado o principal responsável pelo efeito
estufa.
B) Apresenta cor castanho - avermelhado e tem importância na destruição da camada estratosférica
de ozônio.
C) Apresenta odor de ovo podre e enegrece objetos de prata.
As características A, B e C correspondem respectivamente aos gases:
a) CO2, H2S e NO2.
b) CO2, NO2 e H2S.
c) NO2, CO2 e H2S.
d) NO2, H2S e CO2.
e) H2S, CO2 e NO2.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
20
121)Com base na frase seguinte: "A água da chuva em ambientes não poluídos, na ausência de raios e
relâmpagos, é ácida devido à dissolução do ............. , que dá origem ao ácido .......... ".
Identifique a alternativa correta:
a)
b)
c)
d)
e)
CO2, carbônico.
SO2, sulfuroso.
P2O5, fosfórico.
N2O3, nitroso.
N2O5, nítrico.
122)(UFPE) Anidrido sulfúrico é a denominação do óxido de enxofre, que, ao reagir com água, forma o
ácido sulfúrico, sendo assim um dos causadores das chuvas ácidas. Qual deve ser a fórmula molecular
desse óxido?
a) SO2.
b) SO3.
c) S2O3.
d) SO4.
e) S2O4.
123)A chuva ácida ocorre quando há uma alta concentração de agentes poluentes na atmosfera, como SO2,
NO2 e N2O5, que ao reagirem com vapor d’água, também presente, formam:
a)
b)
c)
d)
e)
sais pouco solúveis.
sais ácidos.
hidrácidos.
anidridos.
oxiácidos.
124)(Vunesp-SP) Quando os gases NO2 e SO3 entram em contato com a umidade do ar, originam um efeito
de poluição conhecido como “chuva ácida”. Isto ocorre porque se formam:
a)
b)
c)
d)
e)
monóxido de nitrogênio (NO) e ácido sulfídrico (H2S) em água.
água oxigenada e monóxido de carbono, ambos tóxicos.
gás carbônico e fuligem (carvão finamente dividido).
ácido carbônico, nitratos e sulfatos metálicos solúveis.
ácido nítrico (HNO3) e ácido sulfúrico (H2SO4).
125)As indústrias de produção de vidro utilizam a areia como principal fonte de sílica (SiO2) para conferir o
estado vítreo. Utilizam, ainda, com a finalidade de reduzir a temperatura de fusão da sílica, os fundentes
Na2O, K2O e Li2O. a escolha dos óxidos de sódio, potássio e lítio para reagir com a sílica e dar origem a
um produto vítreo de menor ponto de fusão deve-se ao fato de esses óxidos manifestarem caráter:
a)
b)
c)
d)
e)
básico.
neutro.
ácido.
misto.
anfótero.
126)Análises técnicas concluíram que os gases que constituem as nuvens vulcânicas é constituída pelos
gases sulfeto de hidrogênio, monóxido de carbono, dióxido de carbono e dióxido de enxofre. O item que
contém corretamente as fórmulas dos gases citados acima é:
a)
b)
c)
d)
e)
H2SO4, CO, CO2 e SO3.
CaO, H2SO3, CO2 e H2SO4.
CO, CO2, SO3 e H2SO4.
CO, H2S, SO2 e CO2.
H2S, CO, CO2 e SO3.
127)Uma forma genérica de se obterem ácidos é a reação entre seu anidrido e água. Entre os ácidos
abaixo relacionados, não pode ser obtido por esse processo o:
a) clorídrico.
b) hipocloroso.
c) cloroso.
d) clórico.
e) perclórico.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
21
128)Observe as reações químicas:
I.
II.
III.
IV.
MgO + H2O Mg(OH)2.
CO2 + H2O H2CO3.
K2O + 2 HCl 2 KCl + H2O.
SO3 + 2 NaOH Na2SO4 + H2O
Assinale a alternativa incorreta:
a)
b)
c)
d)
e)
As reações II e IV envolvem óxidos ácidos ou anidridos.
As reações I e III envolvem óxidos básicos.
O sal produzido na reação IV chama-se sulfato de sódio.
O sal produzido na reação III chama-se cloreto de potássio.
O caráter básico dos óxidos se acentua, à medida que o oxigênio se liga a elementos mais
eletronegativos.
129)A espécie química H2S é um gás um gás venenoso, incolor, formado na putrefação de substâncias
orgânicas naturais que contenham enxofre, sendo responsável pelo cheiro de ovo podre. Queima no ar,
com chama azul produzindo SO2 e H2O. É encontrado em pequenas quantidades em algumas águas
minerais (sulfurosas), e sua utilização é restrita a processos de análises químicas.
a) A substância H2S quando se encontra em solução aquosa forma um ácido forte.
b) O composto SO2 é um óxido básico.
c) O composto SO2 reage com água produzindo H2SO3.
d) O composto SO2 reage com água produzindo H2SO4.
e) O H2S é um ácido de Arrhenius classificado como hidrácido e oxiácido.
130)(Vunesp-SP) Quando se coloca ácido clorídrico sobre uma concha do mar, ela é totalmente dissolvida e
há desprendimento de um gás. Este gás é o mesmo que é exalado na respiração animal. Portanto, o sal
insolúvel que constitui a carapaça da concha do mar é:
a) CaCO3.
b) CaSO4.
c) CaF2.
d) Ca(NO3)2.
e) Ca(OH)2.
131)(MACK-SP) A argamassa, que é um produto usado por pedreiros para assentar tijolos, é uma mistura
de cal extinta, areia e água. A cal extinta (hidróxido de cálcio) combina-se com o gás carbônico do ar,
produzindo carbonato de cálcio, que endurece e prende a areia e, conseqüentemente, os tijolos. A
equação corretamente balanceada que representa a reação entre a cal extinta e o gás carbônico é:
a) Ca(HCO3)2 + CaO 2 CaCO3 + H2O.
b) CaO + H2O Ca(OH)2.
c) Ca(OH)2 + CO2 CaCO3 + H2O.
d) 2 Ca(OH)2 + CO2 2 CaCO3 + H2O.
e) 2 CaHCO3 + CaO 3 CaCO3 + H2O.
132)(UFES) Considere a seqüência de reações:
S + O2 I
I + H2O II
FeO + II III + H2O
Mg + 1/2 O2 IV
IV + H2O V
As funções dos compostos I, II, III, IV e V são, respectivamente:
a) óxido ácido, ácido, sal, óxido básico e hidróxido.
b) óxido ácido, ácido, óxido básico, sal e hidróxido.
c) ácido, óxido ácido, sal, óxido básico e hidróxido.
d) ácido, óxido ácido, hidróxido, sal e óxido básico.
e) sal, ácido, óxido ácido, hidróxido e óxido básico.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
22
133)Considera as reações:
• K2O + H2O 2 X
• N2O5 + H2O 2 Y
• X + Y Z + H2O
O coeficiente estequiométrico de Z é:
a)
b)
c)
d)
e)
1.
2.
3.
4.
5.
134) (UEL-PR) A fórmula do decavanadato (duplo) de potássio e dimagnésio com 16 moléculas de água de
cristalização é K2Mg2V10O28.16H2O. De qual óxido de vanádio deriva esse decavanadato?
a) V2O7.
b) V2O5.
c) V2O3.
d) V2O.
e) VO.
135)A alternativa que apresenta respectivamente óxido ácido, óxido básico, óxido neutro e óxido duplo é:
a)
b)
c)
d)
e)
CO; CaO; SO3; Na2O4.
N2O5; BaO ; NO; Pb3O4.
CO2; Al2O3; Fe3O4; Cl2O
N2O; MgO; CO2; Mn3O4.
SO2; K2O; CO; K2O2.
136)(UPE-2004-Q1) Assinale a alternativa que apresenta um gás considerado tóxico, porque forma um
complexo com a hemoglobina do sangue, inutilizando-a para o transporte de oxigênio, causando, entre
outros sintomas, asfixia, aumento de ritmos respiratórios, inconsciência e finalmente a morte.
a)
b)
c)
d)
e)
N2.
CO2.
NH3.
CO.
O3.
137)(MACK-SP) Para se corrigir a acidez de solos, é comum a utilização de:
a) CaCO3.
b) KNO3.
c) Al2(SO4)3.
d) S.
e) NaCl.
138)(UPE-2005-Q1) Sejam os elementos A, B, C e D, com suas respectivas distribuições eletrônicas:
A → 1s2...........................3s1
B → 1s2...........................4s2
2
4
C → 1s ..........................3p
2
D → 1s ...........................3p3
Transformando os elementos A, B , C e D em óxidos, através de reações químicas apropriadas, podese concluir, como verdadeiro, que
a) somente os elementos químicos “A”, “B” e “C” originam óxidos que, em contato com a água, tornam
o meio ácido.
b) o elemento químico “B” forma um óxido que, ao reagir com uma solução aquosa de ácido clorídrico,
origina um gás insolúvel em água.
c) o óxido originado pelo elemento “B”, quando presente na atmosfera, constitui uma névoa branca
que, bastante poluente, em contato com a água, origina soluções ácidas.
d) os óxidos originados pelos elementos “A” e “B” não são considerados poluentes atmosféricos
causadores de chuvas ácidas.
e) somente os elementos “A”, “B” e “D” formam óxidos e são muito usados na agricultura, no combate
a pragas e a solos alcalinos.
Comentários: Os óxidos formados por A (grupo 1A ) e B (grupo 2A) são “óxidos básicos”
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
23
139)(MACK-SP)
I)
II)
III)
IV)
V)
+
Tem fórmula NH4 .
Apresenta apenas ligações covalentes simples.
Tem fórmula NH3.
É hidreto polar.
Reage com água formando o hidróxido de amônio.
Das afirmações acima, a respeito da amônia, são corretas somente:
a)
b)
c)
d)
e)
II, III, IV e V.
I, II e V.
II e III.
III, IV e V.
I e IV.
140)Em qual das alternativas todos os óxidos mencionados têm caráter neutro?
a)
b)
c)
d)
e)
CO, CO2, NO e N2O5.
NO, N2O e SO3.
CO, NO e N2O.
CO, NO e SO3.
Na2O, CaO e BaO.
141)(Covest-90) Várias substâncias são encontradas no comércio e utilizadas como medicamentos,
alimentos, desinfetantes, etc., tais como: água oxigenada (peróxido de hidrogênio), álcool (álcool
etílico), açúcar (sacarose), sal de cozinha (cloreto de sódio), água sanitária (hipoclorito de sódio).
Assinale o item que apresenta as fórmulas químicas desses compostos, na ordem dada:
a) H2O2, CH3OH, C12H22O11, NaCl, NaIO3.
b) H3O, C2H5OH, C6H12O6, NaCl, NaClO.
c) H2O, C2H5OH, C6H12O6, NaCl, NaClO4.
d) H2O2, C3H6OH, C12H22O11, Na2Cl, NaClO2.
e) H2O2, C2H5OH, C12H22O11, NaCl, NaClO.
142)(PUC-SP)
1
Sulfato de alumínio
2
Platina
3
4
5
Hidróxido de sódio
Bicarbonato de sódio
Chumbo em placas
Matéria-prima usada na manufatura de pinos
utilizados em cirurgias ortopédicas.
Usado como um dos componentes de extintores de
incêndio (pó pressurizado).
Usado no tratamento de água.
Usado em baterias de automóveis.
Vendido no comércio com o nome de soda cáustica.
Associando-se as substâncias da coluna da esquerda com as afirmações da coluna da direita, a
seqüência numérica correta encontrada de cima para baixo, é:
a) 2, 1, 4, 3, 5.
b) 5, 4, 1, 2, 3.
c) 2, 1, 3, 5, 4.
d) 5, 3, 4, 2, 1.
e) 2, 4, 1, 5, 3.
143)Assinale a alternativa que contém a correta seqüência relacionando o grupo de fórmulas com o grupo
de nomes:
1
Na2CO3
óxido de sódio
2
NaOH
peróxido de sódio
3
Na2O
bicarbonato de sódio
4
NaHCO3
carbonato de sódio
5
Na2O2
hidróxido de sódio
a)
b)
c)
d)
e)
4 – 3 – 5 – 1 – 2.
5 – 5 – 2 – 1 – 3.
3 – 5 – 4 – 1 – 2.
3 – 1 – 5 – 2 – 4.
2 – 3 – 5 – 1 – 4.
Prof. Agamenon Roberto
FUNÇÕES INORGÂNICAS
www.auladequimica.cjb.net
24
144)(Covest-2002) A tabela abaixo apresenta a classificação das substâncias inorgânicas de maior
produção nos Estados Unidos em 1999:
CLASSIFICAÇÃO
PRODUTO
o
1 lugar
2o lugar
3o lugar
10o lugar
ácido sulfúrico
amônia
ácido fosfórico
dióxido de titânio
As fórmulas químicas das substâncias classificadas em 1º, 2º, 3º, e 10º lugar são respectivamente:
a) H2PO4, NH3, H3SO4, TiO2.
b) H2S, PH3, H3PO4, Ti2O.
c) H2SO4, NH3, HClO4, TiO2.
d) H2SO3, NH4, HClO4, TiO.
e) H2SO4, NH3, H3PO4, TiO2.
145)(Covest-2004) O dióxido de enxofre é produzido como subproduto da queima de combustíveis fósseis.
Pode-se combinar com água e formar ácido sulfuroso, um ácido fraco, que se dissocia em:
H2 S O 3 ( g)
0
1
2
3
0
1
2
3
4
4
H 3 O +( aq )
+ H 2O ( l )
–
+ H SO3
( aq )
H2SO3 é um ácido de Brönsted, e o HSO3 sua base conjugada.
O pH de uma solução aquosa de H2SO3 é maior que sete a 25°C.
Uma solução aquosa 1 molar de H2SO3 contém íons hidrônio numa concentração 1 molar.
O íon HSO3 – também pode ser considerado um ácido, pois em meio aquoso pode
+
2–
produzir H3O e SO3 .
2–
–
O íon SO3 deve ser uma base mais fraca que o íon HSO3 .
VFFVF