Estudo Teórico das Propriedades Geométricas da Zalcitabina no Vácuo
Usando DFT e Dinâmica Molecular de Car-Parrinello
Ítalo Nuta Ribeiro1 (IC)*, Solemar Silva Oliveira1 (PQ). [email protected]
1
Universidade Estadual de Goiás, campus de ciências exatas e tecnológicas, Anápolis, GO.
Resumo: A zalcitabina, também conhecida como dideoxicitidina
(ddc),
é
um
potente
inibidor
da
replicação
do
vírus
da
imunodeficiência humana (HIV) em baixas concentrações. Quando
a molécula penetra no DNA que contém o vírus, a mesma impede
que esse DNA infectado pelo vírus se replique. A zalcitabina é um
fármaco da classe dos inibidores de transcriptase reversa (INTR).
Possui a fórmula química C9H13N3O3, uma massa molar de
211.218 g/mol e foi o terceiro fármaco dessa classe a ser liberada
para uso terapêutico. A empresa que comercializa a zalcitabina é a
Roche sob a marca HIVID® [1]. Os parâmetros geométricos,
distâncias e ângulos de ligação, e a estrutura eletrônica foram
tratadas no vácuo utilizando a Teoria do Funcional de Densidade
(DFT) e Dinâmica Molecular de Car-Parinello, por meio do funcional
de correlação de Perdew-Burke-Ernzerhof (PBE) [2]. Neste método
os sistemas são conduzidos ao mínimo de energia. Comparamos
os resultados obtidos com resultados experimentais, como os
cristalográficos [3]. Analisamos o mapa de potencial eletrostático,
os orbitais de fronteira HOMO e LUMO e inferimos conclusões
sobre as regiões eletrofílicas e nucleofílicas da molécula [2].
Realizamos os nossos cálculos no Cluster de computadores do
Grupo de Química Teórica e Estrutural de Anápolis.
Palavras-chave: Zalcitabina. Simulação. DFT. Car-Parrinello.
Introdução
A Zalcitabina (2’ ,3’-didesoxicitidina, ddc) é um fármaco que, junto com a
didanosina, lamivudina e zidovudina, é da classe dos inibidores nucleosídeos de
transcriptase reversa (INRT) (Cunico et al, 2008). Os fármacos dessa classe foram
os primeiros a serem liberados para uso terapêutico, sendo a zidovudina, em 1987, o
primeiro (Martins, 2010).
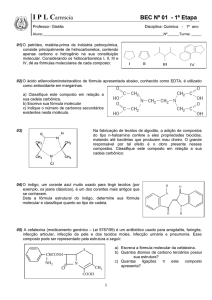
A Zalcitabina (Figura 1), em 1992, foi o terceiro fármaco da classe dos INRT a ser
liberado para uso terapêutico. É comercializada pela companhia farmacêutica Roche
com o nome de HIVID®. Possui uma formula molecular C9H13N3O3 e uma massa
molar de 211.218 g/mol. Também mostra uma solubilidade de 76,4 mg/mL a 25°C,
uma meia vida intracelular longa de 10 horas e meia vida de eliminação de 2 horas e
mostra também uma alta biodisponibilidade oral em torno de 80% (Martins, 2010).
Figura 1- Estrutura da Zalcitabina. Fonte do Autor
Métodos de modelagem molecular são amplamente utilizados na busca da
compreensão de estruturas moleculares simples (pequenas moléculas) e complexas
(enzimas, proteínas, polímeros). Recentemente os modelos são vários e a
tecnologia computacional possibilita grandes avanços na obtenção de resultados em
estruturas cada vez maiores (Aguiar, 2011).
A DFT, com ajuda dos computadores, permite estudar sistemas mais complexos,
contribuindo para o entendimento e previsão das propriedades dos átomos,
moléculas e sólidos (Marques & Botti, 1998).
Em 1985, foi desenvolvido um método de dinâmica molecular ab initio por Roberto
Car e Michelle Parrinello. Neste método, descreve-se o sistema iônico utilizando
mecânica clássica e as coordenadas nucleares e eletrônicas são estudadas
separadamente pela aproximação de Born-Oppenheimer (Car & Parrinello, 1985).
Dentre as dinâmicas moleculares ab initio, a dinâmica molecular de Car-Parrinello
mostra-se bastante eficiente. Alguns critérios que são considerados: O método de
resolução das equações de movimento de Newton para o núcleo associado à
resolução da equação de Schröedinger para o subsistema eletrônico; O cálculo da
energia e dos gradientes a partir da estrutura eletrônica, base teórica utilizada na
dinâmica molecular de Born-Oppenheimer; Minimização do funcional energia a partir
das idéias de Recozimento Simulado desenvolvidas por Kirk Patrick (Kirkpatrick et
al. 1983).
Material e Métodos
A molécula foi desenha utilizando o programa Hyperchem. Os dados estruturais da
molécula foram conduzidos ao pacote de programas GAUSSIAN, para a simulação
de DFT, e CPMD, para a simulação pelo método de Car-Parrinello, ao qual se
realizou, novamente, uma minimização no estado das novas condições do sistema.
Para a simulação no CPMD, foram empregados os algoritmos Damp para o
relaxamento nas posições dos caroços iônicos e otimização dos estados eletrônicos,
e Steepest Descent, para garantir que os elétrons alcancem o mínimo global de
energia, ou seja, a superfície de Born-Oppenheimer. A temperatura que conduziu o
sistema foi de 300K. O tamanho do passo de simulação foi de 0,12 fs. Na simulação
da dinâmica molecular de Car-Parrinello foi empregado o algoritmo Verlet. Serão
realizados cálculos com para um valor superior a 300.000 passos, ou para um tempo
da ordem de 30 ps. Estes cálculos serão realizados nos clusters do grupo teórico e
estrutural de Anápolis (QTEA), localizados na UEG campus de ciências exatas e
tecnologias.
Resultados e Discussão
Átomos
H16-N15
N15-H17
N15-C4
C4-N14
C4-C5
C5-H21
C5-C6
C6-H22
C6-N13
N14-C7
C7-O1
Distância
DFT
1,01366
1,01645
1,37027
1,32692
1,43067
1,08896
1,36717
1,09044
1,35325
1,36788
1,23101
Distância
CPMD
1,01856
1,02128
1,37531
1,33146
1,43732
1,09476
1,36885
1,09870
1,36904
1,37636
1,23627
Erro Relativo
(%)
-0,48340
-0,47518
-0,36781
-0,34215
-0,46482
-0,53262
-0,12288
-0,75749
-1,16682
-0,61994
-0,42729
C7-N13
N13-C8
C8-H23
C8-O2
C8-C11
C11-H27
C11-H28
C11-C10
C10-H26
C10-H25
C10-C9
C9-O2
C9-H24
C9-C12
C12-H18
C12-H19
C12-O3
O3-H20
1,44250
1,48089
1,10038
1,42805
1,53848
1,10138
1,09601
1,53143
1,10073
1,09906
1,52725
1,45886
1,10896
1,52507
1,10675
1,10094
1,42341
0,97510
1,45940
1,49114
1,11028
1,43019
1,54587
1,10583
1,10203
1,54495
1,10383
1,10895
1,53884
1,46919
1,10990
1,52632
1,11485
1,10928
1,44113
0,98032
-1,17158
-0,69215
-0,89969
-0,14985
-0,48034
-0,40404
-0,54927
-0,88283
-0,28163
-0,89986
-0,75888
-0,70809
-0,08476
-0,08196
-0,73187
-0,75753
-1,24490
-0,53533
Tabela 1- Comparação entre as distâncias por DFT e CP.
Átomos
Ângulos DFT
H16-N15-H17
H16-N15-C4
H17-N15-C4
N15-C4-N14
N15-C4-C5
C4-N14-C7
C4-C5-H21
C4-C5-C6
N14-C7-O1
N14-C7-N13
N14-C4-C5
O1-C7-N13
C7-N13-C8
C7-N13-C6
N13-C8-H23
N13-C8-C11
N13-C8-O2
N13-C6-H22
N13-C6-C5
C6-C5-H21
H22-C6-C5
C6-N13-C8
117,280
119,406
115,799
116,647
119,860
120,482
122,644
116,485
124,999
117,101
123,475
117,900
116,047
121,553
105,394
113,484
109,664
115,754
120,868
120,866
123,367
122,399
Ângulos
CPMD
117,398
119,477
116,078
116,862
119,794
120,733
122,517
115,961
123,791
116,855
123,058
119,118
121,379
119,658
103,933
115,706
111,123
115,818
121,957
120,744
121,783
117,928
Erro Relativo (%)
-0,100
-0,059
-0,240
-0,184
0,055
-0,208
0,103
0,44
0,966
0,210
0,337
-1,033
-4,594
1,558
1,386
-1,957
-1,330
-0,055
-0,900
0,100
1,283
3,652
H23-C8-O2
H23-C8-C11
C8-C11-H27
C8-C11-H28
C8-C11-C10
C8-O2-C9
H28-C11-H27
H28-C11-C10
H27-C11-C10
O2-C9-H24
O2-C9-C10
O2-C9-C12
H24-C9-C10
H24-C9-C12
H26-C10-H25
H25-C10-C11
H25-C10-C9
H26-C10-C11
H26-C10-C9
C11-C10-C9
C10-C9-C12
C9-C12-H18
C9-C12-H19
C9-C12-O3
H19-C12-H18
H18-C12-O3
H19-C12-O3
C12-O3-H20
C11-C8-O2
109,754
111,559
109,251
111,153
102,702
110,148
107,922
114,668
111,024
108,897
104,744
106,836
110,899
108,711
108,504
113,042
112,181
111,411
109,277
102,319
116,411
109,182
109,249
112,614
107,790
111,041
111,041
105,936
106,982
107,075
111,173
109,546
110,701
104,235
109,847
108,473
111,340
111,994
107,561
105,071
107,626
111,057
110,023
108,216
110,970
110,238
111,662
111,235
104,034
114,717
109,198
109,027
113,000
108,045
110,406
106,580
106,798
107,259
2,440
0,346
-0,270
0,406
-1,492
0,273
-0,510
2,902
-0,873
1,226
-0,312
-0,739
-0,142
-1,206
0,265
1,832
1,732
-0,225
-1,791
-1,676
1,455
-0,014
0,203
-0,342
-0,236
0,571
4,017
-0,813
-0,258
Tabela 2- Comparação dos ângulos por DFT e CP.
Considerações Finais
Ao longo de todo o projeto e dos resultados que obtivemos da dinâmica feita na
molécula da zalcitabina, podemos concluir então que em algumas partes da
geometria teve algumas variações comparando os resultados entre as duas
dinâmicas utilizadas. Mas, como o método de dinâmica molecular desenvolvida por
Car-Parrinello é mais precisa, principalmente pela quantidade de passos que é
tratada, ela tem um melhor resultado na obtenção dos dados geométricos
Agradecimentos
Gostaria de agradecer a Universidade Estadual de Goiás por proporcionar essa
oportunidade de participar no programa de Iniciação Científica e Tecnológica, ao
grupo de química teórica e estrutural de Anápolis (QTEA) aonde foram realizadas
todas as simulações e também ao professor Dr. Solemar Silva Oliveira por ter me
orientado durante esse projeto.
Referências
Azevedo, F. C. A transcriptase reversa como alvo terapêutico em doenças
retrovirais. Tese (Mestrado) – Universidade Fernando Pessoa, Porto: 2013.
Cunico, W.; Gomes, C. R. B.; Junior, W. T. V. HIV - Recentes avanços na pesquisa
de fármacos. Quim. Nova, 31(8), 2111–2117. 2008.
Martins, F. T. Química supramolecular de fármacos antirretrovirais inibidores
nucleosídeos de transcriptase reversa: novas formas cristalinas e alteração de
propriedades de estado sólido. Tese (Doutorado) – Instituto de Física de São
Carlos, Universidade de São Paulo, São Carlos: 2010.
Aguiar, A. S. N.; et al. Modelagem Molecular: Uma visão detalhada da Dinâmica
Molecular de Car-Parrinello. In OLIVEIRA SS (eds.). Ciências Moleculares.
Universidade Estadual de Goiás. p. 45-81. Goiânia, GO: 2011.
Car, R.: Parrinello, M. Unified Approach for Molecular Dynamics and Density
Functional Theory. Physical Review Letters. 55(22):2471-2474. 1985.
Kirkpatrick, S.; Gelett, C. D.; Vecchi, M. P. Optimization by Simulated Annealing.
Science, 220;671-680. 1983.