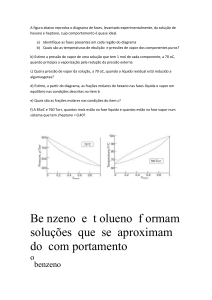
PAAES 2010-2013 2ª ETAPA Os vapores de sulfeto de carbono, metanol e
etanol podem causar lesões e mutações na
parede ocular, dependendo da concentração e
tempo de exposição. O gráfico abaixo mostra
as curvas de pressão de vapor desses líquidos
mais a água.
Fonte: HILL, J. W. General Chemistry. Upper Saddle River,
Prentice Hall, 1996.
A partir da análise do gráfico, marque, para as
alternativas abaixo, (V) Verdadeira, (F) Falsa
ou (SO) Sem Opção.
1 - (
)
2 - (
)
3 - (
)
4 - (
)
Em uma mesma temperatura, a sequência crescente de pressão de vapor
é: água, etanol, metanol e sulfeto de
carbono.
Dentre as substâncias do gráfico,
em dada temperatura, o sulfeto de
carbono é o líquido de maior pressão
de vapor.
Em um mesmo intervalo de tempo e
ambiente fechado, a concentração
de vapores de metanol será menor
que a concentração dos vapores de
etanol.
O sulfeto de carbono, em dada temperatura, é o que apresenta menor
tendência a evaporar.
Resolução:
De acordo com os conceitos de propriedades
coligativas, quanto maior a pressão máxima de
vapor, mais volátil será uma substância.
1 - (V) 2 - (V) 3 - (F) 4 - (F) A ordem crescente de pressão de
vapor, de acordo com o gráfico, é
água, etanol, metanol e sulfeto de
carbono.
De acordo com o gráfico, o sulfeto
de carbono é o que possui maior
pressão de vapor, portanto é mais
facilmente volatilizado.
Em um mesmo intervalo de tempo e
ambiente fechado, a concentração
de vapores de metanol será maior
que a concentração dos vapores de
etanol. Isso se deve ao fato de que o
metanol se volatiliza mais facilmente do que o etanol pois possui uma
maior pressão de vapor.
O sulfeto de carbono, em dada temperatura, é o que apresenta maior
tendência a evaporar. Pois das 4
substâncias é aquele que possui
maior pressão de vapor e sua menor
temperatura de ebulição.
Q
U
Í
M
I
C
A