Ciclo de Krebs ou do ácido cítrico; Rui Fontes
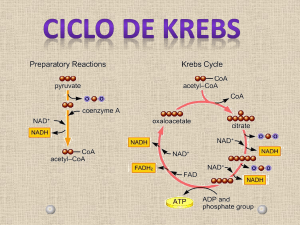
O ciclo de Krebs ou do ácido cítrico
1-
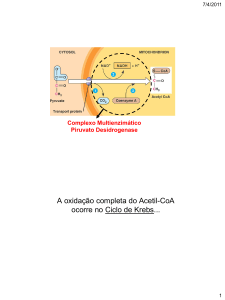
Por acção das enzimas da glicólise a glicose é, no citoplasma das células, parcialmente
oxidada a piruvato. O piruvato entra para a mitocôndria e, através da acção catalítica da
desidrogénase do piruvato (piruvato + NAD+ + CoA → acetil-CoA + NADH + CO2), dá
origem a acetil-CoA. No catabolismo dos aminoácidos, dos ácidos gordos e do etanol
também se forma acetil-CoA. O ciclo de Krebs (do citrato ou dos ácidos tricarboxílicos) é
uma via metabólica central no metabolismo dos nutrientes pois permite a oxidação do grupo
acetilo da acetil-CoA (a CO2) com a concomitante redução do NAD+ e do FAD a NADH e
FADH2 que são intermediários no processo de redução do O2 (a H2O).
2-
As enzimas envolvidas nas reacções do ciclo de Krebs estão todas dentro da mitocôndria e são
as seguintes:
síntase do citrato (acetil-CoA + oxalacetato + H2O → citrato + CoA),
(1)
aconitase (citrato ↔ isocitrato),
(2)
desidrogénase do isocitrato (isocitrato + NAD+ → α-cetoglutarato + CO2 + NADH),
(3)
desidrogénase do α-cetoglutarato (α-cetoglutarato + NAD+ + CoA →
succinil-CoA + NADH + CO2), (4)
sintétase de succinil-CoA [succinil-CoA + GDP (ou ADP) + Pi ↔
succinato + CoA + GTP (ou ATP)] (5)
desidrogénase do succinato (succinato + FAD ↔ fumarato + FADH2),
(6)
fumárase (fumarato + H2O ↔ malato) e
(7)
desidrogénase do malato (malato + NAD+ ↔ oxalacetato + NADH)
(8)
3-
A sintétase de succinil-CoA (equação 5) existe na forma de duas isoenzimas sendo que uma
delas tem maior especificidade para o ADP e a outra maior especificidade para o GDP.
Embora a cínase dos nucleosídeos-difosfatos não seja, habitualmente, considerada uma
enzima do ciclo de Krebs ela tem um papel importante neste contexto já que permite a
transferência do fosfato terminal do GTP (formado pela acção de uma das isoenzimas da
sintétase do succinil-CoA) para o ADP e a formação de ATP (GTP + ADP ↔ GDP + ATP).
Por contraponto com a formação de ATP na fosforilação oxidativa esta fosforilação do ADP
diz-se que ocorre “ao nível do substrato”.
4-
A fase preparatória da oxidação do grupo acetilo da acetil-CoA a CO2 começa com a sua
ligação ao oxalacetato por acção da síntase do citrato. Os passos oxidativos em que ocorre a
redução do NAD+ e do FAD são os catalisados pelas desidrogénases do isocitrato, αcetoglutarato, do malato (NAD+ a NADH) e do succinato (FAD a FADH2). O NAD+ e o
FAD existem nas células em concentrações de ordem micromolar e têm de ser regenerados
para permitir a oxidação da glicose, de ácidos gordos e de aminoácidos que são ingeridos em
quantidades de alguns moles por dia. A regeneração do NAD+ e do FAD é indispensável para
que o processo oxidativo possa prosseguir e, na mitocôndria, o único mecanismo que permite
reoxidar o NADH e o FADH2 é desempenhado pelos complexos da cadeia respiratória sendo
que o oxidante final é o O2: ao contrário do que acontece no caso da glicólise não existe “ciclo
de Krebs anaeróbio”. As descarboxilações (e consequente libertação de CO2) ocorrem
durante as acções catalíticas da desidrogénase do isocitrato [isocitrato (6C) + NAD+ → αcetoglutarato (5C) + CO2 + NADH] e da desidrogénase do α-cetoglutarato [α-cetoglutarato
(5C) + NAD+ + CoA → succinil-CoA (4C-CoA) + NADH + CO2]: as reacções que estas duas
desidrogénases catalisam são frequentemente referidas como sendo oxidaçõesPágina 1 de 4
Ciclo de Krebs ou do ácido cítrico; Rui Fontes
descarboxilativas. As desidrogénases do isocitrato e do α-cetoglutarato (juntamente com a
desidrogénase do piruvato) são responsáveis pela esmagadora maioria das moléculas de CO2
que um ser vivo produz.
5-
A equação que descreve o somatório das reacções que constituem o ciclo de Krebs (1-8 e a
catalisada pela cínase dos nucleosídeos-difosfatos)
CH3CO-CoA + 2 H2O + 3 NAD+ + FAD + ADP + Pi →
2 CO2 + CoA + 3 NADH + FADH2 + ATP
(9)
mostra que, conceptualmente, este pode ser entendido como um somatório de três processos:
(9a) a hidrólise da acetil-CoA, (9b) a oxidação do acetato a CO2 e (9c) a síntese de ATP (a
partir de ADP + Pi).
CH3CO-CoA + H2O → CoA + CH3COOH
(9a)
CH3COOH + 2 H2O + 3 NAD+ + FAD → 2 CO2 + 3 NADH + FADH2
(9b)
ADP + Pi → ATP + H2O
(9c)
Os processos (9a) e (9b) referidos acima são exergónicos enquanto o (9c) é endergónico e só
ocorre porque está acoplado, via acção catalítica da sintétase do succinil-CoA e da cínase dos
nucleosídeos-difosfatos, com os processos exergónicos de rotura da ligação tioéster do
succinil-CoA (catalisada pela sintétase de succinil-CoA) e da ligação anidrido (β-γ) do GTP
(catalisada pela cínase dos nucleosídeos difosfatos).
6-
Nos músculos o principal papel das enzimas do ciclo de Krebs é, tal como indica a equação
(9), catalisar a oxidação completa do resíduo acetilo do acetil-CoA formado durante o
catabolismo da glicose, ácidos gordos e aminoácidos. Nas reacções em que intervêm
catalisadores, porque estes não se consomem nem se formam durante o processo reactivo, o
catalisador não aparece na equação final. O mesmo acontece no caso dos intermediários do
ciclo de Krebs: quando se somam as equações que expressam a actividade de cada uma das
enzimas os intermediários desaparecem da equação. Em cada uma das reacções um
intermediário converte-se no seguinte e o “último” (o oxalacetato) converte-se no “primeiro”
(o citrato). Por isso não é de estranhar que seja costume dizer-se que, no processo de oxidação
do grupo acetilo da acetil-CoA pelo ciclo de Krebs, os intermediários têm um papel
catalítico.
7-
No músculo, a velocidade com que ocorrem as reacções catalisadas pelas enzimas do ciclo de
Krebs é proporcional à despesa energética: a velocidade com que ocorrem as reacções do
ciclo de Krebs (a oxidação do acetil-CoA a CO2) aumenta quando aumenta a velocidade
de hidrólise do ATP. As enzimas que catalisam reacções fisiologicamente irreversíveis são
as catalisadas pela síntase do citrato e pelas desidrogénases do isocitrato e do αcetoglutarato. Estas enzimas são, in vitro, inibidas pelo ATP e estimuladas pelo ADP; dado
que o esforço muscular implica aumento da velocidade da hidrólise do ATP (actividade da
ATPase da actina-miosina) pensou-se durante muito tempo que ocorria diminuição da
concentração de ATP e aumento da de ADP durante o trabalho muscular e que essas variações
de concentração fossem a causa directa da activação destas enzimas e do ciclo de Krebs no
seu conjunto. Contudo, in vivo, as variações de concentração do ATP (mesmo quando o
trabalho muscular é violento) são praticamente nulas e as do ADP são muito modestas; por
isso crê-se, actualmente, que o marcado aumento da actividade das enzimas do ciclo de Krebs
e o consequente aumento de produção de CO2 durante o esforço muscular só, em parte, pode
ser causado pelo aumento do ADP. Pensa-se actualmente que um dos factores responsáveis
pelo aumento da produção de CO2 durante o esforço poderá ser o ião Ca2+ que estimula as
desidrogénases do isocitrato e α-cetoglutarato (activação alostérica) e cuja concentração
aumenta na célula (citoplasma e mitocôndria) durante a actividade contráctil do músculo [1].
Página 2 de 4
Ciclo de Krebs ou do ácido cítrico; Rui Fontes
8-
É de notar que a acetil-CoA não estimula a actividade das enzimas do ciclo de Krebs; ou
seja, não é de esperar que a ingestão aumentada de glicose ou ácidos gordos leve por si só a
um aumento da oxidação da acetil-CoA formada a partir dos nutrientes. Os sistemas
oxidativos e em particular o ciclo de Krebs têm velocidades que permitem manter a
concentração de ATP estacionária: só é possível aumentar a velocidade de oxidação da acetilCoA (e, em última análise, a da oxidação dos nutrientes) aumentando o consumo de ATP, ou
seja, fazendo exercício.
9-
Para além do papel central no processo oxidativo dos nutrientes (catabolismo) as enzimas do
ciclo de Krebs também participam noutros processos metabólicos que podem ser vistos como
anabólicos. Por isso se costuma dizer que o ciclo de Krebs tem carácter anfibólico: os
intermediários deste ciclo são intermediários no catabolismo dos nutrientes mas também
podem ser intermediários em processos anabólicos, como a síntese de ácidos gordos a partir
de glicose (lipogénese), a síntese de glicose (gliconeogénese) ou de glicerol-3-P
(gliceroneogénese) a partir de aminoácidos ou de lactato ou a síntese de alguns aminoácidos a
partir de glicose. O papel anabólico das enzimas do ciclo de Krebs tem particular relevância
nos casos do fígado, rim e tecido adiposo.
10-
Quando um intermediário do ciclo de Krebs é convertido num outro composto que não o
é, diz-se que o processo é cataplerótico [2, 3]. As reacções catapleróticas tenderiam a
“esvaziar” o ciclo de Krebs mas um processo cataplerótico não pode ocorrer sem que, a uma
velocidade semelhante, um outro composto que não é intermediário do ciclo de Krebs
origine um intermediário do ciclo. Os processos deste último tipo chamam-se
anapleróticos. É uma boa aproximação à realidade afirmar-se que os intermediários do ciclo
de Krebs mantêm concentrações estacionárias; mesmo em diferentes estados metabólicos ou
quando um músculo passa do estado de repouso para o de trabalho mecânico as concentrações
dos intermediários do ciclo de Krebs variam muito pouco [2-5].
11-
Durante o jejum o fígado e o rim formam glicose usando oxalacetato do citoplasma como
percursor e ao processo chama-se gliconeogénese. A quantidade total de oxalacetato num
homem é de alguns mmols mas, na gliconeogénese, pode formar-se cerca de ½ mole de
glicose por dia [6]. O fenómeno só é possível porque o oxalacetato citoplasmático é formado
a partir de malato (catálise pela desidrogénase do malato citoplasmática: malato + NAD+ ↔
oxalacetato + NADH) que saiu da mitocôndria. A transformação de malato mitocondrial
(intermediário do ciclo de Krebs) em oxalacetato citoplasmático é um processo cataplerótico.
O processo é sustentável porque durante a gliconeogénese ocorrem simultaneamente
processos anapleróticos que permitem formar intermediários do ciclo de Krebs. Quando um
qualquer intermediário se forma pode, por acção das enzimas do ciclo de Krebs, substituir o
malato consumido. São exemplos de processos anapleróticos importantes durante a
gliconeogénese (i) a conversão de lactato citoplasmático em oxalacetato mitocondrial [via
acção da desidrogénase láctica (lactato + NAD+ → piruvato + NADH), transporte de piruvato
para a mitocôndria e acção da carboxílase do piruvato (piruvato + CO2 + ATP → oxalacetato
+ ADP + Pi)], (ii) a conversão de glutamina e outros aminoácidos em α-cetoglutarato
mitocondrial e (iii) a conversão de propionato em succinil-CoA mitocondrial. Todas as
substâncias que podem, directa ou indirectamente, ser substratos em processos
anapleróticos dizem-se também glicogénicas porque, no fígado e no rim, são substratos
da gliconeogénese. Um exemplo de uma reacção anaplerótica é a catalisada pela
desidrogénase do glutamato (glutamato + NAD+ → α-cetoglutarato + NADH + NH4+): nesta
reacção um aminoácido (o glutamato) converte-se num intermediário do ciclo de Krebs (o αcetoglutarato); o glutamato é, por isso, um substrato da gliconeogénese.
12-
A acetil-CoA, reage com um intermediário do ciclo de Krebs (o oxalacetato) formando citrato
(síntase do citrato: acetil-CoA + oxalacetato + H2O → citrato + CoA). Nesta reacção, ao
contrário do que acontece no caso dos processos anapleróticos, não há formação líquida de
Página 3 de 4
Ciclo de Krebs ou do ácido cítrico; Rui Fontes
um intermediário do ciclo de Krebs a partir de um outro que o não é. A reacção catalisada
pela síntase do citrato pode ser interpretada como a conversão de um intermediário do ciclo
de Krebs (o oxalacetato) noutro intermediário do ciclo de Krebs (o citrato) e não é uma
reacção anaplerótica. A conversão de acetil-CoA em oxalacetato via reversão da reacção
catalisada pela desidrogénase do piruvato e subsequente carboxilação do piruvato também não
é possível porque a reacção catalisada pela desidrogénase do piruvato é fisiologicamente
irreversível (piruvato + NAD+ + CoA → acetil-CoA + NADH + CO2). A acetil-CoA não
pode, por estes motivos, ser considerada um substrato da gliconeogénese.
13-
A maioria dos ácidos gordos contém um número par de carbonos. Estes ácidos gordos
geram, no seu catabolismo, apenas acetil-CoA e não podem, portanto, contribuir para a
formação de glicose: não são glicogénicos. Pelo contrário, a glicose pode dar origem a
ácidos gordos cuja síntese ocorre no citoplasma partindo de acetil-CoA (lipogénese). A
acetil-CoA excedentária relativamente às necessidades energéticas da célula não pode ser
oxidada a CO2 no ciclo de Krebs mas pode ser convertida em ácidos gordos no citoplasma das
células. No entanto, a acetil-CoA não pode atravessar a membrana mitocondrial porque não
existe transportador para esta substância. O mecanismo que permite de forma indirecta
transportar acetil-CoA para o citoplasma é complexo e envolve as actividades catalíticas da
síntase do citrato (oxalacetato + acetil-CoA + H2O → citrato + CoA) dentro da mitocôndria
(10),
do transportador para o citrato e (citrato mitocondrial → citrato citoplasmático), e
(11)
já no citoplasma, da líase do ATP-citrato (ATP + citrato + CoA
→ oxalacetato + ADP + Pi + acetil-CoA) (12).
O somatório das equações 10-12 mostra que o transporte de acetil-CoA ocorre à custa do
gasto de uma “ligação rica em energia” do ATP:
acetil-CoA (mit.) + oxalacetato (mit.) + ATP + H2O →
acetil-CoA (cit.) + oxalacetato (cit.) + ADP + Pi (13).
1. Balaban, R. S. (2002) Cardiac energy metabolism homeostasis: role of cytosolic calcium, J Mol
Cell Cardiol. 34, 1259-71.
2. Brunengraber, H. & Roe, C. R. (2006) Anaplerotic molecules: Current and future, J Inherit
Metab Dis. 29, 327-31.
3. Owen, O. E., Kalhan, S. C. & Hanson, R. W. (2002) The key role of anaplerosis and cataplerosis
for citric acid cycle function, J Biol Chem. 277, 30409-12.
4. Brunengraber, H., Boutry, M. & Lowenstein, J. M. (1973) Fatty acid and 3- -hydroxysterol
synthesis in the perfused rat liver. Including measurements on the production of lactate, pyruvate, hydroxy-butyrate, and acetoacetate by the fed liver, J Biol Chem. 248, 2656-69.
5. Sharma, N., Okere, I. C., Brunengraber, D. Z., McElfresh, T. A., King, K. L., Sterk, J. P.,
Huang, H., Chandler, M. P. & Stanley, W. C. (2005) Regulation of pyruvate dehydrogenase activity
and citric acid cycle intermediates during high cardiac power generation, J Physiol. 562, 593-603.
6. Bisschop, P. H., Pereira Arias, A. M., Ackermans, M. T., Endert, E., Pijl, H., Kuipers, F., Meijer,
A. J., Sauerwein, H. P. & Romijn, J. A. (2000) The effects of carbohydrate variation in isocaloric
diets on glycogenolysis and gluconeogenesis in healthy men, J Clin Endocrinol Metab. 85, 1963-7.
Página 4 de 4