Infecções transmitidas por
vetores
Profa. Claudia Vitral
Infecções transmitidas por
vetores
vacinação
VETORES:
Agentes infecciosos
artrópodes
HOMEM
hematófagos
(insetos e
carrapatos)
Controle do vetor
DOENÇA
Arbovírus (arthropod-born virus)
• Termo epidemiológico
• Definição: grupo de vírus, genoma RNA,
zoonóticos, transmitidos por artrópodes (mosquitos
e carrapatos)
• Mais de 400 vírus isolados
• Cerca de 100 causam doença no homem: febres
indiferenciadas, encefalites e febres hemorrágicas
• Famílias: Flaviviridae
Buniaviridae
Arenaviridae
Togaviridae
Como os arbovírus são mantidos na natureza ?
Hospedeiro vertebrado
natural
Vetor hematófago
Vetor hematófago
Hospedeiro vertebrado
natural
Homem como hospedeiro
acidental carreia vírus
para zona urbana
Homem
Vetor urbano
Vetor urbano
urbano
Homem
Arboviroses emergentes no Brasil
Condições ideais para ocorrência de
diversas arboviroses
Grande extensão territorial
Mais 1/3 território recoberto por
florestas tropicais ou outros ecossistemas
Cidades
grandes,
populosas,
desordenadamente
ocupadas
e
infestadas de Culex e A. aegypti
Risco: entrada no país de seres
humanos/animais infectados por arbovírus
Arboviroses emergentes no Brasil
Família
Vírus
Vetor
Hospedeiro
Ocorrência
Flaviviridae
Encefalite
Japonesa
(Rocio)
Aedes
Passaros
selvagens
1973/80: 1000
casos encefalite,
SP (Vale
Ribeira)*
West Nile
Culex
Pássaros
selvagens
América do
Norte
Zikavirus
Aedes
Macacos
21 Estados
brasileiros
Estima-se 1.500.000
casos/2016**
Bunyaviridae Oropouche
Aedes, Culex,
Culicoides
Homem
Amazônia, CO*
Togaviridae
Haemagogus
Macacos
Manaus*
Homem
Estima-se 1.500.000
Mayaro
Chikungunya Aedes
*Casos ocorridos no país
*Casos autóctones no Brasil em out/2014
* *Casos autóctones Brasil abr/2015, hoje em toda América
casos/2016*
Febre Amarela: histórico
1500 Entrada dos vetores no país no período colonial com os
navios negreiros: Aedes albopictus (Ásia: tigre asiático) e
Aedes aegypti (África)
1900 Identificação do vírus da febre amarela (Construção do
Canal do Panamá)
1920 Campanhas de Oswaldo Cruz
1942 Últimos registros de febre amarela urbana no país
1955 Erradicação do Aedes aegypti nas Américas
ddt
1976 – Reintrodução do Aedes aegypti nas Américas
1980 – Início das epidemias de dengue
http://www.cdc.gov/ncidod/dvbid/dengue
Febre amarela: formas epidemiológicas
Ciclo silvestre (zoonose)
Vertebrado: macacos (macaco
sentinela: gen. Allouata)
Vetor: mosquitos (gen.
Hemagogus)
Hospedeiro
acidental
Ciclo urbano
Ausente
desde
1942
Aedes aegypti
Patogênese e Manifestações Clínicas da Febre
Amarela
Replicação em monócitos, macrófagos, células endoteliais (= dengue)
HEPATOTROPISMO: lesão de hepatócitos (icterícia)
Baixa de fatores de coagulação: manifestações
hemorrágicas (nasal e gastrointestinal)
Vômito negro (perda de sangue pelo estômago)
Viremia, infecção disseminada
3-4 dias evolução para sobrevida ou óbito (até 20%)
Diagnóstico Laboratorial da Febre Amarela:
Importante no controle epidemiológico da doença
Isolamento viral em camundongos
Inoculação em Ovos embrionados
Detecção viral por PCR
Imunohistoquímica
ELISA para detecção de Anticorpos
VIGILÂNCIA EPIDEMIOLÓGICA DA FEBRE AMARELA NO
BRASIL
Até 1999: vigilância exclusiva de casos humanos
A partir de 1999: observação de mortes de macacos (TO,
GO) seguido do aparecimento da doença na população
(eventos sinalizadores de risco de casos humanos de FA
silvestre)
EPIZOOTIAS: Investigação de
surtos de FA em hospedeiros não
naturais (bugios, micos)
Mortes de macacos/epizootias
2007 = 42
2008 = 229
2009 = >2.000
2010 = 130
Ação: diagnóstico
laboratorial (confirmação)
e vacinação da população
no entorno
VIGILÂNCIA EPIDEMIOLÓGICA DA FEBRE
AMARELA NO BRASIL
Locais de risco no país de febre amarela (áreas de
matas e rios)
Norte/Centro-Oeste: Todos os estados
Nordeste: MA, sudoeste PI, oeste/sul BA
Sudeste: MG, oeste SP, norte ES
Sul: oeste PR, SC, RS
Todos os casos de febre amarela no país são considerados
como resultado de Febre Amarela Silvestre, mesmo aqueles
que envolveram moradores de centros urbanos
Vacina contra febre amarela
Vírus vivo atenuado (cepa 17D)
Confere imunidade por 10 anos
Precisa ser tomada 10 dias antes da
viagem
DENGUE
Dengue: doença emergente
Doença permaneceu restrita (África e Ásia) até a metade do sec XX
Segunda Guerra Mundial: disseminação do vírus (aumento na
circulação de pessoas e transporte do mosquito pelo mundo em cargas)
1944 – Isolamento do vírus do dengue (Sabin): doença benigna
A partir de 1950: Primeiras epidemias de dengue hemorrágico (DHF )
nas Filipinas e Tailândia.
1981: Epidemias de DHF começam a ocorrer na
América Latina e Caribe - reinfestação do mosquito
Dengue hoje: áreas de risco
DENGUE HOJE: Representa a virose de maior morbidade no mundo
Cerca de 3 bilhões de pessoas vivem em risco de contrair a doença nos países
onde o dengue é endêmico
Anualmente, a doença atinge 50 milhões de pessoas, dos quais 500 mil são
hospitalizados, e 25 mil morrem.
Brasil: ~1 milhão casos/ano. Desde 2015 já somam quase 2 milhões/ano
DENGUE
Doença infecciosa aguda febril, de evolução majoritariamente benigna,
causada por um dos quatro sorotipos do vírus da dengue 1-4 (Fam
Flaviviridade, gen Flavivirus)
Os vírus são transmitidos ao homem pela picada da fêmea infectada do
mosquito Aedes aegypti e Aedes albopictus
Infecção assintomática em 50% dos casos
DENGUE
Cada sorotipo confere imunidade sorotipo específica permanente
e contra outros sorotipos por curto período, 2-3 meses (resposta por
IgM é inespecífica): FATOR IMPORTANTE QUANDO CIRCULAM
DOIS SOROTIPOS DO VÍRUS
Todos os sorotipos podem causar doença grave e fatal
Variação genética dentro dos sorotipos: Algumas variantes genéticas
parecem ser mais virulentas e possuir maior potencial epidêmico:
(amostras de DENV 1, DENV 2 e DENV 3 que circulam no país são
mais virulentas - origem asiática)
Níveis de anticorpos
Resposta Imune
IgG
Vírus
Vírus
IgM
IgM
5-7 dias
Infecção
Primária
Infecção
Secundária
Transmissão
Mosquito vetor (fêmeas): Aedes aegypti (Américas)
Aedes albopictus (Äsia)
Mosquito doméstico e antropofílico: vive dentro ou ao redor de domicílios
Hábitos preferencialmente diurnos e alimenta-se de sangue humano
Infestação mais intensa no verão (maior temperatura , aumento das chuvas): 4As (água,
abrigo, alimento e acesso = aumento das pragas urbanas no verão)
Principais criadouros: grandes e pequenos reservatórios de água limpa
Epidemias de dengue:
mosquito +
pessoas suscetíveis + oportunidade de contato
COMBATE CONTÍNUO AOS
CRIADOUROS AO LONGO DE TODO O
ANO
Ovos aderidos próximos a superfície da água
(eliminação ou limpeza das paredes dos
recipientes)
Uma fêmea pode dar origem a 1.500 mosquitos
Ovos distribuídos por diversos criadouros
(dispersão da espécie)
Resistência dos ovos a dessecação (450 dias)
Transporte a grandes distâncias dos ovos:
dispersão passiva dos insetos
“As condições atuais nas
cidades, como a
desorganização urbana, a falta
de saneamento básico e a
coleta de lixo precária, são as
principais causas da
manutenção do mosquito,
tornando sua erradicação hoje
quase impossível”
Diferenças entre A. aegypti e pernilongo doméstico Culex quinquefaciatus
O Aedes é escuro e apresenta marcações
brancas nas pernas e no corpo, enquanto o
Culex apresenta coloração marrom.
O Aedes é muito ágil, se reproduz em água
limpa, ataca em plena luz do dia
O Culex prefere a madrugada, coloca seus ovos
em água suja rica em matéria orgânica e
atormenta as noites de sono com seu zumbido.
Dengue: Transmissão
Infecção do mosquito
1.
Mosquito não infectado se alimenta em um hospedeiro
virêmico infectado (período febril - até o 6o dia da doença) e
ingere sangue contendo vírus
2.
Os vírus se replicam em vários tecidos do mosquito, incluindo
as glândulas salivares.
3.
A transmissão ocorre quando o mosquito, agora infectado,
pica outra pessoa
Infecção do homem
Nos vasos, apos a picada,
todas as células são
suscetíveis ao vírus
O virus vai infectar e se replicar
em monócitos, macrófagos,
células endoteliais
Replicação dos Vírus Dengue
(monócitos, macrófagos, linfócitos B, células endoteliais e dendríticas)
ENDOCITOSE
ssRNA(+)
genômico
Nucleocapsídeo é
liberado no citoplasma
ADSORÇÃO
Síntese de molde
de ssRNA (-)
Progênies de
ssRNA (+)
Helicase + RNA
polimerase RNAdependente &
Cofatores
DESNUDAMENTO
Vírus – Célula
hospedeira via
receptor
celular
Proteínas
Não-estruturais
Diminuição do pH
ssRNA(+)
poliproteína
Fusão da membrana
do vírus
Ptn E sofre mudança
conformacional
Proteases virais e
celulares
Proteínas
Estruturais
TRADUÇÃO
Mediada pelo CAP
MONTAGEM
MORFOGÊNESE
VIRAL
CITOPLASMA
Ocorre no
RER
do
nucleocapsídeo
LIBERAÇÃO
Via secretora
do Complexo
de Golgi
CITOPLASMA
Manifestações do Dengue
INFECÇÃO POR DENGUE
ASSINTOMÁTICA
FEBRE
INDIFERENCIADA
SINTOMÁTICA
SÍNDROME DA
FEBRE DO DENGUE
COM
HEMORRAGIA
SEM
HEMORRAGIA
FEBRE DO DENGUE
HEMORRÁGICO
SEM
CHOQUE
SÍNDROME
DO CHOQUE
POR DENGUE
Síndrome do Choque por Dengue
Teoria da Infecção sequencial (história
passada de infecção pelo DENV)
CDC
Exacerbação imunológica (produção de grande quantidade viral)
Teoria da Virulência da Cepa
Variantes de alta virulência: alta capacidade de multiplicação
desencadeando um excesso de anticorpos (p.ex. 2009, reaparecimento de
DENV-3: muitos casos graves em crianças)
Teoria integral - admite os dois fenômenos ocorrendo
simultaneamente.
Reinfecção pelo mesmo tipo de vírus dengue
Infecção pelo DENV-1 com posterior contato com DENV-1
Anticorpos homólogos formam complexos imunes
estáveis que ao serem fagocitados por macrófagos
não são desfeitos, sendo destruídos
Reinfecção por um tipo diferente de vírus dengue
Infecção pelo DENV-1
Reinfecção pelo DENV-2
Anticorpos heterólogos
formam complexos imunes
instáveis que ao serem
fagocitados por macrófagos
são desfeitos permitindo a
infecção destas células
pelo vírus
Síndrome do choque por dengue
Anticorpos heterólogos
ajudam o vírus a entrar na
sua célula alvo !
Muito vírus
Muito anticorpo
Destruição
maciça
macrófagos
com
de
grande
liberação
de
mediadores
químicos:
tempestade
de
Acúmulo de complexos
imunes e deposição nos
vasos
quimiocinas
Forte reação inflamatória: aumento súbito da permeabilidade
vascular, que resulta em perda de plasma, hipovolemia,
hemoconcentração, queda de pressão, plaquetopenia =
CHOQUE HIPOVOLÊMICO
Protocolo de atendimento aos
pacientes com suspeita de dengue
A apresentação típica da dengue inclui a presença de febre
há menos de 7 dias, acompanhada de pelo menos dois dos
seguintes sintomas:
Cefaléia
Dor retro-orbitária
Mialgia
Artralgia
Prostração
Exantema (com ou sem prurido)
Náuseas ou vômitos
Etapas do atendimento:
Pesquisar situações que aumentam o risco de evolução
desfavorável
Gestantes, crianças, idosos,
comorbidades com potencial de
descompensação clínica
Ficar atento ao diagnóstico diferencial (história
epidemiológica, doenças exantemáticas da infância e
situação vacinal):
Zika, chikungunya, gripe, malária,
febre amarela, febre maculosa,
leptospirose, rubéola, e
sarampo
Etapas do atendimento:
Pesquisar sinais e sintomas de alarme durante anamnese
e exame físico
Dor abdominal intensa e contínua; vômitos
persistentes; sangramento de mucosas;
sonolência ou irritabilidade; hipotermia; plaquetas
abaixo de 50.000/mm3; elevação repentina de
hematócrito acima de 10% do valor basal
Pesquisar sinais de choque durante exame físico
Hipotensão arterial; extremidades frias, cianose;
pulso rápido;
Etapas do atendimento:
Medir:
Realizar prova do laço
pressão arterial; freqüência do pulso;
temperatura axilar; peso corporal.
Petéquias: reação de aumento de
permeabilidade vascular
Etapas do atendimento:
Se indicado, coletar sangue para diagnóstico laboratorial
Hemograma (classificação
clínica B/C/D), plaquetas
Sorologia, teste rápido (NS1)
Acompanhamento do paciente a cada 24h/48h:
hemograma diário (o choque é irreversível)
Níveis de anticorpos
Diagnóstico laboratorial
IgG
Vírus
Vírus
IgM
IgM
1-5 dias 6-21 dias
Infecção
Primária
PTN NS1: 1-9 dias
Infecção
Secundária
Diagnóstico Laboratorial do Dengue
1-5 dias após início dos sintomas (fase aguda):
Isolamento viral em cultura de células
Detecção do ácido nucleico viral
Detecção de NS1
6-21 dias após início dos sintomas (fase
convalescente):
Detecção de anticorpos: IgM (infecção
primária) e titulação de IgG (infecção
secundária - risco de DH)
Ideal: teste precoce de NS1 (confirma se é
dengue) e testes complementares para IgM e
IgG (infecção primária ou secundária)
Classificação da gravidade da dengue:
Paracetamol e/ou
dipirona; repouso
e hidratação oral,
retorno na
melhora da febre
ou a qualquer
sinal de alarme.
Hemograma e
contagem de
plaquetas (mesmo
dia); hidratação
durante a espera;
do resultado
Internação
(emergência –
24h), hidratação
parenteral;
monitoramento
Internação UTI;
hidratação
parenteral;
monitoramento
Etapas do atendimento:
Pesquisar sinais e sintomas de alarme durante anamnese
e exame físico
Dor abdominal intensa e contínua; vômitos
persistentes; sangramento de mucosas;
sonolência ou irritabilidade; hipotermia; plaquetas
abaixo de 50.000/mm3; elevação repentina de
hematócrito acima de 10% do valor basal
Pesquisar sinais de choque durante exame físico
Hipotensão arterial; extremidades frias, cianose;
pulso rápido;
TRATAMENTO
Tratamento sintomático
Reposição
hidroeletrolítica
(oral ou venosa)
+
Medida da
+ Controle da + Transfusão de
plaquetas ou
hidratação
pressão arterial
sangue total
Proibido o uso de salicilatos
Dengue
Medidas de prevenção
Wolbachia pipientis
Bactéria intracelular, presente em mais de 70% de
todos os insetos
Pesquisadores da Universidade de Melbourne,
Austrália, demonstraram a sua capacidade de
impedir a multiplicação do vírus da dengue.
Ovos de A. aegypti foram infectados artificialmente
pela Wolbachia
Uma colônia brasileira de A aegypti com Wolbachia
está sendo gerada na Fiocruz e atualmente
submetida a testes de campo (bairro de Tubiacanga,
Ilha do Governador) visando substituir a população
de mosquitos Aedes do local
Mosquito transgênico (Oxitec)
Desenvolvimento de mosquitos
machos de A. aegypti GM que não
chegam a fase adulta
Ovos de Aedes
aegypti são
transfectados com
dois genes
São liberados 800.000 mosquitos GM semanalmente em dois
bairros de Piracicaba para acasalar com fêmeas selvagens.
Mosquito transgênico (Oxitec)
Quando libertados, esses mosquitos GM
cruzam com fêmeas que geram
mosquitos com essa característica (não
chegam a fase adulta)
Os mosquitos da nova geração
também herdam um gene que
torna mais simples o
monitoramento das larvas no
laboratório. Elas ficam
fluorescentes sob uma luz
específica.
A coleta dos ovos nas armadilhas espalhadas estrategicamente pelo
bairro mostra que 60% dos mosquitos Aedes aegypti presentes na
área de soltura já são geneticamente modificados. Isso significa que
não vão sobreviver até a fase adulta, quando transmitem a doença.
Vacina de Dengue – Aprovada pela ANVISA em 12/2015
Sanofi-Pasteur
Eficácia global de 65,6%, tipo 1 58%, tipo 2 47%, tipo 3 74% e tipo 4 83%.
Introdução dos Vírus Dengue no Brasil
160
DENV-1
140
DENV-2
DENV-3
120
100
80
60
40
20
0
J F M A M J J A S O N D J
F M A M J J A S O N D J F M A M J
Rio de Janeiro
1986 - DENV-1
1990 – DENV-2
2000 – DENV-3*
2009 – DENV-2 + DENV-3
2010 – DENV-1, DENV-2, DENV-3
2011 – entrada do DENV-4
Casos prováveis de dengue por semana
epidemiológica, 2014-2016
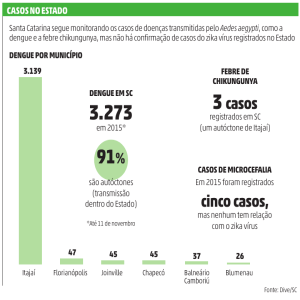
Em 2015, foram registrados 1.649.008 casos prováveis de dengue
(62,2% região SE) até a semana epidemiológica (SE) 52 (04/01/2015 a
02/01/2016)
http://portalsaude.saude.gov.br/images/pdf/2015/marco/13/Boletim-Dengue-SE09-2015.final.pdf
2015: Crise hídrica - população das regiões atingidas pela estiagem
acaba estocando água de forma inadequada.
2016 – Chuvas aumentaram a população de mosquitos
Dengue + Zika + Chikugunya
Comparativo de casos prováveis de dengue entre
2015 e 2016 até a semana epidemiológica 5 por
região
...” e em outubro de 2014...”
Chegada de novos arbovírus!
Alerta: Chikungunya no Brasil
Primeiros casos autóctones no país em outubro/2014:
Feira de Santana (Bahia) e Oiapoque (Amapá)
Distribuição dos casos importados e dos casos autóctones
de febre de chikungunya, por município e Unidade da
Federação de residência, Brasil, 2014 e 2015
Casos autóctones suspeitos:
2014: 3.667 casos em 8 municípios
2015: 20.661 casos em 92 municípios
(14 Unidades de Federação)
ALERTA: Febre chikungunya tem rápida expansão na
América Latina e preocupa Ministério da Saúde
De acordo com um relatório divulgado pela Organização Mundial de Saúde
(OMS), o número de casos de chikungunya nas Américas passou de 111 em
janeiro de 2014 para 1,16 milhão em janeiro de 2016, com 172 óbitos. O
impressionante avanço tem como principais causas a inexistência de uma
vacina e a baixa imunidade da população do continente contra o vírus
causador da doença.
Os países da América Central e do Caribe foram os mais atingidos pela
chikungunya nestes doze meses
A República Dominicana, com 539 mil casos, lidera a lista, seguida por El
Salvador (135 mil casos), Guadalupe (81 mil), Martinica (72 mil) e Haiti (64
mil).
Chikungunya: distribuição mundial
A doença ocorre em quase 40 países da África,
Ásia, Europa e Américas.
O que é a febre Chikungunya ?
Causada por um arbovírus da família da família Togaviridae gênero
Alfavirus
Febre transmitida por mosquitos do gênero Aedes, presente em todo
o Brasil.
Chikungunya significa "aqueles que se dobram" em swahili, um dos
idiomas da Tanzânia.
Refere-se à aparência curvada dos
pacientes que foram atendidos na
primeira epidemia documentada,
na Tanzânia, localizada no leste da
África, entre 1952 e 1953.
Febre Chikungunya
Quais são os sintomas?
Sintomas parecidos com os da dengue, embora mais
intensos
Fase aguda ou febril: febre alta de início súbito e dor intensa
nas articulações* (poliartralgia), acompanhada de fadiga,
dores musculares e na cabeça. Duração: até 10 dias.
Letalidade é rara.
Infecção garante imunidade pelo resto da vida.
Cerca de 30% dos casos não apresentam sintomas.
*Articulações mais afetadas: falanges, tornozelos, pulsos, joelhos,
ombros e coluna
Entretanto...
A Infecção pode levar a dor articular
crônica
Dores articulares prolongadas: 3 meses
(80%) até o resto da vida (42% artralgia
crônica). Dor crônica é resultado de autoanticorpos, em processo autoimune
Chikungunya: diagnóstico
Sintomas semelhantes aos da Dengue e Zikavirus:
necessidade de Diagnóstico diferencial
Vigilância epidemiológica
RT-PCR
ELISA: IgM x IgG
E em abril de 2015...
... confirmada transmissão
autóctone de febre pelo vírus Zika
no país.
No final de 2015 a autoctonia já
havia sido confirmada em 19*
Unidades de Federação
*Hoje são 22 Unidades de Federação – 6 a mais do
que Chikungunya
Zikavirus
2 variantes: asiática (Brasil)
africana
Zikavírus
Transmissão
Vetor: Aedes
● Já foi identificada evidência de transmissão
perinatal do vírus Zika durante um surto na
polinésia francesa em final de 2013 e início de
2014
● Transfusão sanguínea (incluindo transmissão
ocupacional)
● Transmissão sexual
A febre do Zika vírus
Doença febril aguda autolimitada, grande parte das infecções
assintomáticas, período de incubação 4 dias (3 a 12)
SINTOMAS:
- Exantema maculopapular
pruriginoso
- Febre branda
- Hiperemia conjuntival
não purulenta
- Fotofobia
- Artralgia com edema,
mialgia e dor de cabeça
- Linfadenopatia
A história do Zika vírus
O vírus foi isolado pela primeira vez em 1947, a partir do soro de um
macaco rhesus usado como sentinela para febre amarela na Floresta
Zika em Uganda, na África (DICK, 1952; DICK et al., 1952)
Casos humanos de infecção por ZIKV foram descritos 20 anos depois
na Nigéria (década de 1960) e, em seguida, no sudeste da Ásia.
Atualmente a doença é endêmica a leste e oeste do continente
Africano em em algumas áres do sudeste Asiático.
A partir de 2007 surgiram os primeiros casos fora da África
Transmissão autóctone: África, Ásia e Oceania. América do Sul
Casos importados: Ilha de
Páscoa, Canadá, Alemanha,
Itália, Japão, Estados Unidos
e Austrália
Diagnóstico
Não há diagnóstico sorológico
ELISA para Acs dá reação cruzada
com Dengue
Semelhanças filogenéticas e estruturais
RT- PCR (amplificação do RNA viral)
PCR em tempo Real
Laboratórios de Referência
Amostra clínica: sangue (até 4º dia
sintomas)
Imunidade é permanente – só temos Zika uma vez!
.... Em agosto de 2015 a infecção pelo ZIKV mostrou outras
possibilidades de evolução...”
Associação com microcefalia
Semana epidemiológica 3/2016 –
4.180 casos (80% NE) (147 casos
em 2014)
Associação com síndrome de Guillain-Barré