I.
INTRODUÇÃO
Calorímetros são aparelhos que permitem estudar os processos de transferência de
energia térmica e as propriedades térmicas dos materiais. Um calorímetro ideal não permite
qualquer perda de energia térmica para o ambiente e o seu conteúdo pode ser considerado
como um sistema isolado termicamente. Um calorímetro real não tem capacidade térmica
desprezível e há transferência de energia térmica entre o sistema (o calorímetro) e a vizinhança
(o laboratório). Em algumas transformações termodinâmicas a quantidade de energia térmica
recebida por um corpo ao passar de um estado i, em que a temperatura é Ti, a uma estado f ,
com temperatura Tf é proporcional à variação de temperatura ( T f-Ti), isto é:
Q = C.(Tf-Ti),
(1)
onde a constante C é chamada de capacidade térmica do corpo e depende da natureza da
transformação termodinâmica e do intervalo de temperatura. A capacidade térmica de um
corpo é medida em J/K, no SI.
A capacidade térmica C é definida como sendo a quantidade de energia térmica
necessária fornecida a um corpo para que sua temperatura seja elevada de uma unidade de
medida, isto é:
C
Q
,
T
onde T é a diferença entre as temperaturas final T f e inicial Ti.
II. OBJETIVO GERAL
Determinar experimentalmente a capacidade térmica de um calorímetro.
III. LISTA DE MATERIAL
(2)
Tabela 1: Material utilizado
Quantidade
Descrição
M1
1
Calorímetro
M2
1
Termômetro
M3
1
Becher
M4
1
Proveta
M4
1
Garra
M5
1
Aquecedor elétrico
M6
-
Água
VI. ATIVIDADE:
Determinar a capacidade térmica de um calorímetro.
A figura 1 mostra o arranjo experimental que deverá ser montado para o estudo do
fenômeno das trocas de calor.
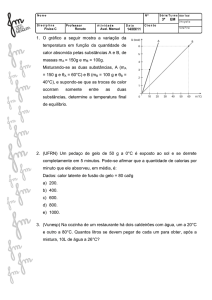
1 - Colocar 250 g de água à temperatura ambiente no calorímetro.
2 - Aguardar o equilíbrio térmico e medir a temperatura inicial do sistema, T 1.
3 - Colocar água no becker e aquecer até a ebulição.
4 - Colocar aproximadamente 100 g água no calorímetro. Aguardar o novo equilíbrio térmico
e medir a temperatura final do sistema, T f.
5 - Determinar a constante do calorímetro.
V. VALORES E CÁLCULOS
m1 = 250 g
T1 =-----------o C
c água= 1 cal g-1.oC-1
m2 =___ g
T 2 = -----------o C
T f =----------o C
T1= Tf - T1 = ------ - --------- = ----------o C
T2 = Tf - T2= --------- - ---------= ---------o C
Dedução da equação:
Pela equação da trocas de calor tem-se
Q 0
ou
Q
recebido
Qcedido 0 . Então:
m1 c T1 + C T1 + m 2 c T2 = 0
C T1 = - m1 c T1 - m 2 c T2
C
(m1T1 m2 T2 )c
(m1cT1 m2 cT2 )
=
T1
T1
VI. OBSERVAÇÕES E CONCLUSÕES:
C =__________ cal oC-1