REAÇÕES DE ADIÇÃO
Hidrocarbonetos insaturados (alcinos, alcenos, ciclanos com 3 ou 4 carbonos, dienos)
Nome
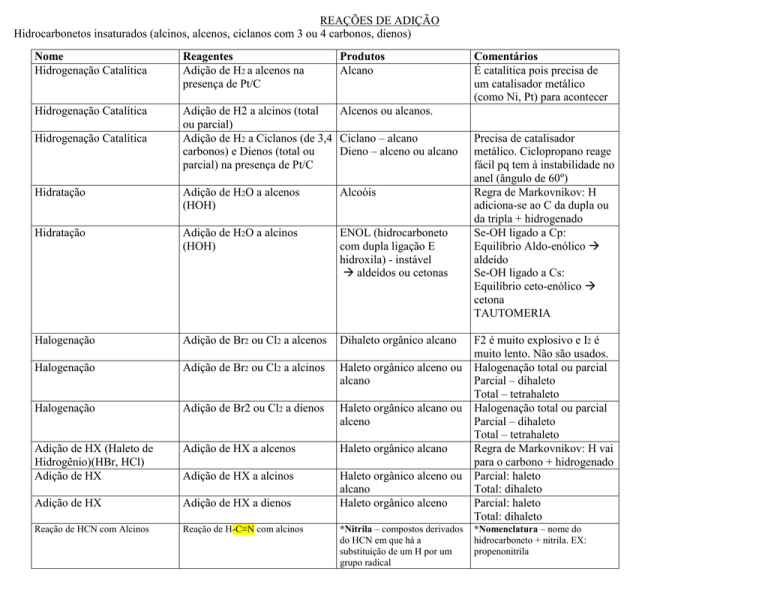
Hidrogenação Catalítica
Reagentes
Adição de H2 a alcenos na
presença de Pt/C
Hidrogenação Catalítica
Adição de H2 a alcinos (total
Alcenos ou alcanos.
ou parcial)
Adição de H2 a Ciclanos (de 3,4 Ciclano – alcano
carbonos) e Dienos (total ou
Dieno – alceno ou alcano
parcial) na presença de Pt/C
Hidrogenação Catalítica
Produtos
Alcano
Hidratação
Adição de H2O a alcenos
(HOH)
Alcoóis
Hidratação
Adição de H2O a alcinos
(HOH)
ENOL (hidrocarboneto
com dupla ligação E
hidroxila) - instável
aldeídos ou cetonas
Halogenação
Adição de Br2 ou Cl2 a alcenos
Dihaleto orgânico alcano
Halogenação
Adição de Br2 ou Cl2 a alcinos
Haleto orgânico alceno ou
alcano
Halogenação
Adição de Br2 ou Cl2 a dienos
Haleto orgânico alcano ou
alceno
Adição de HX (Haleto de
Hidrogênio)(HBr, HCl)
Adição de HX
Adição de HX a alcenos
Haleto orgânico alcano
Adição de HX a alcinos
Adição de HX
Adição de HX a dienos
Haleto orgânico alceno ou
alcano
Haleto orgânico alceno
Reação de HCN com Alcinos
Reação de H-C≡N com alcinos
*Nitrila – compostos derivados
do HCN em que há a
substituição de um H por um
grupo radical
Comentários
É catalítica pois precisa de
um catalisador metálico
(como Ni, Pt) para acontecer
Precisa de catalisador
metálico. Ciclopropano reage
fácil pq tem à instabilidade no
anel (ângulo de 60o)
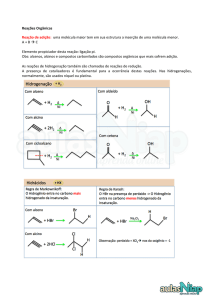
Regra de Markovnikov: H
adiciona-se ao C da dupla ou
da tripla + hidrogenado
Se-OH ligado a Cp:
Equilíbrio Aldo-enólico
aldeído
Se-OH ligado a Cs:
Equilíbrio ceto-enólico
cetona
TAUTOMERIA
F2 é muito explosivo e I2 é
muito lento. Não são usados.
Halogenação total ou parcial
Parcial – dihaleto
Total – tetrahaleto
Halogenação total ou parcial
Parcial – dihaleto
Total – tetrahaleto
Regra de Markovnikov: H vai
para o carbono + hidrogenado
Parcial: haleto
Total: dihaleto
Parcial: haleto
Total: dihaleto
*Nomenclatura – nome do
hidrocarboneto + nitrila. EX:
propenonitrila
SUBSTITUIÇÃO EM HIDROCARBONETOS
Alcanos, aromáticos, ciclanos com 5 ou mais carbonos
Nome
Halogenação em alcanos
Reagentes
Adição de Cl2 ou Br2 a alcanos
(ex: monocloração do metano)
Produtos
Haleto orgânico (preferencial +
outros possíveis) + HCl
Halogenação em cadeia
fechadas
Adição de Cl2 ou Br2 a ciclanos
Haleto orgânico (preferencial +
outros possíveis) + HCl
Halogenação em aromáticos
Adição de Cl2 ou Br2 a aromáticos Haleto orgânico aromático + HCl
Nitração em Alcanos
Substituição de um ou mais Hs
por um grupo Nitro (-NO2) de
origem do HNO3 (HC +
HNO3)
Substituição de um ou mais Hs
por um grupo Nitro em ciclanos
(HNO3)
Substituição de um ou mais Hs
por um grupo Nitro em ciclanos
(HNO3)
Substituição de um ou mais Hs
por um grupo SO3H de origem
do H2SO4
Nitração em Cadeias
Fechadas
Nitração em Aromáticos
Sulfonação em Alcanos
Sulfonação em Cadeias
Fechadas
Nitrocompostos* + H2O
Comentários
SEMPRE NA PRESENÇA DE
LUZ e AQUECIMENTO.
O haleto irá preferencialmente para
o C, segundo a ordem
Ct>Cs>Cp, pois a
eletronegatividade do Cp é mais
forte em relação a seus H.
SEMPRE NA PRESENÇA DE
LUZ e AQUECIMENTO.
O haleto irá preferencialmente para
o C, segundo a ordem
Ct>Cs>Cp, pois a
eletronegatividade do Cp é mais
forte em relação a seus H.
SEMPRE NA PRESENÇA DE
LUZ e AQUECIMENTO.
O aromático só troca um
hidrogênio por um Cl ou Br, mas
não muda sua ressonância.
SEMPRE na presença de H2SO4O
N faz uma ligação dativa no NO2
* Nomenclatura – Nitro + radical,
ex: nitroetano.
SEMPRE na presença de H2SO4O
Nitrocompostos* + H2O
SEMPRE na presença de H2SO4O
Ácidos Sulfônicos* + H2O
Nomenclatura – ácido + nome do
hidrocarboneto correspondente +
sulfônico.
S faz uma ligação dativa
Ex: ácido butanossulfônico.
Ex: ácido ciclopentenossulfônico
Nitrocompostos* + H2O
Substituição de um ou mais Hs
Ácidos Sulfônicos* + H2O
por um grupo SO3H em ciclanos,
p. ex.
Sulfonação em Aromáticos
Substituição de um ou mais Hs
por um grupo SO3H em
aromáticos
Ácidos Sulfônicos* + H2O
EX: ácido benzenossulfônicos
Alquilação – Reação de
Friedel-Crafts
Substituição de um H em um
aromático por um grupo alquila
(Cl – R)
EX: Metilbenzeno/ Tolueno + HCl
SOMENTE EM AROMÁTICOS
É necessário olhar o grupo ligado
ao aromático para sabe onde o
outro R vai se ligar.
Dirigência
Se o grupo for saturado – orto e
para dirigente
Se o grupo for insaturado ou com
dativa – metadirigente.
Acila – era é um ácido carboxílico
em que a hidroxila foi substituída
por um Cl, e que por onde o cloro
sair, vai se ligar a um radical.
Na presença de AlCl3
Acilação – Reação de Friedel- Substituição de um H por um
Crafts – característica de
grupo Acila* - C = O na reação
BENZENO
com um
׀
cloreto ácido R
CETONA + HCl
REAÇÕES DE OXIDAÇÃO
Nome
Combustão Total
Combustão Parcial
Reagentes
Combustível + comburente (O2)
Combustível + comburente (O2)
Oxidação Branda de Alcenos
Alceno + Reativo de Bayer (KMnO4) +
Meio básico (OH-) + H2O
Ozonólise e hidrólise de alcenos
Alceno + O3 + H2O + Zn
Aldeídos – em carbonos secundários
Cetonas – em carbonos terciários
+ H2O2
Oxidação Enérgica de Alcenos
Alceno + KMnO4 + Meio Ácido (H+) +
H2O
Cetonas – em carbonos terciários
Ácidos carboxílicos – em carbono
secundário.
+ H2O
CO2 + H2O
Oxidação Enérgica em Carbonos
Primários Insaturados
Oxidação Enérgica de Ciclanos
Oxidação Enérgica de Aromáticos com
cadeia lateral
Oxidação de Alcoóis
Em alcoóis primários (OH a Cp) Branda
Em alcoóis primários (OH a Cp) Enérgica
Em alcoóis secundários
Ciclano + + KMnO4 + Meio Ácido (H+)
+ H2O
C que sofre a oxidação é o ligado ao OH. Carbonos terciários ligados à
hidroxila não sofrem oxidação.
Álcool + K2CrO7 + Meio Ácido (H+) +
H2O
Álcool + KMnO4 + Meio Ácido (H+) +
H2O
Álcool + KMnO4 + Meio Ácido (H+) +
H2O
Produtos
CO2 + H2O
H2O + C
H2O + CO2
Diálcool
ou
Diácido de cadeia aberta – em ciclanos
não ramificados
Cetona e ácidos em ciclanos ramificados
Somente cetonas em ciclanos
ramificados
SEMPRE ÁCIDO BENZÓICO e CO2 +
H2O
Perde a hidroxila e vira Aldeídos
Perde a hidroxila e vira Ácidos
Carboxílicos
Perde hidroxila e vira Cetona
Comentários
Não libera fuligem
Libera fuligem (no caso do C)
É necessário o reativo, pois ele provocará
a oxidação, e nesse caso somente há
oxigênio o suficiente para quebrar a
ligação π.
Nesse caso ambas as ligações são
quebradas pois há oxigênio o suficiente.
Ele passa por um ozoneto instável, antes
de virar um dos compostos mencionados.
Isso acontece pois há ainda mais
oxigênio reativo para acontecer a
oxidação.
Isso acontece pois o ácido carbônico é
extremamente instável devido as duas
hidroxilas num mesmo carbono.
Em ciclanos haverá a quebra da ligação
sigma, e a cadeia se abrirá. Se houver
ramificação será nesse carbono que
quebrará, e ele virará uma cetona.
Benzeno ligado a um carbono ácido.
O Bafômetro acontece através dessa
reação. Se houver álcool a solução ficará
verde, se não houver, ela permanecerá
alaranjada, por causa do reagente.
Depende da concentração de oxigênio.
Vinho vinagre