imunologia
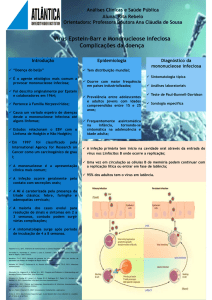
VÍRUS EPSTEIN-BARR
MONONUCLEOSE INFECCIOSA
1. Introdução:
O vírus Epstein-Barr (EBV) é o principal agente da Mononucleose Infecciosa (MI).
Desde a descrição da síndrome em 1920, e dos anticorpos heterófilos na MI, em 1932, por
Paul e Bunnell, grandes avanços foram obtidos no estudo da história natural da infecção
pelo EBV. Em 1950, Epstein, Barr and Achong isolaram o EBV em tecidos de Linfoma de
Burkitt, implicando um papel carcinogênico ao mesmo. Atualmente o EBV têm sido
relacionado com outras doenças além da MI: leucoplasia pilosa, carcinoma de
nasofaringe, desordens mieloproliferativas, linfomas pós-transplantes, linfomas de
células T e Doença de Hodgkin (1,2,3).
Estima-se que 10 a 20% dos pacientes com quadro de MI não tenham infecção
pelo EBV. Síndrome de MI induzida pelo citomegalovírus (CMV) é descrita desde 1965,
sendo que na maioria dos casos não há faringite ou linfonodomegalia cervical posterior.
Ressalta-se que o diagnóstico é dificultado pela possibilidade de reação cruzada do IgM
anti-CMV com o EBV e o fator reumatóide (1,4).
2. Características do vírus:
O EBV pertence à família herpesviridae, infectando células epiteliais da
nasofaringe e linfócitos B que espalham o vírus pelo organismo. Antígenos nucleares
(EBNA) são encontrados nos linfócitos B infectados, que se tornam capazes de
proliferação contínua (imortalizados). Estes linfócitos B produzem imunoglobulinas que
reagem com hemácias de carneiro (anticorpos heterófilos). Pequena parte dos linfócitos B
lisados liberam antígenos específicos do EBV que são divididos em (5,6, 7):
(1) Antígenos precoces, que incluem os antígenos difusos (EA-D) e os antígenos
restritos (EA-R).
(2) Antígenos do Capsídeo Viral (VCA).
Como os demais herpesvírus, o EBV têm a capacidade de estabelecer infecção
crônica, em mais de 90% dos infectados (5,6, 7,8,9).
-1-
imunologia
3. Epidemiologia:
A transmissão do EBV ocorre através da secreção oral. O EBV está presente, em
secreção orofaríngea, em quase 20% dos adultos assintomáticos nos EUA (1,3,5).
Raramente transmissão sexual ou sangüínea é descrita. Homens e primatas são os
reservatórios do vírus, sendo o período de incubação de 30 a 50 dias (7).
Cerca de 90% dos adultos têm evidência sorológica de infecção prévia pelo EBV. A
incidência é maior nas classes sociais mais baixas. O pico de incidência da MI é entre 15 e
19 anos (1,8). Na América do Norte a incidência em brancos é 30 vezes maior que em
negros (1,7, 8).
4. Clínica:
Estima-se que 50 a 75% dos soroconvertidos desenvolvem quadro de MI,
entretanto, em crianças a infecção pelo EBV é geralmente assintomática. Os sinais e
sintomas mais encontrados são: fadiga (70%), mialgias e cefaléia (50%), odinofagia (80%),
exudato
em
amígdalas
(30%),
aumento
das
amígdalas
(80%),
febre
(90%),
linfonodomegalia cervical posterior (80%), esplenomegalia (50%), hepatomegalia (10%),
exantema maculopapular (15%). Após o uso de ampicilina, mais de 90% dos pacientes
apresentam rash cutâneo (reação de hipersensibilidade transitória). O quadro clínico tem
pico em 7 dias e persiste por 1 a 3 semanas (1, 3, 9, 10).
Quadro clínico deve ser diferenciado de infecção pelo CMV, Toxoplasma, HIV, vírus
da
Rubéola,
Micoplasma,
Streptococos
beta-hemolítico,
faringite
viral
e
hipersensibilidade por carbamazepina (3,10).
A maioria dos casos de MI têm evolução benigna, entretanto, complicação são
descritas:
•
Hematológicas:
anemia
hemolítica,
trombocitopenia
e
granulocitopenia
transitórias (10).
•
Quadro neurológico: menos de 1% dos infectados pelo EBV têm complicações
neurológicas: meningite asséptica, encefalite, cerebrite, neurite óptica, retrobulbar, neuropatia do plexo braquial, mononeurite multiplex, mielite transversa,
paralisia de Bell e Síndrome de Guillain-Barre. A associação de EBV e esclerose
múltipla encontra-se sob investigação (11,12,13).
•
Rotura esplênica: ocorre em 0,2% dos casos, em geral, associada a trauma (9).
-2-
imunologia
Não há associação descrita entre infecção por EBV na gestação e aborto ou
defeitos de nascimento (7).
Pacientes imunodeprimidos podem ter quadro clínico atípico, ou reativação de
doença prévia (5). Pacientes com HIV têm quantidade de linfócitos B imortalizados
circulantes 10 a 20 vezes maior que imunocompetentes. Leucoplasia pilosa oral,
Pneumonite Linfóide Intersticial, e Linfoma não-Hodgkin estão associados com o EBV em
portadores de SIDA (3).
5. Infecção crônica e Neoplasias:
Infecção ativa crônica pelo EBV é uma desordem rara, onde ocorre doença severa
com duração superior há 6 meses. Quadro atípico também podem ocorrer em pacientes
portadores de Doença Linfoproliferativa Ligada ao X (Doença de Duncan), uma vez que
não estão aptos a controlar a infecção pelo EBV (3,8).
Cânceres têm sido associados à infecção pelo EBV (1,3,5,6,7,8,10,14):
•
Carcinoma nasofaríngeo: EBV está associado a essa neoplasia que apresenta baixa
incidência no ocidente.
•
Linfoma de Burkitt: é um linfoma de células B de alta malignidade. Em geral,
tumores que se localizam na mandíbula, sendo que 90% dos casos associados ao
EBV. Esse linfomas podem também se apresentar como tumores abdominais.
•
Doença de Hodgkin: material genético do EBV é detectado em 40 a 60% dos
pacientes com essa neoplasia (3,5).
•
Doença linfoproliferativa: associada ao EBV em pacientes com imunodeficiência
congênita ou adquirida.
•
Outros: Linfomas, Leiomiomas, Granulomatose Linfomatóide, Linfoadenopatia
angioimunoblástica, e Linfomas do Sistema Nervoso Central.
6. Diagnóstico laboratorial:
As alterações laboratoriais abaixo descritas são encontradas em pacientes com
quadro clínico de MI:
-3-
imunologia
•
Linfocitose: absoluta (>4.500/mm3) e relativa (> 50% dos leucócitos) em 70% dos
casos. Níveis mais elevados são encontrados nas segundas e terceiras semanas.
Presença de linfócitos atípicos acima de 10% é sugestiva mas não é específica,
podendo também ocorrer na Citomegalovirose, SIDA, Toxoplasmose, Rubéola,
Roséola, Hepatite A, reação a medicamentos, infecções por adenovírus, influenza
A e B, e herpesvírus tipo 6 (15).
•
Neutropenia: em 60 a 90% dos pacientes. A maioria dos casos cursa com
neutrófilos entre 2000 e 3000/mm3, com discreto desvio para esquerda (3,15).
•
Trombocitopenia: 50% casos apresentam contagem de plaquetas inferior a
140.000/mm3. Anemia hemolítica ocorre em 3% dos casos de MI (1,5,15).
•
Elevação de transaminases: aumentos em 2 a 3 vezes ocorrem em 90% dos
pacientes, com pico em 2 a 3 semanas (9).
•
Alterações na sedimentoscopia: proteinúria e piúria são descritos. Hematúria
microscópica em 16% dos casos (5,9).
6.1. Sorologia:
A interpretação judiciosa dos anticorpos heterófilos e dos anticorpos contra
antígenos específicos é de fundamental importância na investigação das infecções pelo
EBV.
6.1.1. Anticorpos heterófilos:
•
Monoteste
•
Reação de Paul Bunnell Davidsohn
São anticorpos (IgM) que reagem contra antígenos da superfície de hemácias de
carneiro e cavalo, mas não com células renais de cobaia. Anticorpos heterófilos não
relacionados ao EBV reagem com células de rim de cobaia. (7,15,16).
•
Reação de Paul Bunnell Davidsohn: caso ocorra aglutinação de hemácias de carneiro
(Paul-Bunnell) em título igual ou maior a 1/56 é efetuado a reação de Davidsohn, por
meio da absorção do soro com hemácias de boi e rim de cobaia. Na MI há redução de
90% do título após absorção por hemácias de boi. Essa absorção permite a
diferenciação dos anticorpos heterófilos da MI daqueles naturalmente encontrados
(anticorpos naturais de Forssman), e dos que ocorrem na Doença do Soro (7,9,15).
-4-
imunologia
•
Monoteste: testes de aglutinação rápida, mais simples, apresentam sensibilidade
semelhante ou ligeiramente superior ao teste de Paul-Bunnell, com a vantagem de
serem mais rápidos (7,15).
•
Interpretação dos Anticorpos Heterófilos: se tornam positivos na MI dentro de 4
semanas após a infecção, diminuem após a fase aguda, mas podem ser detectados por
6 a 12 meses (8,15,16). Cerca de 10 a 20% dos casos de MI podem não apresentar
anticorpos heterófilos. Este fato é mais comum em crianças, uma vez que menos de
50% dos menores de 4 anos de idade têm anticorpos heterófilos detectáveis a
qualquer momento (2,16). Avaliação de diferentes kits comerciais de Monoteste
mostrou sensibilidade de 63 a 84% com especificidade de 84 a 100% (17). Svahn et al.
encontraram sensibilidade de 78 a 85% e especificidade de 99 a 100% para o
Monoteste (5). Bruu et al. encontraram sensibilidade de 81 a 95% e especificidade de
98 a 100% para o Monoteste (18).
Falso-positivos para anticorpos heterófilos têm sido reportados em pacientes com
linfoma, hepatite viral e doenças auto-imunes. Deve-se lembrar que a maioria dos
pacientes imunodeprimidos não produz anticorpos heterófilos (1,5,17).
Nos pacientes com suspeita de EBV, quadro hematológico sugestivo e Monoteste
positivo não há necessidade de determinação de anticorpos para antígenos
específicos. Caso a pesquisa de anticorpos heterófilos seja negativa e ainda exista
suspeita de MI, anticorpos contra antígenos específicos devem ser solicitados (1,8,15).
6.1.2. Anticorpos contra antígenos específicos:
A tabela 1 mostra as características dos anticorpos contra antígenos específicos do
EBV (16). Dos anticorpos descritos os que agregam maior valor diagnóstico são Anti-VCA
IgM e IgG (1,2,7).
•
Anticorpos anti-capsídeo viral: IgM e IgG anti-VCA se tornam rapidamente positivos
em 1 a 2 semanas de infecção. Após 6 meses, IgM anti-VCA se torna indetectável. A
presença de IgM anti-VCA usualmente indica infecção aguda pelo EBV, entretanto,
infecção aguda por outros herpesvírus, podem causar produção de IgM anti-VCA por
células que apresentam infecção latente pelo EBV (1, 19). Falso-positivos de IgM antiVCA também são citados em infecções outras infecções recentes (toxoplasmose,
adenovírus) e auto-anticorpos. IgM anti-VCA falso-negativo pode ocorrer devido à
natureza transitória do IgM (20, 21). IgM VCA persiste por 4 a 8 semanas. Anticorpos
IgG anti-VCA surgem na fase aguda, têm pico em 2 a 4 semanas, persistindo por toda
a vida.
-5-
imunologia
•
Anticorpos anti-EBNA: se tornam detectáveis 6 a 12 semanas após a infecção,
persistindo juntamente com o IgG anti-VCA por toda a vida (5,7).
•
Interpretação dos anticorpos contra antígenos específicos: Imunofluorescência
Indireta foi o método inicialmente utilizado na sorologia para EBV, entretanto é
técnica trabalhosa, apresentando menor reprodutibilidade que o imunoensaio
enzimático (5). Bruu et al. encontraram sensibilidade de 95 a 100% e especificidade de
86 a 100%, utilizando imunoensaios enzimáticos para anticorpos contra antígenos
específicos do EBV. Svahn et al., utilizando imunoensaios enzimáticos (IgM anti-VCA),
encontraram sensibilidade de 95 a 100% e especificidade de 89 a 100% para infecções
agudas por EBV. Observaram ainda sensibilidade de 74 a 88% e especificidade de
100% para o IgG anti-VCA, no diagnóstico de infecção passada (5). Shaade et al. citam
sensibilidade de 100% e especificidade de 97% utilizando imunoensaios enzimáticos,
entretanto, mostram baixa sensibilidade do IgM anti-VCA nos episódios de reativação
da infecção pelo EBV (22). Ressalta-se IgM anti-VCA, por imunoensaio enzimático,
pode ser pouco específico se densidade óptica for próxima ao valor de cutoff
(resultados indeterminados (18,22).
Tabela 1
Anticorpo
Surgimento
Persistência
Específico
VCA IgM
Presença
Comentário
na MI (%)
Fase aguda
4 a 8 semanas
Alta sensibilidade e especificidade.
100
Principal teste para diagnóstico de
infecção primária.
VCA IgG
Fase aguda
Toda a vida
Infecção ativa ou pregressa. Útil
100
EA-D
Pico em 3 a 4 3 a 6 meses
semanas.
para diagnóstico epidemiológico.
Correlaciona-se com doença grave.
70
Presente
em
pacientes
com
carcinoma nasofaríngeo.
EA-R
2
semanas
a 2 meses a mais
vários meses.
de 3 anos
Títulos elevados em portadores de
Baixa
Linfoma de Burkitt Africano. Útil no
diagnóstico de reativação do EBV
em imunodeprimidos.
EBNA
3 a 4 semanas Toda a vida
após a infecção
Aparecimento
100
tardio.
Útil
no
diagnóstico da infecção aguda, onde
não é detectado.
-6-
imunologia
A determinação da carga viral do EBV têm sido descrita como método promissor
no diagnóstico e acompanhamento de pacientes imunossuprimidos e com formas atípicas
de infecção pelo EBV. Necessita-se ainda de padronização das técnicas de PCR utilizadas,
tendo em vista a grande discordância na sensibilidade e especificidade encontradas na
literatura (21,23,24,25).
7. Bibliografia:
1. Godshall SE, Kirchner JT. Infectious
mononucleosis; complexities of a
common
syndrome.
Postgraduate
Medicine. 2000; 107: 175-86.
2. Jacobs SD,DeMott WR, Oxley DK.
Cytomegalovirus serology. In: Laboratory
Test Handbook. Lexi-Comp. 5th. Hudson.
2001. 600.
3. Cohen JI. Epstein-Barr virus infection. N
Engl J Med. 2000; 17: 481-91.
4. Horwitz CA, Henle W, Henle G, et al.
Clinical and laboratory evaluation of
cytomegalovirus-induced mononucleosis
in previously healthy individuals. Report
of 82 cases. Medicine. 1986; 65: 124-34.
5. Svahn A, Magnusson M, Jagdahl L, et al.
Evaluation of three Commercial enzymelinked immunosorbent assay and two
latex aglutination assay for diagnosis of
primary Epstein-Barr virus infection. J
Cin Microbiol. 1997; 35: 2728-2732.
6. Liebowitz D. Epstein-barr virus – na old
dog with new tricks. New Engl J Med.
1995; 332: 55-57.
7. National Center for Infectious Diseases.
Centers for Disease Control and
Prevention. Epstein-barr virus and
infectious
mononucleosis.
http://www.cdc.gov/ncidod/diseases/ebv.
htm. Consultado em 15/05/2002.
8. Tierney LM, Mcphee SJ. Papadakis MA.
Current
Medical
Diagnosis
and
treatment. 41 ed. 2002. 1363-4.
9. Wolf MA. Mononucleose infecciosa. In:
Ferreira AW, Ávila SLM. Diagnóstico
laboratorial das principais doenças
infecciosas e auto-imunes. 2 ed. 2001.
111-5.
10. Rea TD, Russo JE, Katon W, et al.
Prospective study of the natural history
of infectious mononucleosis caused by
Epstein-Barr virus. J Am Board Fam
Pract. 2001; 14: 234-42.
11. Ascherio A, Munger KL, Lennette ET.
Epstein-Barr virus antibodies and risk of
multiple sclerosis. JAMA. 2001; 286:
3083-8.
12. Morré AS, van Beek J, de Groot CJ, et al.
Is Epstein-Barr virus present in the CNS
of patients with MS?. Neurology. 2001;
56: 692.
13. Simon MW. Neurologic Complications of
Epstein-Barr virus infection. Am Fam
Physician. 2000; 61:643-4.
14. Chien YC, Chem JY, Liu MY, et al.
Serologic markers of Epstein-Barr virus
infection and nasopharyngeal carcinoma
in taiwanese men. N Engl J Med. 2001;
345: 1877-82.
15. Schooley
RT.
Epstein-Barr
virus
(infectious mononucleosis). In: Mandell:
Principles and Practice of Infecctious
Disease. 5th. Churchill Livingstone. 2000:
1605-8.
16. Henle W, Henle GE, Horwitz CA. Epsteinbarr virus specific diagnostic test in
infectious mononucleosis. Hum Pathol.
1974; 5: 551-65.
17. Rogers R, Windust A, Gregory J,
Evaluation of a novel dry latex
preparation
for
demonstraion
of
infectious mononucleosis heterophile
antibody in comparison with three
-7-
imunologia
established tests. J Clin Microbiol. 1999;
37: 95-98.
18. Bruu NA, Hjetland R, Holter E, Mortensen
L, et al. Evaluation of 12 commercial
tests for detection of Epstein-Barr virusspecific and heterophile antibodies. Clin
Diagn Lab Immunol. 2000; 7: 451-6.
19. Lang D, Vornhagen R, Rothe M, et al.
Cross-reactivity of Epstein-Barr VirusSpecific Immunoglobulin M antibodies
with citomegalovirus antigens containing
glycine homopolymers. Clin Diagn Lab
Immunol. 2001;8:747-56.
20. Mathenson BA, Chisholm SM, Ho-Yen
DO. Assessment of rapid ELISA test for
detection of Epstein-Barr virus infection.
J Clin Pathol. 1991; 44: 351.
21. Chan KH, NG, MH, Seto WH, Peiris JSM.
Epstein-barr virus (EBV) DNA in sera of
patients with primary EBV infection. J
Clin Microbiol. 2001; 39: 4152-4154.
22. Shaade L, Keines M, Hausler M.
Application
of
virus
specific
Immunoglobulin M (IgM), IgG, and IgA
antibody detection with poliantigenic
enzyme-linked immunosrbent assay for
diagnosis of Epstein-barr virus infection
in Childhood. J Clin Microbiol. 2001; 39:
3902-5.
23. Van Laar JAM, Buysse CMP, Vossen
ACTM,
et
al.
Epstein-barr
load
assessment in imunocompetent patients
with
fulminant
infectious
mononucleosis. Arch Inter Med. 2002;
162: 837-839.
24. Stevens SJC, Pronk I, Middeldorp JM.
Toward standartization of Epstein-Barr
virus
DNA
load
monitoring:
unfractionated whole blood as preferred
clinical specimen. J Clin Microbiol. 2001;
1211-1216.
25. Allen U, Hebert D, Petric M, Telliler R, et
al. Utility of semiquantitative polymerase
chain reaction for epstein-barr virus to
measure virus load in pediatric organ
transplant recipients with and without
posttransplant
lymphoproliferative
disease. Clin Infect Dis. 2001; 33: 145150.
-8-