UFOP
PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA AMBIENTAL PRÓ-ÁGUA
“Redução do teor de sulfato e de metais em águas pela utilização de bactérias
redutoras de sulfato”
Autora: Silvia Nicolato Medírcio
Orientador: Prof. Dr. Versiane Albis Leão
Co-orientador: Adão de Siqueira Ferreira
Dissertação
apresentada
ao
Pró-água, Programa de PósGraduação
Ambiental,
em
Engenharia
como
parte
integrante dos requisitos para
obtenção do título de mestre
em Engenharia Ambiental.
Ouro Preto, Dezembro de 2004
AGRADECIMENTOS
À professora de microbiologia do programa de pós-graduação em Engenharia
Ambiental, Doutora Maria Célia da Silva Lanna, por disponibilizar o laboratório de
microbiologia da UFOP para realização dos ensaios desta tese;
Aos espíritos de luz que me protegem, guiam e inspiram;
Ao companheiro e aliado Pablo dos Santos Pina;
Ao orientador e amigo, prof. Dr Versiane Albis Leão;
Ao amigo e colaborador Adelson Dias Souza;
Aos amigos do NVMM;
À equipe de professores, técnicos, estagiários e alunos dos laboratórios de
Microbiologia, Química, Biofísica e Bioquímica do ICEB;
À equipe de professores, técnicos, estagiários e alunos do laboratório de Biogeoquímica
do DEGEO;
Ao corpo docente e discente do programa de pós-graduação em Engenharia Ambiental;
À coordenação do programa de pós-graduação em Engenharia Ambiental;
Aos professores Mônica Cristina Teixeira e Jorge Adílio Penna;
Muito obrigada.
II
RESUMO
Este projeto objetivou estudar a remoção de sulfato de soluções aquosas utilizando
bactérias redutoras de sulfato (BRS). Na primeira etapa desta pesquisa, utilizou-se um
reator anaeróbio de batelada preenchido com água residuária sintética contendo 4g/L de
sulfato, em pH 7,5. Nesta etapa, foram estipulados os parâmetros mais relevantes para a
identificação da atividade das BRS. Os estudos permitiram a confirmação da presença
de bactérias redutoras de sulfato (BRS); sendo os parâmetros usados para este fim: a
dosagem de sulfato, o teste qualitativo de H2S e as medidas de Eh e de pH. Numa
segunda etapa, foram feitos o isolamento e a caracterização das BRS, paralelamente às
pesquisas de meios de cultivo e aos ensaios de crescimento em pH ácido. Nesta etapa,
foram encontrados dois tipos morfológicos de bactérias na amostra: cocos Grampositivos e bastonetes Gram-negativos; sendo as Gram-positivas mais resistentes à
diminuição do pH e também menos exigentes quanto ao meio nutricional. Nos ensaios
de caracterização, verificou-se que as BRS apresentaram tolerância ao oxigênio devido
à presença da enzima catalase. Para permitir a realização de ensaios em ambiente não
estéril, foi desenvolvido um meio sintético contendo nutrientes semelhantes aos
encontrados no ambiente natural das BRS. Este meio foi denominado meio mínimo
sendo composto, basicamente, por sais inorgânicos e acetato. Os ensaios de pH em meio
tioglicolato 7,5% (v/v) e em meio mínimo foram realizados com o intuito de descobrir
quais condições favoreceriam o crescimento das BRS e a redução de sulfato. Verificouse que existe um pH ótimo, para cada meio de cultivo, no qual o uso de SO4-2 como
aceptor de elétrons é favorecido. Observou-se que, nestes reatores anaeróbios de
batelada, o consumo de sulfato é limitado, mesmo em condições iniciais ótimas. A
biorredução de sulfato a ácido sulfidrico propiciou a precipitação do manganês e do
cádmio. Verificou-se que a precipitação destes metais ocorria somente em reatores que
continham leito de areia; devido à necessidade de formação de biofilme. A alcalinização
do pH ocorreu simultaneamente à precipitação dos metais; enquanto o Eh do meio
chegou a atingir –290mV (Ag/AgCl). Diagramas de EhxpH construídos para o sistema
sugeriram que a precipitação do cádmio ocorreu pela formação de sulfeto enquanto a do
manganês ocorreu pela formação de carbonato.
III
ABSTRACT
This work aimed at the studying of sulfate removal with sulfate reducing bacteria
(SRB). Initially, a laboratory anaerobic reactor was filled with a synthetic wastewater
made up of 4g/L sulfate. The pH was adjusted to 7.5. The results proved that sulfatereduction bacteria are effective in raising pH and removing sulfate from this synthetic
wastewater. The SRB activity was assessed by chemical and microbiological data:
sulfate concentration in solution, redox potential and pH. The presence of hydrogen
sulfide was detected in the aqueous phase by a qualitative test with lead salts. Different
types of growth medium and pH were studied. A “minimum” medium was proposed to
simulate the features of the SRB environment in nature. It was composed of inorganic
salts and acetate as the sole source of organic carbon. Microbiological classification of
SRB included isolation and characterization. During the isolation step, two
morphotypes were observed: coccoid Gram-positive and rod Gram-negative SRB.
Coccoids bacteria were the only morphotype able to growth in the minimum medium.
These bacteria appeared to be more resistance to low pH and low nutrient
concentrations than the rod form ones. The oxygen tolerance, observed during the
experiments, was credited to the presence of the catalase enzyme. The growth of SRB
under acidic conditions was carried out with two different media: tioglicolate 7,5% (v/v)
and the minimum medium. The purpose of these experiments were to analyze: pH range
in which the bacteria remain active, growth potential and efficiency of reducing up to
4g/L of sulfate. It was showed that the reduction of sulfate was limited in batch reactors.
During the experiments with minimum medium containing either manganese or
cadmium, results showed that a chemical precipitation processes occurred and that these
processes accounted for the precipitation of the dissolved metals. Besides reduction and
removal of sulfates, water alkalizing and the decrease of the redox potential were also
ascribed to the SRB activity. However, the presence of a sand layer into the bioreactor
was important for the biological process in laboratory scale. According to EhXpH
diagram, constructed under the conditions of the study, it was suggested that the
precipitation of cadmium and manganese occurred by reaction with sulfide and
carbonate ions, respectively.
IV
SUMÁRIO
I. INTRODUÇÃO
1
II. RELEVÂNCIA DA PESQUISA
5
III. OBJETIVOS
Geral
7
Específicos
7
IV. REVISÃO BIBLIOGRÁFICA
8
V. MATERIAIS E MÉTODOS
1 - Amostra
29
2 - Estudos de Base:
2.1 - Reator
29
2.2 – Solução Nutriente
32
2.3 - Meios de cultura
32
2.4 - Teste qualitativo de H2S
34
2.5 - Contagem de bactérias
34
2.6 - Isolamento das BRS
34
2.7 - Ensaios de pH
35
2.8 - Dosagem de sulfato
35
2.9 - Análise quantitativa de H2S
36
2.10 – Determinação de Eh e pH
36
2.11 - Teste da catalase
36
2.12 - Série bioquímica
37
3 - Aplicação dos Estudos de Base:
3.1 - Preparação do meio mínimo com metal
37
3.2 - Ensaios no reator anaeróbio de batelada
38
3.3 - Ensaios em frascos âmbar, sem adição de areia
38
3.4 - Ensaio em frasco âmbar, com areia
39
3.5 - Ensaios em frascos âmbar de 100mL, com areia
39
3.6 - Diagramas EhxpH
39
V
VI. RESULTADOS E DISCUSSÃO
1. Primeira etapa dos ensaios no reator de bancada.
41
2. Isolamento e caracterização das BRS.
42
3. Meio mínimo e caracterização das BRS.
50
4. Reator anaeróbio de batelada.
55
5. Meios contendo manganês e cádmio em frascos de 100 mL.
60
VII. CONCLUSÃO
73
VIII. SUGESTÕES DE TRABALHOS FUTUROS
75
IX. REFERÊNCIAS BIBLIOGRÁFICAS
76
VI
LISTA DE FIGURAS
Figura 1 - Corte transversal do reator anaeróbio de batelada.
30
Figura 2 - Reator anaeróbio de batelada.
31
Figura 3 - Visão superior do reator anaeróbio de batelada.
31
Figura 4 - Crescimento das BRS em meio sólido formando filamentos;
coletadas do biorreator anaeróbio de batelada.
42
Figura 5 - Isolados B.R., forma de cocos e coloração de Gram positiva.
44
Figura 6 - Isolados T.I., forma de bastonetes e coloração de Gram negativa.
45
Figura 7 - Crescimento da cultura mista (DO de 48 horas) e consumo médio de
sulfato em função do pH, em meio tioglicolato 7,5% (v/v).
48
Figura 8 - Crescimento dos isolados T.I. (DO de 48 horas) e consumo médio de
sulfato em função do pH, em meio tioglicolato 7,5% (v/v).
48
Figura 9 - Crescimento dos isolados B.R. (DO de 48 horas) e consumo médio
de sulfato em função do pH, em meio tioglicolato 7,5% (v/v).
49
Figura 10 - Crescimento dos isolados B.R. em meio mínimo contendo solução
de sulfato de sódio 5,74g/L, acetato de sódio 5,50g/L, nitrato de sódio 1g/L e
fosfato de potássio dibásico 1g/L.
53
Figura 11 - Curva de crescimento do isolado B.R. (BRS Gram positiva) em
meio mínimo (pH = 8,1).
54
Figura 12 - Concentração do manganês dissolvido na parte superior do reator
(PSR) e na parte inferior (PIR) do mesmo. Água de um efluente industrial
contendo, em média, 37,5mg/L de Mn.
56
Figura 13 - Concentração do manganês versus pH.
58
Figura 14 - Concentração do sulfato dissolvido. Água do efluente industrial
contendo 7,7g/L de sulfato em pH 8,0.
60
VII
Figura 15 - Avaliação do crescimento das BRS, em presença de manganês, feita
por turbidimetria (DO) e por contagem direta em câmara de Neubauer.
64
Figura 16 - Avaliação do crescimento das BRS, em presença de cádmio, feita
por turbidimetria (DO) e por contagem direta em câmara de Neubauer.
64
Figura 17 - Relação existente entre crescimento bacteriano e a precipitação do
manganês.
65
Figura 18 - Relação existente entre crescimento bacteriano e a precipitação do
cádmio.
66
Figura 19 - Crescimento bacteriano em presença de manganês e alcalinização do
meio mínimo.
67
Figura 20 - Crescimento bacteriano em presença de cádmio e alcalinização do
meio mínimo.
67
Figura 21 - Crescimento bacteriano, em presença de manganês, versus o
consumo de sulfato.
69
Figura 22 - Crescimento bacteriano, em presença de cádmio, versus o consumo
de sulfato.
69
Figura 23 - Diagrama de EhXpH para o manganês, a 25ºC.
71
Figura 24 - Diagrama de EhXpH para o cádmio, a 25ºC.
71
VIII
LISTA DE TABELAS
Tabela 1: Análises químicas do início e do final da drenagem (Garcia, 2001).
13
Tabela 2: Composição química das camadas de água da barragem (Garcia, 2001).
13
Tabela 3 – Principais dados do reator tipo ABR (Vossoughi, 2003).
23
Tabela 4- Distribuição granulométrica da amostra de areia – Série Tyler.
30
Tabela 5 - Características importantes para classificação das bactérias redutoras de
sulfato (Castro, 2000).
43
Tabela 6 – Resultados da caracterização dos isolados T.I. (Gram-negativas) e B.R.
(Gram-positivas).
46
Tabela 7 – Crescimento das BRS e consumo médio de sulfato em diferentes pH’s.
47
Tabela 8 – Crescimento do isolado T.I. e consumo médio de sulfato em diferentes pH’s.
47
Tabela 9 – Crescimento dos isolados B.R. e consumo médio de sulfato em diferentes
pH’s.
47
Tabela 10 – Crescimento dos isolados B.R. (BRS Gram positivas) e consumo médio de
sulfato em diferentes pH’s.
53
Tabela 11 – Turbidez causada pelo crescimento das BRS em presença dos metais Cu,
Mn e Zn.
62
Tabela 12 – Densidade óptica 600nm (DO600nm) das BRS em presença dos metais Cd,
Mn e Zn.
62
Tabela 13 – DO600nm X Concentração de manganês, em função do tempo.
63
IX
I. INTRODUÇÃO:
No Brasil, as atividades industriais, principalmente as relacionadas à explotação de
minério para obtenção de metais, exercem grande importância econômica e social, com
a geração de divisas externas e absorção de mão-de-obra. Entre os minérios de interesse,
destacam-se os que apresentam em sua constituição os íons de ferro, cobre, alumínio e
zinco. No entanto, a metalurgia extrativa, assim como, as atividades de lavra e de
beneficiamento de minérios apresentam grande potencial de poluição do ar, do solo e
dos aqüíferos. Podem ser citadas como causas da poluição: a extração de metais, a
formação de pilhas dos rejeitos industriais, etc.
Nos processos de remoção de metais contidos em efluentes, rejeitos e resíduos são
adotadas diversas técnicas que envolvem a dissolução, a precipitação, a eletrólise, a
extração por solventes orgânicos, o uso de resinas de troca iônica e de agentes quelantes.
A maioria destas técnicas, isoladas ou em conjunto, têm sido usadas, preferencialmente,
em condições de grande escala, quando as concentrações de metais nos efluentes são
altas. Porém, quando as concentrações de metais são baixas, a utilização de
microrganismos torna-se uma alternativa interessante, tanto do ponto de vista
econômico quanto ambiental (Fortin et al., 2000; Gadd, 2002; Ghigliazza et al., 2000).
Diferentes microrganismos têm sido propostos para remoção de metais, principalmente,
bactérias e fungos.
Particularmente, a mineração e metalurgia de minério sulfetado resultam na oxidação de
enxofre e de ferro podendo levar à formação de água ácida com altas concentrações de
sulfato e de metais pesados, como por exemplo, zinco, cádmio, chumbo, cobre. As
técnicas, tradicionalmente, usadas para o tratamento dessas águas têm sido baseadas em
tratamentos químicos (tratamentos ativos) através da neutralização da acidez e
precipitação dos metais, normalmente, pela adição de cal (Ca(OH)2). As desvantagens
desses tipos de tratamentos estão relacionadas ao custo dos reagentes químicos e a
produção de grande quantidade de resíduos, os quais devem ser dispostos em locais
apropriados (Sengupta, 1993). Além disto, os tratamentos ativos, geralmente, não
1
reduzem a concentração de sulfato para os valores preconizados pela legislação vigente.
Apesar da cal apresentar a propriedade de elevar o pH e de precipitar os metais das
águas residuárias, o nível de sulfato estabiliza-se na faixa de 1400 a 1600mg/L que é
justamente a faixa de solubilidade da gipsita (sulfato de cálcio dihidratado). Em vista
disso, esforços têm sido feitos para desenvolver alternativas para o tratamento de águas
contendo elevados teores de sulfato. O processo biológico de redução de sulfato têm
sido estudado como uma opção de descontaminação dessas águas. O processo é
baseado: na produção biológica de ácido sulfídrico por bactérias redutoras de sulfato
(BRS) (equação 1); na precipitação dos metais pela formação de sulfetos metálicos
(MeS) (equação 2); e, na neutralização da água, decorrente do metabolismo das
bactérias redutoras de sulfato (equação 3) (Widdel, 1988). O símbolo Me representa os
metais bivalentes Cu, Zn, Cd, Mn, Fe, Ni, etc., que encontram-se presentes em
drenagens ácidas de minas (DAM). Os metais que formam íons com valência diferente
de 2 também podem ser precipitados. A fórmula CH2O representa a biomassa.
2CH2O + SO42- → H2S + 2HCO3-
(1)
H2S + Me2+ → MeS(s) + 2H+
(2)
HCO3- + H+ → CO2 (g) + H2O
(3)
Uma das vantagem dos processos biológicos em relação aos processos químicos referese ao seu baixo custo. Outra vantagem, considerando o caso específico das BRS, seria
que os sulfetos metálicos, gerados durante a redução de sulfato a sulfeto, formam um
menor volume de lodo e são menos solúveis, isto é, mais estáveis, do que os hidróxidos
produzidos pelo tratamento químico. Além disso, os metais sulfetados podem ser
recuperados e reciclados. Porém, o tratamento biológico não substitui o tratamento
químico, pois as BRS não sobrevivem em condições drásticas de pH e de concentração
de metais encontradas nas águas ácidas, por exemplo. Ou seja, o processo biológico é
adequado para uma etapa de polimento, após o tratamento químico.
2
As águas ácidas contendo metais, de modo geral, possuem relativamente baixas
concentrações de substâncias orgânicas. Por esta razão, a adição de fontes de carbono
como doadores de elétrons para a redução biológica de sulfato é necessária para
promover a produção de H2S. As bactérias redutoras de sulfatos podem utilizar vários
substratos orgânicos de baixa massa molecular; por exemplo lactato, acetato, etanol,
fumarato e outros. Algumas espécies de bactérias redutoras de sulfato oxidam os
compostos orgânicos completamente, produzindo dióxido de carbono; enquanto que
outras espécies oxidam compostos orgânicos de forma incompleta gerando acetato
(Lens et al., 1998; Burgess e Stuetz, 2002; Beyenal e Lewandowski, 2001; Ingvorsen et
al., 2003; Kaksonen et al., 2003).
Como exemplos da utilização de microrganismos para o tratamento de efluentes podem
ser citadas as estações de tratamento de esgoto (ETES). As ETES utilizam o processo
passivo tanto aeróbio quanto anaeróbio, rotineiramente, no tratamento de esgotos
domésticos. As BRS estão contidas na microfauna dos tanques anaeróbios destas
estações, assim como, de ambientes naturais: brejos, lagoas, rios, oceanos, etc. Estas
bactérias fazem parte do grupo de microrganismos do ciclo do enxofre sendo que a
biorredução do sulfato é uma das muitas etapas de transformação deste elemento na
natureza. Do ponto de vista da saúde pública, a presença de elevadas concentrações de
sulfato nas águas é muito mais danosa que a presença das BRS, pois, além destas
bactérias não serem patogênicas, a simples filtragem da água seria suficiente para retêlas. O problema seria a produção de ácido sulfídrico que é um gás tóxico gerado a partir
do metabolismo das BRS. Porém, este produto pode ser utilizado na precipitação de
metais, ser oxidado a enxofre elementar ou mesmo retido com o uso de carvão ativado
e/ou limalha de ferro.
Este é o primeiro projeto da linha de pesquisa “redução de sulfato com BRS”
desenvolvido no Núcleo de Valorização de Materiais Minerais (NVMM) e visou
estabelecer as condições ótimas para crescimento destas bactérias, bem como, realizar
sua caracterização microbiológica e estudar a precipitação dos metais cádmio e
manganês em reatores de batelada contendo soluções sintéticas. Estas bactérias são
3
responsáveis pela redução do sulfato a ácido sulfídrico, dentro do ciclo do enxofre,
sendo encontradas em regiões anaeróbias ou microaeróbias, como brejos, leitos de rios,
fundo do mar, minas subterrâneas etc. Sua resistência natural a condições adversas,
aliada a sua maleabilidade nutricional, facilita o manuseio das BRS em laboratório e
viabiliza sua aplicação em processos de tratamentos de águas residuárias.
4
II. RELEVÂNCIA DA PESQUISA:
A biotecnologia apresenta amplo potencial de aplicação junto ao setor mineral e
metalúrgico brasileiro, podendo ser citados, como exemplos, a bioflotação, a
biolixiviação, a biooxidação e o tratamento passivo de efluentes. A biorredução de
sulfato, pelo uso de BRS, está incluída entre os processos biotecnológicos aplicados ao
tratamento de efluentes (Von Sperling, 1996). Sendo o ácido sulfúrico um reagente
barato e estável, este é, normalmente, a primeira opção em diversos processos onde fazse necessário o uso de ácidos, como nas indústrias de produção de cobre e de níquel, nas
linhas de galvanização de aços, na produção de ácido fosfórico, etc. Como resultado, os
níveis de sulfato em águas residuárias, destas e de outras indústrias, são superiores aos
permitidos para descarte no curso d’água receptor (250mg/L) (Resolução CONAMA
nº20, 1986). Em função da ineficiência da tecnologia existente para a diminuição dos
teores de sulfato (tratamentos ativos: precipitação com compostos de cálcio, alumínio,
chumbo, bário, etc), faz-se necessário o desenvolvimento de novas tecnologias.
O tratamento de águas residuárias ricas em sulfato pode ser químico, fisico-químico ou
biológico. Por questões ambientais e econômicas, os processos químicos e fisicoquímicos são preteridos sempre que possível. O uso de BRS justifica-se, entre outras
coisas, por: (1) poderem ser manuseadas em condições aeróbias, devido a sua tolerância
ao oxigênio; (2) possuírem capacidade de utilização tanto do nitrato quanto do sulfato
como aceptor final de elétrons, otimizando a desnitrificação; (3) sua capacidade de
remoção de matéria orgânica; (4) liberarem H2S em seu metabolismo, precipitando
metais; e (5) reduzirem a produção de lodo (Lens et al., 1998). O uso das BRS para
redução de sulfato e precipitação de metais mostra-se como uma tecnologia viável, de
baixo custo e que pode contribuir para a diminuição da poluição de cursos d’água. Além
disto, o processo biotecnológico está em acordo com a proposta de “Desenvolvimento
Sustentável”, uma vez que, a biorredução baseia-se no fenômeno natural de autodepuração (Miranda, 2003; Braga, 2002).
5
O tratamento passivo de efluentes industriais, utilizando BRS em reatores anaeróbios,
vem sendo aprimorado, em escala piloto (tanque de 25m3 e vazão de 2m3/h), na
Companhia Mineira de Metais (CMM) do grupo Votorantim e tem apresentado bons
resultados no que se refere à precipitação de metais. O zinco, por exemplo, passa de
500mg/L para 3mg/L após este tratamento. O objetivo do processo é enquadrar os
metais pesados dentro dos níveis estipulados pela Resolução CONAMA nº20 de 1986.
Um grupo de pesquisa do NVMM/UFOP tem acompanhado os trabalhos, não só nesta
empresa, como em outras que apresentam elevadas concentrações de sulfato. A
biotecnologia aplicada na mitigação de impactos ambientais da indústria tem sido tema
de vários editais de instituições relacionadas à pesquisas no Brasil, como, por exemplo,
o CNPq, indicando que o estudo das BRS é um tema em voga e promissor.
No caso brasileiro, a redução dos teores de sulfato acompanha a neutralização da acidez
com a cal que é amplamente disponível e de baixo custo. A precipitação de sulfato com
a cal, porém, não é eficiente a ponto de atingir os limites determinados pela Resolução
CONAMA nº20 de 1986. O efluente deste processo precisa passar por uma etapa de
polimento para adequação do sulfato. Existem, basicamente, duas opções para o
polimento de efluentes ricos em sulfato que são: o tratamento químico (tratamento
ativo) e o tratamento biológico (tratamento passivo). A precipitação química do sulfato
é feita com metais pesados (Pb ou Ba) o que é claramente desaconselhável. O
tratamento passivo, além de utilizar fontes biodegradáveis (esterco, soro de leite, bagaço
de cana, etc) para alimentação do sistema, estas fontes também são amplamente
disponível e de baixo custo. Desta forma, o tratamento biológico apresenta-se como
uma alternativa, ambientalmente correta, para o tratamento do sulfato. Além disso,
existem poucos trabalhos, no país, sobre o assunto e há a necessidade de se adaptar a
tecnologia às condições tropicais.
6
III. OBJETIVOS:
*
Geral
Este projeto tem como objetivo geral estudar a aplicação de bactérias redutoras de
sulfato na remediação de águas com elevados teores de sulfato, pH moderadamente
ácido e contendo metais (manganês e cádmio).
*
Específicos
1. Isolar e caracterizar morfológica e bioquimicamente as BRS.
2. Estudar a redução do teor de sulfato livre em meios de cultura sintéticos.
3. Estudar a precipitação de metais na presença das BRS.
4. Estudar o efeito da variação do pH no crescimento das BRS.
5. Estudar o efeito da variação do pH na redução do sulfato.
6. Avaliar a redução de sulfato em condições reais (amostra de efluente industrial).
7
IV. REVISÃO BIBLIOGRÁFICA
Desde 1960, com o Clube de Roma (Miranda, 2003), a disponibilidade de água doce no
planeta tem feito parte das pautas de discussões de Conferências Internacionais e de
Organizações não Governamentais (ONGs) ligadas ao meio ambiente. Este fato deve-se
ao risco de escassez de água doce no planeta. Sendo a água um recurso natural
fundamental à vida, não só sua quantidade como sua qualidade devem ser preservadas.
Durante a Conferência das Nações Unidas para o Meio Ambiente e o Desenvolvimento,
Rio-92, foi criado um programa de ação denominado Agenda 21 que “apresenta um
roteiro detalhado de ações concretas a serem adotadas até o século XXI pelos governos,
instituições das Nações Unidas, agências de desenvolvimento e setores independentes”
para garantir, dentre outras coisas, a disponibilidade de água para as gerações futuras
(Rebouças et al., 2002; Braga, 2002). Além da Rio-92, outros acontecimentos como a
criação do EMAS - “Eco Management and Audit Scheme” - em 1993, a edição da NBR
ISO 14001, em outubro de 1996 e a priorização do CDM (Mecanismo de
Desenvolvimento Limpo), em 1998, contribuíram para a caracterização da década de 90
como a fase da Gestão Ambiental. Já o século XXI pode ser caracterizado como a fase
do Desenvolvimento Sustentável, sendo os principais temas de discussão a água, a
energia, a saúde, a agricultura e a biodiversidade (Miranda, 2003).
É dentro deste contexto que as “ditas tecnologias limpas” vêm sendo desenvolvidas. Os
objetivos principais desta nova linha tecnológica são: (1) produzir melhor a menores
custos, utilizando materiais adequados, minimizando o consumo de energia, a geração
de resíduos e o impacto ambiental; (2) oferecer produtos seguros e de alto desempenho.
Baseando-se nestes princípios, os processos químicos de tratamento da água vêm sendo
substituídos por processos biológicos (Johnson, 2001). Como exemplos podem ser
citados: os reatores anaeróbios (Von Sperling, 1996), utilizados no tratamento de águas
residuárias; e as Wetlands (Sengupta, 1993), utilizadas no tratamento de águas ácidas de
minas. Tanto os reatores anaeróbios quanto as “Wetlands” foram espelhados em
processos naturais de autodepuração das águas.
8
Quando se refere à disponibilidade de água em uma determinada região, não somente a
sua quantidade como a sua qualidade devem ser avaliadas. No Brasil, em atendimento
ao princípio constitucional de 1988, foi promulgada a Lei nº 9.433, em 9.1.97, que criou
o Sistema Nacional de Gerenciamento de Recursos Hídricos e instituiu a Política
Nacional de Recursos Hídricos cujos objetivos são: (1) assegurar a disponibilidade de
água; (2) assegurar a utilização racional e integrada dos recursos; e (3) assegurar a
prevenção e a defesa contra eventos hidrológicos críticos. Para garantir que os seus
objetivos sejam alcançados, a Política Nacional de Recursos Hídricos faz uso de
instrumentos como os Planos de Recursos Hídricos, o enquadramento dos corpos d’
água em classes de uso (Resolução CONAMA nº 20, 1986), a outorga dos direitos de
uso da água, a cobrança pelo uso da água e o Sistema de Informações sobre Recursos
Hídricos (Braga, 2002; Miranda, 2003).
De um modo geral, a atividade industrial é responsável pela produção de diversos tipos
de poluentes que contaminam os corpos d’água. As atividades de mineração e de
metalurgia, por exemplo, apresentam elevado consumo de água nos seus processos e
apesar do tratamento dado a estes efluentes industriais, uma parte dos poluentes ainda é
liberada nos corpos receptores. Dentre os poluentes pode-se citar o sulfato. Segundo
Lens et al. (1998), são várias as fontes de contaminação de água por sulfato. As
indústrias podem liberar este ânion quando utilizam ácido sulfúrico em larga escala ou
mesmo quando o insumo inclui alimentos ricos em sulfato, como é o caso das indústrias
de alimentos que trabalham com processos fermentativos ou com frutos do mar. Outros
exemplos, são as indústrias que utilizam compostos contendo enxofre, como o H2S
(curtumes, polpa de papel), o SO32- (polpa de papel) ou o tiossulfato (alvejantes,
fixadores fotográficos) que também contribuem para o aumento da concentração de
sulfato no ambiente (Lens et al., 1998).
Em se tratando de qualidade de água, muitos parâmetros são avaliados, dentre eles o pH,
a concentração de sulfato e a presença de metais. Estes parâmetros podem atingir
valores críticos quando determinados em águas provenientes de minerações com
problemas de drenagens ácidas de minas (DAM) (Sengupta, 1993) ou mesmo em
9
indústrias que fazem uso de grande quantidade de ácido sulfúrico em seus processos de
produção. Com o objetivo de reverter ou mesmo de evitar o problema das águas ácidas,
várias pesquisas baseadas em tratamentos biológicos foram desenvolvidas nos últimos
anos. Dentre as linhas desenvolvidas, o uso de bactérias redutoras de sulfato (BRS) em
reatores anaeróbios têm apresentado bons resultados.
As bactérias redutoras de sulfato (BRS) constituem um grupo de procariontes que atua
em funções essenciais no ambiente anaeróbio. Este grupo de BRS pode ser subdividido
em quatro sub-grupos de acordo com as análises de rRNA: Gram-negativo mesofílico;
Gram-positivo formador de esporo; termofílico; e, arqueo-termofílico. Todos estes
grupos têm como característica comum o uso do sulfato como aceptor final de elétrons
(Castro et al., 2000). Algumas características das BRS são utilizadas na classificação
tradicional deste grupo, entre elas a morfologia celular, a motilidade, a temperatura
ótima de crescimento, a oxidação completa ou incompleta do acetato, etc. A tolerância,
em maior ou em menor grau, ao oxigênio e o metabolismo assimilatório ou
dissimilatório do sulfato também devem ser avaliados durante a classificação das BRS
(Castro et al., 2000). A formação de biofilme, inerente a estas bactérias, tem sido
aplicada a processos de tratamento de água (Okabe et al., 2003; Lens et al., 1998).
Os compostos de enxofre podem ser utilizados pelas BRS tanto durante o metabolismo
assimilatório quanto dissimilatório. No metabolismo assimilatório, o microrganismo
precisa reduzir o sulfato para que este seja incorporado aos grupos tiol (valência –2), por
exemplo, dos aminoácidos cisteína, cistina e metionina. No metabolismo dissimilatório,
por sua vez, a redução de sulfato está relacionada ao processo respiratório das BRS,
onde este ânion é utilizado como aceptor final de elétrons. A redução do sulfato durante
a respiração anaeróbia produz ácido sulfídrico que é liberado no ambiente (Grant, 1998).
As características dos microrganismos são importantes para o entendimento de seu
comportamento no ambiente. Observa-se que as BRS Gram-positivas são encontradas,
principalmente, na forma de cocos, apresentam grande tolerância ao oxigênio, podem
utilizar vários tipos de doadores de elétrons (acetato, etanol, anilina, etc) e são
10
resistentes ao calor. Conseqüentemente, este sub-grupo é abundante em ecossistemas
inóspitos para a maioria das outras BRS (Okabe et al., 2003). Esta maior resistência das
bactérias Gram-positivas pode estar relacionada a sua espessa camada de peptidoglicano
na membrana celular. As bactérias são capazes de se adaptar às mais diversas condições
ambientais, incluindo aqüíferos ricos em metais dissolvidos (cobre, zinco, cádmio, ferro,
chumbo, etc) e pobres em matéria orgânica (Esteves, 1998). A capacidade de adaptação
destes microrganismos é uma das vantagens do uso da biorremediação em comparação
ao tratamento químicos e fisico-químicos.
Em se tratando da poluição associada aos processos minero-metalúrgicos, a drenagem
ácida de mina (DAM) é uma de suas formas mais importantes, sendo esta caracterizada
por apresentar elevada acidez (pH<3), alta concentração de metais e de sulfatos
(>3000mg/L) (Sengupta, 1993; Abrahão e Mello, 2003). Assim sendo, o tratamento da
DAM visa alcalinizar, precipitar metais e reduzir o teor de sulfato da água.
Sabe-se que a água considerada classe especial ou classe 1 deve apresentar, entre outros
parâmetros, pH entre 6 e 7, de acordo com a Resolução CONAMA nº 20 de 1986. Este
pH é mantido pelo equilíbrio entre os diversos processos naturais que ocorrem nos
corpos d’água não poluídos. Entre estes processos podem ser citados os anaeróbios.
(Esteves, 1998). As BRS fazem parte destes microrganismos que atuam em condições
anaeróbias e contribuem para a manutenção do pH da água liberando CO2 durante a
redução do teor de sulfato. Parte do CO2 produzido é liberado para atmosfera e parte
permanece em solução aquosa na forma de bicarbonato (HCO3-). Este processo ocorre
naturalmente em corpos d’água não poluídos, contudo, para ser utilizado em um
processo de biorremediação de DAM é necessário adequar as condições do efluente às
condições ambientais específicas que favorecem o crescimento das BRS.
De maneira geral, as BRS requerem um ambiente anaeróbio, com potencial redox menor
que -100mV (Ag/AgCl) e pH maior que 5,5 (Garcia et al., 2001); o que, normalmente,
não é encontrado nas DAM. Porém, as condições presentes no sedimento permanente
dos corpos d’água favorecem o seu crescimento (Esteves, 1998). A formação de micro-
11
ambientes em camadas de solo alagado pode justificar a presença de BRS em barragens
de rejeito, por exemplo, onde as condições gerais são desfavoráveis. Isto pode ser
verificado recolhendo-se água do interstício do sedimento que, normalmente, apresenta
características químicas e microbiológicas distintas das encontradas na água da
barragem. Outra condição ambiental que deve ser observada é a presença de metais. Em
drenagens ácidas, a concentração de metais é elevada e alguns metais, como o cobre, são
tóxicos para as BRS (Garcia et al. 2001).
O estudo das BRS, enquanto alternativa para o tratamento de efluentes ricos em sulfato,
metais e com pH ácido, precisa focar o ambiente natural onde o problema aflorou. Isto
porque, os microrganismos utilizados em uma planta de biorremediação devem estar
adaptados às condições do meio. Com base nesta premissa, Garcia et al. (2001)
desenvolveram um estudo cujo objetivo era tratar a DAM usando BRS coletadas do
sedimento da barragem de rejeito na Espanha. Constatou-se que esta amostra de lodo,
retirada de uma profundidade de 12m (condições anaeróbias), continha uma grande
diversidade de BRS, entre outros microrganismos.
Estes mesmos autores (Garcia et al., 2001) estudaram fenômenos naturais que ocorriam
durante o percurso do rejeito numa mina de pirita; onde foi possível observar, entre
outras coisas, as alterações químicas e microbiológicas desta drenagem, durante o seu
curso. Este rejeito era produzido em um processo de flotação de minério sulfetado
contendo cobre, zinco e chumbo. A composição do rejeito gerado na planta
correspondia a uma polpa de pirita com 30% de sólidos. A polpa percorria 2,3Km, por
gravidade, através de um canal a céu aberto, até chegar à barragem de rejeito. Foi feita
uma caracterização química da fase aquosa despejada na barragem e, para isso, foram
colhidas amostras no início e no final da drenagem. Verificou-se que havia grande
diferença na concentração de metais em condições aeróbias (canal) e anaeróbias
(sedimento da barragem). Garcia et al. (2001) deram continuação aos estudos desta
barragem de rejeito de pirita. Os parâmetros analisados foram pH, Eh, concentração de
sulfato, sulfito, cálcio, magnésio e dos metais Cu, Fe, Zn e Pb. Foi possível observar
que, durante o percurso da polpa até a barragem, a água adquiria características de
12
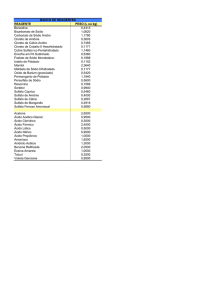
drenagem ácida (condições aeróbias). A tabela 1 apresenta a composição química do
efluente.
Tabela 1: Análises químicas do início e do final da drenagem (Garcia et al., 2001).
Parâmetros
Início da drenagem
Final da drenagem
pH
10
3,5
Eh (mV, Ag/AgCl )
+10
+350
Sulfato (mg/L)
650
2000
Sulfito (mg/L)
120
3
Cu (mg/L)
0,2
0,8
Fe (mg/L)
2,0
55
Zn (mg/L)
2,0
50
Pb (mg/L)
0,2
6
Ca (mg/L)
450
450
Mg (mg/L)
20
55
Uma vez na barragem, ocorria a sedimentação do resíduo sólido e várias transformações
químicas e microbiológicas. O resultado final era a formação de um lodo no sedimento
da barragem e de duas camadas líquidas distintas em função do gradiente de oxigênio:
uma zona anaeróbia, no fundo e uma zona aeróbia, na superfície (água ácida). Estas
camadas apresentavam composições químicas bem diferentes. A água intersticial do
sedimento desta barragem apresentava características semelhantes a água do início da
drenagem enquanto a água superficial da mesma caracterizava-se como água ácida
(tabela 2).
Tabela 2: Composição química das camadas de água da barragem (Garcia et al., 2001).
Parâmetros
pH
Água superficial da
Água do sedimento
barragem
da barragem
3,5
7
Eh (mV, Ag/AgCl)
+350
-45
Sulfato (mg/L)
2000
500
Cu (mg/L)
0,8
0,6
Fe (mg/L)
55
5,0
Zn (mg/L)
50
0,3
13
Paralelamente à diversidade química, avaliou-se também a diversidade microbiológica.
A análise da água superficial da barragem apresentou em torno de 1,1x102 a 7,0x103
NMP/g bactérias litoautotróficas, aeróbias, oxidantes de ferro e de enxofre; e 1,0x103
NMP/g bactérias heterotróficas de várias espécies (NMP = Número Mais Provável). Não
foram encontradas BRS nas amostras de água superficial. Enquanto que a análise de
água intersticial do lodo no sedimento da barragem apresentou BRS na faixa de 1,7x102
a 2,0x103 NMP/g; bactérias litoautotróficas, na faixa de 2,5x101 a 9,5x102 NMP/g; e
heterotróficas, 6,0x101 NMP/g. Com estas análises, foi possível observar que as BRS
cresceram preferencialmente em condições anaeróbias e em locais contendo sólidos
sedimentados (Fortin et al., 2000; Sass et al., 2002). Assim, o sedimento da barragem
funcionou como um biorreator anaeróbio natural.
Estudos em laboratório foram realizados com o objetivo de fornecer dados sobre as
condições ambientais que favoreceram o desenvolvimento das BRS na barragem de
pirita (Garcia et al., 2001). Nesta etapa, foram utilizados os seguintes meios
nutricionais: Postgate’s C; Ágar Nutriente; e meios 9K, sem ferro. Em meio Postgate’s
C, foram feitos três tipos de ensaios, utilizando as BRS, para avaliar: (1) a influência do
pH no desenvolvimento destes microrganismos; (2) a precipitação de metais; (3) o
consumo de sulfato. Nos ensaios de pH, o meio foi ajustado, com a adição de ácido
sulfúrico diluído, para valores iguais a 4, 5 e 7. Nos ensaios de precipitação de metais,
foram utilizadas duas culturas em pH’s diferentes: a cultura Di, adaptada ao pH 5 e a
cultura Ei não adaptada, com pH igual a 7. O meio de cultura Di apresentava 30mg/L de
ferro e diferentes concentrações de Cu (25, 50, 100, 150 e 200mg/L), utilizando-se, para
isso, o sulfato de cobre penta-hidratado. A concentração inicial de sulfato era de
9000mg/L e era analisada pelo método turbidimétrico, com BaCl2. O meio Postgate’s C,
com pH 7 e temperatura de 30ºC, foi utilizado para isolar e enumerar (Número Mais
Provável = NMP) as BRS. As bactérias das amostras de água superficial da barragem de
rejeito foram isoladas e enumeradas utilizando-se os meios 9K sem ferro (Garcia et al.,
2001).
14
Ensaios utilizando o meio Postgate’s C em três diferentes pH’s: 4, 5 e 7, demonstraram
que o pH ótimo para o crescimento da cultura mista de BRS estava entre 7 e 7,5 e que
estas bactérias adaptavam-se a um pH igual a 5. Já em pH moderadamente ácido
(pH=4), as BRS mistas apresentaram dificuldades de crescimento, apesar de terem
demonstrado sinais de atividade como a diminuição do Eh e o aumento do pH do meio
de cultivo. A elevação do pH está relacionada ao consumo de H+ e a produção de CO2
durante o metabolismo destes microrganismos de acordo com a reação de alcalinização
(4) (Garcia et al., 2001). Outros estudos citam o pH 5,5 como ótimo para o crescimento
das BRS que utilizam o lactato como fonte de carbono (Küsel et al., 2001; Lens et al.,
1998) e o pH 3,3 como sendo o valor mais ácido que estes microrganismos suportam
sem perder a capacidade de reduzir sulfato (Elliott et al., 1998). Assim como, a
diminuição do Eh e o aumento do pH, a precipitação de metais é uma conseqüência do
metabolismo das BRS.
Alcalinização: 2H+ + SO42- + 2Corg → H2S + 2CO2 (g)
(4)
Foi observado (Garcia et al., 2001) que tanto as culturas Ei (pH=7) quanto Di (pH=5)
apresentaram bons resultados na precipitação de Cu, para concentrações iguais a 25, 50
e 100mg/L. A concentração de Cu ajustada para 150mg/L, nos meios Ei e Di, fez com
que as BRS apresentassem uma cinética de crescimento extremamente baixa; enquanto
que uma concentração de 200mg/L do mesmo metal levou a inibição total de
crescimento destes microrganismos. Análises de difração de raios-X confirmam a
precipitação dos metais. As formas mais estáveis de precipitação do Fe e do Cu foram,
respectivamente, FeS e CuS (Garcia et al., 2001).
A redução do sulfato é conseqüência da respiração das BRS que gera o H2S por um
processo dissimilatório (Grant, 1998; Widdel, 1988). As análises da concentração de
sulfato demonstraram que em pH 7 houve consumo de 85% (9000mg/L para 1350mg/L)
de sulfato em 27 dias, enquanto, em pH 5, o mesmo consumo ocorreu em 9 dias.
Paralelamente à redução de sulfato, observou-se a alcalinização do pH para um valor
15
igual a 8,2 e a diminuição do Eh para –250mV (Garcia et al., 2001). Estes resultados
foram obtidos em um sistema contínuo.
Os resultados finais demonstraram que o uso das BRS em tratamento de drenagem ácida
de mina era possível desde que fossem respeitadas as exigências ambientais específicas
destes microrganismos (Garcia et al., 2001). Isto significa que os fatores limitantes
como pH, Eh, concentração de sulfato, de H2S, de metais e de matéria orgânica devem
ser avaliados e ajustados, quando possível, para favorecer o crescimento das BRS. Por
outro lado, em ambientes naturais, as bactérias adaptadas são capazes de modificar o seu
micro-ambiente tornando-o propício ao seu desenvolvimento.
Christensen et al. (1996), estudando a biorremediação de águas ácidas, em escala de
bancada, simularam o efeito das BRS no tratamento destas águas usando reatores
anaeróbios de batelada. O objetivo era o mesmo de Garcia et al. (2001), ou seja,
estimular o crescimento das BRS, em seu ambiente natural, para que elas atuassem na
remediação da drenagem ácida de mina. Os reatores utilizados nos ensaios eram
cilindros de acrílico transparente contendo três camadas cada um: duas de sedimento,
compostos de brita e de areia e uma camada superior de água de mina. A mistura de
água usada para alimentar os reatores foi retirada de poços com 120m de profundidade,
visto que, nesta condição, havia maior possibilidade de se encontrar BRS. O soro de
leite de vaca foi usado como fonte de matéria orgânica em todos os reatores exceto no
reator controle. A composição do soro foi relatada como sendo: 5g de lactose, 6g de
proteína, 0,5g de gordura e 6g de cinzas por litro (Christensen, et al., 1996).
Foram utilizados ao todo oito reatores: (1) W1 e W2 - “whey”; (2) WLD - “whey low
dosage”; (3) WCM1 e WCM2 - “whey + cow manure”, eram supridos com 1250mL de
soro mais estrume de vaca; (4) WSRB1 e WSRB2 - “whey + BRS”, foram inoculados
com uma mistura de BRS (5x107 células/mL) e de bactérias fermentadoras (5x107
células/mL) crescidas em um meio composto de lactose e sais minerais. A quantidade de
soro acrescentada em cada reator foi de 1250mL (5,7% v/v), com exceção do reator
WLD que recebeu 50mL (0,2% v/v). A composição da fase aquosa foi previamente
16
analisada, em todos os reatores, segundo os seguintes aspectos: pH; concentração de
sulfato; cálcio; magnésio; alumínio; ferro; cobre; zinco e manganês. Após a adição dos
substrados e dos inóculos característicos de cada reator, os recipientes foram selados e
incubados a 15ºC, no escuro, durante 203 dias.
A princípio, todos os reatores continham oxigênio dissolvido em sua camada líquida,
uma vez que, nenhum cuidado especial foi tomado durante o envase nos recipientes. As
amostras retiradas dos reatores foram avaliadas segundo os parâmetros: Eh; pH; carbono
orgânico total (COT); ácidos graxos voláteis; alcalinidade total e acidez total; número
de bactérias (contagem direta em microscópio); concentração de metais dissolvidos, de
sulfetos, de H2S, de íons amônio, de nitrato e de fosfato.
Passada a fase de adaptação (fase lag), observou-se em todos os reatores, exceto no
controle, o aumento de pH, a formação de biofilme, a diminuição do potencial redox e a
precipitação de um resíduo escuro devido a formação dos sulfetos metálicos de cobre,
zinco, ferro, etc. De um modo geral, o precipitado cinza aparecia primeiro na interface
entre a camada de areia e a camada de brita e expandia-se, paulatinamente, para as
camadas sólidas superiores, de forma que, com o passar do tempo, pôde ser observado a
deposição de um filme escuro sob a parede dos reatores. Testes pontuais mostraram que
a água intersticial da areia e da camada de brita eram alcalinizadas (p.ex. pH=5,9)
prematuramente em relação a água superficial (pH em torno de 3,7). Mas, gradualmente,
as diferenças entre as estratificações diminuiam até deixarem de existir. As alterações
citadas acima ocorreram de forma mais pronunciadas nos reatores WSRB1, WSRB2,
W1 e W2 (Christensen et al., 1996).
No início dos ensaios, todos os reatores que continham 5,7% de soro de leite
apresentaram, na água superficial, 2,0x107 a 3,4x107 bactérias por mL. Sendo que a
forma predominante foi de cocos. Os recipientes inoculados com BRS (WSRB1 e
WSRB2) continham 1,3x106 bactérias em forma de vibrio por mL, além das bactérias
em forma de cocos. Ao longo do experimento, a contagem total, em média, manteve-se
17
em 2,5x107 células por mL, em todos os cilindros supridos com 1250mL de soro
(Christensen et al., 1996).
Analisando-se a presença de ácidos graxos voláteis e de sulfeto livre (40-150mg/L) no
final dos ensaios concluiu-se que os reatores alimentados com 5,7% de soro continham
carbono orgânico em excesso. A conseqüência disto foi o acúmulo de acetato que
chegou a 37% do carbono orgânico total (COT) remanescente no reator W1. O acetato é
produto da fermentação e da oxidação incompleta da matéria orgânica e é substrato da
oxidação completa. Como a fermentação e a oxidação incompleta ocorrem
preferencialmente à oxidação completa, o resultado é o acúmulo de acetato. As três vias
metabólicas – fermentação, oxidação completa e incompleta - podem ser utilizadas por
diferentes grupos de BRS (Lens et al., 1998; Widdel, 1988). Porém, devido à
abundância de substrato, as BRS responsáveis pelo final do processo de transformação
da matéria orgânica (oxidação completa) tiveram seu crescimento inibido (Christensen
et al., 1996). Okabe et al. (2003) consideram a degradação de acetato como uma etapa
limitante em condições anóxicas e sulfidogênicas, devido a maior sensibilidade das BRS
que o utilizam.
Quando vários aceptores de elétrons estão disponíveis no meio, o sistema utiliza aquele
que produz mais energia. E enquanto houver substâncias de maior liberação de energia,
as inferiores não serão utilizadas. Assim sendo, pode-se dizer que a ordem decrescente
de utilização dos aceptores, baseada na liberação de energia, é: oxigênio (O2), nitrato
(NO3-) e sulfato (SO4-2). E as principais reações para geração de energia que ocorrem em
condições aeróbias, anóxicas e anaeróbias são (Von Sperling, 1996):
• Condições aeróbias:
C6H12O6 + 6 O2 → 6 CO2 + 6 H2O
(5)
• Condições anóxicas (-50mV < Eh < 50mV):
2 NO3- + 2 H+ → Ν2 + 2,5 O2 + H2O (redução de nitratos: desnitrificação)
18
(6)
• Condições anaeróbias (Eh < -50mV):
CH3COOH + SO4-2 + 2 H+ → Η2S + 2 CO2 + 2 H2O (redução de sulfatos:
dessulfatação)
(7)
• Condições anaeróbias:
4 H2 + CO2 → CH4 + 2 H2O (redução de CO2: metanogênese hidrogenotrófica)
(8)
• Condições anaeróbias:
CH3COOH → CH4 + CO2 (metanogênese acetotrófica)
(9)
Além do fator energético, a presença de H2S livre em concentrações acima de 40mg/L
começa a inibir a atividade das BRS responsáveis pela oxidação completa, dificultando
ainda mais o consumo do acetato. Porém, a concentração de ácido sulfídrico
considerada tóxica para as BRS depende das espécies presentes, do grau de adaptação
das bactérias e da composição orgânica e inorgânica do meio (Burgess e Stuetz, 2002).
Nos reatores WSRB1, WSRB2, W1 e W2 foram encontrados valores de sulfeto total na
ordem de 6,4x10-3 a 9,3x10-3mol/L, após 203 dias. Tais dosagens de sulfeto
correspondiam a 614 e 893mg/L de sulfato, respectivamente, o que eqüivalia a 19-27%
de consumo de sulfato, sendo que a concentração inicial deste ânion em todos os
reatores era 3306mg SO4-2/L (Christensen et al., 1996).
O maior problema do tratamento biológico de águas residuárias ricas em sulfato é a
produção de gás sulfídrico pelas bactérias redutoras de sulfato (BRS), tanto em
condições anaeróbias (Eh < -50mV) quanto anóxicas (-50mV < Eh < 50mV) (Von
Sperling, 1996). Este gás pode causar falência do sistema de tratamento quando em
concentrações maiores que 150mg/L, devido a sua toxicidade. Esta varia de reator para
reator dependendo da temperatura, do processo adotado (contínuo, batelada, etc), da
alimentação (substratos utilizados: acetato, lactato, propionato, etanol, etc), do pH
(toxicidade diminui em pH alcalino), do lodo (o lodo granular requer concentrações de
sulfeto superiores a 90mg/L para inibir 50% das bactérias metanogênicas, enquanto o
lodo suspenso requer 50mg/L) e da resistência bacteriana.
19
Por outro lado, em águas contaminadas com metais, a presença de H2S é vantajosa. Isto
porque, os sulfetos formam compostos de baixa solubilidade com os metais provocando
a precipitação dos mesmos. Christensen et al. (1996) observaram em seus reatores a
precipitação de alguns metais, entre eles: o cobre, o ferro, o alumínio, o zinco e o
manganês. O cobre foi o primeiro metal a precipitar, devido a formação do sulfeto de
cobre (CuS) que era altamente insolúvel nas condições encontradas na água intersticial
dos reatores. Com a alcalinização do meio, o ferro poderia ter sido precipitado na forma
de FeCO3 ou de FeS considerando-se apenas o pH; porém, verificou-se que a forma
predominante era FeS. A precipitação do alumínio deu-se pela formação de óxido ou
hidróxido deste metal. O zinco e o manganês foram precipitados na forma de sulfetos
(Christensen et al., 1996).
A inoculação extra de BRS nos reatores WSRB1 e WSRB2 encurtou a fase lag e
permitiu a precipitação rápida dos metais, comparativamente aos outros cilindros. Em
contraste, o uso de esterco de vaca apresentou resultados negativos que não foram
esclarecidos (Christensen et al., 1996). Tuppurainen et al. (2002) utilizaram o esterco de
vaca anaerobicamente digerido como inóculo para um reator contínuo do tipo “upflow”
e obtiveram precipitação de zinco (98% de 3,84g) e redução de sulfato (30-40%, na
maioria dos experimentos). A diferença primordial entre os dois processos que
utilizaram o esterco de vaca foi o meio de cultivo. Christensen et al. (1996) utilizaram
um meio rico em matéria orgânica - composição do soro de leite: 5g de lactose, 6g de
proteína, 0,5g de gordura e 6g de cinzas por litro; a quantidade de soro acrescentada em
cada reator foi de 1250mL - o que propiciou o crescimento de vários tipos de
microrganismos presentes no esterco, inclusive microrganismos que competem com as
BRS; enquanto Tuppurainen et al. (2002) utilizaram um meio sintético composto
basicamente por sais inorgânicos e glicose (2000mg/L), com uma elevada concentração
de sulfato (2300mg/L), favorecendo a seleção das BRS.
Christensen et al. (1996) verificaram que a presença de areia no fundo dos cilindros era
de vital importância para o tratamento das águas ácidas pelas BRS. Pois, foi na água
20
intersticial da areia que ocorreram as primeiras alterações químicas, como o aumento do
pH e a precipitação do cobre. Num primeiro momento, verificou-se, também na água
intersticial da areia, o aumento da concentração iônica de ferro e de manganês devido à
dissolução redutiva dos óxidos e hidróxidos destes metais. Outro indício da importância
da areia para o desenvolvimento das BRS foi a deposição prematura de um precipitado
cinza na interface entre a areia e a brita. A explicação para este fenômeno foi
relacionada à necessidade das BRS se fixarem em superfícies sólidas. Estas bactérias
formaram biofilmes sobre a areia e a brita favorecendo a tolerância ao oxigênio e à
presença do cobre em solução (Christensen et al., 1996).
Outros parâmetros avaliados foram as concentrações de fosfato, de nitrato e de amônio,
durante o processo. Com relação ao fosfato e ao amônio, observou-se que, apesar da
concentração de ambos ter diminuido em todos os recipientes contendo soro, suas
concentrações permaneceram relativamente elevadas ao final do experimento. Por outro
lado, o nitrato apresentou concentrações inferiores a 0,1mg/L, durante todo o período de
incubação (Christensen et al., 1996). Esta redução de nitrato pode estar associada ao
crescimento das BRS ou a desnitrificação do meio.
A escolha do processo de tratamento de água residuária rica em sulfato depende do
objetivo do tratamento, que pode ser: remover a matéria orgânica, remover o sulfato,
remover metais ou remover os três. A eficiência na redução do sulfato está relacionada
com a razão DQO/SO4-2 (DQO=Demanda Química de Oxigênio) e com o pH. Em geral,
águas residuárias com DQO/sulfato maior que 10 favorecem a remoção de matéria
orgânica (metanogênese). Em águas residuárias com valores de DQO/SO4-2 inferiores a
10, prevalece a competição por substrato entre as bactérias metanogênicas e as BRS.
Teoricamente, águas residuárias com uma razão DQO/SO4-2 igual ou maior que 0,67
contêm doadores de elétrons suficientes para que as BRS removam todo o sulfato do
meio. Isto porque, a matéria orgânica doa 8 elétrons para cada molécula de sulfato e
apenas 4 elétrons para cada molécula de oxigênio. Desta forma, pode se dizer que 2 mol
de O2 recebem a mesma quantidade de elétrons que 1 mol de SO4-2. Isto equivale a
21
0,67g de O2 por grama de SO4-2, resultando na razão DQO/SO4-2 igual a 0,67 (Lens et at,
1998).
É interessante observar que, para se obter uma razão DQO/SO42- igual a 0,67mg/mg, são
necessários 1200mg de DQO para redução de 1800mg de sulfato. A acidez beneficia a
eliminação do sulfato de duas maneiras: (1) fornecendo o hidrogênio que será
consumido durante o processo de redução de sulfato, o que, consequentemente, aumenta
a produção de H2S(g); e (2) propiciando a pré-acidificação do meio para valores em
torno de 5,0 a 6,5, o que favorece o metabolismo das BRS em detrimento da
metanogênese (Lens et al., 1998; Von Sperling, 1996; Bhattacharya et al., 1995;
Vossoughi et al., 2003). A digestão anaeróbia em dois estágios: acidogênica (para
eliminação de sulfato) e metanogênica (para degradação de matéria orgânica), tem sido
aplicada em vários tipos de reatores, incluindo “upflow filters (reator anaeróbio de fluxo
ascendente com filtro), UASB (reator anaeróbio de fluxo ascendente e manta de lodo) e
fluidized bed reactors (reatores anaeróbios de leito fluidizado)” (Lens et al., 1998).
Vossoughi et al. (2003), utilizando um reator anaeróbio contínuo do tipo ABR
“anaerobic baffled reactor”, estudaram a influência da alteração da razão DQO/SO42(mg O2/mg SO42-) no consumo de sulfato e de matéria orgânica. Neste experimento,
avaliou-se também a interação das BRS com as bactérias acidogênicas e metanogênicas.
O reator era composto de cinco compartimentos, sendo que cada um comportava um
volume de 2L de uma solução sintética contendo melaço como fonte de carbono, uréia
(0,007 g/g DQO) como fonte de nitrogênio e K2HPO4 (0,0006 g/g DQO) como fonte de
fosfato. A concentração da DQO foi ajustada, ao longo do processo, para 3000mg/L
(valor este que foi mantido constante até o final do mesmo) e a de sulfato iniciava com
valor zero (parâmetro inicial de controle), e era aumentada até ajustar-se aos valores
pré-determinados de 150, 180, 350 e 500mg/L, com o acréscimo de sulfato de sódio. A
temperatura do sistema foi mantida em 35ºC e o tempo de retenção hidráulica (HRT) foi
de um dia.
22
A concentração inicial de lodo inoculado no reator foi de 20g/L MLSS “mixed liquor
suspended solids”, ou seja, uma suspensão contendo 20g/L de uma mistura de bactérias
e outros sólidos suspensos. A amostra de lodo em questão foi proveniente de uma planta
de tratamento de água de uma indústria de papel. O tempo de partida do reator foi de
uma semana após a qual determinou-se um ponto zero, referente ao começo das
análises, e o processo ocorreu continuamente. O ponto zero teve início com uma carga
de 1,02Kg DQO/(m3 dia) e 0,09Kg SO42-/(m3 dia), o que equivale a uma razão inicial
DQO/SO42- de 11. Posteriormente, esta razão DQO/SO42- foi aumentada para 12 1,80Kg DQO/m3 e 0,15Kg SO42-/m3 - e depois para 16,7, onde ajustou-se a DQO
afluente para 3,00Kg DQO/(m3 dia) (tabela 3) (Vossoughi et al., 2003).
Tabela 3 – Principais parâmetros estudados por Vossoughi et al., 2003:
Parâmetros
Razão
-2
DQO/SO4
Partida
Período 1
P2
P3
P4
P5
12-16,7
16,7
15
12
8,6
6
DQO afluente (mg/L)
1800-3000
3000
3000
3000
3000
3000
DQO efluente (mg/L)
480
440
480
480
410
430
-2
SO4
afluente (mg/L)
150-180
180
200
250
350
500
-2
SO4
efluente (mg/L)
20
20
13
19
16
16
83
85
84
84
86
86
40-24
24
24
24
24
24
1380
1400
1450
1500
1800
1950
6-7,1
6-7,1
6-7,2
6-7,2
6-7,2
6-7,2
40
43
45
52
57
65
1,02-3
3
3
3
3
3
Remoção de matéria orgânica
no efluente (DQOmg/L)
Tempo de retenção hidráulica
(h)
Alcalinidade do efluente,
bicarbonato (mg/L)
pH (1ºcompartimento-5ºcomp.)
Sólidos suspensos (MLSS) no
efluente (mg/L)
Carga orgânica padrão, Kg
3
DQO/(m .dia)
No final do processo, ou seja, após 115 dias de operação a razão DQO/SO42- apresentou
um valor igual a 6, sendo a concentração de sulfato mantida em 500mg/L. Neste
período, pôde ser observado um pequeno aumento na remoção de matéria orgânica (de
83% para 86%) devido às BRS (Vossoughi et al., 2003). Isto porque, as BRS têm o seu
23
crescimento favorecido pelo aumento da concentração de sulfato no meio e são capazes
de competir por substrato (matéria orgânica) com as bactérias metanogênicas,
aumentando o consumo do mesmo (Lens et al., 1998; Von Sperling, 1996; Bhattacharya
et al., 1995; Vossoughi et al., 2003).
Há situações em que as BRS utilizam a fonte de carbono orgânico por duas vias
metabólicas diferentes (Vossoughi et al., 2003). Isto ocorre, por exemplo, com as
Desulfovibrio desulfuricans que usam o piruvato (CH3COCOO-) tanto na respiração
(reação 10) quanto na fermentação (reação 11), reforçando a tese de que as BRS são
capazes de competir por substrato com as bactérias metanogênicas (Lens et al., 1998;
Von Sperling, 1996; Bhattacharya et al., 1995; Vossoughi et al., 2003).
Respiração: 4CH3COCOO- + SO42- → 4CH3COO- + 4CO2 + S2-
(10)
Fermentação: CH3COCOO- + H2O → CH3COO- + CO2 + H2
(11)
No final do processo, Vossoughi et al. (2003) observaram também a alcalinização da
solução, devido à redução de sulfato. A alcalinização demonstra, também, a estabilidade
operacional do sistema. A remoção do sulfato afluente ocorreu de maneira significativa
(65%) no primeiro compartimento do reator que continha microrganismos acidogênicos
e apresentava um pH em torno de 6. Isto porque, as BRS e as bactérias acidogênicas
coexistem em simbiose (Vossoughi et al., 2003). Estas últimas degradam a matéria
orgânica complexa em substâncias simples (acetato, piruvato, etc) que são utilizadas
pelas BRS como fonte de carbono. A acidez provocada pela fermentação também
favorece a redução do sulfato a sulfeto (Garcia et al., 2001).
Estudos mostram que, tanto em ambientes naturais quanto em reatores anaeróbios, as
BRS e as bactérias produtoras de metano (BPM) competem entre si pelo substrato (Lens
et al., 1998). Bhattacharya et al. (1995), utilizando o acetato como única fonte de
carbono para ambos os tipos de bactérias (BRS e BPM), relacionaram a competição
entre elas à razão acetato/sulfato e ao potencial redox em um sistema anaeróbio
24
contínuo e em série. Para realização desta pesquisa, foram utilizadas três culturasestoque: cultura I, contendo bactérias produtoras de metano (BPM); cultura II, contendo
BRS e BPM; e cultura III, contendo apenas BRS. As culturas-estoque eram compostas
por um meio rico em sais inorgânicos acrescido de 10mg/L de cisteína e 3000mg/L de
bicarbonato. A temperatura de incubação era de 35 ± 1ºC, com tempo de retenção de 50
dias e uma carga de acetato de 500mg/L.dia para todas as culturas-estoque
(Bhattacharya et al., 1995).
Os meios, porém, diferiam entre si no que se refere à razão acetato/SO42-, que
apresentava valores iguais a 20 na cultura I, 5 na cultura II e 0,5 na cultura III. A cultura
III tinha como peculiaridade: a inserção de 2x10-3mol/L de ácido sulfônico 2
bromoetano (BESA) que é inibidor das BPM. As culturas puras foram utilizadas para
ensaios cinéticos - como o estudo das curvas de consumo de acetato usadas para
determinar os valores de k (constante de velocidade, 1/d) e ks (coeficiente de velocidade
média de Monod, mg/L) – e para o cálculo dos coeficientes de crescimento das BRS
(0,0602mg de célula/ mg de acetato) e das BPM (0,0346mg de célula/ mg de acetato).
As equações cinéticas de Monod, para velocidade de utilização de substrato (12a) e para
crescimento da biomassa (12b), apresentam-se abaixo (Vossoughi et al., 2003):
dS
kSX
=−
(k s + S )
dt
(12a)
dX
YkSX
=−
− bX
(k s + S )
dt
(12b)
Onde:
k = constante de velocidade, 1/d
ks = coeficiente de velocidade média de Monod, mg/L
S = concentração de substrato, mg/L
X = concentração da biomassa, mg/L
Y = coeficiente de crescimento, mg de células/ mg de acetato
b = coeficiente de decaimento, 1/d.
25
Fazendo uso do modelo de Monod para avaliar a constante (k) de degradação de acetato
e o coeficiente de velocidade média de Monod (ks), verificou-se que seus valores eram
menores para as BRS (k=2,4/d; ks=102mg acetato/L) quando comparados aos obtidos
para as BPM (k=3,2/d; ks=116mg acetato/L), o que significa que as BRS têm maior
afinidade pelo acetato que as BPM. Desta forma, quando a razão acetato/SO42- apresenta
valores próximos aos valores estequiométricos da reação 13 - acetato/SO42-=0,66g/g - o
consumo de sulfato é favorecido. As equações estequiométricas utilizadas para avaliar a
metabolização do acetato pelas BRS (13) e pelas BPM (14) foram (Vossoughi et al.,
2003):
32CH3COO- + 30SO42- + 49H+ + NH4+ → C5H7O2N + 33H2O + 28CO2 + 31HCO3- +
15H2S + 15 HS55CH3COO- + 51H2O +
(13)
3
105
CO2 + NH4+ → C5H7O2N + 54HCO3- +
CH4
2
2
(14)
A fórmula C5H7O2N representa a biomassa resultante do processo. Após os
modelamentos cinéticos e o cálculo estequiométrico do consumo de acetato pelas BRS e
pelas BPM, foram feitos os ensaios para avaliar a influência da razão acetato/SO42- na
competição entre estas bactérias, acompanhando-se, para isso, a relação entre o
consumo de sulfato, a produção de H2S e o consumo de acetato. A cultura II (mista) foi
inoculada em dois sistemas, um em batelada, “serum bottles”, e outro contínuo, o
“chemostat”, ambos utilizando os mesmos três valores para razão acetato/SO42- que
foram: 0,66, 2,0 e 3,33mg/mg (Bhattacharya et al., 1995).
O sistema “serum bottles” apresentava duas concentrações de acetato: (1) 250mg/L com
razões de acetato/SO42- iguais a 0,66, 2,0 e 3,33mg/mg e (2) 100mg/L com as mesmas
razões acetato/SO42-. A porcentagem de acetato consumida pelas BRS era calculada com
base nas concentrações medidas de sulfato e acetato (equação 13). Considerava-se que o
restante de acetato era utilizado pelas BPM. No sistema “chemostat”, três reatores de
2L, com tempo de retenção de 10 dias, foram usados para determinar o efeito das três
26
razões de acetato/SO42- na competição entre BRS e BPM. Cada “chemostat” continha
1,5L da cultura II. Para valores de acetato/SO42- iguais a 0,67mg/mg, o consumo de
acetato pelas BRS atingiu seu ponto máximo tanto em “serum bottles” (40%) quanto em
“chemostat” (71%) (Bhattacharya et al., 1995).
Quando o valor da razão acetato/SO42- aumentava para 3,33 o consumo de acetato pelas
BRS era de apenas 15% em “serum bottles” e 4% em “chemostat”. Isto eqüivale a dizer
que, por terem maior afinidade pelo acetato, as bactérias redutoras de sulfato
prevalecem em ambientes com baixa concentração deste. Em condições naturais, a
concentração de acetato tende a ser baixa o suficiente para favorecer a utilização deste
substrato pelas redutoras de sulfato (Bhattacharya et al., 1995).
Outro fator que influencia na competição entre as BRS e as BPM é o potencial redox.
Por serem tolerantes ao oxigênio, as sulfato redutoras não necessitam de um ambiente
redutor tão extremo quanto as BPM (Eh=-380mV). Esta tolerância deve-se a presença
das enzimas superóxido dismutase, catalase e NADH oxidase que evitam danos
celulares em condições aeróbias ou anóxicas (Bhattacharya et al., 1995; Cypionka et al.,
1985). O estudo do potencial redox, enquanto fator determinante na competição entre
BRS e BPM, baseou-se na utilização da cultura-estoque II (cultura mista) em duas
condições distintas: -75mV e -175mV (Bhattacharya et al., 1995).
Após os ensaios, observou-se que as BRS aumentavam o seu consumo tanto de acetato
(19% para 35%) quanto o de sulfato (208mg/L para 345mg/L) quando o potencial redox
(Eh) aumentava de -175mV para -75mV. Provavelmente, este fato deve-se mais à
inibição das BPM em condições pouco redutoras do que propriamente pela maior
atividade das BRS neste potencial redox (-75mV). Esta conclusão baseia-se em estudos
anteriores que relatam valores de -100mV a -200mV (Ag/AgCl) como sendo uma faixa
ótima de Eh para as BRS (Garcia et al., 2001; Esteves, 1998). No final do estudo do
potencial redox, observou-se, ainda, que a concentração total de sulfetos dissolvidos era
de 80mg/L para -75mV e de 125mg/L para -175 mV, em um pH de 7,5 ± 0,3. Isto
significa que os sulfetos são mais estáveis em condições mais redutoras (-175mV).
27
Considerando todos os estudos aqui relatados, pode-se concluir que vários fatores
influenciam o metabolismo das BRS, entre eles: (1) o processo – contínuo ou em
batelada; (2) a quantidade e a qualidade da matéria orgânica; (3) o pH; (4) a presença de
suporte sólido para a formação de biofilme; (5) a concentração de H2S; (6) a presença de
outros aceptores de elétrons juntamente com o sulfato; e (7) o Eh. Tratando-se,
especificamente, da redução do sulfato, pode-se dizer que esta está relacionada com a
razão DQO/SO4-2 (DQO=Demanda Química de Oxigênio), com o pH e com o processo.
A utilização das BRS para redução de sulfato requer um sistema contínuo, enquanto que
para precipitação de metais pode ser usado um sistema em batelada. Porém, o uso da
biorredução em um sistema de tratamento em larga escala requer o conhecimento prévio
de questões de ordem prática, como exemplos: a composição química da água a ser
tratada; as vazões do afluente e do efluente; da vazão do corpo d’água receptor; a
cinética do processo; entre outros.
28
V. MATERIAIS E MÉTODOS
1 – Amostra
A amostra de água utilizada foi proveniente do grupo de pesquisa do professor José Luiz
Cortina da Universidade Técnica da Catalunha, que gentilmente a cedeu.
Aproximadamente 250mL de água, contendo BRS, possibilitaram o início da pesquisa.
2 - Estudos de Base:
2.1 - Reator
O reator anaeróbio de batelada (Elliott et al., 1998; Von Sperling, 1996; Christensen et
al., 1996) consistiu de um cilindro de PVC de 49cm de altura e 15cm de diâmetro,
fechado na extremidade inferior e contendo uma tampa móvel na parte superior. Foi
feito um orifício para saída de gás (H2S, CO2). A estrutura dispõe ainda de uma torneira
localizada na parte inferior do reator (figura 1). O volume total foi igual a 7,75L e o
volume útil 4,75L. A parte interna do reator encontra-se dividida em: (1) camada
suporte, contendo esferas de vidro, de diâmetro médio de 1cm; (2) placa vazada de
PVC; (3) duas camadas de fibra de vidro; (4) camada de areia de volume igual a 1,5L;
(5) camada líquida contendo meio líquido.
Retirando-se a tampa do reator foram coletadas amostras da parte superior do mesmo
com auxilio de uma pipeta de 50ml. As coletas de amostras da parte inferior do reator
eram efetuadas pela torneira.
29
Orifício da tampa →
Camada líquida →
Parte superior
do reator
Camada de areia →
Fibra de vidro e Placa de PVC →
Camada suporte →
Parte inferior
do reator
Figura 1 – Corte transversal do reator anaeróbio de batelada
Foi feita análise granulométrica da areia usando as peneiras da série Tyler. Para isto,
foram pesados inicialmente 200g da mesma. O resultado obtido encontra-se na tabela 4:
Tabela 4- Distribuição granulométrica da amostra de areia – Série Tyler
Abertura (mm)
Massa retida (g)
+1,20
% Retida
0,00
-
-1,20
+0,85
0,04
0,02
-0,85
+0,71
0,30
0,15
-0,71
+0,42
6,49
3,24
-0,42
+0,30
53,30
26,65
-0,30
+0,21
82,60
41,3
-0,21
+0,15
46,83
23,42
-0,15
+0,10
8,71
4,36
-0,10
+0,053
1,65
0,82
-0,053
0,06
0,03
Total
199,98
99,99
Foi utilizado um termostato para estabilizar a temperatura da camada líquida em 33ºC.
Este termostato fazia circular água quente em uma serpentina ao redor do reator. Esta
30
serpentina possuía uma camada de isolamento térmico facilitando a manutenção e o
controle da temperatura interna do reator (figuras 2 e 3).
Figura 2 – Reator anaeróbio de batelada.
Figura 3 – Visão superior do reator anaeróbio de batelada.
31
2.2 – Solução nutriente
O meio líquido utilizado no reator era composto por sulfato de sódio 5,74g/L e acetato
de sódio 5,50g/L dissolvidos em água de torneira. Esta solução foi a base para
preparação dos diferentes meios de cultivo utilizados no presente trabalho.
2.3 - Meios de cultura
A padronização do inóculo foi feita pela densidade óptica (DO) em 600nm
(espectrofotômetro UV-Visível) estipulada em 0,09 ± 0,01 de absorvância, o que
eqüivale a um número mais provável (NMP) de bactérias próximo a 107 ufc/mL
(unidade formadora de colônia por mL). Todos os meios de cultura e os materiais
utilizados nos procedimentos foram autoclavados.
O meio fluido de tioglicolato é um meio rico em matéria orgânica, normalmente usado
para crescimento de bactérias anaeróbias. Sua composição em g/L é:
Peptona de caseina......................................................................................15,0g
Extrato de levedura........................................................................................5,0g
D-Glucose.....................................................................................................5,5g
Cloreto de sódio............................................................................................2,5g
L-Cistina.......................................................................................................0,5g
Tioglicolato de sódio....................................................................................0,5g
Ágar...............................................................................................................1,0g
Resazurina certificada...............................................................................0,001g
pH a 25ºC: 7,0
O extrato de levedura é fonte de vitamina B, proteínas, combinações fosfóricas e cinzas
favorecendo o crescimento de leveduras. A peptona de caseína contém nitrogênio
orgânico (15%) e vitaminas. O tioglicolato de sódio e a resazurina são substâncias que
favorecem o caráter redutor do meio (Pelczar, 1996).
32
Foram utilizados 30g do meio fluido de tioglicolato em pó para preparar 1L de solução.
Após o preparo da solução, o meio era autoclavado e então utilizado. No estudo em
questão, este meio foi usado em várias proporções diferentes, de acordo com o objetivo
do ensaio.
Os meios de cultura utilizados neste estudo foram:
a) Meio tioglicolato 7,5% (v/v): solução de sulfato de sódio 5,74g/L e acetato de sódio
5,50g/L + 7,5% de meio fluido tioglicolato (v/v). Usado nos ensaios para verificação do
efeito do pH no crescimento bacteriano.
b) Meio tioglicolato 2% (v/v): solução de sulfato de sódio 5,74g/L e acetato de sódio
5,50g/L + 2% de meio fluido tioglicolato (v/v). Usado para padronizar o inóculo.
c) Meio sólido: 50% da solução de sulfato de sódio 5,74g/L e acetato de sódio 5,50g/L
+ 50% de meio fluido tioglicolato (v/v) + 1,5% de ágar (m/v). Usado na identificação,
contagem e manutenção de colônias;
d) Meio mínimo: solução de sulfato de sódio 5,74g/L, acetato de sódio 5,50g/L, nitrato
de sódio 1g/L e fosfato de potássio dibásico 1g/L. Simula condições encontradas em
sedimentos permanentes (anaeróbios) de corpos d’água (Esteves, 1998).
O meio tioglicolato 2,0% (v/v) foi usado para crescimento de inóculo, em 24 horas. Isto
porque, nestas condições, o crescimento bacteriano enquadrava-se no padrão de DO préestabelecido para inóculo. O meio tioglicolato 7,5% (v/v) foi usado como padrão para
ensaios de pH por permitir um crescimento rápido das BRS e por apresentar uma DO de
24 horas superior a 0,200 de absorvância.
33
2.4 - Teste qualitativo de H2S
O teste qualitativo de H2S consistiu em colocar um papel de acetato de chumbo (Otto
Bier, 1966) no orifício da parte superior do reator, de modo que o gás, ao sair, passe
pelo papel. O papel de acetato de chumbo 0,2% é feito utilizando papel de filtro
embebido em solução de acetato de chumbo 0,2%, secado à temperatura ambiente. Após
a secagem, a presença de cor enegrecida no papel (PbS) é considerada como resultado
positivo para H2S.
2.5 - Contagem de bactérias
O crescimento bacteriano foi avaliado por: contagem direta em câmara de Neubauer,
leitura de densidade óptica de 600nm em espectrofotômetro e número mais provável
(NMP). O método de contagem direta fornece o número aproximado de bactérias por
mL de meio de cultivo, enquanto a DO apenas detecta o aumento da turbidez do meio
pela presença de sólidos suspensos, dando uma estimativa do crescimento bacteriano. O
número mais provável (NMP) foi determinado após diluições seriadas, seguidas de
inoculação em meio sólido. No presente trabalho, após incubação de 24 horas, a 33ºC,
em câmara de anaerobiose, contava-se as colônias da placa que continham de 30 a 300
colônias e multiplicava-se o valor encontrado pelo fator de diluição (Soares et al.,
1987); encontrando, assim, o número mais provável de bactérias por mL.
2.6 - Isolamento das BRS
Para o isolamento das BRS, 200µL de uma diluição 1x107 da amostra de água em
estudo foram inoculados em um meio sólido contendo: 50% da solução de sulfato de
sódio (5,74g/L) e acetato de sódio (5,50g/L), 50% de meio fluido tioglicolato (v/v) e
1,5% de ágar (m/v). Neste meio, identificou-se dois tipos diferentes de colônias:
transparentes-irregulares (T.I.) e brancas-redondas (B.R.). A coloração de Gram foi
utilizada para identificação dos tipos morfológicos destas colônias.
34
2.7 - Ensaios de pH
O efeito do pH sobre o crescimento bacteriano foi estudado utilizando o meio mínimo e
o meio tioglicolato 7,5% (v/v) com o objetivo de avaliar o comportamento das BRS em
condições ácidas. Para isto, preparava-se 5L de cada um dos meios de cultivo, dos quais
retiravam-se alíquotas de 100mL. Estas alíquotas eram transferidas para erlenmyers de
250mL e tinham o pH ajustado com padrões de ácido sulfúrico, cujas concentrações
eram de 1:250 (v/v) e 1:50 (v/v). Após a alteração do pH, os meios eram autoclavados.
O meio tioglicolato 7,5% (v/v) apresentou um pH original igual a 6,9. A faixa de pH
trabalhada, para este meio, foi de 6,9 a 5,1, sendo os valores intermediários: (a) 6,6; (b)
6,3; (c) 6,1; (d) 5,9; (e) 5,7; (f) 5,5; e (g) 5,3. O meio mínimo foi naturalmente mais
alcalino, apresentando um pH igual a 8,1. Para este meio, os valores de pH estudados
foram: (a) 8,1; (b) 6,6; (c) 6,4; (d) 6,2; (e) 5,9; (f) 5,6; e (g) 5,3. Para cada um destes
pH’s, foram utilizados quatro frascos de 20mL, sendo que um era inoculado com 200µL
de cultura mista, um com 200µL de isolado T.I, o terceiro com 200µL de isolado B.R. e
o quarto era o controle negativo (não inoculado). As DO’s dos inóculos estavam em
torno de 0,08 de absorvância. Após 48 horas de incubação a 33ºC, as DO’s dos meios
utilizados nos ensaios de pH eram lidas em espectrofotômetro. Os meios inoculados que
apresentavam crescimento eram repetidos em triplicata. Os que não apresentavam
crescimento, após 48 horas, eram incubados por até um mês antes de serem
considerados inadequados para o crescimento das BRS.
2.8 - Dosagem de sulfato
O método utilizado para dosagem de sulfato foi o de precipitação com cloreto de bário,
seguido de leitura em turbidímetro (Clesceri et al., 1998). O consumo de sulfato das
amostras inoculadas com BRS foi determinado pela diferença entre a concentração de
sulfato dissolvido no branco (mesmo meio de cultura das amostras, porém não
inoculado) e as concentrações de sulfato dissolvido encontradas nas amostras. A
porcentagem de consumo de sulfato foi determinada a partir da média de consumo de
sulfato das amostras, que foram preparadas em triplicata, para cada pH, nos meios
35
mínimo e 7,5% de tioglicolato (v/v). O desvio padrão e o coeficiente de variação do
método turbidimétrico para amostras com uma concentração média de 7,45mg de SO42
/mL são, respectivamente, de 0,13mg/L e 1,7%. Duas amostras, com a mesma
concentração de sulfato (7,45mg de SO4-2/mL), apresentam, neste método, uma
recuperação de 85% e 91%.
2.9 - Análise quantitativa de H2S
A análise quantitativa de H2S foi feita utilizando o Método Iodométrico (Clesceri et al.,
1998). O objetivo desta dosagem foi estimar a quantidade de H2S do reator anaeróbio de
batelada durante a fase “estável” do processo, ou seja, após o término da fase log. A
presença deste gás era inquestionável devido ao cheiro característico do mesmo. A
quantificação foi feita em triplicata e com uma diferença de 15 dias de um teste para o
outro.
2.10 – Determinação de Eh e pH
As medidas de Eh e pH foram realizadas utilizando o aparelho HI 9622 microcomputer
pHmeter, Hanna instruments. Sendo o eletrodo de referência do tipo Ag/AgCl para as
medidas de Eh.
2.11 - Teste da catalase
Catalase é a enzima que catalisa a reação:
H2O2 → H2O + 1/2 O2
(15)
O teste da catalase consiste em colocar em uma lâmina de vidro uma gota de água
oxigenada 10 volumes em contato com um raspado de colônia. Para obter o raspado de
colônia basta utilizar uma alça de platina. Quando o resultado é positivo, ocorre
liberação de bolhas de oxigênio.
36
2.12 - Série bioquímica
Uma série de tubos contendo tipos diferentes de meios de cultura foi inoculada com
auxilio de uma alça de platina. Após incubação por 48 horas, a 33ºC, verificou-se as
alterações de cor, turbidez e/ou produção de gás nos tubos. Os meios utilizados foram o
citrato, a lactose, a glicose e a uréia. O citrato, a lactose e a glicose são fontes de
carbono e a uréia é fonte de nitrogênio. O consumo de citrato é considerado positivo
quando o meio passa de verde para azul. Lactose e Glicose positivas passam de
vermelho para amarelo. E no caso da glicose, ainda pode ser verificada a produção ou
não de gás. O meio contendo uréia, quando positivo, muda de amarelo para vermelho.
3 - Aplicação dos Estudos de Base:
3.1 - Preparação do meio mínimo com metal
Para evitar a precipitação dos metais dissolvidos em meio mínimo, foi necessário fazer
modificações tanto na composição do meio original, tanto na forma de preparo. O
K2HPO4 (fosfato de potássio dibásico) foi substituído pelo KH2PO4 (fosfato de potássio
monobásico). Soluções de acetato na concentração de 4g/L, em água destilada,
apresentam pH em torno de 8,0, o qual teve que ser corrigido para 6,0 com adição de
ácido sulfúrico concentrado. O objetivo desta acidificação foi evitar a precipitação
instantânea dos metais durante a mistura de sais. Verificou-se que, mesmo em pH 6,0, o
aquecimento do meio mínimo contendo os metais dissolvidos causava a precipitação
dos
mesmos.
Por
isso,
os
sais
metálicos
MnSO4.H2O,
CuSO4.5H2O,
(CH3COO)2Zn.2H2O e CdSO4.8/3H2O eram dissolvidos em volumes de água destilada
em torno de 1/20 do volume final do meio, de modo que para 1100mL de solução
utilizava-se 55mL de água destilada para dissolver cada sal. O metal dissolvido e o meio
mínimo eram autoclavados separadamente. A mistura do sal metálico com o meio
mínimo era realizada após o resfriamento. Como resultado, tinha-se quatro misturas
distintas, denominadas Mn, Cu, Zn e Cd de acordo com o sal metálico de origem. No
caso do Cu+2 e do Zn+2, a concentração conseguida para ambos os metais, em pH 6,0,
37
foi de 4,0mg/L. O Mn+2 e o Cd+2 apresentavam concentrações iniciais de 19,9 mg/L e
19,5 mg/L, respectivamente. As análises dos metais foram feitas em espectrofotômetro
de Absorção Atômica Perkin Elmer, modelo Aanalyst 100.
3.2 - Ensaios no reator anaeróbio de batelada
Nos ensaios realizados no reator, utilizou-se uma água de efluente de indústria
metalúrgica com 7,7g/L de sulfato, 37,5 mg/L de manganês, pH inicial 8,0 e rica em
matéria orgânica. A matéria orgânica era proveniente da presença de esterco de vaca,
feno, serragem e bagaço de cana utilizados no processo de tratamento passivo industrial.
Em laboratório, antes de serem feitas as análises de sulfato, manganês e pH, a amostra
de água industrial foi autoclavada e filtrada para retirar os sólidos suspensos e evitar
possíveis contaminações por microrganismos. A filtração foi realizada em etapas,
utilizando primeiro um papel de filtro quantitativo faixa azul (JP42 Quanty) e,
posteriormente, em membrana de celulose de 0,22µm. Antes de ser adicionada ao reator,
a água ainda teve o seu pH ajustado para 6,6. Para um volume de água igual a 4,75L,
que representa o volume útil do reator, foi utilizado 50mL de inóculo de BRS contendo
107 células/mL (NMP).
3.3 - Ensaios em frascos âmbar, sem adição de areia
Foram realizados dois tipos de ensaio: um utilizando, separadamente, os metais
manganês (20mg/L) e cádmio (20mg/L) em meio tioglicolato 2% (v/v) e pH igual a 5,5;
e outro usando os mesmos metais, também separadamente, em meio mínimo, sem o
meio tioglicolato e com pH 6,2. Em ambos os casos, os meios foram envasados em
frascos de vidro âmbar de 1L de modo que o líquido ocupasse 98% do volume
disponível de cada frasco. Todo o material utilizado era autoclavado. Os meios
contendo manganês e cádmio, com ou sem tioglicolato, eram inoculados com 2mL de
BRS, 107células/mL (NMP). O objetivo era verificar se, nestas condições, as BRS eram
capazes de crescer e de precipitar os metais. Quatro frascos estéreis de 100mL com
38
tampa foram utilizados para armazenar os meios sem inóculo, ou seja, os controles
negativos.
3.4 - Ensaio em frasco âmbar, com areia
O procedimento utilizado foi semelhante ao dos ensaios descritos no ítem 3.3. Porém,
foram adicionados 200g de areia no frasco de 1L e 20g no frasco de 100mL antes de
completá-los com meio mínimo contendo manganês (20mg/L).
3.5 - Ensaios em frascos âmbar de 100mL, com areia
Foram também realizados ensaios em frascos de vidro de 100mL, com tampa. Pois,
nestes frascos, os experimentos apresentavam os primeiros resultados com um tempo de
incubação de 5 dias, enquanto que nos frascos de 1000mL os mesmos eram obtidos após
um mês de incubação. Foram utilizados, ao todo, oito frascos: quatro frascos de 100mL
para ensaios com o manganês e quatro frascos para ensaios com o cádmio; sendo que,
dos quatro, um era usado como controle negativo e os outros três eram inoculados com
200µL de BRS. Os inóculos de BRS continham 4,2x107 células/mL (contagem direta
em câmara de Neubauer). Aproximadamente 20g de areia foram envasadas em cada
frasco de 100mL. O volume destes frascos foi preenchido com os meios até completar
98% do total. As concentrações de manganês e de cádmio eram de 20mg/L em meio
mínimo. Foram preparados 500mL de meio para cada metal e o pH inicial destes meios
foi ajustado, com ácido sulfúrico concentrado, para 6,2. As condições de trabalho não
eram estéreis.
3.6 - Diagramas EhxpH
Os diagramas foram construídos utilizando o programa HSC chemistry versão 4.1. Os
dados termodinâmicos foram calculados para os sulfatos e carbonatos a partir das
constantes de equilíbrio do programa NIST critically selected stability constants of
metals complexes versão 7.0. O valor das constantes de equilíbrio, escolhido para as
39
reações, era o que correspondia ao valor da força iônica mais próximo ao calculado para
o meio mínimo (I=0,17). Outros dados termodinâmicos foram provenientes do programa
HSC.
40
VI. RESULTADOS E DISCUSSÃO:
1. Primeira etapa dos ensaios no reator de batelada
Esta etapa objetivava confirmar a presença de BRS na amostra, através do
acompanhamento dos parâmetros de atividade das mesmas, assim como, testar a
eficiência do recipiente utilizado como reator. Dentre os parâmetros de atividade das
BRS foram avaliados o Eh, o pH, a concentração de sulfato e a produção de H2S (g).
Verificou-se que condições redutoras (Eh = -150mV a –290mV) e pH ácido favorecem a
liberação de H2S (g) para atmosfera. De acordo com o sistema S-H2O (Silva e Leão,
1999), o H2S é a forma predominante em pH<7 e Eh<0. O cheiro deste gás começa a ser
percebido em pH próximo a 6,5 e com a acidificação do meio a intensidade aumenta. O
teste qualitativo de H2S, usando “papel de chumbo”, confirmou a volatilização do H2S,
em pH ácido. A presença de ácido sulfídrico é indicativo de redução de sulfato pelas
BRS. Com relação ao sulfato, verificou-se que sua redução no reator, em pH 7,2, foi de
aproximadamente 20%, em 10 dias e houve alcalinização do meio, uma vez que, o pH
aumentou de 7,2 para 7,8.
O biorreator, numa primeira etapa de ensaios, funcionou como simulador de uma
condição hipotética onde a “água residuária”, ou seja, o meio sintético pobre em
nutrientes, continha elevados teores de sulfato (4g/L), Eh igual a -150mV, pH 7,5 e
temperatura de 33ºC. Esta simulação permitiu a constatação de que a amostra continha
BRS, além de fornecer dados preliminares sobre estas bactérias. A estrutura do reator
facilitou a coleta de amostras para dosagem de sulfato, que é o principal parâmetro
químico de avaliação destes microrganismos, ou seja, para serem classificadas como
BRS, é necessário que haja redução de sulfato no meio. Verificou-se que as amostras
retiradas da parte inferior do reator eram límpidas apesar da turbidez da camada
superior. A camada de areia, juntamente, com a malha de fibra de vidro funcionaram
como um filtro retendo os sólidos suspensos. Comparando-se a granulometria da areia
com o tamanho médio das BRS (1,5 µm), especulou-se que estes microrganismos eram
retidos por formarem filamentos (cadeias lineares). Este fato foi confirmado ao repicar,
41
em meio sólido, 200µL de uma amostra líquida (turva), retirada próxima a camada de
areia da parte superior do reator. As colônias cresceram em forma de filamentos (figura
4).
Figura 4 – Crescimento das BRS em meio sólido formando filamentos; coletadas do
biorreator anaeróbio de batelada.
2. Isolamento e caracterização das BRS
As BRS formam um grupo de procariontes muito diversificado, podendo ser dividido
em quatro subgrupos, de acordo com a sequência de 16S - rRNA: (1) BRS Gramnegativas mesófilas; (2) BRS Gram-positivas formadoras de esporos; (3) BRS
termófilas; e, (4) Arqueobactérias termófilas. Uma característica inerente ao grupo é a
capacidade de utilizar o sulfato como aceptor final de elétrons durante a respiração
anaeróbia (Castro et al., 2000). Para uma classificação tradicional, várias características
fisiológicas são avaliadas, entre elas: a morfologia celular, a motilidade, a oxidação
completa ou incompleta do acetato, etc (tabela 5). A classificação das BRS do presente
trabalho foi baseada na classificação de Castro et al. (2000).
42
Tabela 5 - Características importantes para classificação das bactérias redutoras de
sulfato (Castro et al., 2000).
Oxidação
Formato
Temperatura de
de Acetato crescimento (ºC)
Motilidade
BRS Gram-negativa mesófila
Desulfobulbus
Limão-bastão
incompleta
25-40
-/+
Desulfomicrobium
Oval-bastão
incompleta
25-40
+/-
Desulfomonas
Bastão
incompleta
30-40
-
Desulfovibrio
Espiral-vírgula
incompleta
25-40
+
Desulfobacter
Oval-bastão
completa
20-33
+/-
Desulfobacterium
Oval-bastão
completa
20-35
+/-
Desulfococcus
Esférico-limão
completa
28-35
-/+
Desulfomonile
Bastão
completa
37
-
Desulfonema
Filamento
completa
28-32
Planar
33
+/-
Bastão ovalados
Desulfosarcina
ou
cocos, completa
agrupados
BRS Gram-positiva formadora de esporo
Desulfotomaculum
Bastão
reto
curvado
a incompleta/
Maioria 25-40,
completa
algumas 40-65
+
BRS termófila
Thermodesulfobacterium
Vírgula-bastão
incompleta
65-70
-/+
64-92
+/-
Arqueobactéria redutora de sulfato
Archaeoglobus
Coco
incompleta
Segundo Castro et al. (2000), as BRS Gram-negativas podem ser subdivididas em duas
famílias: Desulfovibrionaceae e Desulfobacteriaceae. A primeira família inclui os
gêneros Desulfovibrio e Desulfomicrobium. A família Desulfobacteriaceae inclui os
gêneros
Desulfobulbus,
Desulfobacter,
43
Desulfobacterium,
Desulfococcus,
Desulfosarcina, Desulfomonile, Desulfonema, Desulfobotulus e Desulfoarculus. O
principal gênero que compõe as BRS Gram-positivas formadoras de esporos é o
Desulfotomaculum, sendo que algumas espécies deste gênero são termófilas. As
bactérias deste gênero apresentam formato de bastão, porém os esporos têm a forma de
cocos. A presença de subgrupos de BRS Gram positivas e Gram negativas foi relatada
por Okabe et al. (2003), por Castro et al. (2000), por Widdel (1988), entre outros. A
tolerância ao oxigênio, em maior ou em menor grau, é relatada em todos os subgrupos
das BRS, que são classificadas como anaeróbias (Fareleira et al., 2003; Dilling e
Cypionka, 1990; Cypionka et al., 1985).
O isolamento das BRS foi feito em meio sólido e apresentou dois tipos de colônias, uma
transparente e irregular (isolado T.I) e outra branca e redonda (isolado B.R). A
realização da Coloração de Gram demonstrou a presença de cocos Gram positivos
(B.R.).(figura 5) e de bastonetes Gram negativos (T.I.) (figura 6).
Figura 5 – Isolados B.R., forma de cocos e coloração de Gram positiva.
44
Figura 6 - Isolados T.I., forma de bastonetes e coloração de Gram negativa.
Após o isolamento, foi feita a caracterização, usando meios líquidos contendo sulfato e
testes bioquímicos. Tanto os bastonetes quanto os cocos foram submetidos a testes da
série bioquímica de utilização do citrato, da lactose e da glicose como fontes de
carbono, e da uréia como fonte de nitrogênio; teste de motilidade em meio SIM e, ainda,
ao teste da catalase. Os bastonetes Gram negativos (isolados T.I.) e os cocos Gram
positivos (isolados B.R.) foram capazes de utilizar as três fontes de carbono e não se
mostraram capazes de utilizar a uréia como fonte de nitrogênio. Ambas as amostras
responderam negativamente ao teste de motilidade e positivamente quanto à presença de
catalase. É interessante notar que o fato dos isolados possuírem a enzima ativa catalase
lhes confere tolerância ao oxigênio, possibilitanto, assim o seu cultivo em sistemas com
baixa pressão de O2 dispensando a necessidade da construção de reatores estritamente
anaeróbia. Os ensaios em meio líquido contendo sulfato confirmaram que as bactérias
isoladas utilizaram o sulfato como aceptor final de elétrons e produzindo ácido
sulfídrico como produto final. A emissão de H2S foi facilmente percebida em vista do
odor característico deste gás.
45
Ensaios realizados com os isolados B.R. e T.I. confirmaram a presença da catalase em
ambos os casos, justificando a tolerância ao oxigênio. O uso de citrato, lactose e glicose
pelas BRS, Gram positivas e Gram negativas, confirma a capacidade de utilização de
vários tipos de doadores de elétrons (tabela 6). As bactérias Gram-positivas da amostra
cresceram em meio mínimo, o que indica que estas BRS foram capazes de utilizar o
acetato como única fonte de carbono, ou seja, realizaram oxidação completa do acetato
a CO2. Entretanto, as BRS Gram-negativas não cresceram neste meio. A identificação
destes microrganismos requer uma etapa de seqüenciamento genético que será objetivo
de trabalhos futuros.
Tabela 6 – Resultados da caracterização morfológica e bioquímica dos isolados T.I.
(Gram-negativas) e B.R. (Gram-positivas) da amostra.
Formato
Bastão
(T.I.)
Cocos
(B.R.)
Oxidação de
acetato
Temperatura de
crescimento (ºC)
Motilidade
Citrato
em meio SIM
incompleta
33
negativa
+
+
+
-
+
+
completa
33
negativa
+
+
+
-
+
+
Lactose Glicose Uréia Catalase Sulfato
Dando seqüência à etapa de caracterização dos isolados T.I. e B.R., foi estudado o efeito
do pH no crescimento destes microrganismos, utilizando, para isto, o meio tioglicolato
7,5% (v/v). Com estes ensaios foi possível demonstrar que a eficiência da redução de
sulfato está intimamente ligada ao pH. Os meios moderadamente ácidos apresentaram
maior consumo de sulfato do que os meios com pH próximo à neutralidade; apesar do
crescimento das bactérias ter diminuído (tabelas 7, 8 e 9). É importante observar nas
figuras 7, 8 e 9: (1) a relação entre as DO’s médias de 48 horas, da cultura mista e dos
isolados T.I e B.R; e (2) as porcentagens médias de consumo de sulfato nos respectivos
pH’s.
46
Tabela 7 – Crescimento das BRS e consumo médio de sulfato em diferentes pH’s.
pH
DO 48h da cultura mista
Consumo médio de
sulfato em g/L
6,9
0,96
0,00
6,1
0,60
0,27
5,9
0,33
0,40
5,7
0,11
0,04
5,3
0,00
0,00
Condições: Inóculo de cultura mista em meio tioglicolato 7.5% (v/v).
Tabela 8 – Crescimento do isolado T.I. e consumo médio de sulfato em diferentes pH’s.
pH
DO 48h do isolado T.I.
Consumo médio de
sulfato em g/L
6,9
0,92
0,00
6,1
0,50
0,27
5,9
0,34
0,53
5,7
0,12
0,05
5,3
0,00
0,00
Condições: Inóculo do isolado T.I. em meio tioglicolato 7.5% (v/v).
Tabela 9 – Crescimento dos isolados B.R. e consumo médio de sulfato em diferentes
pH’s.
pH
DO 48h do isolado B.R.
Consumo médio de
sulfato em g/L
6,9
0,70
0,13
6,1
0,55
0,27
5,9
0,24
0,53
5,7
0,16
0,09
5,3
0,00
0,00
Condições: Inóculo do isolado B.R. em meio tioglicolato 7.5% (v/v).
47
0.5
1.0
DO (Cultura mista)
0.4
0.8
DO48h
0.2
SO4-2 g/L
0.3
0.6
0.4
0.1
0.2
Consumo médio de sulfato
0.0
0.0
5.0
5.5
6.0
6.5
-0.1
7.0
pH
Figura 7 - Crescimento da cultura mista (DO de 48 horas) e consumo médio de sulfato
em função do pH, em meio tioglicolato 7,5% (v/v).
1.0
0.6
0.5
0.8
0.4
0.6
DO48h
0.3
0.4
0.2
0.2
SO4-2 g/L
DO (Isolado T.I.)
0.1
Consumo médio de sulfato
0.0
5.0
5.5
6.0
6.5
0.0
7.0
pH
Figura 8 - Crescimento dos isolados T.I (DO de 48 horas) e consumo médio de sulfato
em função do pH, em meio tioglicolato 7,5% (v/v).
48
0.8
0.8
0.6
0.6
0.4
0.4
0.2
SO4-2 g/L
DO48h
DO (Isolado BR)
0.2
Consumo médio de sulfato
0.0
0.0
5.0
5.5
6.0
6.5
7.0
pH
Figura 9 - Crescimento dos isolados B.R. (DO de 48 horas) e consumo médio de sulfato
em função do pH, em meio tioglicolato 7,5% (v/v).
É possível notar nas figuras 7, 8, e 9 que o crescimento das BRS foi maior em pH 6,9.
Porém, o ponto máximo do crescimento destas bactérias não coincide com o ponto de
maior consumo de sulfato. No meio tioglicolato 7,5% (v/v), o pH ótimo para redução de
sulfato foi 5,9. Isto porque, o meio rico em matéria orgânica favorece o uso de outras
vias de liberação de energia, dificultando a redução do sulfato (Lens et al., 1998;
Christensen et al., 1996; Von Sperling, 1996). Porém, em condições limite (stress) as
BRS são “forçadas” a utilizar este aceptor de elétrons. Neste caso, o pH foi o fator
limitante do crescimento bacteriano e o fator “estimulante” (condição limite) do
consumo de sulfato. Os ensaios de pH foram realizados em meio fluido de tioglicolato e
em meio mínimo. Sendo que o meio tioglicolato é um meio rico em matéria orgânica e
pode ser usado para crescimento de bactérias anaeróbias. A proporção deste meio fluido,
em solução de sulfato-acetato (1:1), variou com o objetivo de aumentar ou diminuir o
tempo de crescimento e a concentração celular. Ou seja, para uma proporção de
tioglicolato igual a 7,5% (v/v), mantendo o pH original da mistura (6,9), a DO de 24
horas foi em média 0,200 enquanto para proporção de 2,0% (v/v) a média da DO de 24
49
horas foi 0,080. Isto facilitou a observação das variações no crescimento por alteração
do pH. Esta observação permite salientar a influência da acidez sobre o número de
bactérias e sobre o consumo de sulfato. Garcia et al. (2001) estudando um sistema
contínuo real, citaram que as análises da concentração de sulfato, em pH 7,
demonstraram um consumo de 85% (redução do teor de sulfato de 9000mg/L para
1350mg/L) de sulfato em 27 dias, enquanto que, em pH 5, o mesmo consumo ocorreu
em 9 dias. Paralelamente à redução de sulfato, observou-se a alcalinização do pH para
um valor igual a 8,2 e a diminuição do Eh para –250mV (Garcia et al., 2001).
O tempo de residência de 48 horas é aplicável em sistemas reais e é um fator importante
na redução de sulfato, pois o processo anaeróbico, por gerar menos energia, é sempre
mais lento que o processo aeróbico. O pH é um dos fatores limitantes mais importantes
no que se refere ao crescimento das BRS (Elliott et al., 1998; Küsel et al., 2001; White
et al., 1997). O crescimento das BRS foi acompanhado dentro de uma faixa de pH que
variou de 6,9 a 5,1 em meio tioglicolato 7,5% (v/v), utilizando-se inóculos de cultura
mista e de isolados T.I. e B.R. O pH 5,3 foi o limite de acidez que as BRS Gram
negativas suportaram, nas condições experimentais do presente trabalho. As redutoras
de sulfato mais resistentes são as Gram positivas, crescendo em meio tioglicolato 7,5%
(v/v) com pH igual a 5,3 (após um mês de incubação) e em meio mínimo com pH igual
a 6,2.
3. Meio mínimo e caracterização das BRS
Todo ser vivo necessita de alguns elementos que são essenciais para o metabolismo
celular. Entre estes elementos estão o carbono, o oxigênio, o nitrogênio, o hidrogênio, o
fósforo e o enxofre. No caso dos microrganismos cultivados “in vitro”, estes elementos
devem ser fornecidos pelo meio de cultivo. Desta forma, para elaborar um meio de
cultivo faz-se necessário que se considere o metabolismo celular. Além disto, deve-se
considerar as condições naturais em que o microrganismo desenvolve-se. Isto porque os
elementos essenciais podem ser encontrados como constituintes de várias substâncias
diferentes de acordo com o ambiente onde estão. No caso das BRS, por exemplo, elas
50
podem ser encontradas na camada permanente (profunda) do leito dos rios. Este
ambiente apresenta características redutoras, contém pouca matéria orgânica - que,
normalmente, encontra-se em processo final de decomposição – e apresenta os
elementos nitrogênio, fósforo e enxofre na forma de sais inorgânicos – nitratos,
ortofosfatos e sulfatos. Com base nestes conhecimentos, entre outros, foi elaborado um
meio de cultivo para o crescimento das BRS “in vitro”. Este meio foi denominado
“meio mínimo” por conter, basicamente, os elementos essenciais para o metabolismo
biológico, ou seja, fosfato (HPO4-2), nitrato, acetato e sulfato, em solução aquosa. Os
ortofosfatos (PO4-3, HPO4-2, H2PO4-, H3PO4), são fontes de fósforo prontamente
disponíveis para o metabolismo biológico, sendo o HPO4-2 mais comum no meio
ambiente em pH próximo à neutralidade (Von Sperling, 1996). O acetato é uma fonte de
carbono, encontrado em condições anaeróbias, ou seja, em processo final de
decomposição da matéria orgânica e o nitrato é uma fonte de nitrogênio, presente em
condições anóxicas (Eh variando de +50 a -50mV). Já o sulfato atua como aceptor final
de elétrons na respiração anaeróbia das BRS (Lens et al., 1998).
O grupo das BRS, como um todo, é capaz de utilizar um grande número de substâncias
doadoras de elétrons, entre elas: acetato, anilina, succinato, catecol, etanol, fenol,
acetona, propionato, lactato, etc. Porém, para compor o meio mínimo, optou-se pela
escolha de apenas um doador de elétrons, o acetato. Isto porque, as BRS ficam
subdivididas em dois subgrupos de acordo com o consumo ou não desta substância: as
que realizam oxidação completa a CO2 e as que realizam oxidação incompleta a acetato.
Esta diferenciação em subgrupos facilitou a caracterização das BRS isoladas da amostra.
Ou seja, o meio mínimo tornou-se seletivo para bactérias capazes de utilizar o acetato
como única fonte de carbono.
O uso de sulfato como aceptor final de elétrons é inerente às bactérias redutoras de
sulfato durante o processo de respiração anaeróbia. Porém, o meio de cultivo e as
condições ambientais precisam ser favoráveis à redução do sulfato. Assim sendo, outro
ponto avaliado foi a relação entre a concentração de sulfato e a concentração de nitrato.
O uso do sulfato em uma concentração de aproximadamente 4g/L baseou-se na
51
definição de água ácida. Considera-se uma água ácida quando a concentração de sulfato
é maior que 3000mg/L, entre outras características (Sengupta, 1993; Abrahão e Mello,
2003). Além disto, quanto mais elevada for a concentração deste ânion, maior a chance
de ocorrer a redução do mesmo, pois, quando vários aceptores de elétrons estão
disponíveis no mesmo ambiente, o sistema utiliza aquele que produz mais energia
(oxigênio, nitrato, etc). E enquanto houver substâncias de maior liberação de energia, as
que liberam menos energia não serão utilizadas (Von Sperling, 1996).
O sulfato é um dos aceptores de elétrons que menos libera energia e as BRS são capazes
de utilizar o nitrato (Christensen et al., 1996; Lens et al., 1998; Tuppurainen et al.,
2002; Okabe et al., 2003). Assim sendo, a composição do meio mínimo apresenta uma
concentração de sulfato quase 6 vezes maior que a de nitrato. Christensen et al. (1996),
estudando a remediação de águas ácidas em presença de BRS, observaram que a
concentração de fosfato dos reatores anaeróbios em batelada, contendo soro de leite,
permaneceu relativamente elevada no final dos ensaios, enquanto o nitrato apresentou
concentrações inferiores a 0,1mg/L, durante todo o período de incubação. Este
experimento exemplifica a capacidade de redução de nitrato pelas BRS e demonstra que
o fosfato não interfere na redução de sulfato.
O meio mínimo simula as condições encontradas em sedimentos permanentes,
anaeróbios, de corpos d’águas (Fortin et al., 2000; Sass et al., 2002). E foi utilizado por
proporcionar condições seletivas às BRS, pois, em ambiente não estéril, ácido e com
temperatura ambiente, o meio tioglicolato favorece o crescimento de leveduras. O meio
mínimo foi testado em pH de 8,1 a 5,3 – sendo que o primeiro representa o pH normal
da solução e o último foi o pH mais ácido em que verificou-se o crescimento das BRS,
em questão. A tabela 10 e a figura 10 apresentam o crescimento bacteriano e o consumo
de sulfato em função do pH, em meio mínimo. Neste meio, apenas as BRS Gram
positivas apresentaram crescimento. Em função disto, no restante desta dissertação
sempre que o meio em questão for o meio mínimo estará sendo feita referência aos
isolados B.R.
52
Tabela 10 – Crescimento dos isolados B.R. (BRS Gram positivas) e consumo médio de
sulfato em diferentes pH’s.
Consumo médio de
pH
DO 48h do isolado B.R.
6,6
0,10
0,10
6,4
0,05
0,36
6,2
0,01
0,10
5,9
0,00
0,00
sulfato em g/L
Condições: Meio Mínimo contendo solução de sulfato de sódio 5,74g/L, acetato de
sódio 5,50g/L, nitrato de sódio 1g/L e fosfato de potássio dibásico 1g/L.
0.4
0.10
0.3
Consumo médio de sulfato
0.06
0.2
0.04
SO4-2 g/L
DO48h
0.08
0.1
DO (Isolado B.R.)
0.02
0.0
0.00
5.8
6.0
6.2
6.4
6.6
pH
Figura 10 – Crescimento dos isolados B.R. em meio mínimo contendo solução de
sulfato de sódio 5,74g/L, acetato de sódio 5,50g/L, nitrato de sódio 1g/L e fosfato de
potássio dibásico 1g/L.
Comparando as figuras 9 e 10, nota-se semelhanças de comportamento dos isolados
B.R. em meio mínimo e em meio tioglicolato 7,5% (v/v). Pois, em ambos os casos, o
pH ótimo de consumo de sulfato não coincide com o máximo de crescimento. Porém,
em meio mínimo, o maior valor de DO48h, que indica o ponto máximo de crescimento
53
destas bactérias, foi sete vez menor que no meio tioglicolato 7,5% (v/v). E o pH ótimo
para redução de sulfato foi 6,4. No caso do meio mínimo, que é composto, basicamente,
de sais inorgânicos e acetato, o fato do pH ótimo de consumo de sulfato não coincidir
com o máximo de crescimento das BRS, pode estar relacionado a presença de nitrato
(aceptor de elétrons). Pois, segundo Von Sperling (1996), o nitrato é reduzido
preferencialmente ao sulfato durante o processo de digestão anaeróbia. Porém, em
condições “desfavoráveis”, ou seja, diante do stress causado pelo aumento da acidez de
6,6 para 6,4 estas bactérias realizam a função inerente ao grupo que é a redução do
sulfato.
Foi feita uma curva de crescimento do isolado B.R. em meio mínimo com pH inicial 8,1
para avaliar o comportamento destes microrganismos neste meio sintético composto de
sulfato de sódio 5,74g/L, acetato de sódio 5,50g/L, nitrato de sódio 1g/L e fosfato de
potássio dibásico 1g/L (ver figura 11).
0.25
0.20
DO
0.15
0.10
0.05
0.00
0
50
100
150
200
250
300
350
Tempo (h)
Figura 11 - Curva de crescimento do isolado B.R. (BRS Gram positiva) em meio
mínimo (pH = 8,1).
54
Verificou-se que para o meio mínimo, sem alteração de pH, a fase lag durou 48 horas e
que o decaimento bacteriano ocorreu após 200 horas. Estes dados serviram como
referência para os ensaios em presença de metais.
4. Reator anaeróbio de batelada
O reator anaeróbio de batelada, descrito na figura 1 (ítem V, 2.1), baseou-se naqueles
utilizados por Christensen et al. (1996). Estes últimos eram cilindros de acrílico
transparente contendo três camadas cada um: duas de substrato sólido, composto de
brita e de areia e uma camada superior de água de mina. Após a adição dos substrados e
dos inóculos característicos de cada reator, os recipientes eram selados e incubados a
15ºC, no escuro, durante 203 dias.
Os fatores considerados limitantes para o crescimento das BRS são o pH, o Eh e as
concentrações de sulfato, de H2S, de metais e de matéria orgânica (Garcia et al., 2001).
Dentre estes fatores, o pH, o Eh, a precipitação de metais e as concentrações de sulfato e
de gás sulfídrico são, também, parâmetros de avaliação da atividade das BRS
(Christensen et al., 1996). No presente trabalho, o reator de 4,75L continha água de
efluente industrial que apresentava as seguintes características: presença de matéria
orgânica, com concentração de sulfato de 7,7g/L, pH 6,6 e concentração de manganês
37,5 mg/L. Estes três últimos parâmetros foram acompanhados para avaliar a eficiência
das BRS no processo de tratamento de água no reator anaeróbio de batelada. O primeiro
indício de crescimento das BRS no reator foi o cheiro característico do gás sulfídrico.
Este cheiro de H2S(g) era facilmente percebido durante a coleta de amostras da parte
inferior do reator, o que não acontecia na parte superior do mesmo.
Os processos anaeróbios ocorreram, inicialmente, na camada de areia e na parte inferior
do reator, devido à menor concentração de oxigênio nestes locais e, também, pela
presença de suporte sólido para formação do biofilme. A presença de substrato sólido no
fundo dos cilindros é de vital importância para o tratamento das águas ácidas pelas BRS,
em escala laboratorial. Pois, é na água intersticial da areia que ocorrem as primeiras
55
alterações químicas, como o aumento do pH e a precipitação de metal. Estes resultados
estão em acordo com os relatos de Christensen et al. (1996).
Os experimentos de Christensen et al. (1996) servem como base para justificar os
resultados obtidos nas amostras do reator anaeróbio de batelada. Observando a figura
12, é possível verificar que a precipitação do manganês ocorreu mais rapidamente na
parte inferior do que na superior do reator. Isto porque, a atividade bacteriana teve início
no fundo de areia do cilindro. Com o passar do tempo, o número de BRS aumenta (108
células/mL) e, consequentemente, a produção de H2S também.
40
40
Mn mg/L
30
30
Branco
PSR
20
20
PIR
10
10
0
0
0
200
400
600
800
1000
1200
Tempo (h)
Figura 12 – Concentração do manganês dissolvido na parte superior do reator (PSR) e
na parte inferior (PIR) do mesmo. Água de um efluente industrial contendo 37,5mg/L de
manganês. Condições: Branco em aerobiose e temperatura ambiente. Reator, parte
inferior e superior, em anaerobiose e temperatura de 330C.
Concentração de H2S igual ou superior a 40mg/L pode inibir a atividade das BRS.
Porém, a concentração de sulfeto considerada tóxica para estas bactérias depende das
espécies presentes, do grau de adaptação das bactérias e da composição orgânica e
56
inorgânica do meio (Burgess e Stuetz, 2002). A concentração de sulfeto solúvel presente
na água intersticial da camada de esferas de vidro chegou a 90mg/L, na fase “estável” entendendo fase estável como a fase após crescimento bacteriano (log). Este gás percola
em direção às camadas superiores, propiciando uma precipitação de manganês posterior
à observada na base.
A concentração de manganês na camada líquida superior do reator anaeróbio diminuiu
de 37,5mg/L para 1,2mg/L, em 49 dias. Enquanto na camada contendo esferas de vidro,
no mesmo período, a concentração deste metal diminui de 37,5mg/L para 7,5mg/L. A
explicação para a diferença encontrada entre as concentrações finais de manganês na
parte inferior do reator (7,5mg/L) quando comparada à parte superior (1,2mg/L) baseiase na reação:
MnS + 2H+ → Mn2+ + H2S
logK=10,
I=0,0
(16)
É possível calcular, para esta reação (16), a solubilidade do manganês em função do pH
(T=25ºC; [H2S]=90mg/L) como sendo:
Log [Mn2+] = 12,57 – 2pH
(17)
Para pH 7,5 (base do reator) a solubilidade teórica do sulfato de manganês é de
200mg/L. Este valor cai para 8mg/L em pH 8,2 (topo do reator). Embora os valores
medidos da concentração de Mn2+ no reator sejam menores, é possível observar a
mesma tendência. Ou seja, a solubilidade do manganês na base do reator (menor pH) é
maior que no topo. É importante citar ainda que, além dos efeitos da força iônica, a
produção de íons bicarbonato pelo metabolismo bacteriano também pode influenciar a
precipitação deste metal. Pois, o carbonato de manganês é um produto sólido passível de
ser formado neste sistema (pKps = 9,3). Um indício que sugere a participação do
bicarbonato na precipitação é o pH mais elevado no topo do reator. Um pH mais
elevado indica uma maior alcalinização da solução pela produção de HCO3-. Além
disso, a solubilidade do CO2 é relativamente baixa, o que facilita seu acúmulo na parte
57
superior do reator, contribuindo para o aumento do pH e para a possível precipitação do
manganês na forma de carbonato.
Em ambientes redutores, como as águas de subsolo, o manganês encontra-se na forma
de Mn+2 e sua concentração raramente ultrapassa 2mg/L. Em tratamentos químicos de
águas residuárias, a adição de carbonato de sódio precipita o Mn+2 como MnCO3, em
pH 8,5 (Manahan, 2000). A precipitação do manganês pela produção biológica de
sulfeto e alcalinização, em reator anaeróbio de batelada, foi confirmada por Christensen
et al. (1996). Na figura 13, é possível observar que a concentração de Mn+2 diminui à
medida que o pH aumentou. Isto porque, a alteração do valor de pH no meio está
relacionada, entre outras coisas, à produção de H2S(aq) e de HCO3-. Ainda na figura 13,
observa-se a concentração do manganês dissolvido em três condições diferentes: (1) no
controle negativo (meio sem inóculo); (2) na camada líquida superior do reator (PSR); e
(3) na parte inferior contendo esferas de vidro (PIR).
40
40
Mn mg/L
Branco
30
30
20
20
PSR
PIR
10
10
0
0
6.0
6.5
7.0
7.5
8.0
8.5
9.0
pH
Figura 13 – Concentração do manganês versus pH. Branco = controle negativo; PIR =
parte inferior do reator; PSR = parte superior do reator. Condições: O pH original da
água do efluente industrial era 8,0 e foi ajustado para 6,6.
58
É possível especular que a formação de hidróxido metálico não foi o fator responsável
pela precipitação do manganês, neste caso. Observando os círculos da figura 13,
verifica-se que para um pH igual a 7,7 existem quatro concentrações diferentes de
manganês: 8mg/L, 23mg/L, 33mg/L e 37,5mg/L, indicando que a precipitação deste
metal foi resultado da formação de um outro tipo de precipitado, nestas condições.
Considerando-se que as BRS liberam H2S e CO2 em sua respiração anaeróbia, supõe-se
que os precipitados formados sejam o sulfeto e/ou o carbonato de manganês. Segundo
os resultados obtidos, o pH não é o fator determinante na precipitação deste metal e sim
a formação dos dois agentes precipitantes (H2S e CO2).
As concentrações de HCO3-, H2S e dos ácidos orgânicos voláteis interferem no pH do
meio de cultivo. A decomposição da matéria orgânica presente na água do efluente
industrial gera ácidos orgânicos voláteis que acidificam o meio (Tuppurainen et al.,
2002). Por outro lado, as BRS produzem CO2(g) e H2S(g). Em ambientes aquáticos
naturais, o dióxido de carbono transforma-se em bicarbonato que, por sua vez, reage
com outras substâncias do meio tamponando as águas. O bicarbonato (HCO3-) é a
espécie predominante em pH 8,3. Assim sendo, o bicarbonato favorece a estabilização
do pH em valores próximos a 8,2, como observado no presente trabalho (Sawyer et al.,
1994; Manahan, 2000). O ácido sulfídrico, por sua vez, apresenta uma solubilidade de
4,0g/L à 20ºC e 2,5g/L à 40ºC, permanecendo protonado em pH ácido e desprotonado
em pH maior que 7,0 (Martel e Smith, 2003; Sawyer et al., 1994):
CO2(g)+ H2O ↔ H+ + HCO3-
(18)
H2CO3 ↔ H+ + HCO3-
pKa1 = 6,35 (19)
HCO3- ↔ H+ + CO3-2
pKa2 = 10,33 (20)
H2S ↔ H+ + HS-
pKa1 = 7,02 (21)
HS- ↔ H+ + S-2
pKa2 = 12,89 (22)
59
Outro parâmetro avaliado, no reator anaeróbio de batelada, foi o consumo de sulfato
pelas BRS (figura 14). O sulfato em concentrações elevadas (7,7g/L) funcionou de
maneira seletiva o que favoreceu o crescimento destes microrganismos. Os resultados
obtidos de amostras colhidas no reator demonstraram que o consumo máximo de
sulfato, em batelada, ficou em torno de 890mg/L (12% de remoção), após 85 dias.
Christensen et al. (1996), em seus reatores anaeróbios de batelada, obtiveram, após 203
dias, um consumo de sulfato na ordem de 614 a 893mg/L, o que equivalia a 19-27%, da
concentração total inicial de sulfato (3306mg/L).
8.0
8.0
7.5
SO4-2 mg/L
7.5
Branco
PSR
7.0
7.0
PIR
6.5
6.5
0
500
1000
1500
2000
Tempo (h)
Figura 14 – Concentração do sulfato dissolvido. Água do efluente industrial contendo
7,7g/L de sulfato em pH 8,0. Condições: Branco em aerobiose e temperatura ambiente.
Reator, parte inferior e superior, em anaerobiose e temperatura de 330C.
5. Meios contendo manganês e cádmio em frascos de 100 mL
Ensaios, referentes a precipitação de metais pelo sulfeto gerado biologicamente, foram
realizados com o manganês e com o cádmio em frascos de vidro vedados contendo meio
60
mínimo e leito de areia. Porém, antes dos ensaios com manganês e com cádmio foram
feitos ensaios preliminares, em ambiente estéril, que geraram dados importantes para
montagem dos ensaios propriamente ditos. Os ensaios preliminares podem ser
subdivididos em duas etapas: a primeira, sem leito de areia e a segunda, com leito de
areia. O objetivo era verificar em qual(is) condição(ões) as BRS eram capazes de crescer
e de precipitar os metais; sendo que o cobre foi o metal mais tóxico para as BRS, dentre
os metais estudados. Utilizou-se uma concentração de 20mg/L de cobre por ser
considerada não inibitória para as BRS, segundo a literatura (Fortin et al., 2000).
Verificou-se, porém, que em frascos contendo meio 2% (v/v) de tioglicolato as bactérias
não cresceram na presença de cobre e as que cresceram em presença de manganês e
zinco não precipitaram estes metais. No meio mínimo, com pH 6,2, o resultado foi
semelhante, ou seja, o crescimento bacteriano foi observado em presença de manganês e
de zinco, mas também não houve precipitação.
Durante a adição de acetato de zinco e de sulfato de cobre em meio mínimo, com pH
6,2, ocorreu a precipitação dos metais devido à formação de hidróxidos dos mesmos. A
solubilidade destes metais, no meio mínimo, varia conforme o pH. Para conseguir uma
concentração de cobre e zinco igual a 20mg/L era necessário que se abaixasse o pH para
cinco, segundo os diagramas de solubilidade (Silva e Leão, 1999). Este valor de pH é
incompatível com o crescimento das BRS em estudo. A alternativa foi substituir o cobre
pelo cádmio, que permanece na forma de Cd+2 em pH 6,2; e, diminuir a concentração de
zinco para 1,5mg/L. A turbidez, causada pelo crescimento das BRS em presença dos
metais cobre, manganês, zinco, foi avaliada através da leitura em espectrofotômetro
utilizando uma densidade óptica de 600nm (DO600nm), conforme mostrado nas tabelas
11 e 12.
61
Tabela 11 – Turbidez causada pelo crescimento das BRS em presença dos metais cobre,
manganês e zinco.
DO600nm medida em presença de diferentes metais
Horas
Cu
Mn
Zn
0
0,000
0,000
0,000
72
0,010
0,076
0,050
216
0,013
0,154
0,013
288
0,012
0,173
0,012
552
0,012
0,167
0,012
Condições: Meio Mínimo adicionado de meio 2% (v/v) de tioglicolato, com pH 5,5 e
temperatura de 33ºC. Ambiente Estéril.
Tabela 12 – Densidade óptica 600nm (DO600nm) das BRS em presença dos metais
cádmio, manganês e zinco.
DO600nm medida em presença de diferentes metais
Horas
Cd
Mn
Zn
0
0,000
0,000
0,000
144
0,002
0,014
0,011
192
0,000
0,077
0,011
Condições: Meio Mínimo, com pH 6,2 e temperatura de 33ºC. Ambiente estéril.
Observando os resultados das densidades ópticas de 600nm, referentes à turbidez do
meio, foi possível verificar a influência dos metais manganês, zinco, cobre e cádmio
sobre o crescimento das BRS. O cádmio e o cobre inibiram o crescimento das BRS. A
toxicidade destes metais, em ordem decrescente, neste caso, pode ser escrita da seguinte
forma: Cd>Cu>Zn>Mn. E, a taxa de crescimento das BRS, em presença dos mesmos,
foi: (1) Mn>Zn>Cu, em meio contendo 2% (v/v) de tioglicolato e pH 5,5; e, (2)
Mn>Zn>Cd, em meio mínimo e pH 6,2.
O manganês foi o metal escolhido para ser utilizado em uma segunda etapa de ensaios,
por apresentar, durante a primeira etapa, os maiores valores de DO tanto em meio
mínimo quanto em meio contendo 2% (v/v) de tioglicolato. Os resultados obtidos nos
ensaios com manganês e leito de areia, após 192 horas de incubação, a 33ºC, foram:
62
DO600nm igual a 0,260 de absorvância; alcalinização do meio (de 6,2 para 7,9); e,
precipitação do metal (de 20mg/L para 1,59mg/L). Comparativamente, a turbidez em
presença de areia foi 3,4 vezes maior do que na ausência desta estrutura de fixação, ou
seja, a DO de 600nm que foi igual a 0,077 em meio mínimo, sem a areia, passou a ser
igual a 0,260, com a areia. A alcalinização do meio e a precipitação de metais indicam
que as condições foram propícias para o metabolismo das BRS (Garcia et al., 2001;
Lens et al., 1998). Estes resultados confirmaram a importância da areia, enquanto
estrutura de fixação, na atividade destes microrganismos. Observando a tabela 13, é
possível verificar o aumento da turbidez e a diminuição da concentração de manganês,
em presença de leito de areia.
Tabela 13 – DO600nm X concentração de manganês, em função do tempo.
Horas
DO600nm
Concentração de Mn em mg/L
0
0,000
20
144
0,021
19
192
0,260
1,6
Condições: Meio Mínimo, com pH 6,2 e temperatura de 33ºC, em presença de leito de
areia. Ambiente estéril.
Em outra etapa foi estudada a precipitação de manganês e de cádmio. Os parâmetros
avaliados foram: (1) o crescimento bacteriano; (2) a concentração destes metais; (3) a
variação do pH e do Eh do meio; e (4) o consumo de sulfato. Comparando as figuras 15
e 16, nota-se que o crescimento das BRS, em presença de manganês, ocorre
abruptamente enquanto que, em presença de cádmio, este processo é gradual. Nota-se,
também, que o número de bactérias por volume de solução é dez vezes maior no meio
contendo manganês. Estas diferenças ocorreram devido a maior toxicidez do cádmio em
comparação ao manganês (Esteves, 1998; Manahan, 2000).
63
200
0.5
População
(Contagem direta)
0.4
DO
0.3
100
0.2
DO
106 células/mL
150
50
0.1
0
0.0
0
50
100
150
200
250
300
Tempo (h)
Figura 15 – Avaliação do crescimento das BRS, em presença de manganês, feita por
turbidimetria (DO) e por contagem direta em câmara de Neubauer.
20
0.05
População
(Contagem direta)
0.04
DO
0.03
10
0.02
5
DO
106 células/mL
15
0.01
0.00
0
0
50
100
150
200
250
300
Tempo (h)
Figura 16 – Avaliação do crescimento das BRS, em presença de cádmio, feita por
turbidimetria (DO) e por contagem direta em câmara de Neubauer.
64
Segundo a Resolução CONAMA nº20 de 1986 as concentrações de manganês e de
cádmio devem estar na faixa de 0,1 a 0,5mg/L Mn e 0,001 a 0,01mg/L Cd, dependendo
da classificação do corpo d’água receptor. Assim sendo, a precipitação de metais pelo
sistema biológico de redução de sulfato pode ser uma alternativa interessante no
polimento de alguns efluentes industriais. É possível observar nas figuras 17 e 18 a
relação, inversamente proporcional, do crescimento bacteriano com a precipitação dos
metais. A precipitação do manganês ocorre em menor tempo que a precipitação do
cádmio. Isto porque, a produção do sulfeto e do CO2 dependem da redução biológica do
sulfato que em presença de cádmio fica inibida. Os resultados são curvas com
inclinações mais suaves no caso do cádmio e mais abruptas no caso do manganês.
200
20
(BRS)
10
Meio sem inóculo
Meio inoculado
150
100
106 células/mL
Mn mg/L
População
15
50
5
0
0
0
50
100
150
200
250
300
Tempo (h)
Figura 17 – Relação existente entre crescimento bacteriano e a precipitação do
manganês.
65
20
20
População
(BRS)
15
Cd mg/L
Meio sem inóculo
Meio inoculado
10
10
106 células/mL
15
5
5
0
0
0
50
100
150
200
250
300
Tempo (h)
Figura 18 – Relação existente entre crescimento bacteriano e a precipitação do cádmio.
Analisando o pH e o crescimento bacteriano (contagem direta), verifica-se que há
relação direta entre os mesmos. Isto porque, o sulfato é utilizado como aceptor final de
elétrons na respiração anaeróbia. Logo, o crescimento bacteriano (fase log) favorece a
cinética do processo de dessulfatação, reduzindo maior quantidade de sulfato (Von
Sperling, 1996). E a redução de sulfato, por sua vez, implica em consumo de H+ e
produção de CO2, como já visto nas equações 19 e 21. Observa-se que, tanto na figura
19 quanto na figura 20, as curvas de pH acompanham a inclinação da curva de
crescimento bacteriano, confirmando a relação direta entre estes parâmetros.
66
200
9.0
150
pH
8.0
pH
100
7.5
106 células/mL
População
(BRS)
8.5
50
7.0
6.5
0
6.0
0
50
100
150
200
250
300
Tempo (h)
Figura 19 – Crescimento bacteriano em presença de manganês e alcalinização do meio
mínimo.
20
8.0
População
pH
7.5
pH
10
7.0
106 células/mL
15
(BRS)
5
6.5
6.0
0
0
50
100
150
200
250
300
Tempo (h)
Figura 20 – Crescimento bacteriano em presença de cádmio e alcalinização do meio
mínimo.
67
A fase log das BRS, em presença de manganês, durou 24 horas. Enquanto, em presença
de cádmio, durou 4 dias. Este fato está relacionado à diferença de toxidez entre estes
metais. O crescimento bacteriano, em presença dos metais cádmio e manganês, foi
modelado tomando-se como base a fase log das figuras 19 e 20. Assim, pôde-se
escrever:
a) Manganês: ln(população) = 0,123(tempo) – 12,206
µ=0,123 (23)
b) Cádmio: ln(população) = 0,0139(tempo) + 0,148
µ=0,0139 (24)
Onde µ é a velocidade de crescimento específica. A reta resultante, com inclinação igual
a µ , permitiu o cálculo do tempo de duplicação (g) que pôde ser determinado aplicandose a equação:
g=
ln 2
µ
(25)
Os tempos de duplicação das BRS encontrados, em presença de manganês e de cádmio,
foram, respectivamente, 6 horas e 50 horas; o que confirma a maior dificuldade de
crescimento das BRS em presença do cádmio. Para que o sistema de tratamento em
reatores anaeróbios seja eficiente, o tempo de residência deve ser maior que o tempo de
duplicação, o que sugere a necessidade de adaptação das BRS à presença de cádmio em
sistemas industriais.
Observando as figuras 21 e 22, verifica-se que a concentração de sulfato, nos reatores de
100mL, reduziu-se com o tempo, como esperado. Porém, a taxa de redução ficou em
torno de 10%, em 12 dias. Sendo, que os primeiros 4 dias de incubação, tanto em
presença de manganês quanto de cádmio, equivalem à fase lag do processo. Tabak e
Govind (2003) desenvolveram estudos em biorreatores de membrana, onde foi possível
verificar a relação direta entre o consumo de sulfato e o crescimento bacteriano. E
observaram que o consumo de sulfato ocorria durante a fase log, estabilizando-se, no
sistema batelada, após esta fase; confirmando os resultados do presente trabalho.
68
200
4.4
4.2
150
População
4.0
100
3.8
3.6
SO4-2 g/L
106 células/mL
(BRS)
50
Sulfato
3.4
0
3.2
0
50
100
150
200
250
300
Tempo (h)
Figura 21 – Crescimento bacteriano, em presença de manganês, versus o consumo de
sulfato.
4.4
20
Sulfato
População
15
4.2
4.0
10
SO4-2 g/L
106 células/mL
(BRS)
3.8
5
3.6
0
0
50
100
150
200
250
300
Tempo (h)
Figura 22 – Crescimento bacteriano, em presença de cádmio, versus o consumo de
sulfato.
69
Os ensaios realizados nos reatores anaeróbios de batelada com leito de areia, utilizando
meio mínimo e pH 6,2, apresentaram 90% de precipitação do manganês (de 20mg/L
para 2mg/L) e 85% de remoção de cádmio (de 20mg/L para 3mg/L), após 13 dias.
Ginter e Grobicki (1997), estudando a precipitação do manganês (50mg/L) em reator
UASB, verificaram que a ausência de sulfato no meio de cultura dificulta a remoção
deste metal no sistema. Nesta condição, o manganês poderia ser removido por adsorção
no lodo em suspensão, porém, este processo não se mostrou eficiente. Em presença de
88,4mg/L de sulfato houve uma precipitação de 40% de manganês, enquanto na
ausência deste ânion a precipitação foi de apenas 7,2%. A solução de alimentação do
reator era composta de 0,67g de sucrose, 0,2g peptona, 0,675g NaHCO3 e 0,02g de
K2HPO4 por litro (DQO final de 1g/L) e tinha o pH ajustado para 6,3. Ginter e Grobicki
(1997) observaram ainda que a precipitação ocorreu pela formação do carbonato de
manganês (MnCO3). Em uma etapa posterior deste mesmo trabalho, estes autores
acrescentaram 50mg/L de cádmio ao meio de cultura (contendo sulfato) e obtiveram
uma remoção de 56% de manganês, ou seja, a mistura dos metais favoreceu a
precipitação do manganês pelo processo de co-precipitação.
Com o intuito de esclarecer qual(is) composto(s) de cádmio e de manganês precipitam
nos reatores anaeróbios, foram construidos diagramas de EhXpH para estes dois metais.
Foram considerados como possíveis ligantes: os sulfetos, os carbonatos e os hidróxidos.
A análise dos gráficos baseia-se no valor de Eh medido, durante a atividade bacteriana,
que foi igual a –290mV (Ag/AgCl) e no pH que variou de 6,2 a 8,5 (figuras 23 e 24). A
faixa cinza ,nas figuras 23 e 24, representa os valores de Eh (-290mV) e de pH (6,2 a
8,5) medidos durante os ensaios de biorredução.
70
E(Ag/AgCl) (Volts)
1.8
1.6
Mn(+3a)
1.4
1.2
1.0
0.8
0.6
0.4
0.2
0.0
-0.2
-0.4
-0.6
-0.8
-1.0
-1.2
-1.4
-1.6
-1.8
-2.0
-2.2
0
2
Mn(OH)2(+a)
Mn(+2a)
Mn(OH)2
MnCO3
MnS
Mn
4
6
8
10
12
14
pH
Figura 23 – Diagrama de EhXpH para o manganês, a 25ºC. Condições: [Mn]T=3,6x10-4
mol/Kg H2O, [CO3]T=5,2x10-3 mol/Kg H2O e [S]T=2,6x10-3 mol/Kg H2O.
E(Ag/AgCl) (Volts)
1.8
1.3
Cd(+2a)
CdCO3
0.8
Cd(OH)2
0.3
Cd(OH)3(-a)
-0.2
-0.7
-1.2
CdS
-1.7
-2.2
0
2
4
6
8
10
12
14
pH
Figura 24 – Diagrama de EhXpH para o cádmio, a 25ºC. Condições: [Cd]T=1,78x10-4
mol/Kg H2O, [CO3]T=5,2x10-3 mol/Kg H2O e [S]T=2,64x10-3 mol/Kg H2O.
71
A figura 23 sugere que o manganês, nas condições estudadas, pode precipitar na forma
de carbonato. Entretanto, como diagramas EhXpH não consideram aspectos cinéticos, a
precipitação de sulfeto pode estar ocorrendo simultaneamente. A precipitação deste
metal na forma de carbonato justificaria a sua maior remoção no topo do reator de
bancada (figura 12). Uma vez que, o CO2 tende a acumular-se na parte superior do
reator, devido a sua baixa solubilidade em água.
Observando a figura 24, verifica-se que o cádmio, nas condições estudadas, pode
precipitar tanto na forma de sulfeto quanto de carbonato. Porém, os produtos de
solubilidade do CdS e do CdCO3 diferem de 6 a 7 ordens de magnitude em favor da
formação do sulfeto de cádmio. Em função da menor solubilidade do sulfeto de cádmio
(K=107, equação 26) quando comparada ao carbonato deste metal (Kps=10-12,1)
acredita-se que o precipitado predominante seja o de sulfeto como sugerido por Ginter e
Grobicki (1997).
Cd+2 + H2S → 2 H+ + CdS
(26)
Observando os resultados como um todo, verifica-se que, apesar de algumas limitações,
as BRS estudadas foram capazes de reduzir sulfato, alcalinizar o meio e precipitar
metais. Sendo que os compostos precipitados, tanto na forma de carbonato quanto de
sulfeto, são estáveis no meio.
72
VII. CONCLUSÃO
Apesar de serem classificadas como anaeróbias estritas (potencial redox em torno de 100mV), as BRS apresentam tolerância ao oxigênio devido à presença da enzima
catalase, o que permite o seu manuseio em aerobiose. A eficiência na redução do sulfato
e o crescimento das BRS estão diretamente relacionados ao pH e ao meio utilizado. O
meio mais rico em nutrientes, como é o caso do meio tioglicolato 7,5% (v/v), permite o
crescimento das BRS em pH mais ácido (5,6), enquanto em meio mínimo, a acidez não
deve ser inferior a 6,2. A acidez favorece o consumo de sulfato apesar de prolongar a
fase lag, tanto em meio tioglicolato 7,5% (v/v) quanto em meio mínimo. A redução de
sulfato em reator de batelada é limitada por ser um sistema passível de saturação; desta
forma, o consumo máximo de sulfato, conseguido em 85 dias, foi 890mg/L. O meio
mínimo é seletivo para as BRS Gram positivas (isolados B.R.), pois, estas bactérias são
mais resistentes a diminuição do pH e também menos exigentes quanto ao meio
nutricional. Para ensaios “in vitro”, verificou-se que a presença de um leito de areia é de
suma importância para a precipitação de metais.
A aplicação das BRS em processo final (polimento) de tratamento de águas ácidas de
minas é viável, pois, além destes microrganismos crescerem em meios compostos,
basicamente, de sais inorgânicos, eles também precipitam metais e alcalinizam o meio.
Porém, alguns pontos são fundamentais para a utilização das BRS em tratamento de
corpos d’água: (1) o controle do pH do sistema; (2) o acompanhamento da quantidade e
da qualidade da matéria orgânica; e (3) a utilização de bactérias adaptadas as condições
do sistema em questão.
Referindo-se ao uso BRS no tratamento de efluentes, dois cenários podem ser
construídos: (1) quando a precipitação dos metais é o principal objetivo; (2) quando o
objetivo é a redução do teor de sulfato. No primeiro caso, o tempo de residência nos
reatores anaeróbios pode ser reduzido (em torno de 13 horas, por exemplo), uma vez
que, pequenas concentrações dos íons sulfeto e carbonato, produzidos pelas BRS, são
capazes de remover os metais. Esta tecnologia mostrou-se eficiente para reduzir os
73
teores de manganês e de cádmio em meio sintético e em efluentes industriais. No
segundo caso, o tempo de residência nos reatores é maior (48 horas no mínimo), devido
à cinética do processo. Exemplificando cada caso, pode-se dizer que reatores anaeróbios
seriam apropriados para precipitar metais enquanto a redução de sulfato seria melhor
conduzida em lagoas de estabilização.
No caso brasileiro, o maior potencial de aplicação da biorredução de sulfato seria
associada ao uso da cal. Como a cal é um insumo de baixo custo e amplamente
disponível no país, esta seria a primeira opção para neutralização de efluentes ácidos.
Entretanto, para reduzir os teores de sulfato que permanecem em torno de 1400mg/L,
devido a solubilidade do gesso, necessita-se de uma etapa de polimento. Neste caso, a
biorredução seria aplicada ao sulfato objetivando o seu enquadramento às normas da
Resolução CONAMA nº20 de 1986.
74
VIII. SUGESTÕES DE TRABALHOS FUTUROS
•
Tratamento de DAM utilizando BRS em reator anaeróbio de batelada.
•
Tratamento de DAM utilizando BRS em reator anaeróbio de alimentação
contínua.
•
Estudo de fontes naturais de carbono para alimentação do reator em sistema
contínuo
75
IX. REFERÊNCIAS BIBLIOGRÁFICAS:
ABRAHÃO,W. A. P.; MELLO, J. W. V. (2003). Aspectos químicos e mineralógicos
relacionados à geração de drenagem ácida em materiais sulfetados, Universidade
Federal de Viçosa, Departamento de solos, Viçosa-MG.
BEYENAL, H.; LEWANDOWSKI, Z. (2001). Mass-transport dynamics, activity, and
structure of sulfate-reducing biofilms, Environmental and energy engineering 47, 7.
BHATTACHARYA, S. K.; UBEROI, V.; DRONAMRAJU, M. M. (1996). Interaction
between acetate fed sulfate reducers and methanogens, Pergamon, Water Research.30,
10, pp. 2239-2246.
BRAGA, B. (2002). Introdução à engenharia ambiental. São Paulo: Prentice Hall.
BURGESS, J. E.; STUETZ, R. M. (2002). Activated sludge for the treatment of
sulphur-rich wastewaters, Pergamon, Minerals Engineering 15, pp. 839-846.
CASTRO, H. F.; WILLIAMS, N. H.; OGRAM, A. (2000). Phylogeny of sulfatereducing bacteria, Elsevier, FEMS Microbiology Ecology 31, pp. 1-9.
CLESCERI, L. S.; GREENBERG, A. E.; EATON, A. D. (1998). Standard Methods for
the examination of water and wastewater 20ª ed, USA: Ed APHA.
CHRISTENSEN, B.; LAAKE, M.; LIEN, T. (1996). Treatment of acid mine water by
sulfate-reducing bacteria; results from a bench scale experiment, Pergamon,
Water.Research.30, 7, pp. 1617-1624.
CYPIONKA, H.; WIDDEL, F.; PFENNIG, N. (1985). Survival of sulfate-reducing
bacteria after oxygen stress, and growth in sulfate-free oxygen-sulfide gradients,
Elsevier, FEMS Microbiology Ecology 31, pp. 39 - 45.
DILLING, W.; CYPIONKA H. (1990). Aerobic respiration in sulfate-reducing bacteria
Elsevier, FEMS Microbiology Letters 71, pp. 123-128.
ELLIOTT, P.; RAGUSA, S.; CATCHESIDE, D. (1998). Growth of sulfate-reducing
bacteria under acidic conditions in na upflow anaerobic bioreactor as a treatment system
for acid mine drainage, Pergamon, Wat. Res. 32, 12, pp. 3724-3730.
ESTEVES, F.A. (1998). Fundamentos de limnologia., 2ª ed., Rio de Janeiro: Ed
Interciencia.
FARELEIRA, P.; CHEN, L.; LIU, M. Y.; LEGALL, J.; SANTOS, H.; XAVIER, A. V
(2003). Response of a strict anaerobe to oxygen: survival strategies in Desulfovibrio
gigas, Great Britain, Microbiology 149, pp.1513-1522.
76
FORTIN D.; ROY M.; RIOUX JEAN-P.; THIBAULT PIERRE-J. (2000). Occurrence
of sulfate-reducing bacteria under a wide range of physico-chemical conditions in Au
and Cu-Zn mine tailings, Elsevier, FEMS Microbiology Ecology 33, pp. 197-208.
GADD, G. M. (2002). Bioremedial potential of microbial mechanisms of metal
mobilization and immobilization, Elsevier Science Ltda, Current Opinion in
Biotechnology 11, pp.271 - 279.
GARCIA, C.; MORENO, D.A.; BALLESTER, A.; BLÁZQUEZ, M.L.; GONZÁLEZ,
F. (2001). Bioremediation of an industrial acid mine water by metal-tolerant sulphatereducing bacteria, Pergamon, Minerals Engineering. Vol. 14, nº 9, pp. 997-1008.
GHIGLIAZZA, R.; LODI, A.; ROVATTI, M. (2000). Kinetic and process
considerations on biological reduction of soluble and scarcely soluble sulfates, Elsevier,
Resources, Conservation and Recycling 29, pp. 181-194.
GINTER, M. O.; GROBICKI, A. M. (1997). Manganese removal mechanismis in a
stirred UASB reactor, Pergamon, Wat. Res. 31, 6, pp. 1261-1268.
GRANT, W. D. (1998). Microbiologia Ambiental, Editorial Acribia S. A., Zaragoza –
España. Capitulo 7: Transformaciones microbianas de otros elementos, pp. 151-190.
INGVORSEN K.; NIELSEN M. Y.; JOULIAN C. (2003). Kinetics of bacterial sulfate
reduction in an activated sludge plant, , Elsevier, FEMS Microbiology Ecology 1570,
pp. 1-9.
JOHNSON, D. B. (2001). Importance of microbial ecology in the development of new
mineral technologies, Elsevier, Hydrometallurgy 59, pp. 147-157.
KAKSONEN, A. H.; FRANZMANN, P. D.; PUHAKKA, J. A. (2003). Performance
and ethanol oxidation kinetics of a sulfate-reducing fluidized-bed reactor treating acidic
metal-containing wastewater, Biodegradation 14, pp. 207-217.
KÜSEL, K.; ROTH, U.; TRINKWALTER, T.; PEIFFER, S. (2001). Effect of pH on the
anaerobic microbial cycling of sulfur in mining-impacted freshwater lake sediments,
Elsevier, Environmental and Experimental Botany 46, pp. 213 - 223.
LENS, P. N. L.; VISSER, A.; JANSSEN, A. J. H.; HULSHOFF POL, L. W.;
LETTINGA, G. (1998). Biotechnological treatment of sulfate-rich wastewaters, Critical
Reviews in Environmental Science and Technology 28, 1, pp. 41-88.
MANAHAN, S. E. (2000). Environmental Chemistry, 7ª ed., Boca Raton, Florida:
Lewis Publishers, pp 898.
77
MARTEL, A. E.; SMITH, R. M. (2003). NIST critically selected stability constants of
metals complexes Version 07, The National Institute of Standards and Technology –
USA.
MIRANDA, F. (2003). Gestão Ambiental e desenvolvimento sustentável, V Semana
Integrada de Estudos de Engenharia, Ouro Preto.
OKABE S.; ITO T.; SATOH H. (2003). Sulfate-reducing bacterial community structure
and their contribution to carbon mineralization in a wastewater biofilm growing under
microaerophilic conditions, Microbiol Biotechnol 63, pp 322-334.
OTTO, Bier. (1966). Bacteriologia e Imunologia, 13ª ed., Ed Melhoramentos, Capítulo
XXXVI: Métodos Bioquímicos, pp. 824 a 827.
PELCZAR, M. J. Jr. (1996). Microbiologia: conceitos e aplicações, 2ª ed. São Paulo:
Ed. Makron books, vol 1.
REBOUÇAS, A. C.; BRAGA, B.; TUNDISI, J. G. (2002). Águas doces no Brasil:
capital ecológico, uso e conservação organização e coordenação científica, 2ª ed., São
Paulo: Ed. Escrituras.
SASS, A. M.; ESCHEMANN, A.; KÜHL, M.; THAR, R.; SASS, H.; CYPIONKA H.
(2002). Growth and chemosensory behavior of sulfate-reducing bacteria in oxygensulfide gradients, Elsevier, FEMS Microbiology Ecology v. 40, p. 47 – 54.
SAWYER, C. N.; McCARLY P. L.; PARKIN, G. F. (1994). Chemistry for
environmental engineering, 4ª ed., New York: McGraw-Hill Book Company.
SENGUPTA, M. (1993). Environmental impacts of mining monitoring, restoration and
control, 1ªed., Florida: Boca Raton. - Lewis Publishers, Chapter 5: Acid Rock Drainage
and Metal Migration, pp. 167 – 259; Chapter 8: Wetlands, pp. 325 - 424.
SILVA, A. J.; VARESCHE, M. B.; FORESTI, E.; ZAIAT, M. (2002). Sulphate removal
from industrial wastewater using a packed-bed anaerobic reactor, Elsevier, Process
Biochemistry 37, pp. 927 - 935.
SILVA, C. A.; LEÃO V. A. (1999). Diagramas de Pourbaix, Departamento de
Metalurgia, Escola de Minas da UFOP.
SOARES, J. B.; CASIMIRO, A. R. S.; AGUIAR, L.M.B.A. (1987). Microbiologia
básica, Fortaleza, Ed UFC.
TABAK, H. H.; GOVIND, R. (2003). Advances in biotreatment of acid mine drainage
and biorecovery of metals: 1) Metal precipitation for recovery and recycle
Biodegradation 14, pp.423-436. 2) Membrane bioreactor system for sulfate reduction
Biodegradation 14, pp.437-452.
78
TUPPURAINEN, K. O.; VAISÄNEN, A. O.; RINTALA, J. A. (2002). Zinc removal in
anaerobic sulphate-reducing liquid substrate process, Pergamon, Minerals Engineering
15, pp. 847-852.
Von SPERLING, M. (1996). Princípios básicos do tratamento de esgotos. Belo
Horizonte: DESA-UFMG, volumes 1 e 2.
VOSSOUGHI, M.; SHAKERI, M.; ALEMZADEH, I. (2003). Performance of anaerobic
baffled reactor treating synthetic wastewater influenced by decreasing COD/SO4-2 ratios,
Elsevier, Chemical Engineering and Processing 42, pp. 811 - 816.
WHITE, C.; SAYER, J. A.; GADD, G. M. (1997). Microbial solubilization and
immobilization of toxic metals: key biogeochemical processes for treatment of
contamination, Elsevier, FEMS Microbiology Reviews 20, pp. 503 - 516.
WIDDEL, F. (1988). Produção de ácido sulfídrico por bactérias redutoras de sulfato e
outras atividades - traduzido por Maria Emília Costa Lima, do alemão para o português,
Universität München.
79