UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO
EVELYN VODOVOZ
FACOEMULSIFICAÇÃO PARA CORREÇÃO DE
CATARATA SEGUIDA DE IMPLANTE DA LENTE
INTRAOCULAR
Acri-Lens® VetH 41D –
RELATO DE CASO
CURITIBA- PR
2009
EVELYN VODOVOZ
FACOEMULSIFICAÇÃO PARA CORREÇÃO DE
CATARATA SEGUIDA DE IMPLANTE DA LENTE
INTRAOCULAR
Acri-Lens® VetH 41DRELATO DE CASO
Monografia
apresentada
a
Universidade Federal Rural do SemiÁrido – UFERSA, Departamento de
Ciências Animais para obtenção do
título de especialista em Clínica
Médica de Pequenos Animais.
Orientador: Prof. Dr. João Alfredo Kleiner
CURITIBA-PR
2009
Resumo
A catarata é definida como qualquer opacidade lenticular e pode estar localizada no
córtex, no núcleo ou na cápsula do cristalino. Dentre as causas principais pode-se
destacar a senilidade, traumas, anomalias congênitas, fatores genéticos, toxinas,
radiações, outras doenças oculares e doenças sistêmicas. O diagnóstico da catarata é
feito através de um bom exame oftálmico e seu tratamento é unicamente cirúrgico. Com
o advento da facoemulsificação e do implante de lentes intraoculares dobráveis, a
cirurgia de catarata evoluiu muito e seus resultados tornaram- se muito melhores,
principalmente com a recuperação da acuidade visual dos pacientes. Este trabalho tem
como objetivo descrever os resultados obtidos em um cão da raça Coker Spaniel que foi
submetida a cirurgia da catarata com facoemulsificação seguida de um implante de uma
lente artificial dobrável, a Acri-Lens VetH de 41D.
Palavras- chave: Cães, catarata, facoemulsificação, lente intraocular.
Abstract
Catarct is defined as any opacity and it can be localized in cortical, nuclear or capsular
region of the cristalin. Among the mainly causes one can point out aging, trauma,
congenital anomalies, genetic factors, toxins, radiation, other ocular diseases or
systemic diseases. The
diagnostic is made by good ophthalmic exam and the only treatment is only surgery.
With the advent of phacoemulsification followed by a foldable intraocular lens implant
the cataract surgery evoldved very much and its results became much better, mainly
pertaining to restore the visual acuity. This article intends to describe the results
achieved in a Cocker Spaniel that underwent cataract surgery by phacoemulsification
followed by an intraocular foldable lens implant. (Acri-Lens VetH 41D).
Keywords: Dogs, cataract, phacoemulsification, intraocular lenses.
Lista de Figuras
Figura 1: Catarata madura em olho de cão da raça Schnauzer............................................31
Figura 2: Emulsificação do núcleo opaco.......................................................................41
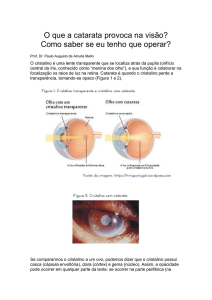
Figura 3: Visão de um cão após facoemulsificação e sem implante de lente intraocular. Boa visão de longe e sem detalhes (hipermetropia)............................................42
Figura 4: Visão de um cão normal e após o implante de uma lente intra- ocular. A cor
azul é distinta e o vermelho e verde tentem a se confundir.............................................43
Figura 5: Lente Acrílica dobrável de 40D implantada em um cão da raça Schnauz .......43
Figura 6: Acri-Lens® VetH ............................................................................................48
Figura 7: Figura ilustrativa da lente Acri-Lens® VetH mostrando sua anatomia..........48
Figura 8: Pré-operatório da cirurgia (pupila dilatada). Reparar a opacidade do cristalino
com catarata.....................................................................................................................49
Figura 9: Lente intra- ocular acrílica sendo implantada..................................................49
Figura10: Imagem imediatamente após implante da lente Acri-Lens® VetH................50
SUMÁRIO
RESUMO..........................................................................................................................2
ABSTRACT.....................................................................................................................3
LISTA DE FIGURAS.....................................................................................................4
1
INTRODUÇÃO...................................................................................................7
2
REVISÃO DE LITERATURA...........................................................................8
2.1 HISTÓRIA DA CATARATA.............................................................................8
2.2 ANATOMIA.......................................................................................................11
3 CATARATA..........................................................................................................14
3.1 CLASSIFICAÇÃO..............................................................................................16
3.1.1 Idade de Início..................................................................................................16
3.1.1.1 Anomalias Congênitas...................................................................................16
3.1.1.2 Catarata Hereditária Congênita.....................................................................17
3.1.1.3 Catarata Evolutiva Hereditária......................................................................18
3.1.1.4 Catarata Hereditária.......................................................................................18
3.1.1.5 Catarata Senil (início tardio)..........................................................................22
3.1.2 Cataratas Adquiridas........................................................................................23
3.1.2.1 Catarata Traumática......................................................................................23
3.1.2.2 Catarata Tóxica.............................................................................................24
3.1.2.3 Catarata Secundária a Outras Doenças Oculares..........................................25
3.1.2.4 Catarata Secundária a Doença Sistêmica......................................................26
3.1.3 Classificação de Acordo com a Localização....................................................27
3.1.3.1 Catarata Nuclear............................................................................................27
3.1.3.2 Catarata Capsular...........................................................................................28
3.1.3.3 Catarata Subcapsular.....................................................................................28
3.1.3.4 Catarata Cortical............................................................................................29
3.1.4 Estágios de Desenvolvimento...........................................................................30
3.1.4.1 Incipiente.......................................................................................................30
3.1.4.2 Imatura...........................................................................................................30
3.1.4.3 Madura...........................................................................................................30
3.1.4.4 Hipermatura...................................................................................................31
3.1.4.5 Reabsorvente.................................................................................................32
4 SINAIS CLÍNICOS E DIAGNÓSTICO ............................................................33
5 TRATAMENTO...................................................................................................34
5.1 MEDICAMENTOS PRÉ- OPERATÓRIOS .....................................................36
5.2 MEDICAMENTOS PÓS- OPERATORIOS......................................................37
6 SELEÇÃO DO PACIENTE................................................................................39
7 A CIRURGIA PARA REMOÇÃO DA CATARATA......................................40
8 LENTES INTRA- OCULARES.........................................................................42
9 RELATO DE CASO...........................................................................................44
10 MATERIAL E MÉTODOS..............................................................................45
11 DISCUSSÃO......................................................................................................47
12 CONCLUSÃO...................................................................................................51
REFERÊNCIAS.............................................................................................................53
1 INTRODUÇÃO
A catarata é uma das alterações oculares mais comuns na oftalmologia
veterinária. Com o aumento da expectativa de vida de cães e gatos, cada vez mais
aparecerão animais, principalmente cães, com catarata na rotina do clínico veterinário.
O único tratamento para a catarata é a cirurgia corretiva e a melhor técnica é
através da facoemulsificação. Os proprietários devem estar conscientes que o quanto
antes realizada a cirurgia de catarata utilizando-se a facoemulsificação maiores são as
chances de um resultado muito bom e maiores as chances da realização do implante de
uma lente artificial.
O cão afácico (sem cristalino) que passou pela cirurgia corretiva da catarata,
enxerga bem de longe e pouco de perto, mas recupera bem sua visão funcional e tem
grande melhora na qualidade de vida. A falta do cristalino resulta em alta hipermetropia
(14 D), a visão fica fora de foco e com estereoscopia (visão 3D) prejudicada. A correção
pode ser feita com a utilização de lente intra-ocular (LIO).
O implante de lentes intra-oculares em animais é um grande diferencial na
cirurgia de catarata, porque melhoram muito a visão de perto e o detalhe da imagem
obtida e é por isso que hoje existe a preocupação do estudo de novas tecnologias para o
aperfeiçoamento das lentes intra-oculares implantadas em cães.
O uso do facoemulsificador foi uma grande revolução nas cirurgias de catarata,
pois requer uma incisão menor, envolve um período encurtado, menor manipulação no
interior do globo ocular e mantém a câmara anterior, proporcionando maior êxito em
comparação com a técnica de extração extracapsular a céu aberto. O desconforto pósoperatório é mínimo, as inflamações mais discretas e o sucesso cirúrgico chegam a mais
de 95% dos casos.
Este trabalho tem como objetivo estudar um novo modelo de lente intra-ocular
desenvolvida especialmente para cães.
Serão discutidas as vantagens do uso da lente intra-ocular com superfície
heparinizada, assim como as características e a forma como a heparina ajuda na
prevenção de complicações pós-cirúrgicas.
2. REVISÃO DE LITERATURA
2.1 A HISTORIA DA CIRURGIA DA CATARATA
A história da cirurgia da catarata apresenta um curso circular, pois à medida que
algumas técnicas iam sendo abandonadas, novas técnicas com detalhes e materiais
novos iam sendo usadas.
O deslocamento do cristalino para câmara vítrea foi uma técnica usada por muito
tempo, há mais de 3000 anos, e teve inicio na Índia, mas infelizmente muitos dos relatos
antigos se perderam ou encontraram-se incompletos.
Até a data de 1515, quando Vesalius confirmou a função da retina e Francisco
Manrolycus estabeleceu a função óptica do cristalino, acreditava-se que a catarata era
uma doença semelhante ao glaucoma, pois aparentemente ambas levavam à cegueira e
ao “embranquecimento do olho”. Em 1650 Rolfinck descreveu a catarata com sendo a
opacidade do cristalino.
O primeiro a empregar o método de sucção para remoção da catarata foi o grego
Antyllos, no século III. As técnicas mais bem aceitas eram a de luxação do cristalino
para a câmara vítrea e a fragmentação do mesmo, para posterior reabsorção pelo próprio
organismo. As duas eram realizadas sem amplas aberturas do olho.
Só em 1750, o cirurgião francês Jacques Daviel realizou, com sucesso, a
primeira extração extracapsular planejada. Mas esta técnica foi abandonada devido às
difíceis técnicas impostas pelo procedimento na época.
As cirurgias que eram feitas abrindo o olho, apesar de não bem aceitas por
muitos cirurgiões, deram início a uma nova era do tratamento da catarata. Esta técnica
só ganhou força na metade do século XIX, quando foi introduzida a anestesia geral. Isto
facilitou a tolerância do paciente à operação, possibilitando uma manipulação do olho
pelo cirurgião. Além disso, em 1884, Carl Koller descobriu o efeito anestésico local da
cocaína. Com a revolução dos materiais e substâncias, no início do século XX foram
melhoradas as técnicas de ecinesia do olho. Em 1928, Anton Elsching, pela primeira vez
propôs a técnica de injeção retrobulbar de anestésico para imobilizar e anestesiar o
globo ocular. Van Lint, em 1914, já havia conseguido imobilizar o músculo orbicular,
injetando anestésico diretamente nas fibras musculares.
O segundo grande avanço foi a introdução de suturas para o fechamento da
ferida. Henry Willard Williams foi o primeiro a reportar esta técnica, ao suturar o limbo
usando uma agulha de costura e um fio fino de seda. Por este material ser muito
grosseiro, esta técnica foi deixada de lado por mais trinta anos. Mais tarde, em 1894, o
francês Jean Eugène Kalt reintroduziu a técnica de sutura córneo-escleral, utilizando
agulhas e fios mais bem adaptados aos interesses oftalmológicos.
O terceiro avanço foi quando Albrecht von Graefe, propôs em 1864, a abertura
do olho através da incisão limbal periférica. Isto proporcionou uma incisão menor, mais
eficiente e que protegia mais o olho, reduzindo drasticamente a incidência de
endoftalmite.
Entre a primeira e a segunda guerra mundial, a técnica intracapsular voltou a
ganhar projeção, desbancando a extracapsular e tornando-se o método de escolha para o
tratamento da catarata. Como não havia microscópio, era muito difícil remover todo o
córtex lenticular na técnica extracapsular e este córtex residual provocava uma grande
reação inflamatória, que poderia culminar na perda total ou parcial da visão e não era
incomum a opacidade da cápsula posterior devido aos restos corticais. Por outro lado, a
técnica intracapsular, por remover todo o cristalino juntamente com sua cápsula, não era
susceptível a estes tipos de complicações. Na cirurgia extracapsular o cirurgião deveria
ter muita habilidade e treinamento, e a perda vítrea inadvertida era considerada uma
complicação grave da cirurgia. Então, os cirurgiões pouco habilidosos conseguiam mais
sucesso com a técnica intracapsular.
No início do século XX, a facectomia intracapsular era o método de escolha para
o tratamento da catarata. Foram alcançados grandes avanços médicos durante metade do
século XX, em decorrência da Segunda Guerra Mundial e o primeiro avanço foi a
introdução da microcirurgia. Em 1950 Harms e Barraquer modificaram os
microscópios, adaptando-os para o uso oftalmológico. Em 1958 Joaquim Barraquer
descreveu uma enzima pra desfazer a zônula e em 1961, o polonês T. Krwawicz propôs
a crioextração. Ambas facilitaram a remoção do cristalino e contribuíram bastante com
a melhoria dos resultados cirúrgicos.
A partir de 1960, a cirurgia extracapsular voltou a ganhar força e o primeiro, e
talvez o mais importante passo para que isto acontecesse, foi o desenvolvimento e a
implantação de uma lente intra-ocular, pela primeira vez, em 1949, feita por Harold
Ridley. As primeiras lentes eram grandes e pesadas, causando muitas complicações.
Cerca de dez anos depois, Cornelius Birkhorst conseguiu desenvolver, a partir do
modelo de Ridley, uma lente melhor adaptada ao olho humano. Birkhorst não só
aprimorou a lente intra-ocular de Ridley, como também determinou que a melhor
técnica cirúrgica para o implante da lente seria a extracapsular, por preservar a cápsula
posterior, permitindo o posicionamento ideal da lente dentro do saco capsular.
Em 1965, Charles Kelman sugeriu que o equipamento de ultra-som utilizado
pelos dentistas poderia ser adaptado para fragmentar o cristalino, diminuindo o tamanho
da incisão cirúrgica. Dois anos depois, Kelman apresentou o aparelho de
facoemulsificação. Com este aparelho seria diminuído o tamanho da incisão, o cirurgião
trabalharia em um sistema fechado e evitaria a exposição excessiva do interior do globo.
A primeira cirurgia em olho humano demorou cerca de três horas, o equipamento era
grande, pouco eficiente, de difícil controle e extremamente pesado, por isso esta técnica
foi muito criticada.
O progresso tecnológico, as novas técnicas cirúrgicas (principalmente a abertura
da cápsula anterior por meio de uma incisão curvilínea contínua, a capsulorréxis) e o
desenvolvimento de lentes intra-oculares dobráveis possibilitaram o desenvolvimento
da moderna cirurgia de facoemulsificação.
Hoje em dia os resultados obtidos são muito gratificantes e o sucesso cirúrgico
chega a mais de 97% dos casos.
As incisões tornam-se cada vez menores, diminuindo assim o astigmatismo
residual.
Existem diferentes formatos, poder refrativo e materiais que constituem as
modernas lentes e estas podem ser feitas de acordo com a necessidade e característica de
cada paciente.
Deve-se levar em consideração também o grande avanço que os aparelhos de
facoemulsificação apresentam hoje em dia, com recursos avançados permitindo uma
cirurgia mais rápida e com menos complicações.
2.2 ANATOMIA
A lente é uma estrutura transparente de origem ectodermal, biconvexa, em
constante crescimento durante a vida, através da formação de novas fibras pelo
alongamento das células epidermais equatoriais. As fibras velhas formam o núcleo,
enquanto o córtex consiste de células jovens (PEIFFER JR.; PETERSEN- JONES,
2001).
A lente é avascular, impedindo reações inflamatórias típicas (PEIFFER JR.;
PETERSEN- JONES, 2001). Sua superfície anterior é mais plana e menos curva que a
posterior. Os centros das superfícies se denominam pólos anterior e posterior. As fibras
das lentes se encontram nestes pólos, nos cães formam um Y em pé anteriormente e um
Y invertido posteriormente (PEIFFER JR.; PETERSEN- JONES, 2001). A
circunferência cilíndrica é o equador, que tem numerosas irregularidades onde se
aderem as fibras zonulares (SLATTER, 1992).
O cristalino do cão e do gato normal é composto de uma cápsula externa, células
epiteliais por baixo da cápsula anterior e fibras formadas pela migração de células
epiteliais para o equador do cristalino, onde as células se alongam e criam um arranjo de
fibras regular. O arranjo regular dessas fibras responde pela transparência do cristalino
(BIRCHARD; SHERDING, 2003). O cristalino é posterior a íris, anterior ao humor
vítreo (ao qual se fixa) e suspenso por zônulas (que surgem a partir do corpo ciliar e se
fixam na cápsula do cristalino no equador) (BIRCHARD; SHERDING, 2003;
KLEINER, 2007a).
As alterações na tensão das fibras zonulares, mudam a superfície do cristalino e
a potência óptica: é o fenômeno da acomodação. Durante a acomodação, a contração do
músculo ciliar relaxa as zônulas, a elasticidade natural dos cristalóides faz com que a
lente se torne mais esférica, aumenta o poder óptico e o sistema óptico é acomodado
para ver objetos próximos. Os mecanismos que fazem acomodação nos animais
domésticos são pouco desenvolvidos, tais como o músculo ciliar (SLATTER, 1992).
A córnea é a superfície refringente mais importante no olho, que apresenta a
maior parte do poder óptico (SLATTER, 1992).
O cristalino está dividido em duas regiões generalizadas: o córtex (áreas externas
perto da cápsula) e o núcleo (áreas centrais). À medida que o cristalino cresce durante
toda a vida, produzem camadas de fibras na área equatorial que se depositam sobre a
parte superior das restantes, formando as fibras mais antigas em direção ao centro do
cristalino. Estas sucessivas capas são visíveis clinicamente e são designadas núcleos
adulto, fetal e embrionário, respectivamente (SLATTER, 1992).
O cristalóide é uma capa elástica transparente que está ao redor do cristalino. A
lâmina da membrana basal do epitélio invertido forma as fibras lenticulares e está
composta por fibras de colágeno e carboidratos complexos (SLATTER, 1992). A
cápsula regula a formação do cristalino mediante a sua elasticidade e proporciona
integração para as fibras zonulares. A cápsula do cristalino é impermeável às grandes
moléculas (por exemplo, albumina, globulina), mas permite a passagem de água e
eletrólitos. E devido à sua elasticidade, a penetração destas moléculas pela cápsula
lenticular resulta na retração das suas bordas (SLATTER, 1992).
Debaixo da cápsula anterior existem células epiteliais cubóides e no equador
encontram-se células cilíndricas. O epitélio corneano no equador forma as fibras
lenticulares novas. Devido à atividade mitótica desta área, as células são suscetíveis às
influências tóxicas e patológicas, que pode se mostrar como opacidades equatoriais. O
epitélio lenticular é importante no transporte de cátions através dos cristalóides
(SLATTER, 1992).
As células lenticulares compõem a sustentação do córtex e se dispõem em
estratos interdigitados unidos entre si por semento. As células velhas (núcleo) são mais
densas e menos transparentes que as mais jovens (córtex) depositadas ao seu redor. O
cristalino é sustentado pelas zônulas ou ligamentos zonulares e pelo humor vítreo,
situando-se em uma depressão chamada fossa hialóidea. As fibras de colágeno desde o
corpo vítreo se inserem nos cristalóides posteriores unindo os dois com firmeza. Nos
seres humanos esta fixação se debilita com a idade e pode se romper mecanicamente
com ajuda da α- quimotripsina (um processo conhecido como zonulólises, porque as
zônulas são digeridas), de modo que o cristalino e a cápsula são removidas se ocorrer
uma perda vítrea importante. Nos animais domésticos a fixação é muito mais firme e as
tentativas de extrair o cristalóide posterior também causam a perda do corpo vítreo
(SLATTER, 1992).
O cristalino requer oxigênio e metabólitos para a manutenção e a produção
contínua de células lenticulares e para a manutenção da elasticidade capsular e da
transparência. A maior parte do oxigênio necessário vem do humor aquoso, ainda que
esta demanda seja reduzida e consumida pelas células corticais e o epitélio anterior. O
metabolismo da glicose confere grande parte da energia requerida pelo cristalino. Quase
toda a glicose é desdobrada anaerobicamente até ácido lático mediante a via de
Embden-Meyerhof, ocorrendo certa glicólise aeróbica por intermédio do ciclo de ácido
cítrico. A conversão da glicose em frutose pela via do sorbitol é significativa
(SLATTER, 1992).
O cristalino é rico em proteínas (35%) e água (65%) e pobre em minerais. A
proporção de proteínas presentes varia com a espécie, idade e tamanho do cristalino
(SLATTER, 1992).
Sendo que o cristalino é avascular, seu metabolismo é precário e depende da
composição constante do humor aquoso, os distúrbios em tal composição afetam o
metabolismo lenticular (SLATTER, 1992).
Como o cristalino está confinado dentro de uma cápsula e suspenso no humor
aquoso, a gama de reações exibidas é muito ampla. O complicado metabolismo
lenticular está orientado na preservação da transparência e esta gama de reações pode
resultar em muitas alterações, causando degeneração e opacidade. A maioria das
reações lenticulares caem dentro dos seguintes grupos: liberação de material do
cristalino dentro do olho; trocas na posição do cristalino; perda da transparência
(SLATTER, 1992).
Depois de lesionado, o epitélio subcapsular é a única parte do cristalino que
mostra uma atividade reparadora limitada. Quando a cápsula é perfurada, o orifício pode
muitas vezes persistir e o líquido do humor aquoso entrar no cristalino. As fibras do
cristalino ficam embebidas com este líquido, inchando e ficando opaco em poucas
horas. Os orifícios minúsculos da região polar anterior podem se fechar com opacidade
residual nos cães. Habitualmente, o material lenticular tumefado sobre digestão
proteolítica, expondo mais substância do cristalino e finalmente aparecendo opacidade e
inchaço (intumescência) (SLATTER, 1992).
O material nuclear e cortical do cristalino pode alcançar o líquido do humor
aquoso, quer através de liquefação e passagem através da cápsula ou por ruptura do
cristalóide. Isto pode causar uma reação imune celular e humoral da úvea contra a
proteína liberada e ingestão de material lenticular pelos macrófagos, os quais se
ampliam e obstruem o ângulo de drenagem (glaucoma facolítico) (SLATTER, 1992).
As alterações na posição do cristalino se denominam luxação (deslocação
completa da fossa hialóidea) e subluxação (desprendimento parcial desde a fossa
hialóidea) (SLATTER, 1992).
3 CATARATA
Originário do grego, o termo catarata significa “água que cai”. Como um termo
médico, catarata define toda opacidade não fisiológica das fibras da lente e/ou da
cápsula, independentemente da etiologia (PEIFFER JR.; PETERSEN- JONES, 2001),
resultante de alterações patológicas na composição protéica do cristalino ou uma
destruição do arranjo de fibras lenticulares (BIRCHARD; SHERDING, 2003).
A lente normal se encontra em estado desidratado. O núcleo do cristalino tem
menos água que o córtex. Em muitos aspectos, a lente funciona como um medidor
osmótico. A desidratação da lente depende da bomba íon água sódio que depende da
energia do epitélio anterior da lente e das fibras da lente (GELATT, 1991).
Nas lentes com catarata, os vários mecanismos químicos ficam danificados;
estes eventos eventualmente progridem, resultando em hidratação do cristalino e
prejudicando a transmissão de luz e imagem pela lente. Na formação da catarata, as
proteínas insolúveis (normalmente por volta de 15%) aumentam por estarem associadas
à morte das células da lente; as proteínas insolúveis (também denominadas
albuminóides) aparecem primariamente nas células do núcleo, e as proteínas solúveis
estão no córtex da lente (GELATT, 1991).
As proteínas solúveis diminuem durante a formação da catarata, assinalando
uma diminuição na síntese de proteína (GELATT, 1991).
O transporte de água e eletrólitos ou o sistema da bomba, na formação da
catarata é defeituosa. A bomba excretora do íon Na+ é energia dependente; com a má
formação e morte do epitélio anterior da lente e fibras da lente, aumenta o sódio e íons
de potássio são perdidos, os quais regulam a hidratação da lente (GELATT, 1991).
Com as desintegrações graduais dos eventos bioquímicos da lente, durante a
formação da catarata, outros caminhos como de eletrólitos, glicose e lipídio, ficam
afetados. Muitas enzimas mostram decréscimo na atividade, enquanto as enzimas
hidrolíticas aumentam suas funções. Com retenção de sódio e cálcio e diminuição na
formação de junção de dissulfito (S-S), as proteínas da lente aumentam sua turbidez e
insolubilidade. A glicosidase hidrolítica quebra as células da membrana e as proteases
que quebram as proteínas da lente podem aumentar. Com essa quebra generalizada no
metabolismo do cristalino, e perda de ATP da lente, a hidratação da lente resulta no
estágio final de catarata osmótica opaca (GELATT, 1991).
A catarata hereditária trata-se da causa mais comum de catarata em cães. A
localização, a progressão e o modo de herança da catarata variam entre as raças. A
maioria das cataratas herdadas é bilateral, mas é frequentemente assimétrica em inicio e
progressão (BIRCHARD; SHERDING, 2003).
As cataratas são causadas por alguns fatores como: anormalidades congênitas,
fatores genéticos, toxinas, radiação, trauma, outras doenças oculares, doenças sistêmicas
e senilidade (GELATT, 1991).
As cataratas originadas por uveítes são comuns em gatos. Como o cristalino
necessita dos humores aquoso e vítreo para nutrição e remoção de resíduos metabólicos,
uma inflamação intra-ocular pode resultar em opacidades capsulares e corticais. Uma
sinéquia posterior decorrente de uveíte anterior pode resultar em catarata capsular
anterior (BIRCHARD; SHERDING, 2003).
Cataratas desenvolvidas depois da oitava semana de vida são chamadas
evolutivas. Catarata senil pode ocorrer em cães de idade, mas não pode ser confundida
com esclerose nuclear, uma alteração normal devido a senilidade (PEIFFER JR.;
PETERSEN- JONES, 2001).
3.1 CLASSIFICAÇÃO
A catarata pode ser classificada através de vários métodos incluindo idade de
aparecimento, localização, grau de maturação e causas. Cada método tem suas
vantagens e limitações; frequentemente todos podem ser usados simultaneamente para
descrever a catarata. A classificação da catarata pode predizer a associação da perda de
visão e progressão da catarata. Múltiplos métodos de classificação podem prover uma
descrição mais precisa da catarata. Por exemplo: Catarata equatorial evolutiva cortical
em Afegan Hound e poodle Standard, pode representar uma anormalidade hereditária
destas raças (GELATT, 1991).
3.1.1 Idade de início
As
cataratas
são
classificadas
pela
idade
de
início
da
opacidade.
Tradicionalmente se dividem em congênita (presente no nascimento ou logo depois),
evolutiva (juvenil, adulto ou primário) e tipo senil. A idade de início é uma
característica importante das cataratas hereditárias em algumas raças de cães. Quando
identificada, pode ser usada clinicamente para diagnóstico destes tipos de catarata
(GELATT, 1991).
3.1.1.1 Anomalias Congênitas
O desenvolvimento do cristalino ocorre cedo na embriogênese e está completo
no trigésimo dia gestacional. Qualquer anormalidade genética que afeta o
desenvolvimento do cristalino ou afecções ocorridas durante o início da gestação do feto
(incluindo lesões infecciosas, nutricionais, químicas ou relacionadas com drogas)
podem resultar em anomalias lenticulares congênitas (BIRCHARD- SHERDING, 2003;
GELATT, 1991). Essas anomalias se associam frequentemente com outras anomalias
oculares congênitas [incluindo microftalmia (globo ocular pequeno), persistência de
membranas pupilares, persistência de artéria hialóide, displasia retineana, descolamento
de retina, coloboma/estafiloma posterior e hipoplasia de nervo óptico]. (BIRCHARDSHERDING, 2003; GELATT, 1991).
Quando o crescimento da lente é interrompido temporariamente em um estágio
inicial de seu desenvolvimento, durante a formação primária das fibras, a catarata
resultante é nuclear em posição e geralmente não progressiva. A maioria das cataratas
congênitas é bilateral (GELATT, 1991).
3.1.1.2 Catarata Hereditária Congênita
Na catarata hereditária congênita o núcleo e córtex perinuclear são os mais
afetados. Cataratas congênitas restritas ao núcleo são geralmente não progressivas:
envolvimento cortical é um sinal de prognóstico ruim. Cataratas congênitas primárias
não associadas a defeitos de formações do olho podem ser encontradas em raças como
Satffordshire Bull Terrier, no West highland White Terrier e no Boston Terrier
(PEIFFER JR.; PETERSEN- JONES, 2001).
Catarata congênita associada à microftalmia é diagnosticada, entre outras, no
Schnauzer Miniatura, Cocker Spaniel Inglês, Cavalier King Charles Spaniel, West
highland White Terrier e Old English Sheepdog. No Cavalier King Charles Spaniel,
catarata congênita frequentemente ocorre em combinação com lenticonus ou
lentiglobus. (PEIFFER JR.; PETERSEN- JONES, 2001).
Além da catarata no Schnauzer Miniatura, que é herdado de um autossomo
recessivo, a forma de herança não foi estabelecida (PEIFFER JR.; PETERSEN- JONES,
2001). É importante notar que nem todas as cataratas congênitas são herdadas
(GELATT, 1991; PEIFFER JR.; PETERSEN- JONES, 2001).
3.1.1.3 Catarata Evolutiva Hereditária
Cataratas evolutivas (juvenil ou adulta) são aquelas que se desenvolvem nos
primeiros anos de vida. Assim como na catarata congênita, esta tem várias causas.
Cataratas evolutivas podem ser hereditárias, assim como no Afegan Hound, no qual
opacidades equatoriais na lente ocorrem cedo, por volta dos quatro meses de vida, ou no
Poodle Standard, no qual catarata equatorial se desenvolve antes dos dois anos de vida
(GELATT, 1991).
Outras causas não hereditárias de catarata evolutiva incluem trauma, diabetes,
inflamação intra-ocular e tóxico (GELATT, 1991).
A maioria das cataratas que se desenvolvem começam no córtex e podem
progredir e envolver toda a lente, incluindo o núcleo. A velocidade de progressão varia,
de apenas visível a mudanças rapidamente progressivas. A catarata triangular polar
posterior visto no Golden Retriver e Labrador, assim como em outras raças incluindo
Rottweilers e Sheepdog Bélgicos é considerada evolutiva se ocorrer depois dos seis
meses de idade na maioria dos cães. A lista das raças provadas ou suspeitas de herdar
catarata evolutiva é longa, com variações locais (PEIFFER JR.; PETERSEN- JONES,
2001).
3.1.1.4 Catarata Hereditária
Cataratas hereditárias primárias são as cataratas mais comumente encontradas
em cães; elas têm sido descritas em várias raças de cães e a lista está crescendo
continuamente. Dependendo da genética de cada país, a incidência da catarata
hereditária ligada às raças pode ser diferente significativamente. Catarata hereditária é
de longe mais rara em gatos, mas são suspeitos em Persas, Birman e himalaias
(PEIFFER JR.; PETERSEN- JONES, 2001).
Cataratas hereditárias podem ser congênitas ou desenvolvidas. Pode ser difícil de
determinar se uma catarata é considerada hereditária ou não (PEIFFER JR.;
PETERSEN- JONES, 2001). Entretanto, a maioria dos critérios a seguir que são
encontrados em conjunto com um animal afetado, levará, provavelmente a característica
de catarata hereditária:
∙catarata hereditária é previamente descrito na raça;
∙a catarata ocorre bilateralmente;
∙a idade quando aparece e a localização das mudanças lenticulares correspondem
ao descrito naquela raça;
∙a catarata é progressiva, apesar de lenta em alguns casos.
O problema surge quando uma forma suspeita de catarata congênita é
diagnosticada em uma raça “nova”. Avaliação dos pais e dos filhotes deve ser realizada
para posterior análise e relato do caso (PEIFFER JR.; PETERSEN- JONES, 2001).
A catarata hereditária em cães pode ser dividida em três categorias: cataratas
hereditárias não associadas a outras doenças oculares; catarata associada a atrofia retinal
progressiva; e cataratas associadas a múltiplos defeitos oculares. A primeira afeta
várias raças de cães. No Schnauzer Miniatura dois tipos de catarata hereditária acontece;
as duas são hereditárias por um gene simples autossomal recessivo. No primeiro tipo, a
catarata congênita é manifestada no nascimento e envolve o núcleo e, em uma pequena
porção, o córtex posterior; microftalmia ocorre concomitantemente. A progressão da
catarata é variável e relacionada ao envolvimento dos córtex posterior e equatorial. A
maioria das mudanças lenticulares progride para catarata madura dentro de poucos anos.
No segundo tipo de catarata hereditária em Schnauzer Miniatura, a catarata é vista em
filhotes com várias semanas de idade e primariamente envolve o córtex posterior
(GELATT, 1991).
Assim como no Schnauzer Miniatura, o Staffordshire Bull Terrier e Boston
Terrier também têm catarata hereditária que é evidenciada em poucos meses depois do
nascimento, afetando núcleo e córtex posterior, geralmente progride para maduro e não
é associada
com microftalmia. Nestas três raças estas cataratas primárias são
hereditárias transmitidas por um gene autossomo recessivo (GELATT, 1991).
O Golden Retriver desenvolve catarata posterior subcapsular assim como
catarata cortical completa. A maioria destas cataratas aparece como opacidades
triangulares subcapsulares no pólo posterior da lente (GELATT, 1991). Cataratas
posteriores subcapsulares tendem a permanecer focais na maioria dos pacientes; elas
não são aparentes para o dono, e normalmente não leva a cegueira. Imagina-se que a
catarata do Golden Retriver é transmitida por um traço dominante e que aqueles cães
com catarata triangular são heterozigotos, considerando que aqueles com catarata
madura são homozigotos, apesar de nenhuma comprovação ter sido relatada. O
Labrador Retriver também desenvolve catarata polar posterior e catarata cortical que é
muito similar àquela que ocorre no Golden Retriver. A forma de herança parece ser um
traço dominante (GELATT, 1991).
O Cocker Spaniel Americano desenvolve catarata hereditária, a forma de
herança é suspeita de ser autossomal recessiva, apesar de que a herança poligenética
possa ser possível. Neste caso a catarata tende a afetar os córtex anterior e posterior e se
tornar aparente em poucos anos. A taxa de progressão é variável; existe uma tendência à
rápida progressão a maturidade em cães jovens (GELATT, 1991).
Uma catarata equatorial familiar ocorre em Afghan Hound. Mudanças iniciais
ocorrem como vacúolos no equador da lente. Elas são desenvolvidas em Afghan Hound
jovens entre quatro meses a dois anos. Progressão é bastante rápida; diminuição da
visão pode ocorrer com dois anos de idade. Evidências de transmissão autossomal
recessiva da catarata, têm sido apoiadas pelos resultados de testes de reprodução
(GELATT, 1991).
Cataratas equatoriais são observadas em famílias de Poodle Standard. A catarata
inicialmente afeta o equador da lente em uma idade muito jovem e progride para afetar
a visão em seis a dezoito meses. Acredita-se que a catarata do Poodle Standard é
transmitida por um fator autossomal recessivo (GELATT, 1991).
Um segundo tipo de catarata hereditária afeta o Boston Terrier. Opacidades da
lente envolvendo o equador e córtex anterior, podem ser detectadas em cães com três a
quatro anos de idade. Afeta o Boston Terrrier bilateralmente, mas não necessariamente
simetricamente, a progressão desta catarata é freqüentemente lenta (GELATT, 1991).
Catarata equatorial e subcapsular ocorrem no Husky Siberiano. Estas cataratas
ocorrem em cães antes dos seis a dezoito meses e é normalmente de progressão lente. O
modo de herança é provavelmente recessivo.
Catarata hereditária também afeta o West Highland White Terrier e a raça Chow
Chow. Nesta, a aparência da catarata é um pouco variável, envolvendo as regiões
subcapsular anterior e posterior, o córtex anterior e posterior, o núcleo e o equador.
Podem existir anormalidades adicionais em cães afetados, como entrópio, microftalmia,
membrana pupilar persistente e displasia multifocal retinal (GELATT, 1991).
A catarata é observada em associação a doenças retinianas, mas a relação exata
entre mudanças lenticulares e doenças retinais não são conhecidas. A catarata pode ser
uma desordem genética ou ser secundária a degeneração retinal e possibilitar mudanças
no vítreo. Em ratos com degeneração retinal hereditária, a formação da catarata pode ser
iniciada por produtos tóxicos geradas pela oxidação de um lipídio poliinsaturado. O
Labrador Retriver e o Poodle miniatura e toy são essas raças que alterações por
cataratas, muito frequentemente, acompanha doença retiniana hereditária (GELATT,
1991).
Em Poodle Miniatura, Cocker Spaniel Inglês, Tibetan Terrier, e Setter Irlandês
com atrofia retinal progressiva, formação de catarata bilateral afetando os cortes
posterior e anterior nas regiões axial e equatorial pode ser rapidamente progressiva
(GELATT, 1991).
Nos Labrador Retrivers atrofia retinal progressiva central (CPRA) ou distrofia
retiniana do epitélio pigmentar, catarata cortical ocorre concomitantemente com
frequência. CPRA tende a ocorrer em cães maduros; o modo de herança pode ser
dominante com penetrância incompleta. A exata relação entre as alterações de cataratas
e a degeneração retinal não é conhecida (GELATT, 1991).
Muitas raças de cães com catarata congênita manifestam concomitantemente
defeitos oculares múltiplos, particularmente microftalmia e displasia retinal. Springer
Spaniels Inglês, Bedlington Terrier e Labrador Retrivers com displasia retinal e também
microftalmia normalmente tem catarata cortical bilateral. Formação de catarata
congênita associada com múltiplas doenças oculares, representa defeitos desenvolvidos,
às vezes hereditário, que frequentemente resultam em cegueira se a catarata for
completa ou parcial. No Cocker Spaniel vermelho a catarata bilateral congênita ocorre
com membrana da pupila persistente, microftalmia, hipotonia e nistagmo. Estas
cataratas são tipicamente anterior subcapsular e não progressiva. O modo exato de
herança não é conhecido (GELATT, 1991).
No Sheepdog Inglês, catarata nuclear bilateral e cortical são associados com
descolamento retinal. Esta raça pode desenvolver displasia retinal, anisocoria, catarata e
microftalmia. Catarata congênita e microftalmia ocorrem em muitas raças; no
Schnauzer Miniatura esta condição é hereditária por um fato autossomal recessivo; no
Cocker Spaniel Inglês o modo de herança parece complexo (GELATT, 1991).
3.1.1.5 Catarata Senil (início tardio)
Catarata senil é simplesmente associada com idade avançada, geralmente
ocorrendo depois de seis anos de idade. Catarata senil ocorre menos frequentemente em
cães do que em homens e afeta o núcleo e ocasionalmente o córtex (GELATT, 1991).
Uma catarata cortical senil típica aparece em camadas equatoriais profundas
com listras opacas se estendendo até o eixo como raios. A opacificação continua até que
se apresentem áreas claras somente nas linhas de suturas Y do córtex. As áreas claras
denominam fissuras de água dão ao cristalino uma aparência segmentada. Continuando
a opacificação, as fissuras de água ficam delgadas e finalmente desaparecem. Quando o
cristalino tem uma opacidade uniforme a catarata é madura. A opacificação cortical e a
nuclear acontecem no mesmo momento (SLATTER, 1992).
A catarata madura avança até perder líquido e reduzir de tamanho. Pode manterse firme durante vários anos antes de apresentar-se hipermatura: sinais de contração e
desidratação ou de colapso nuclear (catarata morganiana). O encolhimento pode separar
o cristalino de suas estruturas de fixação e causar luxação. A visão retorna na catarata de
Morgagni, similar ao fenômeno comprovado na reabsorção de uma catarata juvenil,
sempre que não seja intenso o dano ocular promovido pela uveíte facoanafilática. Os
pacientes idosos (passada a idade em que se aconselha a extração da catarata)
comumente toleram baixos níveis de uveítes, controlada mediante dexametasona tópica
(uma a duas vezes por dia), durante intervalos prolongados com bastante comodidade
(SLATTER, 1992).
Esclerose nuclear, uma forma comum de alteração lenticular, é presente em
quantidade variável, em muitos cães acima de seis anos de idade. A esclerose nuclear é
considerada uma alteração pela idade normal associada a compressão das fibras
epiteliais da lente, pelo núcleo da lente (GELATT, 1991).
Deve-se diferenciar a catarata da esclerose nuclear. A esclerose nuclear é uma
névoa homogênea, bem definida e bilateralmente simétrica no centro do cristalino,
observada em animal com mais de seis anos de idade. Não constitui uma opacidade
verdadeira nem obstrui um exame com a pupila dilatada de fundo de olho ou causa
prejuízo visual clinicamente importante (BIRCHARD; SHERDING, 2003).
A diferenciação entre catarata e esclerose pode ser feita através de um bom
exame oftálmico de fundo de olho. Na catarata existe uma perda de detalhe parcial ou
total da retina devido ao bloqueio da luz pelas opacidades presentes e na esclerose não
(KLEINER, 2008).
3.1.2 Cataratas Adquiridas
3.1.2.1 Catarata Traumática
Um traumatismo rombudo intenso no olho pode resultar em formação de
catarata ou pode ser secundária a inflamação e/ou luxação lenticulares (BIRCHARD;
SHERDING, 2003). O trauma pode ser resultado de esmagamento, golpe de impacto
por um automóvel (GELATT, 1991).
Lesões permanentes que puncionam a cápsula lenticular anterior (por exemplo,
lesões por garras de gato, estilhaços de arma de fogo, vidro, espinhos) resultam em
cataratas focal ou difusa, dependendo da intensidade do trauma capsular (GELATT,
1991; BIRCHARD; SHERDING, 2003). Quando arrancada a cápsula anterior, podem
ocorrer desintegração de muitos dos ligamentos zonulares ou todos (GELATT, 1991). A
uveíte pode acontecer secundariamente a uma ruptura de cápsula lenticular
(BIRCHARD; SHERDING, 2003). Quanto maior o envolvimento da cortical, a
progressão da catarata também aumenta (GELATT, 1991).
A catarata traumática pode se desenvolver como resultado de um trauma abrupto
ou perfurante com ou sem ruptura da cápsula da lente. Pequena perfuração da cápsula
pode cicatrizar com fibrina e sinéquia posterior, com conseqüente catarata não
progressiva. Traumas abrupto ou perfurante maiores podem causar mudanças mais
extensas, progredindo para catarata completa. A ruptura da cápsula da lente com
liberação de proteínas (estranha para o sistema imune) dentro do humor aquoso
normalmente resulta em resposta severa e uveíte intensa (GELATT, 1991; PEIFFER
JR.; PETERSEN- JONES, 2001). A uveíte induzida pela lente é notada por vários
estágios de dor, lacrimejamento, congestão conjuntival bulbar, miose, uveíte anterior,
formação de sinéquia, pressão intraocular baixa, ou (ocasionalmente) glaucoma
secundário (GELATT, 1991). Bom manejo da catarata traumática com ruptura capsular
depende de diagnóstico precoce e tratamento vigoroso. Em alguns casos, a uveíte
induzida pela lente pode ser tratada com medicamentos, com terapia midriática intensa
(sulfato de atropina 1% e hidróxido de penilefrina 10% a cada hora antes que ocorra
midríase, e então duas ou três vezes ao dia) combinado com corticoterapia tópico e
sistêmico. Em casos mais severos com extrusão do material lenticular, uma intervenção
cirúrgica para remoção da lente (extração intra-capsular) seguida de intensa terapia
medicamentosa, é indicada (GELATT, 1991).
3.1.2.2 Catarata Tóxica
Muitas substâncias podem causar catarata quando administradas sistemicamente.
Estas incluem agentes mitóticos, enzimas inibitórias, sais de certos metais (talium,
cobalto, selênio), certos hidrocarbonos ou subprodutos do hidrocarbono (como
dinitropreno) (GELATT, 1991; PEIFFER JR.; PETERSEN- JONES, 2001). Altas
voltagens do irradiação de orbitol, para neoplasias nasais e paranasais, pode também
produzir catarata em cães (GELATT, 1991).
A formação da catarata depois de longo tempo de tratamento com cetoconazol
tem sido descrita (PEIFFER JR.; PETERSEN- JONES, 2001).
Algumas marcas comerciais de substitutos do leite produzem catarata em filhotes
órfãos, apesar de esse tipo de catarata ser melhor classificada como tipo nutricional
(PEIFFER JR.; PETERSEN- JONES, 2001). As mudanças lenticulares são ligeiras a
moderadas e consistem em vacuolização cortical posterior e equatorial. Proeminentes
anéis na junção cortico nuclear são às vezes presentes e às vezes persistente na idade
adulta (GELATT, 1991). Deficiência tanto de arginina quanto defenilanina tem sido
sugerido como causa; suplementação destes aminoácidos pode causar regressão da
catarata em lobos e ratos. Quando os filhotes afetados são desmamados e colocados em
dieta completa. Os vacúolos corticais e as estrias desaparecem, mas a opacidade
perinuclear proeminente permanece (GELATT, 1991).
Diazóxido, um derivado benzodiazepínico não diurético usado em tratamento de
emergência para hipertensão humana, tem produzido catarata em Beagles quando
administrado em altas doses. As alterações lenticulares são passageiras e foram
consideradas associadas com hiperglicemia (GELATT, 1991).
3.1.2.3 Catarata Secundária a Outras Doenças Oculares
Em um grande número de outras doenças oculares, a catarata pode se
desenvolver secundariamente. Atrofia progressiva da retina (PRA) em cães (em gatos
não) geralmente resulta em catarata secundária, disfarçando a doença primária.
Questionar o proprietário sobre o início, a visão de dia e em condições de pouca luz,
assim como considerar a idade do cão e sua raça, é essencial para estabelecer o
diagnóstico. A eletroretinografia (ERG) deve sempre ser analisada antes da cirurgia de
catarata se for suspeito de uma doença na retina e a retina não puder ser avaliada
oftalmoscopicamente (PEIFFER JR.; PETERSEN- JONES, 2001).
Uveítes, luxações de lente, e glaucoma frequentemente levam a formação de
catarata, especialmente em gatos. Essas cataratas são causadas por uma alteração na
composição do humor aquoso, o qual é responsável pela nutrição da lente (PEIFFER
JR.; PETERSEN- JONES, 2001).
3.1.2.4 Catarata Secundária a Doença Sistêmica
Diabetes Melito é uma causa comum de catarata e a maioria dos medicamentos
para diabetes, causa alterações na lente. A catarata é bilateral, rapidamente progressiva e
envolve a lente inteira, devido ao desvio irreversível nos trajetos metabólicos (PEIFFER
JR.; PETERSEN- JONES, 2001; BIRCHARD; SHERDING, 2003). Um achado típico
na catarata por diabetes é uma notável linha lenticular ampla e clara (PEIFFER JR.;
PETERSEN- JONES, 2001).
Provavelmente todos os cães diabéticos vão desenvolver catarata se
acompanhados por um ano ou mais. O desenvolvimento das mudanças da catarata pode
estar associada com alterações de certos fatores osmóticos (GELATT, 1991).
Todos os pacientes que possivelmente tenham catarata são avaliados por uma
elevação da glicose lacrimal com tiras reativas para urina prévia a instilação de
midriáticos e anestésicos tópicos (deve haver resultados falsos negativos, mas não falsos
positivos fortes). Todos os diabéticos clinicamente afetados requerem uma avaliação
completa (hematológica, bioquímica e radiologia torácica) antes de tomar a decisão de
extrair uma catarata (SLATTER, 1992).
Em geral, os paciente diabéticos são bons candidatos cirúrgicos sempre que
exibam um controle insulínico estável durante no mínimo três meses e não apresentem
complicações maiores da diabete, como a cetoacidose e a insuficiência hepática ou
renal. Isto é fundamental porque as drogas dadas antes e durante a cirurgia podem
prejudicar este controle e causar glicosúria, necessitando continuar o uso de insulina em
dose pré-operatória até que o paciente volte a se estabilizar (SLATTER, 1992).
Todo cão de três anos ou mais com catarata que evolui com rapidez, deve ser
questionado sobre Diabete Mellitus (SLATTER, 1992).
A causa da catarata tem sido considerada o aumento da glicose no humor
aquoso. O excesso de glicose é metabolizado pela via aldose redutase, resultando no
aumento de sorbitol. O sorbitol age como um agente osmótico, puxando água para
dentro das células da lente, causando então, inchaço das fibras e perda de transparência
(GELATT, 1991; BIRCHARD- SHERDING, 2003). Excesso de glicose afeta
diretamente também as proteínas da lente, alterando sua estrutura, o que causa uma
luminosidade difusa atravessar a lente (PEIFFER JR.; PETERSEN- JONES, 2001).
No estágio inicial do desenvolvimento da catarata por diabetes, revelam-se
vacúolos subepiteliais corticais no equador. Com rápida progressão, para madura, a
lente com catarata intumescida pode desenvolver fissuras na lente anterior (GELATT,
1991).
3.1.3 Classificação de Acordo com a Localização
A catarata é descrita de acordo com sua localização como nuclear, anterior ou
posterior cortical ou subcapsular, equatorial ou capsular (PEIFFER JR.; PETERSENJONES, 2001).
Pode-se localizar uma catarata focal como anterior ou posterior por meio de
comparação da direção nasal/temporal do movimento da catarata com o olho. Uma
catarata anterior se moverá na mesma direção que o globo ocular; logo, se o animal
olhar temporalmente, uma opacidade anterior mover-se-á temporalmente e uma
posterior mover-se-á nasalmente. Pela localização da catarata, pode-se ajudar a
determinar se ela é hereditária ou prever sua progressão. Por exemplo, uma catarata
nuclear é geralmente estática, enquanto uma catarata equatorial (onde se formam as
fibras lenticulares novas) é geralmente progressiva (BIRCHARD; SHERDING, 2003).
A catarata nuclear geralmente ocorre na forma congênita (PEIFFER JR.; PETERSENJONES, 2001).
O processo da catarata pode ser confinado a uma simples área da lente e sua
cápsula ou pode afetar toda a estrutura da lente GELATT, 1991).
3.1.3.1 Catarata Nuclear
Catarata nuclear ocorre mais freqüentemente na forma congênita e pode ser
hereditária ou associada a uma anormalidade sistêmica na loba quando ela está prenhe.
Esta condição é geralmente bilateral, com mais de um filhote da ninhada afetado.
Devido a sua posição, a catarata usualmente permanece estática ou até regride. Um
significante enfraquecimento visual pode ocorrer se a opacidade for densa. Catarata
nuclear congênita freqüentemente envolve o córtex (GELATT, 1991).
3.1.3.2 Catarata Capsular
A cápsula da lente anterior está sujeita a laceração e lacrimejamento devido a
corpos estranhos e traumas. Quando a cápsula está lacerada, esta tende a se curvar. As
fibras lenticulares subjacentes podem sobrepor a lesão, inchando com fluido, e
resultando em uma catarata focal que aumenta a proporção que mais fibras lenticulares
são envolvidas. O resultado pode ser uma catarata completa ou focal. Lágrimas
capsulares podem ser associadas com iridociclite, aderências focais da íris posterior
(sinéquia posterior), o qual pode fechar o ferimento, resultando em catarata focal. Uma
lesão na lente sem lacrimejamento, pode afetar a semipermeabilidade da cápsula,
resultando no aumento de líquido e formação da catarata (GELATT, 1991).
Depósito de pigmento na cápsula anterior da lente é freqüentemente associado a
trauma externo, manipulação da íris durante cirurgia e inflamação intraocular severa. O
depósito de pigmento não representa formação verdadeira de catarata, porque a lente
pode estar clara, mas clinicamente isto pode afetar a visão, se for extenso (GELATT,
1991).
Uma outra causa de depósito de pigmento na cápsula anterior da lente é
membrana pupilar persistente (GELATT, 1991).
3.1.3.3 Catarata Subcapsular
Imediatamente abaixo da cápsula anterior da lente existe uma exclusiva camada
de células epiteliais se estendendo ao equador da lente.
Estas células podem se
proliferar se houver traumas ou lesões tóxicas, formando uma catarata subcapsular
focal. Este epitélio pode proliferar posteriormente abaixo da cápsula posterior. Algumas
células epiteliais podem se tornar distendidas e vesicular “células bexigas”. Estas
células representam fracassadas tentativas de formação de fibras lenticulares (GELATT,
1991).
O déficit visual com catarata subcapsular anterior depende do seu tamanho e
posição; a catarata central (axial) resulta em uma perda maior do que a em posição
periférica (GELATT, 1991).
Catarata subcapsular posterior ocorre como hereditária em Schnauzer Miniatura
e Beagle. A maioria das cataratas subcapsulares posteriores são axiais; a progressão é
variável. Com envolvimento cortical associado, a progressão será mais rápida. Catarata
subcapsular posterior pode ocorrer com vítreo hiperplásico primário e outros defeitos
congênitos do segmento posterior (GELATT, 1991).
3.1.3.4 Catarata Cortical
A catarata cortical em cães é comum. Em estágio inicial, são usualmente
subdivididos em três áreas de envolvimento: cortical anterior, posterior e equatorial.
Exame através de uma dilatação ampla da pupila pode revelar uma variedade de
mudanças incluindo vacúolos, fissuras por água e opacidades. Vacúolos corticais são
áreas pequenas focais de acúmulo de líquido. Fissuras por água são acúmulo de líquido
que são orientados radialmente no córtex. Opacidades são opacidades corticais em
formato de cunha que são orientados radialmente que aparecem primeiramente na
periferia da lente e então estendendo tanto anterior quanto posteriormente para o núcleo
(GELATT, 1991).
Mudanças corticais são usualmente manifestadas em uma variável progressão da
catarata por alguns meses até anos. Herança de catarata cortical acontece no Golden
Retriver, Poodle Miniatura, e Cocker Spaniel Americano. Nestas raças envolvimento
cortical, juntamente com atrofia retiniana, frequentemente progride rapidamente para
catarata madura. Catarata cortical pode também ocorrer por exposição a agentes tóxicos
como dinitrifeno e diazoxide (GELATT, 1991).
3.1.4 Estágios de Desenvolvimento
3.1.4.1 Incipiente
Opacidades lenticulares focais ou multifocais que não causam perdas de visão
clínica e não prejudicam a reflexo da zona tapetal ou a fundoscopia (BIRCHARD;
SHERDING, 2003; GELATT, 1991). Esta pode ou não progredir (PEIFFER JR.;
PETERSEN- JONES, 2001). Muitas cataratas incipientes são difíceis de ser detectadas
sem midríase máxima, iluminação adequada e aumento (GELATT, 1991). Pode ser
confundida com esclerose nuclear (SLATTER, 1992).
3.1.4.2 Imatura
Catarata imatura representa o segundo estágio de progressão de maturidade. O
tamanho da lente está aumentado significativamente (fica intumescida) por que fica
embebida de líquido. O embebimento de líquido pode ser rápido (dias ou semanas),
resultando em completa opacidade
(GELATT, 1991).
Opacidade lenticular
significativa. A reflexão tapetal permanece, mas ocorre uma visão incompleta do fundo
ocular. Afeta-se a visão, dependendo da extensão do envolvimento lenticular
(BIRCHARD; SHERDING, 2003; GELATT, 1991; PEIFFER JR.; PETERSENJONES, 2001). O fundo de olho pode estar parcialmente escurecido na oftalmoscopia
(SLATTER, 1992).
3.1.4.3 Madura
Opacidade lenticular densa, sem reflexão tapetal ou visibilidade de fundo ocular,
resultando em perda total da visão do olho afetado (BIRCHARD; SHERDING, 2003;
GELATT, 1991; PEIFFER JR.; PETERSEN- JONES, 2001). O exame de
oftalmoscopia é impossível e a visão está perdida. Áreas de relativa melhora na
opacidade podem estar presentes. A lente é normalmente de tamanho normal
(GELATT, 1991).
Este é o estágio ideal para extração cirúrgica da catarata, evitando o começo de
uma uveíte facotóxica (SLATTER, 1992).
Figura 1: Catarata madura em olho de cão da raça Schnauzer .
Fonte: Site www.vetweb.com.br, acesso em: dez. 2008
3.1.4.4 Hipermatura
À medida que a proteína lenticular se degenera e liquefaz, o cristalino pode ficar
menor no eixo antero-posterior, resultando em uma cápsula anterior enrugada e uma
cápsula posterior profunda (PEIFFER JR.; PETERSEN- JONES, 2001). Se a liquefação
aumentar, áreas de “clareamento” cortical podem acontecer. O núcleo da lente pode
instalar-se na posição da lente com uma pequena queda de gravidade. Ocasionalmente
durante a liquefação do córtex, uma difusão do material do córtex liquefeito através da
cápsula aparentemente intacta, pode ocorrer (GELATT, 1991). Estas cataratas
hipermaturas são encolhidas, com a borda áspera devido à mínima reabsorção cortical.
A maioria das lentes é difusamente opaca e a visão é ainda ausente. Derrame de proteína
cortical liquefeito da catarata hipermatura resulta em uma iridociclite porque as
proteínas da lente são estranhas ao sistema imune do animal. O olho (ou os dois olhos)
pode simular uma conjuntivite crônica, o cão pode esfregar o olho com a pata
(GELATT, 1991).
3.1.4.5 Reabsorvente
À medida que a proteína se degenera e liquefaz, pode extravasar através da
cápsula. Isso se associa geralmente com catarata hipermatura, mas também pode ocorrer
em catarata imatura e madura. O processo é mais rápido em cães jovens. Um cristalino
reabsorvente possui quantidade variável de córtex liquefeito e claro, com o material
lenticular remanescente assumindo frequentemente uma aparência cintilante. Embora
alguns animais recuperem a visão por meio de reabsorção lenticular significativa, o
processo resulta geralmente em uma uveíte leve a intensa induzida por cristalino, devido
à antigenicidade do extravasamento protéico lenticular (BIRCHARD; SHERDING,
2003).
Segundo Slatter (1992), há uma sexta classificação quanto ao estágio evolutivo
das cataratas denominada intumescente. Esta ocorre quando o cristalino começa a
inchar. Nem todas as cataratas passam por este estágio. Com a tumefação, o olho é
suscetível ao glaucoma de ângulo fechado secundário e derrame das proteínas
lenticulares, que causa uveíte facoanafilática.
4 SINAIS CLÍNICOS E DIAGNÓSTICO
Os proprietários descobrem uma mudança no comportamento devido a uma
menor visão ou cegueira total ou alteração do aspecto do olho, na maioria dos cães com
catarata (SLATTER, 1992). Se a catarata afeta menos de 30% da lente ou se afeta
apenas um dos olhos, geralmente passa desapercebida pelos donos. A maioria dos
proprietários apenas consegue notar um déficit visual de seu animal de estimação
quando a catarata afeta mais de 60% da lente ou se esta for bilateral (KLEINER, 2008).
Por exemplo, uma aparência branca que piora a noite quando há midríase. Com bastante
freqüência, mantem-se certo grau de visão até os estágios maduros avançados das
cataratas bilaterais. Com exceção das cataratas traumáticas e secundárias, no outro olho
também acontece o mesmo problema (SLATTER, 1992).
Os clientes só perguntam em quanto tempo a catarata será madura no olho
oposto e aparecerá a cegueira total. Sem considerar as cataratas diabéticas, que podem
progredir com rapidez para a fase madura (em duas a quatro semanas), é difícil
responder a estas perguntas. Também é importante perguntar ao proprietário por
antecedentes de escassa visão noturna durante o desenvolvimento da catarata. Um
antecedente de pouca visão diurna se apresenta nas cataratas axiais; a pupila fica
miótica na claridade, restringindo a entrada de luz através da pupila pequena até a área
opaca do cristalino (SLATTER, 1992).
A catarata é mais facilmente diagnosticada pela retroiluminação através da
pupila dilatada. A opacidade da lente vai aparecer como uma área escura e mais ou
menos opaca contrastando com o brilho do reflexo do fundo do olho. Para um exame
mais profundo dos danos à lente, usa-se um microscópio com lâmpada de fenda
(PEIFFER JR.; PETERSEN- JONES, 2001).
O grau de prejuízo visual depende da extensão do desenvolvimento da catarata
em um ou ambos os olhos. Além disso, deve-se considerar o propósito da raça do
animal. Cataratas incipientes e imaturas são mais significativas em cães de caça e de
trabalho, com relação ao prejuízo visual (BIRCHARD; SHERDING, 2003).
5
TRATAMENTO
Nenhum tratamento medicamentoso é efetivo (PEIFFER JR.; PETERSENJONES, 2001).
Antigamente, devido aos riscos associados com a cirurgia de catarata, ao custo
para o proprietário e à capacidade de um cão cego se adaptar ao seu ambiente, a cirurgia
era considerada um procedimento eletivo reservado para animais com catarata madura
bilateral (BIRCHARD; SHERDING, 2003).
Extração da catarata intracapsular em cães foi descrita em 1936 e mais tarde em
1941, como melhor método de remoção cirúrgica. Em 1953, Magrane descreveu a
aspiração de catarata canina e no ano seguinte defendeu a técnica de cirurgia de catarata
canina. Knight, em 1957, apresentou bons e justos resultados de 29% dos 106 casos de
extração da catarata em cães. Três anos depois. Knight apresentou 34% de taxa de
sucesso em 233 casos de cirurgia de catarata (GELATT, 1991).
Em 1961, Magrane apresentou, de uma série de 104 extrações de catarata em
cães, 76% de taxa de sucesso alcançados naqueles cães depois da cirurgia para catarata
juvenil; uma taxa de 37% de sucesso foi alcançada com cataratas senis. A diferença
entre estes dois grupos acreditou-se que tenha sido associado com alterações
concomitantes não detectadas degenerativas, inflamações intra-oculares exageradas e
complicações pós-operatórias (GELATT, 1991).
Um grande estudo sobre cirurgia de catarata por Magrane (429 casos) em 1969
revelou uma taxa de sucesso de 80%. Acredita-se que esta alta taxa de sucesso estava
associada à melhora no procedimento de extração extracapsular e administração pré e
pós cirúrgica de corticóides. Uma taxa de sucesso de 79% foi descrita em 240 extrações
de catarata extracapsular; alguns parâmetros influenciaram neste resultado. Quanto
maior for a experiência em cirurgia do veterinário oftalmologista, maior será a taxa de
sucesso das cirurgias. O sucesso da cirurgia foi 15% mais alta nas cirurgias de extração
de catarata congênita e juvenil do que nas por diabetes e senil (GELATT, 1991).
Gelatt descreveu que em 1991, uma série de extrações de catarata
extracapsulares, 113 unilaterais e 77 bilaterias, foram alcançadas melhora ou
restauração da visão em 79,6% dos olhos dos cães com extração unilateral e 85,7% dos
olhos dos cães com extração bilateral na quarta a sexta semana de pós-operatório. O
sucesso após três a nove meses foi de 68,9 % (extração unilateral) e 69,4% (extração
bilateral). Em cães com extração bilateral de catarata, 93,5% exibiu restauração ou
melhora da visão com sucesso na cirurgia em um ou dois olhos.
A taxa de sucesso da extração da lente extracapsular varia, dependendo do tipo
de catarata, da habilidade do cirurgião, o método usado, e a cooperação do paciente; em
geral, em mãos experientes, uma taxa alta de sucesso pode ser prevista (PEIFFER JR.;
PETERSEN- JONES, 2001).
Em 2003 Bichard e Sherding descreveram que a taxa de êxito com a
facoemulsificação era de 90-95%, com um declínio pequeno com o tempo, enquanto a
taxa de êxito da técnica de extração extracapsular a céu aberto é de aproximadamente
50%, com um declínio uniforme com o tempo após a cirurgia para menos de 30%.
Recentemente, melhora na taxa de sucesso da facoemulsificação, a
disponibilidade de implantes lenticulares intra-oculares e o aumento do êxito associado
com uma intervenção cirúrgica precoce, resultou na cirurgia de catarata sendo oferecida
em casos de catarata unilateral e imatura. A cirurgia é indicada em qualquer fase de
desenvolvimento das opacidades, sendo que as cataratas incipientes e maduras tem um
resultado muito melhor devido a rapidez da emulsificação (núcleos moles) e pouca
presença de opacidades capsulares posteriores extensas possibilitando um implante de
uma lente artificial (KLEINER, 2007b).
Os proprietários devem ficar cientes de que a não remoção de catarata poderá
resultar na sua progressão, uveíte induzida por cristalino (UIC) secundária e
complicações associadas como glaucoma e até mesmo perda do globo ocular
(BIRCHARD; SHERDING, 2003).
Tratamento cirúrgico através da facoemulsificação seguida do implante de lente
intra-ocular devolve o estado de emetropia nos animais. A condição geral do paciente
assim como sua saúde e comportamento devem ser considerados. Cirurgia de catarata
deve ser deixada para o veterinário especialista em oftalmologia e com experiência em
micro cirurgia (PEIFFER JR.; PETERSEN-JONES, 2001).
5.1 MEDICAMENTOS PRÉ- OPERATÓRIOS
O tratamento medicamentoso pré e pós-operatório de catarata é essencial para
todo o sucesso da cirurgia. As duas áreas difíceis do manejo medicamentoso no cão, são
obter uma dilatação razoável da pupila durante e depois da cirurgia e controlar a
inflamação da úvea anterior no pós-cirúrgico. Um grande número de falhas na cirurgia
de catarata são associadas com problemas em uma das duas áreas (GELATT, 1991).
Midríase é obrigatório para o sucesso da cirurgia de catarata. Sulfato de atropina
(1%) é freqüentemente administrado topicamente três a quatro vezes no dia um a dois
dias antes da cirurgia. No cão normal, sulfato de atropina (1%) fornece o máximo de
dilatação da pupila e 1 hora com 96 a 120 minutos de duração da ação. Entretanto, com
uveíte anterior a duração da midríase da atropina tópica é significativamente reduzida, e
a droga deve ser administrada até surtir efeito. A midríase é muito mais difícil de manter
durante a cirurgia intra-ocular. A liberação de prostaglandinas pode ser um fator
significante na miose da pupila canina durante e durante a cirurgia. Por isso o uso de
anti-prostaglandina tópico e sistêmico pode ser válido na manutenção da pupila dilatada
(GELATT, 1991).
O uso de corticosteróides 24 horas antes da cirurgia (predinisona 2 mg/ Kg) é
rotineiro. O uso de corticosteróides parece reduzir significativamente a inflamação pósoperatória (GELATT, 1991).
Antibióticos tópicos podem ser instilados um a três dias antes da cirurgia.
Infecções intra-oculares seguidos da cirurgia da catarata são raras em cães (GELATT,
1991).
5.2 MEDICAMENTOS PÓS- OPERATÓRIOS
A terapia medicamentosa pós-operatória da cirurgia de catarata canina é
extremamente importante e não pode ser enfatizada. Uma uveíte anterior pós-operatória,
frequentemente intensa, pode ser desenvolvida mesmo na extração não complicada da
catarata. Diversos fatores críticos a serem avaliados diariamente são a proteção do olho,
controle de infecções e minimização da inflamação. O paciente deve ser monitorado de
perto logo depois da cirurgia para se evitar uma auto-mutilação; o cão pode danificar de
outra forma o procedimento cirúrgico de sucesso. Se necessário, um colar elizabetano
pode ser utilizado para prevenir traumatismos oculares. Bandagem em volta do olho
pode proteger o globo, apesar destes métodos serem algumas vezes limitados. Pacientes
ativos e intratáveis podem necessitar de tranquilização para proteger e medicar o olho
(GELATT, 1991).
Antibióticos são habitualmente administrados topicamente em seguida da
cirurgia. A escolha do antibiótico é variável mas deve ser de amplo espectro. A
incidência de infecções após a cirurgia intra-ocular em cães é muito baixa (GELATT,
1991).
A inflamação intra-ocular manifestada com uveíte anterior, ocorre em
intensidade variável em todos os cães durante o pós-cirúrgico. O vigor da terapia
necessária para controlar a uveíte varia muito de caso para caso e é ajustado de acordo
com o necessário. Midriáticos, corticóides e anti-prostaglandinas são usados no controle
da uveíte anterior pós-operatória (GELATT, 1991).
A administração de midriáticos, iniciados antes da cirurgia é continuada e é
frequentemente intensificada no pós-operatório. Sulfato de atropina (1 a 2%) e
hidróxido de fenilefrina 10% são administrados topicamente a cada 4 a 12 horas para
manter a midríase. A frequência da medicação é aumentada se a inflamação intensificar
(GELATT, 1991).
Anti-prostaglandinas tópica e sistêmica são usadas com aumento da frequência
para controlar a inflamação da uveíte anterior. Elas podem ser mais efetivas no pré-
operatório e nos primeiros dias do pós-operatório. Corticóides são rotineiramente
administrados antes e depois da cirurgia de catarata. Prednisolona é administrada
sistemicamente em uma dose inicial de 2 mg/kg; a dosagem é reduzida gradualmente
assim que a resposta inflamatória diminui. Corticosteróides podem ser administrados
topicamente, subconjuntivalmente ou as duas formas. Corticosteróides tópicos como o
acetato de prednisolona (0,25 a 1%) ou dexametasona (0,1%), pode ser instilado a cada
4 a 6 horas ou com mais frequência se indicado. O acetato de metilprednisolona e
triancinolona em doses de 5 a 15 mg podem ser usados imediatamente após a cirurgia
para reduzir a inflamação. Esteróides subconjuntivais podem reduzir a freqüência da
aplicação de corticosteróides tópicos e diminuir a dose sistêmica. Este procedimento é
empregado com cautela porque a medicação subconjuntival de longa ação é difícil de
ser removida se ocorrerem complicações pós-operatória como úlcera de córnea e
cicatrização inadequada da ferida. Todos os protocolos de drogas pós-cirúrgicos são
modificados para cada paciente e monitorada diariamente até que a inflamação e a
infecção sejam controladas. As medicações podem ser reduzidas gradualmente após a
primeira semana e paradas após três a seis semanas (GELATT, 1991).
Freqüentes, mas geralmente insignificantes, complicações depois da cirurgia de
catarata são sinéquia posterior focal e fibrose capsular. Glaucoma, descolamento de
retina, edema de córnea, e endoftalmia são complicações críticas que raramente ocorrem
(BIRCHARD; SHERDING, 2003; GELATT, 1991; PEIFFER JR.; PETERSENJONES, 2001).
6 SELEÇÃO DO PACIENTE
As falhas na cirurgia de catarata têm sido associadas a uma pobre seleção dos
pacientes. Exames ocular e psicológico minuciosos devem ser feitos para decisão da
cirurgia de catarata. Os dois olhos devem ser examinados antes e depois de induzir com
fármacos a midríase. Qualquer evidência de atividade de uveíte anterior é indicado
atrasar a cirurgia. Pacientes com uveíte induzida pela lente tem grande incidência de
complicações cirúrgicas e também uma taxa baixa de sucesso na cirurgia (GELATT,
1991).
Exame do fundo do olho deve ser considerado para avaliação do paciente. Em
alguns casos o fundo do olho pode ser observado através de pequenas porções da lente.
Sinais de degeneração da retina podem contra-indicar a remoção da catarata;
eletroretinografia deve ser realizada nesses pacientes (GELATT, 1991).
Exames de sangue devem ser feitos anteriormente a cirurgia e devem incluir
uma completa contagem de células sanguíneas e perfil bioquímico. Diabete Melito é
uma causa não incomum de catarata em cães. Uma vez que a diabete está controlada, a
remoção da lente é possível (GELATT, 1991).
O temperamento do paciente é também uma consideração importante antes da
cirurgia. Se o paciente não pode ser medicado em casa ou no hospital veterinário, a
possibilidade de sucesso da cirurgia é muito diminuída. Diante destas circunstâncias, a
cirurgia não deve ser realizada (GELATT, 1991).
Por isso, o paciente para cirurgia de catarata em potencial deve ser
minuciosamente avaliado antes da cirurgia. O cão deve estar em bom estado geral de
saúde e temperamento, exibindo um déficit visual devido à formação da catarata, e não
ter nenhuma outra doença ocular que comprometa a cirurgia. Otimizando a seleção do
paciente, o cirurgião irá melhorar a porcentagem de sucesso da extração da catarata
(GELATT, 1991).
7 A CIRURGIA PARA REMOÇÃO DA CATARATA
Existem praticamente três técnicas para remover a lente com catarata: extração
da lente intracapsular, extracapsular e facoemulsificação. Na extração intracapsular a
lente é removida por completo, ou seja, as fibras zonulares são rompidas e a lente é
removida com a cápsula. Existe um grande risco de complicação, e o método não é
usado em gatos e cães, exceto nos casos de luxação da lente (GELATT, 1991).
O procedimento é idêntico à técnica extracapsular no que diz respeito à
abordagem cirúrgica e fechamento da ferida. A diferença é o método de remoção da
lente. Na extração intracapsular, a lente com catarata é removida dentro da cápsula da
lente intacta. Se parte da cápsula posterior da lente permanecer, o procedimento se torna
extracapsular (GELATT, 1991).
Na cirurgia extracapsular uma abertura é feita na cápsula anterior (capsuloréxis)
e o núcleo é removido através da incisão corneana, com subseqüente limpeza do saco
capsular irrigando e aspirando o material cortical residual (PEIFFER JR.; PETERSENJONES, 2001). Nesta técnica, a cápsula anterior da lente, o córtex da lente o material do
núcleo são retirados. A cápsula posterior da lente permanece intacta e freqüentemente
anexa à membrana hialóide anterior (GELATT, 1991).
A maior vantagem da técnica extracapsular é que a cápsula posterior da lente
permanece intacta, reduzindo muito a ocorrência de ruptura da membrana hialóide. A
forte junção entre a cápsula anterior da lente a da membrana anterior hialóide no cão, é
perturbada na extração intra-capsular. Esta técnica extrarcapsular também é essencial
para implante de lente intra-ocular, permitindo o alojamento da lente artificial no saco
capsular (GELATT, 1991).
Existem algumas limitações para o procedimento extra-capsular. Com o
dilaceramento da cápsula anterior, o material cortical macio ou liquefeito é liberado no
humor aquoso. Este material, que é antigênico para o corpo, é difícil de ser removido
completamente, e resulta em uma iridociclite pós-operatória pode ser intensa (GELATT,
1991).
Apesar da cápsula posterior intacta reduzir complicações associadas com o
vítreo, isto pode também causar problemas. A própria cápsula posterior pode se tornar
opaca pode perder sua transparência depois da cirurgia. Se a opacidade for de tamanho e
densidade suficientes, a visão pode não ser possível, necessitando também de remoção
da porção central (axial) da cápsula posterior durante a cirurgia ou em uma segunda
cirurgia seguindo a perda da transparência (capsulectomia posterior). A cápsula
posterior da lente pode também desenvolver depósitos de pigmentos da íris, ou sinéquia
posterior e fibrose pos-operatória (GELATT, 1991).
Na facoemulsificação, o material da lente é fragmentado por ultrassom (alta
freqüência de vibração) para emulsificar ou quebrar a lente em pequenos pedaços, e
então este é aspirado (GELATT, 1991; PEIFFER JR.; PETERSEN- JONES, 2001). O
aparelho para facoemulsificação é caro, mas a técnica é vantajosa em termos de
tamanho da incisão e a inflamação pós-operatória é mínima. Tempo excessivo de ultrasom e muita manipulação intra-ocular pode resultar em danos ao endotélio corneal. Por
causa da consistência dura do material nuclear em muitos cães, o procedimento com
ultra-som pode não quebrar adequadamente o material do núcleo, assim exigindo um
aumento da incisão do limbo ou corneal para retirada do núcleo com catarata
(GELATT, 1991).
Figura 2: Emulsificação do núcleo opaco.
Fonte: Site www.vetweb.com.br, acesso em: dez. 2008
Deve-se lembrar que o quanto antes realizada a cirurgia de catarata utilizando-se
tal procedimento maiores são as chances de um resultado favorável e a possibilidade de
implante de uma implante de uma lente intra-ocular, pois as opacificações da cápsula
posterior são mais comuns nas cataratas maduras e quando temos áreas muito extensas
de opacidade o implante de lente fica contra-indicado (KLEINER, 2007a).
8 LENTES INTRAOCULARES
Um animal afácico (sem lentes) é fortemente hipermétrope (visão de longe) e o
uso de lente intra-ocular na cirurgia de catarata tem ganhado aumento na popularidade
por permitir que o cão tenha sua visão normal, recuperando a visão de perto e com
detalhes (PEIFFER JR.; PETERSEN- JONES, 2001).
Figura 3: Visão de um cão após facoemulsificação e sem implante de lente intraocular.
Boa visão de longe e sem detalhes (hipermetropia).
Fonte: Site www.vetweb.com.br, acesso em: dez. 2008
Figura 4: Visão de um cão normal e após o implante de uma lente intraocular. A cor
azul é distinta e o vermelho e verde tentem a se confundir.
Fonte: Site www.vetweb.com.br, acesso em: dez. 2008.
Os implantes de lentes intraoculares (LIOs) foram introduzidos no homem nos
anos 70 para corrigir um erro refratário pós-operatório afácico. Lentes intraoculares têm
sido implantadas em cães por muitos anos; infelizmente descrições dos implantes são
limitados e incompletos. O implante de lente intra-ocular plástica depois da extração da
catarata em cães tem sido descrito antes de 1956 (GELATT, 1991).
A refração do paciente canino pode ser feita com retinoscopia, ultrassonografia
ou autorrefração; primeiramente dois métodos foram descritos em cães. Muitas LIO
estavam disponíveis, sendo que a com 7 a 8 mm de diâmetro, combinado com haptics
com um total de 13 a 14 mm, pareceram caber na “bolsa” (endocapsular) da lente
canina. O poder de restabelecer emetropia da LIO no pós-operatório para os cães pode
ser diferente da do homem, pois a lente do cão é mais larga e com aproximadamente 35
a 40 dioptrias (GELATT, 1991).
Figura 5: Lente Acrílica dobrável de 40D implantada em um cão da raça
Schnauzer.
Fonte: Site www.vetweb.com.br, acesso em: dez. 2008.
A LIO é inserida depois da remoção da catarata inteira
durante a
facoemulsificação. A solução de visco elástico assim como o hialuronato de sódio,
metilcelulose hidroxipropil, são importantes para proteger o endotélio corneal durante a
inserção da LIO. Este material é então aspirado da câmara anterior, pouco antes do
limbo ou da ferida corneal ser completamente fechada e a câmara anterior ser
reconstituída. A solução de visco elástico dentro da câmara pode aumentar a pressão
intra-ocular no cão e deve ser aspirada da câmara anterior antes que a ferida cirúrgica é
fechada (GELATT, 1991).
A lente intraocular, assim como no ser humano, fica muito bem posicionada e
estável no espaço intraocular e não existe a mínima possibilidade de ela se deslocar ou
"cair" com a movimentação da cabeça do paciente no seu dia a dia (KLEINER, 2007b).
9 RELATO DE CASO
No Hospital Veterinário São Bernardo foi atendida uma cadela de nome Bunny,
raça Cocker Spaniel Inglês, com oito anos de idade, apresentando catarata bilateral e em
começo de uveíte facolítica.
O paciente já era totalmente cego, devido à catarata, há mais ou menos quatro
anos.
Esta cadela passou por minucioso exame clínico e oftálmico, antes da realização
da cirurgia de facoemulsificação, seguida do implante de uma lente artificial, e ela
deveria estar livre de dermatopatias, odontopatias, oftalmopatias (ex.: olho seco,
uveítes, ceratites, etc) e qualquer outra patologia que fosse potencialmente causadora de
uma infecção intraocular.
Antes da cirurgia também foi realizado o exame de Eletrorretinografia, o qual se
apresentou normal, comprovando a funcionalidade da retina.
Foram feitos exames pré-operatórios (hemograma e perfil bioquímico) de rotina
e os resultados foram compatíveis com a normalidade.
No dia 06 de setembro de 2008 foi realizada a cirurgia no olho direito para
correção da catarata através da facoemulsificação, seguida de implante de uma lente
intraocular artificial.
Para evitar transtornos pós-cirúrgicos como uma resposta celular exacerbada,
opacidade da cápsula posterior, rejeição da lente pelo organismo ou endoftalmites
severas, foi utilizada uma lente intraocular especial desenvolvida com uma tecnologia
nova de recobrimento da sua superfície com heparina.
10 MATERIAIS E METODOS
Aproximadamente dez dias antes de o procedimento ser realizado, os pacientes
são tratados com de colírios com lágrimas artificiais e associações de antibiótico com
corticóide na freqüência de três vezes ao dia.
Após restrição alimentar de doze horas, dilata-se a pupila dos pacientes através
do emprego de tropicamida e diclofenaco sódico intercalados a cada vinte minutos e
iniciados três horas antes do procedimento.
A anestesia consiste em indução com ketamina (10 mg/kg IV) e diazepam (0,5
mg/kg IV) e manutenção com Isoflurano. Os pacientes são posicionados em decúbito
dorsal com o plano rostral paralelo ao teto. Com a utilização de Lidocaína a 2% sem
vasoconstritor, realiza-se um bloqueio peribulbar em 3, 6, 9 e 12 horas, administrandose aproximadamente 0,8 ml em cada ponto para obtenção de uma boa centralização do
globo ocular. Nos pacientes nos quais se tem uma órbita ocular profunda, administra-se
2 a 3 ml de solução de Ringer com Lactato retrobulbar para obter-se uma melhor
exposição do bulbo ocular e evitar-se a necessidade de uma cantotomia lateral,
diminuindo assim o tempo do procedimento.
Com o auxílio de um anel de fixação ocular tipo “Thornton” para incisão em
córnea clara e utilizando-se um bisturi de safira de 3,2 mm realiza-se uma incisão
corneana em 4 a 5 horas. Após, administra-se 0,5 ml de Azul de tripan na câmara
anterior para coloração da cápsula anterior do cristalino, o que facilita a sua visualização
e consequentemente a capsulorréxis (abertura da cápsula anterior). Passados 2 minutos
de espera para fixação do corante, injeta-se 1 ml de viscoelástico dispersivo de
metilcelulose a 2% na câmara anterior no sentido distal-proximal a incisão principal, de
modo que todo o azul de tripan seja removido e promova-se uma midríase mecânica e
um bom recobrimento do endotélio visando sua proteção. A capsulorréxis é feita com
auxílio de uma pinça de cápsula tipo Masket de forma simétrica e central. Após, realiza-
se a hidrodissecção e hidrodelineação utilizando-se uma cânula de irrigação/aspiração e
solução salina balanceada abaixo da cápsula anterior e no centro do núcleo lenticular.
Realiza-se um sulco central no núcleo do cristalino utilizando-se uma ponteira de faco
de 450 e logo depois de sulcado, o núcleo é fragmentado (fraturado) utilizando-se um
pré-chopper de Akahoshi ou um manipulador de núcleo (chopper) quando utilizada a
técnica de duas mãos. Com a utilização de uma ponteira de 30 0 tipo flared, realiza-se a
emulsificação lenticular final. Nos núcleos mais moles, pode-se utilizar apenas a
ponteira de 30o, dispensando às vezes a utilização do pré-choper. Depois de concluída
esta etapa e removidos todos os fragmentos remanescentes de córtex nuclear utilizandose uma ponteira de irrigação e aspiração, o saco capsular está pronto para receber a lente
dobrável acrílica de 41 D, que somente não é implantada nos casos em que existem
lesões capsulares radiais ou opacidades importantes na cápsula posterior. Foi utilizada a
lente de nome comercial Acri-Lens® VetH neste paciente. Para o implante da lente
utiliza-se um visco elástico coesivo dentro do saco capsular e a lente depois de dobrada
no cartucho próprio é injetada no interior do bag através de um injetor descartável e esta
vai aos poucos se abrindo e por conter quatro pontos de apoio, devido ao seu design
diferenciado, torna-se auto-estática.
Ao final do procedimento todo visco elástico remanescente é aspirado e deve-se
realizar uma boa aspiração da cápsula anterior na região da capsulorréxis, visando evitar
a proliferação celular nesta região, o que poderá originar opacidades futuras. A
corneorrafia é realizada utilizando-se 3 pontos interrompidos simples com um fio 8-0 de
poliglactina 910 e após reconstituído o globo utilizando-se solução salina balanceada,
aplica-se 0,3 ml de dipropionato e fosfato dissódico de betametasona via subconjuntival.
No pós-operatório utiliza-se colar elisabetano durante 12 dias e a a terapia
instituída constitui-se apenas de colírios tópicos que são: lágrima artificial 4 x ao dia por
30 dias; cicloplegia através da atropina 0,5% ou tropicamida BID por 10 dias, colírio de
gatifloxacino (Zymar®) TID durante 15 dias, colírio de prednisolona a 1% BID por 15
dias e colírio de cetorolac de trometamina (Acular ®) BID durante 35 a 40 dias. É
importante que o corticóide tópico seja diminuído gradativamente durante mais 20 dias,
para evitar-se o efeito rebote da retirada abrupta desta droga.
11 DISCUSSÃO
A lente intraocular utilizada, Acri- Lens® VetH, é um dispositivo óptico de
precisão. Esta lente é composta de acrílico hidrofílico com bloqueador UV para
diminuir o risco de danos para a retina pela luz UV natural. Possui também uma
superfície modificada com heparina com a finalidade de diminuir a proliferação celular
na cápsula posterior, o que pode dar origem a opacidades importantes a longo prazo.
Cada lente intraocular está acondicionada em um frasco dentro de uma bolsa
estéril. As lentes são esterilizadas por meio do calor.
Esta lente é indicada para animais afácicos depois da remoção cirúrgica do
cristalino do olho animal.
O uso desta está contra indicado quando há doenças pré-existentes ou
fisiológicas que podem ser agravadas pelo implante ou quando o implante pode
interferir com a possibilidade de exame ou do tratamento de uma doença ocular. Está
contra indicada também em casos de uveítes crônicas ou recorrentes, distrofia endotelial
corneana, complicações severas durante a cirurgia (rupturas graves de cápsula posterior,
instabilidade do saco capsular após a remoção da catarata), perda excessiva do vítreo,
doença ou infecção aguda do globo e anexos oculares ou quando existe hemorragia de
coróide antes ou durante o procedimento cirúrgico.
As complicações são muito raras e são basicamente as mesmas encontradas na
cirurgia para remoção do cristalino e dentre elas podemos citar: descompensação
corneana, edema corneano temporário, Iridociclite, herniação do vítreo para a câmara
anterior, descolamento de retina, endoftalmite, catarata secundária, bloqueio pupilar.
Algumas destas complicações acima listadas podem requerer segunda intervenção
cirúrgica e podem ser resultado do implante de qualquer lente intraocular e não
necessariamente único deste modelo de lente.
A lente deve ser implantada no saco capsular. A capsulorexis deve ser feita
grande o suficiente para permitir a entrada da lente. O cirurgião deve passar por um
treinamento exaustivo para realizar este tipo de cirurgia.
A Acri-Lens® VetH é formada de uma única peça constituída por 26% de
acrílico hidrofílico com superfície heparinizada, possui poder dióptrico de 41 D, 13 mm
de diâmetro total, 6,5 mm de diâmetro óptico, angulação de alça de 5°, índice de
refração 1.46 e design da borda tipo quadrado.
Figura 6: Acri-Lens® VetH.
Fonte: Site www.vetweb.com.br, acesso em: dez. 2008
Figura 7: Figura ilustrativa da lente Acri-Lens® VetH mostrando sua anatomia.
Fonte: Site Veterinary Intraocular Lenses, acesso em: Jan. 2009
A heparina é uma molécula de carboidrato endógeno de invertebrados e
mamíferos. Ela não é reconhecida como uma substância estranha pelo organismo, e não
parece produzir reações imunológicas. Além disso, a modificação da superfície com
heparina foi testada em vários dispositivos implantáveis para fins de redução aderência
bacteriana, diminuindo assim o risco de infecção. Esta superfície heparinizada provoca
uma forte ligação molecular entre a heparina e os polímeros da superfície da lente.
Tem-se demonstrado que a heparina tensoativa modificada reduz a resposta
inflamatória no período pós-operatório imediato.
As lentes intraoculares com esta tecnologia originam uma menor resposta celular
observada um ano após a cirurgia de catarata. Também observa-se uma menor reação
tipo corpo estranho, especialmente no período de pós-operatório imediato.
Os pacientes que são diabéticos ou têm glaucoma também podem utilizar a lente
com esta tecnologia.
No caso da cadela Bunny o implante da lente Acri-Lens® VetH foi muito bem
sucedido, não tendo nenhuma complicação pós-operatória e nem tanto durante a
cirurgia. O resultado a longo prazo foi muito satisfatório e como proposto pelo
fabricante da lente intraocular utilizada, não houve crescimento bacteriano ou de células
na superfície da lente.
Figura 8: Pré-operatório da cirurgia (pupila dilatada). Reparar a opacidade do cristalino com
catarata.
Fonte: Site www.vetweb.com.br, acesso em: dez. 2008
Figura 9: Lente intra- ocular acrílica sendo implantada.
Fonte: Site www.vetweb.com.br, acesso em: dez. 2008
Figura10: Imagem imediatamente após implante da lente Acri-Lens® VetH.
Fonte: Site www.vetweb.com.br, acesso em: dez. 2008
O eixo visual encontrava-se totalmente limpo e sem a presença de opacidades
importantes. Existia uma retração capsular periférica que não interferia no
posicionamento ou estabilidade da lente artificial implantada.
As opacidades na região equatorial também eram discretas e iguais às notadas
em qualquer outro tipo de lente artificial utilizada.
Não existia qualquer tipo de reação inflamatória, desconforto ocular ou alteração
do posicionamento da lente utilizada. A pupila apresentava-se simétrica e movimentavase normalmente com a variação da intensidade de luz.
O paciente encontrava-se com uma acuidade visual muito grande e até mesmo
brincando de pegar bolinha com muita perícia, segundo informações do proprietário.
A cadela Bunny retornou depois de seis meses (31 de Janeiro) para a cirurgia no
olho contra-lateral (esquerdo), mas, por motivos financeiros, optaram por não implantar
uma lente artificial desta vez.
13 CONCLUSÃO
Hoje a cirurgia de catarata é muito bem aceita por causa da evolução tecnológica
que trouxe grande melhoria na taxa de sucesso da cirurgia para correção da catarata com
facoemulsificador, a disponibilidade de implantes lenticulares intra-oculares e o
aumento do êxito associado com uma intervenção cirúrgica precoce.
Hoje a sobrevida dos animais de estimação aumentou muito, bem como os
cuidados e exigências de seus proprietários e isto favoreceu o crescimento e aumentou a
procura da cirurgia corretiva da catarata.
Os profissionais da área estão mais treinados e atualizados, proporcionando,
junto com o surgimento de técnicas novas, melhores resultados pós-cirúrgicos.
O uso de lentes intra-oculares com alta tecnologia trouxe a possibilidade do cão,
que passou por esta cirurgia, ter uma excelente acuidade visual e levar uma vida normal,
podendo brincar, correr e nadar sem problema nenhum.
Ao longo deste trabalho, pode-se concluir que todos estes eventos citados são
importantes para ter melhores resultados cirúrgicos e clientes mais satisfeitos com a
cirurgia de catarata em seus cães. O surgimento de novas tecnologias para garantir
melhores resultados da cirurgia com facoemulsificador tem se intensificado nos últimos
anos.
Analisando o caso relatado da Bunny, colocamos em teste e aprovamos a lente
utilizada. Esta proporcionou um resultado a longo prazo muito bom, pois não houve
crescimento bacteriano ou de células na superfície da lente. Se o crescimento tivesse
ocorrido, haveria opacidade da lente que acarretaria déficit visual.
O que proporcionou este resultado foi a superfície heparinizada da lente. Além
de diminuir o implante de células na superfície da lente, esta tecnologia fez com que não
houvesse reação inflamatória exacerbada por não ser reconhecida como estranha ao
organismo da cadela.
Este tipo de lente proporcionou, também, boa estabilidade dentro do saco
capsular por conter quatro pontos de apoio devido ao seu design diferenciado, tornandose auto-estática. Esta estabilidade foi comprovada depois de seis meses e vai
permanecer por toda a vida deste cão.
Este foi o primeiro caso relatado de implante de uma lente artificial intra-ocular
com superfície heparinizada em cães, realizado em Curitiba.
Pode-se concluir com isso que os benefícios do uso da lente com superfície
heparinizada foram válidos e a cirurgia teve sucesso total. O paciente encontrava-se
com uma acuidade visual muito grande e apresentava uma vida normal, correndo e
brincando de bolinha com o seu dono.
REFERÊNCIAS
BIRCHARD, S.J.; SHERDING, R. G., Manual Saunders Clínica de Pequenos
Animais. 3 ed., São Paulo: W.B.Saunders Company, 2003; p. 1473- 1476
CARNEIRO FILHO, L. SOVE Serviço de Oftalmologia Veterinária. Seção Cirurgia de
Catarata
em
Cães
e
Gatos.
Disponível
em:
www.
Compuland.com.br/
oftalvet/index.html. Acesso em: out. 2008.
GELATT, K.N.. Veterinary Ophthalmology, 2ª ed., São Paulo: Manole, 1991. p. 432454.
KLEINER, J.A., O Uso de Lentes Intra-oculares Acrílicas Dobráveis após Cirurgia
de Facoemulsificador em Cães. Revista CRMV PR Nº25/ Ano V/ Dez/2007a.p. 22-23.
KLEINER, J.A., Implante de Lente Intra-ocular dobrável após cirurgia de
Facoemulsificação. Anais do XXVIII Congresso Brasileiro da Anclivepa, realizado em
Florianópolis – SC, no Centro de Convenções Centro-Sul, no período de 24 a 27 de
maio de 2007b.
KLEINER, J.A, Cirurgia de Catarata com facoemulsificação seguida de implante de
lente
dobrável.
Disponível
em
http://www.vetweb.com.br/vetweb/index.php?option=com_weblinks&catid=28&Itemid
=42 Acesso em: dez. 2008.
KLEINER,
J.A.
História
da
Cirurgia
da
Catarata:
Disponível
http://www.fmrp.usp.br/revista/2006/vol39n4/revisao_historia_cirurgia_catarata.pdf
Acesso em: Jan. 2009
em
PEIFFER JR.; PETERSEN- JONES., Visual Impairment, In: Small Animal
Ophthalmology, 3ª ed., Malaysia, W.B. Saunders, 2001, p. 153- 159.
SLATTER, D. H., Cristalino. In: Slatter, D.H.: Fundamentos de Oftalmologia
Veterinária, 2ª ed. Buenos Aires: Inter-Médica, 1992, p. 429-453.
Veterinary
Intraocular
Lenses:
Disponível
http://www.imedpharma.com/vet_iols.php Acesso em: Jan. 2009
em