EQUILÍBRIO QUÍMICO
REAÇÃO REVERSÍVEL
Reação reversível é aquela
simultaneamente nos dois sentidos.
1
A+B
que
ocorre
C+D
2
com que, ao ser atingido o equilíbrio, as concentrações
molares das substâncias participantes permaneçam
constantes; cada transformação de moléculas reagentes
em produtos é compensada por uma transformação de
moléculas produtos em reagentes.
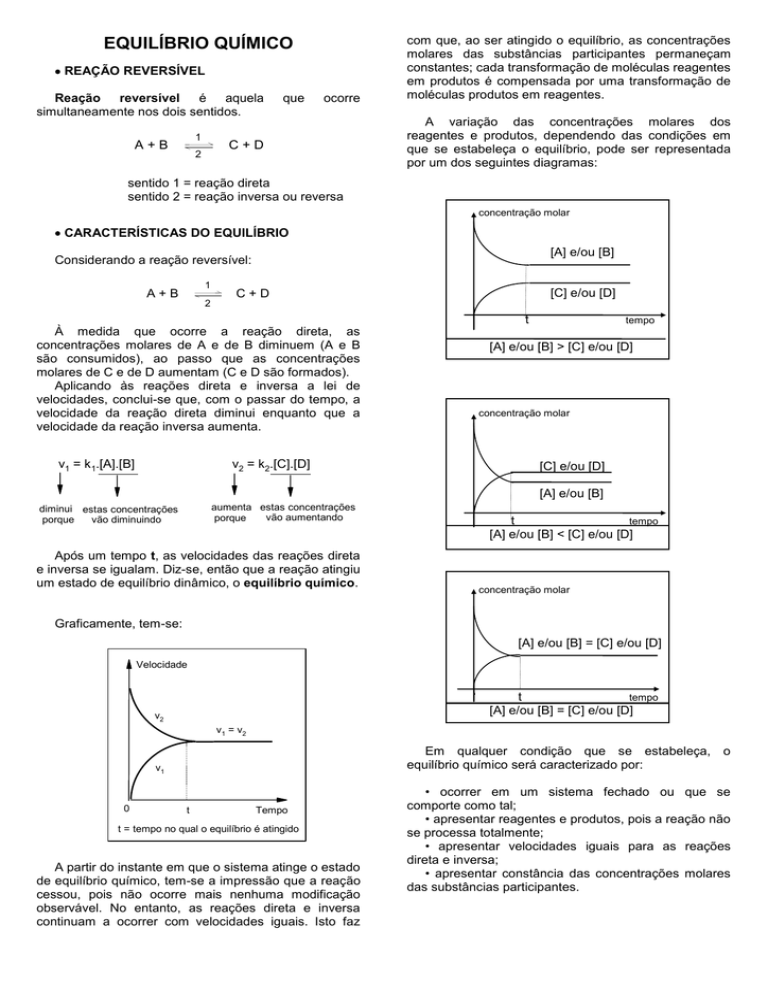
A variação das concentrações molares dos
reagentes e produtos, dependendo das condições em
que se estabeleça o equilíbrio, pode ser representada
por um dos seguintes diagramas:
sentido 1 = reação direta
sentido 2 = reação inversa ou reversa
concentração molar
CARACTERÍSTICAS DO EQUILÍBRIO
[A] e/ou [B]
Considerando a reação reversível:
1
A+B
[C] e/ou [D]
C+D
2
t
À medida que ocorre a reação direta, as
concentrações molares de A e de B diminuem (A e B
são consumidos), ao passo que as concentrações
molares de C e de D aumentam (C e D são formados).
Aplicando às reações direta e inversa a lei de
velocidades, conclui-se que, com o passar do tempo, a
velocidade da reação direta diminui enquanto que a
velocidade da reação inversa aumenta.
v1 = k1.[A].[B]
v2 = k2.[C].[D]
tempo
[A] e/ou [B] > [C] e/ou [D]
concentração molar
[C] e/ou [D]
[A] e/ou [B]
aumenta estas concentrações
vão aumentando
porque
diminui estas concentrações
porque
vão diminuindo
Após um tempo t, as velocidades das reações direta
e inversa se igualam. Diz-se, então que a reação atingiu
um estado de equilíbrio dinâmico, o equilíbrio químico.
t
tempo
[A] e/ou [B] < [C] e/ou [D]
concentração molar
Graficamente, tem-se:
[A] e/ou [B] = [C] e/ou [D]
Velocidade
t
tempo
[A] e/ou [B] = [C] e/ou [D]
v2
v1 = v2
Em qualquer condição que se estabeleça, o
equilíbrio químico será caracterizado por:
v1
0
t
Tempo
t = tempo no qual o equilíbrio é atingido
A partir do instante em que o sistema atinge o estado
de equilíbrio químico, tem-se a impressão que a reação
cessou, pois não ocorre mais nenhuma modificação
observável. No entanto, as reações direta e inversa
continuam a ocorrer com velocidades iguais. Isto faz
• ocorrer em um sistema fechado ou que se
comporte como tal;
• apresentar reagentes e produtos, pois a reação não
se processa totalmente;
• apresentar velocidades iguais para as reações
direta e inversa;
• apresentar constância das concentrações molares
das substâncias participantes.
CONSTANTES DE EQUILÍBRIO
1
x A(g) + y B(g)
Qualquer equilíbrio químico é caracterizado por uma
constante de equilíbrio, a qual é obtida através da lei do
equilíbrio que diz:
"O produto das concentrações molares dos produtos
da reação dividido pelo produto das concentrações
molares dos reagentes, estando cada concentração
elevada a um expoente igual ao seu coeficiente na
equação química considerada, é constante."
Esta constante de equilíbrio é representada por Kc e
é denominada de constante de equilíbrio em função
das concentrações molares.
tem-se:
Kp
pCw .pDt
pA x .pBy
onde p corresponde à pressão parcial do gás
considerado, após atingido o equilíbrio.
Exemplos:
N2(g) + 3 H2(g)
Considerando a reação reversível:
w C(g) + t D(g)
2
2 NH3(g)
(pNH3)2
Kp =
(pN2) . (pH2)3
1
x A(g) + y B(g)
2
w C(g) + t D(g)
2 SO3(g)
2 SO2(g) + O2(g)
Kp =
(pSO2)2 . (pO2)
(pSO3)2
pela aplicação da lei do equilíbrio, obtém-se:
Kc
Cw .Dt
Ax .By
Atenção !
A constante de equilíbrio é característica de cada
reação química e seu valor depende somente da
temperatura.
Para qualquer reação tem-se que, quanto maior o
valor de Kc, maior será o rendimento ou a extensão da
reação, isto é, a concentração dos produtos presentes
no sistema será maior que a concentração dos
reagentes. Caso contrário, quanto menor o valor de Kc,
menor o rendimento ou a extensão da reação, ou seja,
haverá maior concentração dos reagentes em relação à
de produtos.
• Nos equilíbrios em que existirem participantes sólidos, estes não devem ser
representados na expressão da constante
de
equilíbrio
em
função
das
concentrações molares (Kc), pois suas
concentrações são sempre constantes.
• Na expressão de Kp só devem ser
representados os componentes gasosos.
Observe as expressões de Kc e Kp para os
equilíbrios a seguir:
Exemplos:
N2(g) + 3 H2(g)
2 SO3(g)
2 CO(g) + O2(g) ⇄ 2 CO2(g)
2 NH3(g)
2 SO2(g) + O2(g)
Kc =
[NH3]2
[N2] . [H2]3
Kc =
[CO 2 ] 2
Kp
[CO] 2 . [O 2 ]
(pCO 2 ) 2
(pCO) 2 . (pO 2 )
[SO2]2 . [O2]
C(s) + O2(g) ⇄ CO2(g)
[SO3]2
• Constante de equilíbrio em função das pressões
parciais (Kp)
Quando um equilíbrio envolver gases, a constante de
equilíbrio poderá ser determinada através das pressões
parciais desses gases. Neste caso, a constante de
equilíbrio é representada por Kp e é denominada de
constante de equilíbrio em função das pressões
parciais.
A expressão da constante de equilíbrio em função
das pressões parciais (Kp) é obtida da mesma maneira
que o foi a constante de equilíbrio em função das
concentrações (Kc).
Assim, para o equilíbrio:
Kc
Kc
[CO 2 ]
[O 2 ]
Kp
(pCO 2 )
(pO 2 )
Zn(s) + 2 HCl(aq) ⇄ ZnCl2(aq) + H2(g)
Kc
[ZnCl 2 ] . [H 2 }
[HCl]
2
• Relação entre Kc e Kp
Para o equilíbrio:
Kp (pH 2 )
1
x A(g) + y B(g)
2
w C(g) + t D(g)
Kp = Kc . (RT)n
tem-se:
α
nreagem
ninicial
6,5
0,65 ou 65%
10
onde
CÁLCULOS DE EQUILÍBRIO
Kp = constante de equilíbrio em função das pressões
parciais;
Kc = constante de equilíbrio em função das
concentrações molares;
R = constante universal dos gases perfeitos;
T = temperatura Kelvin do equilíbrio;
n = variação do n.º de mols = (w + t) (x + y)
Exemplo 1:
No sistema em equilíbrio N2(g) + 3 H2(g) ⇌ 2 NH3(g),
as pressões parciais de cada gás são: pN2 = 0,4 atm;
pH2 = 1,0 atm e pNH3 = 0,2 atm. Calcular as constantes
Kp e Kc para esse equilíbrio, a 27°C. (Dado: R = 0,082
atm.L/K.mol)
Resolução:
Exemplos:
H2(g) + I2(g) ⇄ 2 HI(g)
n = 2 - (1 + 1) = 0
0
n = 0 Kp = Kc.(RT) Kp = Kc
• Cálculo de Kp:
Sendo fornecidas as pressões parciais dos gases
no equilíbrio, efetua-se o cálculo aplicando a lei do
equilíbrio.
N2(g) + 3 H2(g) ⇄ 2 NH3(g)
Kp
n = 2 - (1 + 3) = -2
-2
n = -2 Kp = Kc.(RT)
pNH 3 2
pN2 . pH2 3
0,2 2
0,4 . 1,0 3
0,1
• Cálculo de Kc:
2 SO3(g) ⇄ 2 SO2(g) + O2(g)
∆n = 2 – (1 + 3) = -2
n = (2 + 1) - 2 = 1
1
n = 1 Kp = Kc.(RT)
∆n
Kp = Kc . (RT)
0,1 = Kc . (0,082 . 300)
-2
Kc = 60,5
GRAU DE EQUILÍBRIO ()
Grau de equilíbrio () de uma reação, em relação a
um determinado reagente, é o quociente entre o número
de mols desse reagente que realmente reagiu até o
equilíbrio e o número de mols inicial desse mesmo
reagente.
n.º mols que reagiram até o equilíbrio
n.º mols inicial
Exemplo:
Exemplo 2:
2 mols de H2 e 1,5 mol de I2 foram colocados num
balão de 10 litros.
Estabelecido o equilíbrio H2(g) + I2(g) ⇌ 2 HI(g),
encontrou-se no balão 2 mols de HI. Calcular a
constante de equilíbrio Kc do sistema.
Resolução:
Transformando os números de mol fornecidos em
concentrações molares, tem-se:
• Cálculo das concentrações molares.
No interior de um reator previamente evacuado,
colocou-se 10 mols de SO3(g).
Após o estabelecimento do equilíbrio:
2 SO3(g) ⇄ 2 SO2(g) + O2(g)
observou-se que existiam 3,5 mols de SO3(g) em
equilíbrio com SO2(g) e O2(g).
Calcule o grau de equilíbrio () da reação.
Resolução:
• N.º mols de SO3(g) que reagem até o equilíbrio:
n reagem = n inicial - n equilíbrio = 10 - 3,5 = 6,5
• Grau de equilíbrio ():
Concentração molar inicial do H2:
♏=
2 mol
n
= 0,2 mol/L
V 10 litros
Concentração molar inicial do I2:
♏=
n 1,5 mol
= 0,15 mol/L
V 10 litros
Concentração molar, no equilíbrio do HI:
♏=
2 mol
n
= 0,2 mol/L
V 10 litros
• Cálculo da constante de equilíbrio Kc.
Com base nos dados, se constrói uma tabela que irá
auxiliar na dedução das concentrações molares, no
equilíbrio, de todas as espécies participantes.
H2
Início
+
0,2
I2
⇄
2 HI
0,15
O enunciado da questão diz que 40% de PCℓ5 se
dissocia (é consumido). Isto corresponde a 0,4 mol/L.
Portanto, na linha reação,coloca-se esse valor e,
observando a proporção dada pelos coeficientes da
equação (1:1:1), se deduz as concentrações de PCℓ 3 e
de Cℓ2 que se formam até o equilíbrio ser atingido.
PCℓ5
0
Início
reação
equilíbrio
0,2
Se, no início, a concentração do HI era nula e no
equilíbrio há 0,2 mol/L, conclui-se que esta substância
foi formada na reação. Observando a proporção dada
pelos coeficientes da equação (1:1:2), para formar 0,2
mol/L de HI houve o consumo de 0,1 mol/L de H2 e 0,1
mol/L de I2.
Colocando estas concentrações na linha reação, temse:
H2
Início
reação
equilíbrio
+
I2
⇄
equilíbrio
PCℓ3
+
Cℓ2
1
0
0
−0,4
+0,4
+0,4
0,6
0,4
0,4
Na linha do equilíbrio estão as concentrações molares
necessárias para o cálculo de Kc.
Substituindo estes valores na expressão matemática de
Kc, tem-se:
Kc
[PC 3 ].[C 2 ] 0,4.0,4
0,27
[PC 5 ]
0,6
2 HI
0,2
0,15
0
−0,1
−0,1
+0,2
0,1
0,05
0,2
Na linha do equilíbrio estão as concentrações molares
necessárias para o cálculo de Kc.
Substituindo estes valores na expressão matemática de
Kc, tem-se:
Kc
reação
⇄
[HI] 2
(0,2) 2
8
[H 2 ].[I 2 ] (0,1).(0,0 5)
DESLOCAMENTO DO EQUILÍBRIO QUÍMICO
O estado de equilíbrio de uma reação pode sofrer
modificações em função dos fatores de equilíbrio a que
está submetido o sistema. Os fatores que provocam
essa alteração são a concentração dos participantes,
a pressão e a temperatura.
O efeito provocado pela alteração de qualquer um
dos fatores de equilíbrio é regido pelo Princípio de Le
Chatelier, que estabelece:
“Quando se exerce uma ação num
sistema em equilíbrio, este se desloca
no sentido da reação que neutraliza
essa ação”.
Exemplo 3:
Aqueceram-se dois mols de pentacloreto de fósforo
num recipiente fechado com capacidade de 2 litros.
Atingido o equilíbrio, o pentacloreto de fósforo se
encontra 40% dissociado em tricloreto de fósforo e
cloro. Calcular a constante de equilíbrio Kc do sistema.
Baseado neste princípio é possível prever os efeitos
de ações impostas a um sistema em equilíbrio.
• Influência da concentração dos participantes
Regra geral:
Resolução:
• Cálculo da concentração molar inicial do PCℓ5.
♏=
adição de uma
substância
2 mol
n
= 1 mol/L
V 2 litros
Com base nos dados, se constrói uma tabela que irá
auxiliar na dedução das concentrações molares, no
equilíbrio, de todas as espécies participantes.
PCℓ5
Início
1
⇄
PCℓ3
+
0
reação
equilíbrio
No início, as concentrações de são nulas.
Cℓ2
0
retirada de uma
substância
desloca o equilíbrio
no sentido que irá
consumi-la
(lado oposto)
desloca o equilíbrio
no sentido que irá
refazê-la
(mesmo lado)
Supondo a reação em equilíbrio:
N2(g) + 3 H2(g)
2 NH3(g)
A adição de uma certa quantidade de N2(g) ao reator
que contém o equilíbrio, aumentará a concentração
desta substância e isto provocará um deslocamento
deste equilíbrio para a direita (lado oposto daquele onde
se encontra o N2(g), ou seja, no sentido da reação que
consome o N2(g)).
1 H2(g) + 1 I2(g)
2 volumes
2 volumes
N2(g) + 3 H2(g)
2 HI(g)
2 NH3(g)
não ocorre variação de volume. Neste caso, a pressão
não afetará o estado de equilíbrio da reação.
A retirada de uma certa quantidade de N2(g) do reator
que contém o equilíbrio, diminuirá a concentração desta
substância e isto provocará um deslocamento deste
equilíbrio para a esquerda (mesmo lado em que se
encontra o N2(g), ou seja, no sentido da reação que refaz
o N2(g)).
N2(g) + 3 H2(g)
2 NH3(g)
• Influência da temperatura
Regra geral:
aumento da
temperatura
desloca o equilíbrio no
sentido endotérmico
diminuição da
temperatura
desloca o equilíbrio no
sentido exotérmico
• Influência da pressão
Regra geral:
Supondo a reação em equilíbrio:
aumento
da
pressão
desloca o equilíbrio
no sentido de
menor volume
diminuição
da
pressão
desloca o equilíbrio
no sentido de
maior volume
N2(g) + 3 H2(g)
2 NH3(g) H = -92 kJ
A H que acompanha a equação está associada à
reação direta.
Portanto, a reação direta é exotérmica e a inversa é
endotérmica.
N2(g) + 3 H2(g)
exot.
endot.
2 NH3(g)
Supondo a reação em equilíbrio:
1 N2(g) + 3 H2(g)
2 NH3(g)
1 volume
2 volumes
3 volumes
4 volumes
Se a pressão sobre este equilíbrio for aumentada,
ocorrerá deslocamento para a direita (sentido de menor
volume).
2 NH3(g)
Se a pressão sobre este equilíbrio for diminuída,
ocorrerá deslocamento para a esquerda (sentido de
maior volume).
N2(g) + 3 H2(g)
2 NH3(g)
Observação:
Quando o volume total do sistema permanecer
constante, a variação da pressão não afetará o estado
de equilíbrio desse sistema.
No equilíbrio:
N2(g) + 3 H2(g)
2 NH3(g)
2 volumes
Observe que os coeficientes dos gases da equação
balanceada nos fornecem a relação em volume entre
esses gases.
N2(g) + 3 H2(g)
Se a temperatura do sistema for aumentada, o
equilíbrio se deslocará para a esquerda (sentido
endotérmico).
Se a temperatura do sistema for diminuída, o
equilíbrio se deslocará para a direita (sentido
exotérmico).
N2(g) + 3 H2(g)
2 NH3(g)
EXERCÍCIOS DE SALA
01. (UFPB) Numa reação química, o equilíbrio é
observado quando:
a) O número de mols dos reagentes é igual ao
número de mols dos produtos.
b) A temperatura do sistema reacional fica
constante.
c) As velocidades das reações direta e inversa são
iguais.
d) Os reagentes são totalmente consumidos.
e) As reações direta e inversa ocorrem
simultaneamente.
02. (CEFET – PR) Com relação ao equilíbrio químico,
afirma-se:
I. O equilíbrio químico só pode ser atingido em
sistemas fechados (onde não há troca de
matéria com o meio ambiente).
II. Num equilíbrio químico, as propriedades
macroscópicas do sistema (concentração,
densidade, massa e cor) permanecem
constantes.
III. Num equilíbrio químico, as propriedades
macroscópicas do sistema (colisões entre
moléculas, formação de complexos ativados e
transformações de uma substâncias em outras)
permanecem em evolução, pois o equilíbrio é
dinâmico.
É (são) correta(s) a(s) afirmação(ões):
a) Somente I e II.
b) Somente I e III.
c) Somente II e III.
d) Somente I.
e) I, II e III.
03. (PUC-PR) O gráfico relaciona o número de mols de
M e P à medida que a reação: mM + nN ⇄ pP + qQ
se processa para o equilíbrio:
número de mols
07. Calcule a constante de equilíbrio Kc para a reação
2 SO2(g) + O2(g) ⇄ 2 SO3(g) sabendo que, nas
condições de temperatura e pressão em que se
encontra o sistema, existem as seguintes
concentrações dos compostos no equilíbrio: [SO 3] =
0,1 mol/L; [O2] = 1,5 mol/L e [SO2] = 1,0 mol/L.
08. O pentacloreto de fósforo é um reagente muito
importante em Química Orgânica. Ele é preparado
em fase gasosa através da reação:
PCℓ3(g) + Cℓ2(g) ⇄ PCℓ5(g).
Um frasco de 3,00 L contém as seguintes
o
quantidades em equilíbrio, a 200 C: 0,120 mol de
PCℓ5; 0,600 mol de PCℓ3 e 0,0120 mol de Cℓ2.
Calcule o valor da constante de equilíbrio, em
-1
(mol/L) , a essa temperatura.
P
M
to
t1
t2
tempo
De acordo com o gráfico, é correto afirmar:
a) em t1, a reação alcançou o equilíbrio;
b) no equilíbrio, a concentração de M é maior que
a concentração de P;
c) em t2, a reação alcança o equilíbrio;
d) no equilíbrio, as concentrações de M e P são
iguais;
e) em t1, a velocidade da reação direta é igual à
velocidade da reação inversa.
04. Escreva
as
expressões
matemáticas
das
constantes de equilíbrio Kc e Kp dos seguintes
equilíbrios em fase gasosa.
a) H2 + I2 ⇄ 2 HI
b) 2 H2 + S2 ⇄ 2 H2S
c) 2 N2H4 + 2 NO2 ⇄ 3 N2 + 4 H2O
05. (UFPE) Considere o sistema em equilíbrio:
2 HI(g) ⇄ H2(g) + I2(g) Kc = 0,02
Qual a constante de equilíbrio da reação inversa
nas mesma condições?
o
06. (UECE) a 1.200 C, Kc é igual a 8 para a reação:
NO2(g) ⇄ NO(g) + ½ O2(g).
Calcule Kc para: 2 NO2(g) ⇄ 2 NO(g) + O2(g).
09. Um equilíbrio envolvido na formação da chuva
ácida está representado pela equação:
2 SO2(g) + O2(g) ⇄ 2 SO3(g).
Em um recipiente de 1 litro, foram misturados 6
mols de SO2 e 5 mols de O2. Depois de algum
tempo, o sistema atingiu o equilíbrio; o número de
mols de SO3 medido foi 4. Calcule a constante de
equilíbrio Kc dessa reação.
10. Um método proposto para coletar energia solar
consiste na utilização dessa energia para aquecer,
o
a 800 C, trióxido de enxofre, SO3, ocasionando a
reação: 2 SO3(g) ⇄ 2 SO2(g) + O2(g). Os compostos
SO2(g) e O2(g), assim produzidos, são introduzidos
em um trocador de calor de volume correspondente
a 1,0 L e se recombinam produzindo SO3 e
liberando calor. Se 5,0 mols de SO3 sofre 60% de
dissociação nessa temperatura, marque o valor
correto de Kc.
a) 1,1
b) 1,5
c) 3,4
d) 6,7
e) 9,0
11. (VUNESP) O hidrogênio pode ser obtido do
metano, de acordo com a equação química em
equilíbrio:
CH4(g) + H2O(g) ⇄ CO(g) + 3 H2(g).
A constante de equilíbrio (Kp) dessa reação é igual
a 0,20 a 900 K. Numa mistura dos gases em
equilíbrio a 900 K, as pressões parciais de CH4(g) e
de H2O(g) são ambas iguais a 0,40 atm e a pressão
parcial de H2(g) é de 0,30 atm.
a) Escreva a expressão da constante de equilíbrio.
b) Calcule a pressão parcial de CO(g) no equilíbrio.
b) é desfavorecida pelo aumento da pressão total
exercida sobre o sistema.
c) não é afetada pelo aumento da pressão parcial
de SO3.
d) tem seu rendimentos aumentado quando o
equilíbrio é estabelecido em presença de um
catalisador.
e) é exotérmica.
TESTES DE VESTIBULARES
12. (PUC – SP) No equilíbrio N2(g) + 3 H2(g) ⇄ 2 NH3(g)
-3
-2
o
verifica-se que Kc = 2,4 x 10 (mol/L) a 727 C.
Qual o valor de Kp, nas mesmas condições físicas?
-2
-1
-1
(R = 8,2 x 10 atm.L.K .mol ).
13. Qual o efeito produzido sobre o equilíbrio
2 NO(g) + O2(g) ⇄ 2 NO2(g) H < 0
quando se provoca:
a) aumento da concentração de NO?
b) diminuição da concentração de O2?
c) diminuição da concentração de NO2?
d) diminuição da pressão total?
01. (UFRGS) Uma reação química atinge o equilíbrio
quando:
a) ocorre simultaneamente nos sentidos direto e
inverso.
b) as velocidades das reações direta e inversa são
iguais.
c) os reagentes são totalmente consumidos.
d) a temperatura do sistema é igual à do ambiente.
e) a razão entre as concentrações dos reagente e
produtos é unitária.
02. (ACAFE-SC) Dado o sistema
N2 + 3 H2 ⇄ 2 NH3,
a constante de equilíbrio é:
[N2] . [H2] 3
[NH3] 3
a) Kc =
b) Kc =
[NH3] 2
[N2] . [H2]
[NH3]
c) Kc =
[N2] 2. [H2]
e) aumento da temperatura?
e) Kc =
14. (UFRJ) A reação de síntese do metanol a partir do
monóxido de carbono e hidrogênio é:
CO(g) + 2 H2(g) ⇄ CH3OH(g)
o
Admita que a entalpia padrão (H ) dessa reação
-1
seja constante e igual a −90 kJ.mol de metanol
formado e que a mistura reacional tenha
comportamente de gás ideal.
A partir de um sistema inicialmente em equilíbrio,
explique como aumentos independentes de
temperatura e pressão afetam o equilíbrio dessa
reação.
_________________________________________
_________________________________________
_________________________________________
_________________________________________
_________________________________________
_________________________________________
_________________________________________
15. (VUNESP) Em uma das etapas da fabricação do
ácido sulfúrico ocorre a reação
SO2(g) + ½ O2(g) ⇄ SO3(g).
Sabendo-se que as constantes de equilíbrio da
reação diminuem com o aumento da temperatura, e
que o processo de fabricação do ácido sulfúrico
ocorre em recipiente fechado, conclui-se que a
reação acima:
a) é favorecida pelo aumento do volume do
recipiente.
d) Kc =
[NH3] 2
[N2] . [H2] 3
[2 NH3]
[N2] . [3 H2]
03. (UFMG) Considere a reação hipotética
A+B
v1
v2
C+D
Considere também o gráfico da velocidade em
função do tempo dessa reação.
Velocidade
v1
v2
0
x
y
Tempo
Com base nessas informações, todas as afirmativas
estão corretas, exceto:
a) no instante inicial, a velocidade v1 é máxima.
b) no instante inicial, as concentrações de C e D são
nulas.
c) no instante x, as concentrações dos reagentes e
produtos são as mesmas.
d) no instante x, a velocidade v2 é máxima.
e) no instante x, as concentrações de A e B são as
mesmas que no instante y.
04. (PUC-PR) Atingido o equilíbrio químico na reação:
H2(g) + I2(g)
2 HI(g)
medimos os valores das constantes de equilíbrio, em
função das concentrações molares (Kc) e em função
das pressões parciais (Kp). Em conseqüência,
teremos:
a) sempre Kc = Kp;
b) sempre Kc > Kp;
c) sempre Kc < Kp;
d) Kc Kp, dependendo da temperatura;
e) Kc Kp, dependendo da temperatura.
05. (PUCCAMP-SP) Indique o único sistema, em
equilíbrio, cujo valor de constante, em pressões
parciais, é o mesmo do medido em mols/litro:
a) 2 NH3(g) ⇄ N2(g) + 3 H2(g)
b) C(s) + H2O(g) ⇄ CO(g) + H2(g)
c) CO(g) + Cl2(g) ⇄ COCl2(g)
d) CO(g) + H2O(g) ⇄ CO2(g) + H2(g)
e) PCl5(g) ⇄ PCl3(g) + Cl2(g)
06. (CESGRANRIO-RJ) Assinale, entre as opções
abaixo, a razão Kp/Kc relativa à reação
2 NaHCO3(s) ⇄ Na2CO3(s) + CO2(g) + H2O(g)
a) 1
b) RT
-2
c) (RT)
2
d) (RT)
3
e) (RT)
07. (VUNESP-SP) Estudou-se a cinética da reação
S(s) + O2(g) SO2(g)
realizada a partir de enxofre e oxigênio em um
sistema fechado. Assim, as curvas I, II e III do gráfico
representam as variações das concentrações dos
componentes com o tempo desde o momento da
mistura até o sistema atingir o equilíbrio.
Mol/L
III
I
tempo
As variações das concentrações de S, de O2 e de
SO2 são representadas, respectivamente, pelas
curvas:
a) I, II e III
b) II, III e I
c) III, I e II
d) I, III e II
e) III, II e I
8. (UFPR) Quais das informações abaixo podem ser
extraídas apenas pelo exame da equação
2 NH3(g) ?
09. (UFRJ) 0,10 mol de H2 e 1,24 mol de HI foram
colocados em um balão de 10 litros no qual se fez
previamente o vácuo e aquecidos a 425°C por
algumas horas; depois de arrefecido, seu conteúdo
foi analisado, tendo sido encontrados os seguintes
valores:
H2 = 0,20 mol I2 = 0,10 mol HI = 1,04 mol
A constante de equilíbrio do sistema, considerando a
reação H2 + I2 ⇄ 2 HI é:
a) 0,54
b) 5,4
c) 54
d) 0,52
e) 5,2
10. (FUVEST-SP) O equilíbrio de dissociação do H2S
gasoso é representado pela equação
2 H2S(g) ⇄ 2 H2(g) + S2(g).
3
Em um recipiente de 2,0 dm estão em equilíbrio 1,0
mol de H2S, 0,20 mol de H2 e 0,80 mol de S2.
Qual o valor da constante de equilíbrio Kc?
a) 0,016
b) 0,032
c) 0,080
d) 12,5
e) 62,5
11. (UFPR) Temos representadas no gráfico as concentrações dos reagentes e produtos de uma reação do
tipo
II
N2(g) + 3 H2(g)
01) A reação somente se processará se os
reagentes estiverem exatamente nas proporções
dadas pela equação.
02) Para cada molécula de N 2 consumida, são
necessárias três moléculas de H2, produzindo
duas moléculas de NH3.
04) Para cada mol de H2, é necessário 1/3 de mol de
N2.
08) A reação é muito lenta e necessita de catalisador
para ser acelerada.
16) Se a reação se processar em recipiente fechado
e se, inicialmente, estiverem presentes um mol de
N2 e três mols de H2, no final da reação teremos
somente moléculas de amônia.
A + B ⇄ C + D
ocorrendo no sentido à direita a partir do tempo zero.
Tem-se sempre [A] = [B] e [C] = [D], estando estes
valores representados no gráfico.
Concentração (mol/L)
10
8 .................................................
6
.................................................
4
2 .................................................
Tempo
Calcular a constante de equilíbrio Kc da reação.
12. (PUC-SP) Um mol de H2 e um mol de Br2 são colocados em um recipiente de 10 L de capacidade, a
575°C. Atingindo-se o equilíbrio, a análise do
sistema mostrou que 0,20 mol de HBr está presente.
Calcule o valor de Kc, a 575°C, para a reação
H2(g) + Br2(g) ⇄ 2 HBr(g).
13. (FUVEST-SP) Na reação de esterificação
etanol(l) + ácido acético(l) ⇄ acetato de etila(l) + água(l)
quando se parte de 1 mol de cada um dos reagentes
puros, o equilíbrio se estabelece formando 2/3 mol
de éster. Calcule o valor da constante de equilíbrio
Kc da reação.
14. (MED POUSO ALEGRE-MG) A constante de
equilíbrio Kc da reação A + B ⇄ C + D é igual a 9.
Se 0,4 mol de A e 0,4 mol de B forem postos a
reagir, o número de mols de D formado é:
a) 0,30
b) 0,60
c) 0,40
d) 0,36
e) 0,18
15. (UFSE) A 250°C, PCl5 se decompõe em PCℓ3 e Cℓ2.
-4
Quando se estabelece o equilíbrio, [PCℓ5] =4.10
mol/L.
Qual o valor de [PCℓ3]?
(Dados: a 250°C a constante de equilíbrio da reação
PCℓ5(g) ⇄ PCℓ3(g) + Cℓ2(g) vale 4.10 )
3
a) 4.10 mol/L
2
b) 4.10 mol/L
-1
c) 4.10 mol/L
-2
d) 4.10 mol/L
-3
e) 4.10 mol/L
-2
(CESCEM-SP) Para responder às questões 16 e 17,
utilize os dados abaixo:
A reação A +B ⇄ C + D foi estudada em cinco
temperaturas bem distintas. As constantes de
equilíbrio encontradas estão relacionadas a seguir:
-2
K1 = 1,00 x 10 à temperatura T1
K2 = 2,25 à temperatura T2
K3 = 1,00 à temperatura T3
K4 = 81,0 à temperatura T4
-1
K5 = 4,00 x 10 à temperatura T5
16. A que temperatura ocorrerá a maior transformação
de A e B em C e D quando o equilíbrio for atingido?
a) T1
b) T2
c) T3
d) T4
e) T5
17. Se as concentrações de A e B fossem iguais, a que
temperatura todas as quatro substâncias estariam
presentes no equilíbrio com concentrações iguais?
a) T1
b) T2
c) T3
d) T4
e) T5
18. (UFPA) Em um recipiente de 1 litro, colocou-se 1,0
mol de PCℓ5. Suponha o sistema
PCℓ5 ⇄ PCℓ3 + Cℓ2,
homogêneo e em temperatura tal que o PCℓ5 esteja
80% dissociado. A constante de equilíbrio para esse
sistema é:
a) 0,48 mol/L
b) 0,82 mol/L
c) 1,65 mol/L
d) 3,20 mol/L
e) 6,40 mol/L
19. (FAAP-SP) Sob determinadas condições, um mol de
HI gasoso encontra-se 20% dissociado em H2 e I2,
segundo a equação de reação:
2 HI(g) ⇄ H2(g) + I2(g).
O valor da constante de equilíbrio da reação (em
termos de concentrações) é, aproximadamente, igual
a:
-1
a) 1,25 . 10
-1
b) 2,5 . 10
c) 4
d) 80
-2
e) 1,56 . 10
20. (PUC-SP) Um mol da substância A2 é colocado num
recipiente de 1 litro de capacidade e, aquecido a
22°C, sofre a dissociação:
A2(g) ⇄ 2 A(g).
Medindo-se a constante de dissociação térmica,
nessa temperatura, encontrou-se o valor Kc = 4
mols/litro.
Conseqüentemente, o grau de dissociação térmica
de A2, na temperatura da experiência, vale
aproximadamente:
a) 20%
b) 40%
c) 60%
d) 80%
e) 100%
21. (USP-SP) Aumentando a pressão no sistema
gasoso
H2 + I2 ⇄ 2 HI
a) o equilíbrio desloca-se no sentido da formação de
HI.
b) o equilíbrio desloca-se no sentido da decomposição de HI.
c) o equilíbrio não se altera.
d) o valor da constante de equilíbrio aumenta.
e) o valor da constante de equilíbrio diminui.
22. (PUC-PR) Consideremos o equilíbrio a 1000°C:
2 CO(g) + O2(g) ⇄ 2 CO2(g) H = -130 kcal
Devemos esperar um aumento na quantidade de
monóxido de carbono quando:
a) a temperatura aumentar e a pressão aumentar.
b) a temperatura diminuir e a pressão diminuir.
c) a temperatura diminuir e a pressão aumentar.
d) a temperatura aumentar e a pressão diminuir.
e) somente com adição de catalisadores especiais.
23. (PUC-PR) Considere o sistema em equilíbrio:
N2(g) + 3 H2(g) ⇄ 2 NH3(g) H = -22 kcal.
A melhor maneira de aumentar o rendimento de NH3
é:
a) aumentar a temperatura.
b) aumentar a pressão.
c) juntar um catalisador.
d) adicionar um gás inerte.
e) aumentar o volume do reator.
Exemplos:
• Ionização do ácido cianídrico:
Ka
[H ] . [CN ]
[HCN]
1.ª etapa: H2S ⇄ H + HS
Ka 1
[H ] . [HS ]
[H 2 S]
2.ª etapa: HS ⇄ H + S
Ka 2
HCN ⇄ H + CN
+
24 (PUC-PR) Os seguintes fatores podem deslocar um
sistema em equilíbrio químico, exceto um:
a) pressão total.
b) temperatura.
c) concentração de um participante da reação.
d) catalisador.
e) pressão parcial de um participante da reação.
-
• Ionização do ácido sulfídrico:
+
-
25. (UFSC) Dada a reação:
2 NO2(g) ⇄ N2O4(g) H = -14,1 kcal,
qual das alterações abaixo aumenta a concentração
molecular do produto?
01) Aumento da temperatura.
02) Aumento da concentração de NO2.
04) Diminuição da temperatura.
08) Diminuição da pressão.
16) Adição de um catalisador.
-
+
2-
[H ] . [S 2- ]
[HS - ]
Para as bases, a constante de ionização é freqüentemente representada por Kb.
Exemplos:
• Ionização da amônia:
NH3 + H2O ⇄ NH4 + OH
+
-
Ki
[NH 4 ] . [OH ]
[NH 3 ] . [H 2 O]
A concentração molar da água é considerada
constante e, sendo assim, pode-se fazer:
EQUILÍBRIO IÔNICO
Ki . [H 2 O]
Equilíbrio iônico é um caso particular de
equilíbrio químico que envolve a participação de íons.
Exemplos:
[NH 4 ] . [OH ]
[NH 3 ]
sendo Ki . [H2O] = Kb obtém-se:
• Ionização do HCN (ácido fraco)
HCN ⇄ H + CN
+
Kb
-
• Ionização do NH3 (base fraca)
NH3 + H2O ⇄
+
NH4
+ OH
-
Um equilíbrio iônico é caracterizado através do grau
de ionização () e da constante de ionização(Ki).
GRAU DE IONIZAÇÃO OU DE DISSOCIAÇÃO
IÔNICA ()
α
n.º mols ionizados
n.º mols inicial
CONSTANTE DE IONIZAÇÃO OU DE
DISSOCIAÇÃO (Ki)
A constante de ionização ou de dissociação (Ki) é
obtida pela aplicação da lei de velocidades ao equilíbrio
iônico.
Para os ácidos, a constante de ionização é freqüentemente representada por Ka.
[NH 4 ] . [OH ]
[NH 3 ]
Este exemplo mostra que a concentração molar da
água é omitida na expressão da constante de
ionização.
Importante: a constante de ionização depende
apenas da temperatura.
LEI DA DILUIÇÃO DE OSTWALD
Relaciona constante de ionização (Ki), grau de
ionização () e concentração molar (♏).
Considerando a solução aquosa de um monoácido
HA de concentração molar ♏ mol/L e sendo o grau de
ionização desse ácido, tem-se:
Início
Ionização
Equilíbrio
HA
♏ mol/L
♏
mol/L
♏-♏ mol/L
ou
♏.(1 - ) mol/L
⇄
+
-
H
+
zero
A
zero
♏
mol/L
♏
mol/L
♏
mol/L
♏
mol/L
Efetuando o cálculo da constante de ionização (Ki),
tem-se:
[H ] . [A ]
♏ . ♏
Ki
♏.(1 - )
[HA]
temperatura, ao passo que aquela, além da
temperatura, depende também da concentração da
solução.
Como regra geral, pode-se estabelecer que:
força
ou
Ki
força
2
Ki =
♏.
(1 – )
Exemplos de constantes de ionização de ácidos, a
25°C:
Esta é a expressão matemática da Lei da Diluição de
Ostwald.
Para ácidos e bases fracos o valor de é muito
pequeno ( < 5%), podendo se admitir que (1 ) é,
aproximadamente igual a 1. Assim:
Ác. clorídrico: HCl
Ác. sulfúrico: H2SO4
Ác. Sulfuroso: H2SO3
Ác. fosfórico: H3PO4
Ki = ♏ .
2
Esta expressão nos mostra que, sendo Ki constante
a dada temperatura, ao se diluir a solução de um ácido
fraco ou de uma base fraca (diminuir a concentração
molar ♏), o valor de aumenta.
Portanto:
Quando se dilui um ácido ou base fracos, o
seu grau de ionização ou de dissociação ()
aumenta.
Este é o enunciado da Lei da Diluição de Ostwald.
Através da expressão matemática da Lei da Diluição
de Ostwald, pode-se efetuar cálculos envolvendo Ki, e
♏.
Exemplo:
O grau de ionização da amônia, NH3, em solução 1
mol/L, é 0,40% a 20°C. A constante de ionização da
amônia, nesta temperatura é, aproximadamente, igual a:
-1
a) 1,6 x 10
-1
b) 4,0 x 10
-3
c) 1,0 x 10
-3
d) 4,0 x 10
-5
e) 1,6 x 10
Resolução:
-3
Dados: ♏ = 1 mol/L; % = 0,4% → = 4 . 10
Aplicando a expressão matemática da Lei da
Diluição de Ostwald, tem-se:
2
Ki = ♏. /(1-)
Como < 5%, pode-se admitir que (1 - ) = 1.
Portanto:
-3 2
Ki = 1 . (4 . 10 )
-5
Ki = 1,6 x 10
A alternativa “e” é a correta.
FORÇA DE ELETRÓLITOS
A força de um eletrólito é determinada pelo seu grau
de ionização ou pela sua constante de ionização, sendo
esta a grandeza mais segura, pois depende apenas da
Ác. acético: CH3COOH
Ác. cianídrico: HCN
Ka muito alto
Ka1 muito alta
-2
Ka2 = 1,9 x 10
-2
Ka1 = 1,7 x 10
-8
Ka2 = 6,3 x 10
-3
Ka1 = 6,9 x 10
-8
Ka2 = 6,2 x 10
-13
Ka3 = 4,7 x 10
-5
Ka = 1,8 x 10
-10
Ka = 5,0 x 10
Observações:
• Quanto maior a constante de ionização (Ka) de um
+
ácido, maior a [H ] e mais acentuadas serão as
propriedades ácidas da solução.
• Os poliácidos ionizam em tantas etapas quantos
são os hidrogênios ionizáveis presentes em sua
molécula, sendo que cada etapa possui sua constante
de ionização. Tais constantes são representadas por
Ka1, Ka2, Ka3, etc.
Observa-se que a ordem de grandeza dessas
constantes de ionização é:
Ka1 > Ka2 > Ka3 > .....
Exemplos de constantes de dissociação de bases, a
25°C:
Hidróxido de amônio: NH4OH
Hidróxido de metilamônio: CH3NH3OH
Hidróxido de dimetilamônio: (CH3)2NH2OH
Hidróxido de trimetilamônio: (CH3)3NHOH
Hidróxido de etilamônio: C2H5NH3OH
Kb = 1,8 x 10-5
Kb = 5,0 x 10-4
Kb = 7,4 x 10-4
Kb = 7,4 x 10-5
Kb = 5,6 x 10-4
Quanto maior a constante de dissociação (Kb) de
uma base, maior a [OH ] e mais acentuadas as
propriedades básicas da solução.
• Potencial de Ionização (pKi)
Considerando-se que os valores de Ki são muito pequenos, é usual expressá-lo através de logaritmos,
segundo a expressão:
pKi = log Ki
Exemplos:
ácido
HCN
H3PO4
1.º
2.º
3.º
Ka
-10
5 x 10
-3
6,9 x 10
-8
6,2 x 10
-13
4,7 x 10
pKa
9,3
2,2
7,2
12,3
base
NH4OH
H3CNH3OH
Observa-se que:
Ki
Kb
-5
1,8 x 10
-4
5,0 x 10
pKi
pKb
4,7
3,3
força
03. Um determinado produto de limpeza, de uso
-3
doméstico, é preparado a partir de 2,5 x 10 mol de
o
NH3 para cada litro do produto. A 25 C, esse
produto contém, dentre outras espécies químicas,
-4
1,0 x 10 mol de OH (aq). Considere-se que a
equação de ionização da amônia em água é:
NH3(g) + H2O(ℓ) ⇄ NH4 (aq) + OH (aq).
Calcular, em porcentagem, o grau de ionização da
amônia nesse produto.
+
EFEITO DO ÍON COMUM
-
Efeito do íon comum é uma aplicação do Princípio de
Le Chatelier ao equilíbrio iônico.
O ácido acético, H3CCOOH, é um ácido fraco. Na
solução aquosa deste ácido existe o equilíbrio:
H3CCOOH ⇄ H + H3CCOO
+
-
Se à solução adicionarmos o sal acetato de sódio,
que tem íon acetato em comum com o ácido, o sal se
dissociará completamente,
+
Na H3CCOO
-
Na + H3CCOO
+
04. Calcular a concentração molar de uma solução de
ácido cianídrico sabendo-se que este ácido está
0,01% ionizado e que sua constante de ionização,
-10
na mesma temperatura, é 7,2 x 10 .
-
-
aumentado a concentração de íons H3CCOO .
Para minimizar o efeito do aumento na concentração
do íon acetato, o equilíbrio é deslocado para a
esquerda,
H3CCOOH
+
H + H3CCOO
-
reprimindo a ionização do ácido acético.
Como conseqüência, diminui o grau de ionização
do ácido acético.
Do exposto, conclui-se que:
Efeito do íon comum é a diminuição do grau
de ionização () de um eletrólito fraco por
ação de um sal que com ele tem um íon em
comum.
EXERCÍCIOS DE SALA
05. Frutas cítricas, como o limão e a laranja, possuem
ácido cítrico e ácido ascórbico (vitamina C). A
o
constante de ionização, a 25 C, do ácido cítrico é 8
-4
-5
x 10 e a do ácido ascórbico é 8 x 10 . Com
relação a esses dados, analise as afirmações
abaixo. Assinale (V) se a afirmação for verdadeira e
(F) se for falsa.
( ) O ácido cítrico é mais forte que o ácido
ascórbico.
( ) Em soluções de mesma concentração molar
o
+
dos dois ácidos, a 25 C, a [H ] é maior na
solução de ácido ascórbico.
-5
o
( ) O ácido acético (Ka = 2 x 10 , a 25 C) é mais
forte que os ácidos cítrico e ascórbico.
-4
o
( ) O ácido fluorídrico (Ka = 7 x 10 , a 25 C) é
mais fraco que o ácido cítrico e mais forte que
o ácido ascórbico.
( ) A ordem crescente de força entre os ácidos
citados é: acético < ascórbico < fluorídrico <
cítrico.
o
06. Numa solução aquosa de ácido cianídrico ocorre o
seguinte equilíbrio:
o
HCN(aq) ⇄ H (aq) + CN (aq).
Que efeito provoca nesse equilíbrio a adição de
NaCN(s)? Justifique sua resposta.
_________________________________________
_________________________________________
_________________________________________
_________________________________________
_________________________________________
_________________________________________
01. A 25 C, o grau de ionização do ácido acético, em
-2
-1
solução 2 x 10 mol.L , é 3%. Calcular a constante
de ionização, Ka, do ácido acético, naquela
temperatura.
02. A 25 C, a constante de ionização do ácido
-4
fluorídrico é 7 x 10 . Calcular, em porcentagem, o
grau de ionização desse ácido em uma solução
-1
1,75 mol.L , naquela temperatura.
+
-
07. (Fuvest – SP) No vinagre ocorre o seguinte
equilíbrio:
H3C-COOH ⇄ H + H3C-COO .
Que efeito provoca nesse equilíbrio a adição de
uma substância básica? Justifique sua resposta.
_________________________________________
_________________________________________
+
-
_________________________________________
_________________________________________
_________________________________________
_________________________________________
TESTES DE VESTIBULAR
01. Uma solução de ácido fraco HCℓO foi analisada
verificando-se, no equilíbrio, a existência das
seguintes concentrações:
+
-4
[H ] = 1,78 x 10 mol/L
-4
[CℓO ] = 1,78 x 10 mol/L
[HCℓO] = 1,00 mol/L
A constante de ionização do ácido HClO é igual a:
-4
a) 3,56 x 10
-8
b) 3,56 x 10
-8
c) 3,17 x 10
-4
d) 1,78 x 10
-4
e) 3,17 x 10
06. (FEI-SP) Uma solução 0,01 mol/L de um monoácido
está 4,0 % ionizada. A constante de ionização desse
ácido é:
-3
a) 16,6 x 10
-5
b) 1,6 x 10
-5
c) 3,3 x 10
-5
d) 4,0 x 10
-6
e) 3,0 x 10
07. (FEI-SP) A constante de equilíbrio Ka dos ácidos
HA, HB e HC, a 25°C, são, respectivamente, 1,8 x
-5
-8
-4
10 , 5,7 x 10 e 1,8 x 10 . A ordem crescente de
força desses ácidos é:
a) HB < HA < HC
b) HC < HA < HB
c) HB < HC < HA
d) HC < HB < HA
e) HA < HB < HC
02. Ao realizar-se a ionização
H2S(aq) ⇄ H (aq) + HS (aq)
verificou-se que, no equilíbrio, que:
[HS ] = 0,1 mol/L
[H2S] = 0,4 mol/L
O valor da constante de ionização na temperatura
-7
em que a experiência foi realizada é 1 x 10 .
Nas condições da experiência, a concentração molar
+
do H é:
-1
a) 1 x 10 mol/L
-3
b) 2 x 10 mol/L
-3
c) 3 x 10 mol/L
-7
d) 4 x 10 mol/L
-9
e) 5 x 10 mol/L
+
-
-2
03. (UFGO) Uma solução 2 x 10 mol/L de ácido
acético tem um grau de ionização 0,03 a uma dada
temperatura. A sua constante de ionização (Ka)
nesta temperatura é:
-2
a) 4,50 x 10
-5
b) 1,75 x 10
-4
c) 1,75 x 10
-5
d) 1,80 x 10
-5
e) 2,80 x 10
04. (CESCEM-SP) Uma solução 0,05 mol/L de um ácido
fraco HA é 0,1% ionizada. Qual é, aproximadamente,
a sua constante de ionização?
-8
a) 5 x 10
-7
b) 5 x 10
-6
c) 5 x 10
-5
d) 5 x 10
-3
e) 5 x 10
05. (PUC-SP) Um monoácido fraco tem constante de
-9
ionização igual a 10 em temperatura ambiente. Este
ácido, numa solução decimolar, terá grau de
ionização aproximadamente igual a:
a) 1%
b) 0,1%
c) 0,01%
d) 0,001%
e) 0,0001%
A tabela a seguir contém dados para a resolução das
os
questões de n. 08 a 10.
Reação
Ka
I. H3CCOOH + H2O ⇄ H3O + H3CCOO
1,8 x 10
II. HCOOH + H2O ⇄ H3O + HCOO
1,8 x 10
III. H2S + H2O ⇄ H3O + HS
9,0 x 10
+
-
+
+
-
-
IV. HF + H2O ⇄ H3O + F
+
-
-5
-4
-8
6,8 x 10
V. H3PO4 + H2O ⇄ H3O + H2PO4
+
-
-4
4,4 x 10
-7
08. (UFSC) O ácido mais ionizado é:
a) IV
b) V
c) III
d) I
e) II
09. (UFSC) O ácido mais fraco é:
a) III
b) V
c) I
d) II
e) IV
10. (UFSC) Os ácidos são (não necessariamente na
ordem):
a) fosfórico, sulfídrico, metanóico, fluorídrico e
etanóico.
b) fluorídrico, etanóico, fórmico, sulfuroso e
fosforoso.
c) fórmico, acético, sulfúrico, fosforoso e fluórico.
d) fluoroso, fórmico, fosfórico, sulfídrico e acético.
e) acético, fluorídrico, sulfuroso, fórmico e fosforoso.
os
As questões de n.
11 e 12 referem-se aos
seguintes ácidos e suas correspondentes constantes
de ionização, a 25°C.
ácido cianídrico
ácido propiônico
ácido acético
-10
4,0 x 10
-5
1,3 x 10
-5
1,8 x 10
-4
ácido fórmico
ácido fluorídrico
11.
1,8 x 10
-4
6,7 x 10
(UEL-PR) Dentre eles,
carboxílicos?
a) 1
b) 2
d) 4
e) 5
quantos
são
ácidos
c) 3
12. (UEL-PR) Dentre eles, o mais forte e o menos
ionizado são, respectivamente:
a) cianídrico e propiônico
b) cianídrico e fluorídrico
c) fórmico e acético
d) fluorídrico e cianídrico
e) fluorídrico e fórmico
13. (CESCEM-SP) Considere os oxiácidos do cloro e
suas respectivas constantes de ionização:
-8
HCℓO
3,0 x 10
-2
HCℓO2
1,1 x 10
2
HCℓO3
5,0 x 10
7
HCℓO4
2,0 x 10
A ordem de grandeza das constantes de ionização
K1, K2 e K3 será:
a) K3 > K2 > K1
b) K1 = K2 = K3
c) K1 > K2 > K3
d) K1 > K3 > K2
e) K2 > K1 > K3
17. (PUC-SP) Tem-se uma solução de ácido acético,
+
HAc, onde há íons H (aq) e Ac (aq) em equilíbrio com
HAc não dissociado.
Se adicionarmos acetato de sódio, NaAc, a essa
solução:
+
a) a concentração dos íons H (aq) deverá aumentar.
+
b) a concentração dos íons H (aq) permanecerá
inalterada.
+
c) a concentração dos íons H (aq) deverá diminuir.
d) a concentração do HAc não dissociado diminuirá.
e) não há deslocamento do equilíbrio químico.
18. (FEI-SP) No equilíbrio representado pela equação:
2+
Mg
O exame dos dados permite afirmar que:
I. a força do ácido é maior quanto maior o número
de oxidação do cloro.
II. dos oxiácidos representados, o mais forte é o
HCℓO.
III. o número de oxidação do cloro no HCℓO3 é +3.
a) Somente I é correta.
b) Somente II é correta.
c) Somente III é correta.
d) I, II e III são corretas.
e) I, II e II são incorretas.
14.
(PUC-PR) Temos duas soluções de igual
molaridade:
a 1.ª de ácido acético, cujo pK é igual a 4,76;
a 2.ª de ácido butírico, cujo pK é igual a 4,82.
Com estes dados, podemos afirmar que:
a) a 1.ª solução é mais ácida que a 2.ª.
b) a 1.ª solução é menos ácida que a 2.ª.
c) as duas soluções apresentam a mesma acidez.
d) a constante de ionização do ácido acético é
menor que a do ácido butírico.
e) nenhuma destas respostas.
-
qual das substâncias abaixo o deslocaria para a
direita se adicionada ao sistema?
a) NH4NO3
b) NaCℓ
c) H2SO4
d) HCℓ
e) NaOH
19. (MAPOFEI-SP) Dado o equilíbrio:
HCN + H2O
1
H3O+ + CN-
2
a adição de cianeto de sódio:
a) desloca o equilíbrio no sentido 1.
b) não desloca o equilíbrio.
+
c) aumenta a concentração de H3O .
d) desloca o equilíbrio no sentido 2.
e) diminui a concentração de HCN.
20. (PUC-PR) Em solução aquosa existe o equilíbrio:
2-
2 CrO4
amarelo
15. (UFPR) Pelos seus pKa ou Ka indique o ácido mais
ionizado.
Dados: log 514 = 2,7; log 63 = 1,79
-5
a) Cℓ2CH-COOH (Ka = 5140 . 10 )
b) orto-O2N-C6H4-COOH (pKa = 2,81)
-5
c) C6H5-COOH (Ka = 6,3 . 10 )
d) para-O2N-C6H4-OH (pKa = 7,14)
e) C6H5-OH (pKa = 9,95)
+ 2 OH ⇄ Mg(OH)2
+ H2O ⇄ Cr2O7
2-
+ 2 OH
-
alaranjado
Assinale a proposição falsa:
a) Adicionando HCℓ, o sistema fica alaranjado.
b) Adicionando NaOH, o sistema fica amarelo.
c) O Princípio de Le Chatelier não se aplica a
equilíbrios iônicos.
d) No equilíbrio, a velocidade da reação direta é igual
à velocidade da reação inversa.
e) A constante de equilíbrio não varia pela adição de
HCℓ ao sistema.
16. (CESCEM-SP) A dissociação do ácido ortoarsênico, H3AsO4, em solução aquosa diluída, se
processa conforme as equações:
PRODUTO IÔNICO DA ÁGUA (Kw)
H3AsO4 ⇄ H + H2AsO4
K1
H2AsO4 ⇄ H + HAsO4
K2
HAsO4 ⇄ H + AsO4
K3
+
-
2-
-
+
+
2-
3-
Medidas de condutibilidade elétrica mostram que a
água está ligeiramente ionizada segundo a equação:
H2O ⇄ H + OH
+
-
Esta ionização da água, como as demais, é
reversível e atinge um equilíbrio dinâmico denominado
equilíbrio iônico da água.
Numa mesma temperatura, o valor de Kw
permanece constante, qualquer que seja a substância
dissolvida em água.
-9
A 25°C, o grau de ionização () da água é 1,81x10 .
Considerando 1 litro de água pura (1000 g de água
pura) e aplicando ao equilíbrio iônico da água a lei da
ação das massas, tem-se:
Observações:
• Em água pura ou em solução neutra, a 25°C:
+
18 g H2O 1 mol
1000 g H2O x
x = 55,5 mols
• Cálculo das concentrações molares no equilíbrio.
⇄
H2O
55,5
(n . )
início
ionização
(55,5 . 1,81 . 10-9)
+
H
0
10
(n - n)
-7
(55,5 - 10 )
-7
(55,5 - 10 )
mol/L
-7
equilíbrio
concentr.
molares
+ OH
0
-
(n . )
-7
10
(n . )
-7
10
n
-7
10
-7
10
mol/L
n
-7
10
-7
10
mol/L
-
-7
[H ] = [OH ] = 10 mol/L
• Cálculo do número de mols existentes em 1000 g
de H2O.
• Ao se adicionar um ácido HA em água, ocorre sua
ionização,
+
HA H + A
+
com conseqüente aumento da concentração de íons H .
Como Kw é constante, um aumento da concentração de
+
íons H acarretará uma diminuição da concentração de
íons OH .
Kw = [H+] . [OH-] = 10-14 (a 25°C)
esta concentração
aumenta
esta concentração
diminui
Assim sendo, em soluções ácidas, a 25°C:
Nota-se que a concentração molar da água no
equilíbrio é praticamente a mesma do início. Portanto,
pode-se dizer que a concentração molar da água é
constante,
+
-7
[H ] > 10 mol/L
-7
[OH ] < 10 mol/L
• Ao se adicionar uma base B(OH) em água ocorre
sua dissociação,
[H2O] = constante.
• Cálculo da constante de equilíbrio
B(OH) B + OH
+
[H+] . [OH-]
Kc =
[H2O] = constante
[H2O]
+
-
Kc . [H2O] = [H ] . [OH ]
O produto da constante de equilíbrio pela
concentração molar da água dá uma nova constante
denominada produto iônico da água, Kw. Portanto:
+
-
Kw = [H ] . [OH ]
-7
Kw = 10
esta concentração
diminui
esta concentração
aumenta
Assim sendo, em soluções básicas, a 25°C:
(a 25°C)
O valor de Kw depende da temperatura. A elevação
da temperatura acarreta um aumento do grau de
ionização da água e, conseqüentemente, um aumento
do valor de Kw.
A tabela abaixo mostra valores do produto iônico da
água (Kw) em diferentes temperaturas.
Temperatura
0°C
10°C
20°C
25°C
30°C
40°C
60°C
80°C
com conseqüente aumento da concentração de íons
OH . Como Kw é constante, um aumento da
concentração de íons OH acarretará uma diminuição da
+
concentração de íons H .
Kw = [H+] . [OH-] = 10-14 (a 25°C)
-7
Kw = 10 . 10
-14
-
Kw
-14
0,11 . 10
-14
0,29 . 10
-14
0,69 . 10
-14
1,00 . 10
-14
1,48 . 10
-14
3,02 . 10
-14
9,33 . 10
-14
23,40 . 10
+
-7
[H ] < 10 mol/L
-7
[OH ] > 10 mol/L
• Ao se preparar uma solução ácida ou básica de
concentração molar ♏ e conhecido o grau de ionização
ou de dissociação () do ácido ou da base, pode-se
+
calcular a [H ] ou a [OH ].
Em solução ácida:
[H ] = ♏ .
Em solução básica:
[OH ] = ♏ .
pH e pOH
+
-
-9
+
-
Em função dos valores baixos de [H ] e [OH ],
costuma-se indicar a acidez ou a basicidade de uma
solução através de seu pH (potencial hidrogeniônico) e
pOH (potencial hidroxiliônico).
Por definição:
pH = log [H ]
+
pOH = log [OH ]
-
e
Aplicando as definições
temperatura de 25°C, obtém-se:
+
água pura ou
solução neutra
solução
ácida
solução
básica
e
considerando
-7
a
pH = 7
pOH = 7
pH < 7
pOH > 7
pH > 7
pOH < 7
[H ] = 10 mol/L
-7
[OH ] = 10 mol/L
+
-7
[H ] > 10 mol/L
-7
[OH ] < 10 mol/L
+
-7
[H ] < 10 mol/L
-7
[OH ] > 10 mol/L
Para qualquer meio aquoso, a 25°C, a soma entre o
pH e o pOH é igual a 14. Observe:
+
-
[H ] . [OH ] = 10
aplicando logaritmo em
igualdade
+
-14
ambos
-
os
log [H ] + log [OH ] = log 10
membros da
-
03. (UFRGS) O acidente ocorrido com o navio
Bahamas provocou o vazamento de milhares de
toneladas de ácido sulfúrico na lagos dos Patos.
Em determinados locais, foram registrados valores
de pH entre 3 e 4. Podemos afirmar que, nesses
locais, a concentração aproximada de íons
-1
hidroxila, em mol;L , foi:
-11
a) maior que 10 .
-9
b) maior que 10 .
-7
c) maior que 10 .
-5
d) maior que 10 .
-4
e) maior que 10 .
04. (FAAP – SP) O vinagre é uma substância muito
utilizada como tempero em saladas. Sabe-se que
uma amostra de vinagre apresentou pH igual a 2,0.
Isso corresponde a uma solução de ácido acético
+
cuja concentração molar de íons H deve ser:
a) 55,50
b) 0,01
c) 1,00
d) 0,10
e) 10,10
05. (UFRRJ) Em um potenciômetro, faz-se a leitura de
uma solução de hidróxido de sódio (utilizada na
neutralização do ácido láctico). Sabendo que o grau
de dissociação é total, o valor do pH encontrado
corresponde a:
a) 2,7
b) 5,4
c) 12,0
d) 11,0
e) 9,6
-14
multiplicando por (-1)
+
c) 5,0 x 10
-8
d) 5,0 x 10
-9
e) 2,0 x 10
-14
(-log [H ]) + (-log [OH ]) = (-log 10 )
pH + pOH = 14
06. (UNIP – SP) O fluoreto de hidrogênio (HF) é um
ácido que se encontra 10% ionizado em solução
-1
0,1 mol.L . Calcule o pH dessa solução.
EXERCÍCIOS DE SALA
01. (Mackenzie – SP) Com os dados da tabela abaixo,
+
Soluções
[H ]
I
Urina
1 x 10
II
Clara de ovo
1 x 10
III
Lágrima
1 x 10
IV
Café
1 x 10
-6
07. (PUC – MG) A concentração hidrogeniônica do
-2
-1
suco de limão puro é 10 mol.L . O pH de um
refresco preparado com 30 mL de suco de limão e
água suficiente para completar 300 mL é igual a:
a) 2
b) 3
c) 4
d) 6
e) 11
-8
-7
-5
pode-se afirmar que:
a) I, II, III e IV são soluções ácidas.
b) somente II é uma solução básica.
c) somente I, III e IV são soluções ácidas.
d) somente I, II e III são soluções básicas.
e) somente III é uma solução básica.
+
02. (CEETEPS – SP) A concentração de íons H (aq) de
-5
-1
uma certa solução aquosa é 2,0 x 10 mol.L , a 25
o
C. Sendo assim, nessa mesma solução a
-1
concentração de íons OH (aq), em mol.L , deve ser:
-10
a) 5,0 x 10
-10
b) 2,0 x 10
08. (Fuvest – SP) A auto-ionização da água é uma
reação endotérmica. Um estudante mediu o pH da
o
água recém-destilada, isenta de CO2 e a 50 C,
encontrado o valor 6,6. Desconfiado de que o
aparelho de medida estivesse com defeito, pois
esperava o valor 7,0, consultou um colega que fez
as seguintes afirmações:
I. O seu valor (6,6) pode estar correto, pois 7,0 é o
o
pH da água pura, porém a 25 C.
II. A aplicação do princípio de Le Chatelier ao
equilíbrio da ionização da água justifica que,
com o aumento da temperatura, aumente a
+
concentração de H .
III. Na água, o pH é tanto menor quanto maior a
+
concentração de H .
Está correto o que se afirma:
a) somente em I.
b) somente em II.
c) somente em III.
d) somente em I e II.
e) em I, II e III.
07. (PUC-MG) Misturando-se 100 mL de suco de laranja
+
cuja [H ] = 0,6 mol/l com 200 mL de suco de laranja
+
cuja [H ] = 0,3 mol/L, não se obtém:
+
a) uma solução onde [H ] = 0,4 mol/L.
b) uma solução completamente neutra.
c) uma solução de acidez intermediária.
+
d) uma solução menos ácida do que a de [H ] = 0,6
mol/L.
+
e) uma solução mais ácida do que a de [H ] = 0,3
mol/L.
08. (UFMG) A tabela mostra o pH característico de
alguns sistemas.
Sistema
Vinagre
Suco de laranja
Suco de tomate
Saliva
Leite
Sangue
Clara de ovo
TESTES DE VESTIBULAR
01. (FUVEST-SP) Observe os líquidos da tabela:
+
Leite
Água do mar
Coca-Cola
Café preparado
Lágrima
Água de lavanderia
[H ]
-7
1,0 . 10
-8
1,0 . 10
-3
1,0 . 10
-5
1,0 . 10
-7
1,0 . 10
-12
1,0 . 10
-
[OH ]
-7
1,0 . 10
-6
1,0 . 10
-11
1,0 . 10
-9
1,0 . 10
-7
1,0 . 10
-2
1,0 . 10
Sobre esses sistemas, pode-se afirmar que:
a) clara de ovo é o sistema menos ácido.
b) sangue é o líquido mais próximo da neutralidade.
c) suco de laranja é 1,5 vez mais ácido do que a
saliva.
d) suco de tomate é duas vezes menos ácido do que
o vinagre.
e) todos os líquidos da tabela são ácidos.
Tem caráter ácido apenas:
a) o leite e a lágrima.
b) a água de lavanderia.
c) o café preparado e a Coca-Cola.
d) a água do mar e a água de lavanderia.
e) a Coca-Cola.
+
-2
02. Calcular, a 25°C, a [H ] de uma solução 2 x 10
mol/L de HCℓ, sabendo que o ácido está totalmente
ionizado.
-1
03. A 25°C, em uma solução aquosa 1 x 10 mol/L, o
+
ácido acético está 1% ionizado. Calcular a [H ] desta
solução.
04. A 25°C, em uma solução aquosa 0,5 mol/L, o grau
de ionização do hidróxido de amônio, NH4OH, é 2 x
-4
x 10 .
+
Calcular a [OH ] e a [H ] desta solução.
-
+
05. Calcular a [OH ] e a [H ] de uma solução aquosa 5 x
-2
x 10 mol/L de NaOH, a 25°C, sabendo que a base
está totalmente dissociada.
+
pH
3,0
4,0
5,0
6,0
6,8
7,4
8,0
09. (PUCCAMP-SP) Considere as seguintes amostras:
I. Vinagre
II. Água destilada
III. Leite de magnésia
Comparando-se os valores de pH das amostras,
obtém-se a seqüência:
a) pHI > pHII > pHIII
b) pHI = pHII > pHIII
c) pHII > pHIII > pHI
d) pHIII > pHII > pHI
e) pHIII = pHI > pHII
10. (UFMG) A água do mar tem pH aproximadamente
igual a 8. Todas as afirmativas sobre a água do mar
estão corretas, exceto:
+
a) Apresenta uma concentração de H (aq) igual a 8
mol/L.
b) Colore de vermelho uma solução de fenolftaleína.
+
c) Contém cem vezes mais íons OH do que íons H .
d) É básica.
e) É eletricamente neutra.
-6
06. (CEFET-PR) Uma solução aquosa A tem [H ] = 10
-6
mol/L e outra B, tem [OH ] = 10 mol/L. A razão
+
entre as concentrações de H das soluções A e B é
igual a:
a) zero
12
b) 1,0 . 10
c) 1,0
2
d) 1,0 . 10
-2
e) 1,0 . 10
11. (UFRS) As leis de proteção ambiental de certas
cidades não permitem o lançamento em rios, entre
outros, de efluentes com pH inferior a 5,0 ou superior
a 9,0.
No que se refere à acidez, os efluentes aquosos das
indústrias X, Y e Z apresentam as seguintes
concentrações:
Indústria
X
Y
Concentração no
efluente
-3
+
10 mol/L de H
-4
+
10 mol/L de H
Z
-6
10 mol/L de OH
-
Poderiam ser lançados em rios, sem tratamento
prévio, apenas os efluentes de:
a) X
b) Y
c) Z
d) X e Y
e) Y e Z
12. (FUND. C. CHAGAS-BA) Para corrigir a acidez do
solo é comum a utilização da cal extinta, Ca(OH) 2.
Com esse procedimento provoca-se no solo:
a) aumento de pH, uma vez que a cal extinta é ácida.
b) aumento de pH, uma vez que a cal extinta é
básica.
c) diminuição de pH, uma vez que a cal extinta é
ácida.
d) aumento de pOH, uma vez que a cal extinta é
básica.
e) diminuição de pOH, uma vez que a cal extinta é
ácida.
13. (UFMG) Tem-se notado um abaixamento de pH da
água das chuvas em muitas regiões do mundo. Uma
das causas é a emissão de dióxido de enxofre, SO 2,
feita por centenas de indústrias, o qual é oxidado e
hidrolisado na atmosfera. Em relação ao exposto,
qual das seguintes alternativas é errada?
a) Uma chuva com pH=4,6 é dez vezes mais ácida
do que uma chuva com pH=5,6
b) A oxidação e a hidrólise do SO2 na atmosfera
levam à formação de ácido sulfúrico.
c) Ácidos fortes podem dissociar-se na água das
chuvas, abaixando seu pH.
d) O abaixamento do pH da água das chuvas
significa diminuição na concentração dos íons
hidrogênio.
e) Estátuas e monumentos de mármore, CaCO3,
expostos a chuvas de baixo pH, podem ser
eventualmente destruídos.
14. (UnB-DF) O pH padrão da água da chuva em áreas
não-poluídas é 5,6. Chuvas com pH abaixo desse
valor são denominadas “chuvas ácidas” e causam
sérios problemas ambientais. Sobre esse assunto,
aponte os itens corretos:
01) As chuvas ácidas destroem monumentos,
florestas e causam a mortalidade de peixes.
02) O dióxido de enxofre proveniente das caldeiras e
fornos das indústrias é um dos principais
responsáveis pelas chuvas ácidas.
04) Água de chuva em áreas não-poluídas é mais
ácida do que água pura.
08) A água da chuva que apresenta concentração de
+
-2
H igual a 10 mol/L não é considerada chuva
ácida.
16) A concentração de dióxido de carbono na
atmosfera não influi no pH da chuva.
15. (UFPE) Em três recipientes A, B e C estão contidas
soluções ácidas desconhecidas, de concentração 0,1
mol/L.
Medindo o pH das três soluções com papel indicador
universal, obtiveram-se os seguintes valores,
respectivamente: pH=5,0, pH=3,5 e pH=1,0. Aponte
as alternativas corretas:
01) No frasco A está contido um ácido fraco.
02) O Ka do ácido A é maior que o Ka do ácido B.
04) O ácido B conduz melhor a corrente elétrica do
que o ácido C.
08) O ácido C está completamente ionizado.
+
-1
16) A concentração de H no ácido C é 10 mol/L.
16. (FCMSC-SP) Tem-se uma solução em que a
-3
concentração hidrogeniônica é 4,3 x 10 mol/L. Seu
pH será: (log 4,3 = 0,63)
a) 4,0
b) 3,7
c) 2,37
d) 6,27
e) 1,27
17. (UNIMOGI-SP) O pH de uma solução de ácido
clorídrico de concentração igual a 0,001 mol/L é igual
a:
a) 3
b) 4
c) 5
d) 6
e) 11
18. (PUC-RJ) Qual é o pH de uma solução de hidróxido
de sódio 0,1 mol/L (a 25°C)?
-14
(Dado: Kw = 1 . 10 a 25°C)
a) 0
b) 1
c) 13
d) 14
e) 0,1
19. (PUC-PR) Uma solução de monobase apresenta
concentração de íons hidróxido igual a 17 mg/L. Qual
é o pH dessa solução?
(Massa molar do OH = 17 g/mol)
a) 3,0
b) 5,0
c) 7,0
d) 9,0
e) 11,0
20. (PUCCAMP-SP) Em São Paulo, a Cetesb constatou,
em 1986, uma “chuva ácida” de pH = =5. Isto
+
significa uma concentração de íons H da ordem de:
-5
a) 10 mol/L
-1
b) 5 . 10 mol/L
-5
c) 5 . 10 mol/L
-2
d) 5 . 10 mol/L
e) 5 mol/L
21. (CESGRANRIO-RJ) Constatou-se que uma amostra
de suco de laranja possui pH = 4. As concentrações
+
de H e OH no suco são, respectivamente:
-2
-12
a) 10 e 10
-4
-10
b) 10 e 10
-6
-8
c) 10 e 10
-7
-7
d) 10 e 10
-8
-6
e) 10 e 10
22. (FM POUSO ALEGRE-MG) Uma solução de ácido
acético (CH3COOH) é preparada de tal modo que
seja 0,004 mol/L. O pH dessa solução aquosa,
sabendo que o ácido se encontra 25% ionizado, está
mais bem representado pela opção:
a) 1
b) 2
c) 3
d) 4
e) 5
29. (FCMSC-SP) A 45°C, o produto iônico da água é
-14
igual a 4,0 x 10 . A essa temperatura, o valor de
+
[H ] de uma solução aquosa neutra é:
-7
a) 0,6 x 10
-7
b) 2,0 x 10
-7
c) 4,0 x 10
-14
d) 2,0 x 10
-14
e) 4,0 x 10
23. (UNIP-SP) O ácido láctico é um monoácido presente
em músculos doloridos depois de exercícios
vigorosos. O pH de uma solução 0,100 mol/L de
ácido láctico 4% ionizado é: (log 4 = 0,6)
a) 11,6
b) 2,7
c) 2,4
d) 3,3
e) 4,8
30. (ITA-SP) A 60°C, o produto iônico da água, [H ] x
-13
x [OH ], é igual a 1,0 x 10 . Em relação a soluções
aquosas, nesta temperatura, assinale as afirmações
corretas:
01) Soluções ácidas são aquelas que têm pH < 6,5.
02) Soluções neutras têm pH = 6,5.
04) Soluções básicas têm pH > 6,5.
08) pH + pOH tem que ser igual a 13,0.
16) Solução com pH = 14 é impossível de ser obtida.
24. (PUC-PR) O pH de uma solução 0,25 mol/L de uma
monobase que está 0,4% dissociada é:
a) 13
b) 11
c) 9
d) 7
e) 5
25. (CESGRANRIO-RJ) O HF é um ácido cuja
-4
constante de dissociação é Ka = 4,0 x 10 a 25°C.
Assinale a opção que indica, aproximadamente, o
valor do pH de uma solução 0,25 mol/L desse ácido
a 25°C.
a) 1
b) 1,6
c) 2
d) 2,5
e) 4
26. (FEI-SP) Determine o grau de ionização de uma
monobase em solução 0,5 mol/L, sabendo que o pH
dessa solução é igual a 10:
a) 0,2%
b) 0,02%
c) 0,5%
d) 0,8%
e) 1%
e) 3,70 e 10,30
+
HIDRÓLISE DE ÍONS
Hidrólise de um íon é a reação entre este íon e a
água.
• Hidrólise de ânions
A hidrólise de um ânion pode ser representada pela
equação:
H+
A- + HOH
ânion
HA + OHácido
A reação de hidrólise de um ânion ocorre quando o
ácido formado for um ácido fraco.
-
Devido à formação de íons OH , a solução resultante
é básica (pH > 7).
Exemplos:
-
27. (UFGO) Na água de um aquário, a concentração de
um monoácido produzido pela decomposição de
-4
bactérias é 10 mol/L e sua constante de ionização
-8
Ka = 1,0 x 10 . O pH da água do aquário é:
a) 2
b) 3
c) 4
d) 5
e) 6
Hidrólise do ânion cianeto, CN :
CN + HOH
HCN + OH
ácido
fraco
solução
básica
-
Hidrólise do ânion bicarbonato, HCO3 :
HCO3 + HOH
H2CO3 + OH
ácido
fraco
solução
básica
• Hidrólise de cátions
-4
28. (FESP-PE) Uma solução 10 mol/L de ácido acético
a 25°C está 33,5% ionizada. Seus pH e pOH são,
respectivamente: (log 3,35 = 0,53)
a) 4,47 e 9,53
b) 4,47 e 18,47
c) 10,30 e 3,70
d) 9,53 e 4,47
A hidrólise de um cátion pode ser representada
pela equação:
+
A produção de cátions H torna a solução ácida
(pH < 7).
Este comportamento é característico de sais
formados por cátions de bases fracas e ânions de
ácidos fortes.
OH-
C+ + HOH
COH + H+
cátion
base
A hidrólise de um cátion ocorre quando a base
formada for uma base fraca.
+
Devido à formação de íons H , a solução resultante
é ácida (pH < 7).
+
Exemplo 3: Bicarbonato de amônio, (NH4) (HCO3)
-
(NH4) (HCO3) NH4 + HCO3
+
-
+
-
+
O cátion NH4 hidrolisa. A base formada é fraca.
Exemplos:
+
NH4 + HOH
+
Hidrólise do cátion amônio, NH4 :
+
+
NH4 + HOH
NH4OH + H
base
fraca
O ânion HCO3 hidrolisa. O ácido formado é fraco.
HCO3 + HOH
H2CO3 + OH
Devido ocorrer a hidrólise do cátion e do ânion, o
pH da solução resultante será determinado através das
constantes de ionização do ácido fraco (Ka) e da base
fraca (Kb). Se:
+
Hidrólise do cátion prata, Ag :
+
+
Ag + HOH
AgOH + H
solução
ácida
Ka > Kb solução ácida (pH < 7)
Ka < Kb solução básica (pH > 7)
Ka = Kb solução neutra (pH = 7)
• Hidrólise de sais
+
+
-
solução
ácida
base
fraca
NH4OH + H
-
Seja um sal C A . Em água ele sofre dissociação
iônica:
+ +
C A C + A
Uma vez dissociado, poderá:
• ocorrer a hidrólise do ânion A ,
+
• ocorrer a hidrólise do cátion C ,
• ocorrer a hidrólise de ambos os íons,
• não ocorrer a hidrólise de nenhum dos íons.
+
-
Exemplo 1: Bicarbonato de sódio, Na (HCO3) :
Na (HCO3) Na + HCO3
+
-
+
-
+
O cátion Na
não hidrolisa, pois a base
correspondente é forte.
O ânion HCO3 hidrolisa. O ácido formado é fraco.
-
HCO3 + HOH
H2CO3 + OH
-
Este comportamento é característico de sais
formados por cátions de bases fracas e ânions de
ácidos fracos.
+
-
Exemplo 4: Cloreto de sódio, Na Cℓ :
Na Cℓ Na + Cℓ
+
-
+
-
+
O cátion Na não hidrolisa. A base correspondente
é forte.
O ânion Cl não hidrolisa. O ácido correspondente é
forte.
Como não ocorre a hidrólise de íons, a solução
resultante é neutra (pH = 7).
Este comportamento é característico de sais
formados por cátions de bases fortes e ânions de ácidos
fortes.
-
A produção de ânions OH torna a solução básica
(pH>7).
Este comportamento é característico de sais
formados por cátions de bases fortes e ânions de ácidos
fracos.
+
-
Exemplo 2: Cloreto de amônio, NH4 Cℓ .
+
NH4 Cℓ
-
NH4 + Cℓ
+
-
+
NH4OH + H
Solução-tampão, solução buffer ou solução
reguladora é toda solução que tem por finalidade evitar
variações bruscas de pH quando à mesma se adiciona
um ácido forte ou uma base forte.
Uma solução-tampão é constituída por um ácido
fraco (HA) e seu sal (BA) ou por uma base fraca (BOH)
e seu sal (BA).
-
O ânion Cl não hidrolisa, pois o ácido
correspondente é forte.
+
O cátion NH4 hidrolisa. A base formada é fraca.
NH4 + HOH
SOLUÇÃO TAMPÃO
+
Exemplos
Solução de ácido acético (HAc) e acetato de sódio
(NaAc).
Solução de hidróxido de amônio (NH4OH) e
cloreto de amônio (NH4Cℓ).
Seja o tampão HAc/NaAC.
[ácido] = 0,10 mol/L,
Em solução o HAc (ácido fraco) está pouco
ionizado e o NaAc (eletrólito forte) está totalmente
dissociado.
HAc ⇄ H + Ac
+
+
-
NaAc → Na = Ac
-
tem-se:
pH 2,85 log
[0,15]
2,85 log1,5
[0,10]
pH = 2,85 + 0,18 = 3,03
Ao se adicionar ácido forte à esta solução, o
equilíbrio iônico do HAc sofrerá deslocamento para a
+
esquerda, consumindo o H adicionado, o que impede a
variação brusca de pH.
EXERCÍCIOS DE SALA
+
Ao se adicionar base forte à esta solução, o H do
equilíbrio iônico do HAc irá consumir o OH adicionado
+
+
(H + OH → H2O). Para repor o H consumido junto
com o OH , o equilíbrio sofrerá deslocamento para a
direita, o que impede a variação brusca do pH.
A ação da solução-tampão tem limites. A adição
de quantidades excessivas de ácido ou base destruirá o
efeito tampão.
Para se calcular o pH de uma solução tampão,
pode-se demonstrar que:
• para solução-tampão de um ácido fraco e seu
sal,
pH pK a log
[ânion do sal]
[ácido]
• para solução-tampão de uma base fraca e seu
sal,
pH pKw pK b log
[cátion do sal]
[base]
Onde pKa = −log Ka, pKb = −log Kb e pKw = −log
Kw.
Estas fórmulas são conhecidas como equações
de Henderson-Hasselbach.
Exemplo:
Sabendo que a constante de ionização (Ka) do
o
-3
ácido cloroacético, a 25 C, é 1,4 x 10 , calcular o pH
de uma solução-tampão contendo ácido cloroacético
0,10 mol/L e cloroacetato de sódio 0,15 mol/L.
Dados: log 1,4 = 0,15; log 1,5 = 0,18.
01. Nitrato de potássio e nitrato de amônio são dois
sais usados na fabricação de fertilizantes. O que se
pode afirmar sobre o caráter (ácido, básico, neutro)
das soluções aquosas de cada um desse sais?
_________________________________________
_________________________________________
_________________________________________
_________________________________________
_________________________________________
_________________________________________
02. (FEI – SP) Os compostos cianeto de sódio (NaCN),
cloreto de zinco (ZnCℓ2), sulfato de sódio (Na2SO4)
e cloreto de amônio (NH4Cℓ), quando dissolvidos
em água, tornam o meio respectivamente:
a) básico, ácido, ácido, neutro.
b) ácido, básico, neutro, ácido.
c) básico, neutro, ácido, ácido.
d) básico, ácido, neutro, ácido.
e) ácido, neutro, básico, básico.
03. (VUNESP) Quando se adiciona o indicador
fenolftaleína a uma solução aquosa incolor de uma
base de Arrhenius, a solução fica vermelha. Se a
fenolftaleína for adionada a uma solução aquosa de
ácido de Arrhenius, a solução continua incolor.
Quando se dissolve cianeto de sódio em água, a
solução fica vermelha após a adição de
fenolftaleína. Se a fenolftaleína for adicionada a
uma solução aquosa de cloreto de amônio, a
solução continua incolor.
a) Explique o que acontece no caso do cianeto de
sódio, utilizando equações químicas.
______________________________________
______________________________________
______________________________________
______________________________________
______________________________________
______________________________________
______________________________________
______________________________________
Resolução:
Utilizando a expressão
pH pK a log
[ânion do sal]
[ácido]
onde:
-3
pKa = -log Ka = -log (1,4 x 10 ) = 2,85,
[ânion do sal] = [cloroacetato] = 0,15 mol/L,
b) Explique o que acontece no caso do cloreto de
amônio, utilizando equações químicas.
______________________________________
______________________________________
______________________________________
______________________________________
______________________________________
______________________________________
______________________________________
______________________________________
04. (UEPG – PR) No interior das células de nosso
organismo ocorre, a todo instante, um número
incontável de reações químicas. A maioria dos
fluídos biológicos onde as reações ocorrem são
meios tamponados. Sobre os tampões e o efeito
que exercem, assinale o que for correto.
01. O efeito tampão age aumentando a
solubilidade das enzimas em meio aquoso.
02. Os pares H2CO3/NaHCO3 e NH4OH/NH4Cℓ são
exemplos de substâncias que agem como
tampão.
04. O efeito tampão impede variações bruscas de
+
pH, quando ocorre a adição de íons H ou OH
no meio.
08. Os meios tamponados são neutros e
apresentam pH igual a 7.
16. Os tampões mantêm constante o volume de
solvente no meio, o que impede as variações
de concentração.
05. (UFMG) Considere duas soluções aquosa diluídas,
I e II, ambas de pH = 5. A solução I é tampão e a II
não.
Um béquer contém 100 mL da solução I e um
segundo béquer contém 100 mL da solução II. A
cada uma dessas soluções adicionam-se 10 mL de
NaOH aquoso concentrado.
Assinale a alternativa que apresenta corretamente
as variações de pH das soluções I e II, após a
adição de NaOH(aq).
a) O pH de ambas irá aumentar e o pH de I será
maior do que o de II.
b) O pH de ambas irá aumentar e o pH de I será
igual ao de II.
c) O pH de ambas irá diminuir e o pH de I será
igual ao de II.
d) O pH de ambas irá aumentar e o pH de I será
menor do que o de II.
e) O pH de ambas irá diminuir e o pH de I será
maior do que o de II.
TESTES DE VESTIBULAR
01. (UFSC) O carbonato monohidrogenado de sódio é
conhecido como bicarbonato e sua dissolução
aquosa tem, como característica básica, neutralizar a
acidez estomacal.
Esta característica deve-se ao fato de que, ao se
dissolver em água, o bicarbonato:
01) permanece inalterado.
02) apresenta reação de hidrólise.
04) elimina próton.
08) desprende gás carbônico.
16) forma íons OH .
+
32) permanece em íon Na e HCO3 .
02. (ITA-SP) Numa solução aquosa de acetato de sódio
há:
+
a) mais íons H do que íons OH .
+
b) mais íons OH do que íons H .
+
-
c) o mesmo número de íons H e íons OH .
+
d) não há íons H nem íons OH .
+
e) o mesmo número de íons Na e íons CH3COO .
03. (UFRGS) A única das espécies que, ao ser
dissolvida em água, resulta em uma solução com pH
menor que o do solvente puro é:
a) NaCl
b) Na2CO3
c) CaCl2
d) NH3
e) (NH4)2SO4
04. (FUVEST-SP) Carbonato de sódio, quando colocado
em água, a 25°C, se dissolve:
+
Na2CO3(s) + H2O(l) HCO3 (aq) + 2 Na (aq) + X
X e o pH da solução resultante devem ser:
a) CO2, maior que 7.
b) OH (aq), maior que 7.
+
c) H (aq),igual a 7.
d) CO2, igual a 7.
e) OH (aq), menor que 7.
05. (CEFET-MG) A seguir, estão relacionados alguns
produtos comerciais/industriais e as substâncias
ativas dos mesmos:
Produtos comerciais/
Substâncias
industriais
ativas
mármore
carbonato de cálcio
detergente
amônia (amoníaco)
solução de bateria
ácido sulfúrico
leite de magnésia
hidróxido de magnésio
fertilizante
nitrato de potássio
Em relação a esses compostos, é incorreto afirmar
que:
a) o detergente amoniacal é ácido.
b) a solução de bateria tem pH<7.
c) o nitrato de potássio é um sal neutro.
d) o leite de magnésia é uma solução básica.
e) o mármore reage com HCl, liberando CO2.
06. (FM POUSO ALEGRE-MG) Dos sais abaixo, indique
aquele que em solução aquosa apresenta reação
ácida:
a) KCN
b) NaCl
c) Na2CO3
d) NH4Br
e) K2SO4
07. (UFRGS) Preparam-se 5 soluções 1 mol/L das
seguintes substâncias:
sol. 1
CH3COOH
sol. 2
NaCℓ
sol. 3
NH4OH
sol. 4
HCℓ
sol. 5
NaOH
Pode-se prever que o pH das soluções terá valores
tais que permitem que se escreva:
a) pH sol. 1 > pH sol. 2 > pH sol. 3 > pH sol. 4 > pH
sol. 5
b) pH sol. 5 > pH sol. 4 > pH sol. 3 > pH sol. 2 > pH
sol. 1
c) pH sol. 1 > pH sol. 4 > pH sol. 3 > pH sol. 2 > pH
sol. 5
d) pH sol. 5 > pH sol. 3 > pH sol. 2 > pH sol. 1 > pH
sol. 4
e) pH sol. 4 > pH sol. 1 > pH sol. 2 > pH sol. 3 > pH
sol. 5
Ag+(aq)
Cl-(aq)
solução saturada
de AgCl
AgCl(s)
08. (UFRGS) O soluto que em água forma uma solução
com pH maior que 7,0 é o:
a) nitrato de amônio
b) gás carbônico
c) vinagre
d) cloreto de sódio
e) sabão
09. (MACKENZIE - SP) Entre as soluções aquosas das
seguintes substâncias:
I. acetato de sódio
II. cianeto de potássio
III. fenol
IV. cloreto de amônio
apresentam pH maior que 7:
a) I e II
b) II e III
c) I, II e IV
d) II, III e IV
e) I, III e IV
10. (UFRGS) As soluções aquosas de três substâncias
A, B e C apresentam os seguintes valores de pH;
Substância
A
B
C
a)
b)
c)
d)
e)
Substância
HCℓ
CaO
KOH
SO3
H2SO4
Kc =
[Ag+] . [Cl-]
[AgCl]
Mas a [AgCℓ] é constante, podendo ser incorporada
no valor de Kc:
+
-
Kc . [AgCℓ] = [Ag ] . [Cℓ ]
O produto (Kc . [AgCℓ]) é uma outra constante
denominada produto de solubilidade e simbolizada
por Kps.
Então:
+
-
Kps = [Ag ] . [Cℓ ]
Para uma substância genérica AxBy, que se
dissocia de acordo com a equação:
AxBy(s)
y+
xA
(aq)
+ yB
x(aq)
o Kps é dado pela expressão:
pH
2,7
6,8
10,4
y+ x
x- y
Kps = [A ] . [B ]
Das substâncias relacionadas a seguir, indique o
grupo que poderia ser enquadrado nos valores de
pH anteriormente citados:
Grupo
A constante de equilíbrio para este sistema é dada
pela expressão:
Substância
Substância
K2O
K2SO4
CO2
NaCℓ
NaHSO4
NaOH
HNO3
H2S
Na2CO3
Ba(OH)2
Exemplos:
• Solução saturada de sulfato de bário:
BaSO4(s)
2+
Ba
2-
(aq)
+ SO4
2+
(aq)
2-
Kps = [Ba ] . [SO4 ]
• Solução saturada de fosfato de cálcio:
PRODUTO DE SOLUBILIDADE (Kps ou PS)
Quando um sólido é adicionado a um solvente, ele
se dissolve até o limite definido pelo seu coeficiente de
solubilidade. A partir desse limite ele não mais se
dissolve, permanecendo como sólido no fundo do
recipiente que o contém formando o denominado corpo
de fundo.
Considerando o cloreto de prata, que ao se
dissolver, sofre dissociação de acordo com a equação:
AgCℓ(s)
+
Ag
-
(aq)
+ Cℓ (aq)
Experimentalmente, verifica-se que um sistema
+
como esse está em equilíbrio. Continuamente, íons Ag
e Cl passam da solução para o corpo de fundo e igual
quantidade de AgCl passa do corpo de fundo para a
solução.
Ca3(PO4)2(s)
3 Ca
2+ 3
2+
3-
(aq)
+ 2 PO4
(aq)
3- 2
Kps = [Ca ] . [PO4 ]
Observações:
• Só se aplica o produto de solubilidade às
soluções saturadas.
• Para uma dada substância, o Kps só varia com a
temperatura.
• Quanto maior for o Kps de uma substância, maior
será sua solubilidade.
• Em uma solução saturada, o produto das
concentrações molares dos íons dissolvidos (cada uma
delas elevada à potência igual ao seu coeficiente) é
exatamente igual ao Kps.
• Quando, em uma solução, o produto das
concentrações molares dos íons dissolvidos (cada uma
delas elevada à potência igual ao seu coeficiente) for
superior ao Kps, ocorrerá precipitação da substância.
• Efeito do íon comum sobre a solubilidade
Se, à solução saturada de uma substância AxBy,
juntarmos uma segunda substância que possua um íon
comum com AxBy, esta segunda substância provocará
precipitação de AxBy como conseqüência do Principio
de Le Chatelier.
Consideremos, como exemplo,
saturada de AgCl, com corpo de fundo.
+
AgCℓ(s)
Ag
uma
solução
-
+ Cℓ (aq)
(aq)
Exemplo 1:
A solubilidade do iodato de chumbo II, Pb(IO 3)2, a
-5
25°C, é 4,0 . 10 mol/L. Calcular o Kps deste sal, na
temperatura indicada.
Resolução:
2+
Pb(IO3)2
Pb
-
+ 2 IO3 (aq)
(aq)
Observando a proporcionalidade fornecida pelos
coeficientes da equação de dissociação do sal (1:1:2), a
-5
-5
dissolução de 4,5.10 mol/L de Pb(IO3)2 produz 4,5.10
2+
-5
mol/L de Pb e 9,0.10 mol/L de IO3 . Portanto, no
equilíbrio:
2+
-5
-
-5
[Pb ] = 4,5.10 mol/L e [IO3 ] = 9,0.10 mol/L.
Calculando o Kps, tem-se:
Ag+(aq)
2+
- 2
Kps = [Pb ] . [IO3 ]
Cl-(aq)
-5
-5 2
Kps = (4,5 . 10 ) . (9,0 . 10 )
Kps 3,65 . 10
-13
AgCl(s)
Adicionemos a esta solução o sal NaCℓ, o qual se
dissocia completamente.
NaCℓ(s) Na
+
-
(aq)
+ Cℓ (aq)
Exemplo 2:
A 25°C, o produto de solubilidade do carbonato de
-9
bário, BaCO3, é 4,9 . 10 . Calcular a solubilidade deste
sal naquela temperatura.
-
Com isso, aumenta-se a [Cl ] na solução.
Resolução:
Na+
Cl-
Ag+(aq)
Cl-(aq)
(aq)
2+
Ba
2-
(aq)
+ CO3
(aq)
(aq)
AgCl(s)
Para minimizar o aumento na concentração de íon
Cℓ , o equilíbrio será deslocado no sentido do processo
que forma AgCl(s). Como conseqüência, ocorre a
precipitação do AgCl(s), acarretando, portanto, uma
diminuição em sua solubilidade.
Na+
Cl-
Ag+(aq)
Cl-(aq)
(aq)
BaCO3(s)
(aq)
AgCl(s)
Um raciocínio equivalente pode ser feito a partir da
+
expressão: Kps = [Ag ] . [Cℓ ].
Como o valor de Kps é constante, um aumento da
+
[Cℓ ] implica uma diminuição da [Ag ]. Uma diminuição
+
da [Ag ] acontecerá pela precipitação de AgCℓ(s).
Note que, pelo efeito do íon comum, a solubilidade
de uma dada substância é diminuída, mas seu Kps não
é alterado.
• Cálculos envolvendo Kps
Vamos estabelecer que a solubilidade do BaCO3(s)
é X mol/L.
Observando a proporcionalidade fornecida pelos
coeficientes da equação de dissociação do sal (1:1:1), a
dissolução de X mol/L de BaCO3 produz X mol/L de
2+
22+
Ba e X mol/L de CO3 . Portanto, no equilíbrio, [Ba ] =
2
[CO3 ] = X mol/L.
Aplicando a expressão do Kps, tem-se:
2+
2-
Kps = [Ba ] . [CO3 ]
-9
4,9 x 10 = X . X
-5
X 4,9 . 10 9 = 7,0 . 10
EXERCÍCIOS DE SALA
01. (Fuvest – SP) Em determinada temperatura, a
solubilidade do sulfato de prata (Ag2SO4) em água
-2
-1
é 2,0 x 10 mol.L . Qual o valor do produto de
solubilidade (Kps) desse sal, à mesma temperatura?
02. (Fuvest – SP) O produto de solubilidade do sulfato
-8
o
de chumbo é 2,25 x 10 , a 25 C. Calcule a
-1
solubilidade do sal, em g.L , nesta temperatura.
-1
(Massa molar do PbSO4 = 303 g.mol )
-5
a) 1,1 . 10
-5
b) 2,0 . 10
-10
c) 2,0 . 10
-10
d) 1,21 . 10
e) 1,1
TESTES DE VESTIBULAR
01. (FUVEST-SP) O equilíbrio de dissolução do fosfato
de cálcio é representado por:
Ca3 (PO4)2(s)
2+
3 Ca
3-
(aq)
A
expressão
do
produto
correspondente é:
2+
3a) Kps = [3 Ca ] . [2 PO4 ]
2+ 2
3- 3
b) Kps = [Ca ] . [PO4 ]
2+
3c) Kps = [Ca ] . [PO4 ]
2+ 3
3- 2
d) Kps = [Ca ] . [PO4 ]
2+
3e) Kps = [3 Ca ] . [ PO4 ]
+ 2 PO4
de
(aq)
solubilidade
02. (CESCEA-SP) Fosfato de prata é parcialmente
solúvel em água. Seu produto de solubilidade é dado
por:
+
3a) [Ag ] . [PO4 ]
+
3b) 3[Ag ] . [PO4 ]
+
3c) [Ag ] . 3[PO4 ]
+ 3
3d) [Ag ] / [PO4 ]
+ 3
3e) [Ag ] . [PO4 ]
03. (FURRN) Com base na tabela de produto de
solubilidade abaixo:
Substância
Ca(OH)2
AgCℓ
Mn(OH)2
CdS
Ag2S
P.S.
-6
4,0 . 10
-10
2,6 . 10
-14
3,5 . 10
-27
8,0 . 10
-51
3,2 . 10
a substância mais solúvel é:
a) Ca(OH)2
b) AgCℓ
c) Mn(OH)2
d) CdS
e) Ag2S
04. (FUC-MT) Com base nos valores do produto de
solubilidade (Kps) de sais em água, da tabela,
podemos afirmar que o sal mais solúvel é:
Sal
CaSO4
PbI2
AgCℓ
AgBr
ZnS
Kps (25°C)
-5
2,4 . 10
-98,3 . 10
-10
1,8 . 10
-13
5,0 . 10
-20
1,0 . 10
a) CaSO4
b) PbI2
c) AgCℓ
d) AgBr
e) ZnS
05. (PUC-PR) A solubilidade do cloreto de prata, AgCℓ,
-5
é de 1,1 . 10 mol/L. O sal dissolvido é totalmente
dissociado. Seu Kps é:
06. (ITA-SP) Sabendo-se que a solubilidade em água, a
-2
0°C, do sulfato de prata, Ag2SO4, é 1,8 . 10 mol/L,
podemos concluir que o produto de solubilidade
desse sal, nesta temperatura, vale:
-4
a) 1,6 . 10
-4
b) 6,5 . 10
-3
c) 6,0 . 10
-2
d) 1,8 . 10
-5
e) 2,3 . 10
07. (FUVEST-SP) O produto de solubilidade do BaSO4
-10
vale 1,0 . 10 , a 25°C. Nessa temperatura, a
quantidade, em mols, de BaSO4 que se dissolve em
1 L de água pura é, aproximadamente:
10
a) 10
5
b) 10
-5
c) 10
-10
d) 10
-20
e) 10
08. (FEI-SP) Os sulfetos metálicos são encontrados em
grande quantidade na natureza. Sabendo-se que a
25°C o produto de solubilidade do sulfeto de zinco,
-23
ZnS, vale 1,3 . 10 , determine sua solubilidade, em
mol/l, nessa temperatura.
-12
a) 3,6 . 10
-8
b) 3,6 . 10
-5
c) 6,4 . 10
5
d) 3,49 . 10
4
e) 3,6 . 10
o
09. (CESGRANRIO-RJ) A solubilidade do AgCℓ a 18 C
é 0,0015 g/L. Sabendo-se que a sua massa molar é
143,5 g/mol, qual será o seu produto de solubilidade,
considerando-se a concentração iônica igual à
concentração molar?
-10
a) 1,0 . 10
-5
b) 1,0 . 10
-3
c) 1,5 . 10
-3
d) 3,0 . 10
-3
e) 6,0 . 10
10. (CESGRANRIO-RJ) Um sal, representado pela
o
-9
fórmula XY2, tem, a 25 C, Kps = 4 . 10 .
Assinale a opção que identifica a quantidade de íons
+
X e Y contidos em 500 mL da solução saturada
o
deste sal a 25 C.
+
mols X
mols Y
-9
-9
a) 2 . 10
4 . 10
-9
-9
b) 4 . 10
8 . 10
-9
-9
c) 8 . 10
4 . 10
-4
-3
d) 5 . 10
1 . 10
-3
-4
e) 1 . 10
5 . 10
11. (FUVEST-SP) À temperatura T, a reação
N2O4(g) ⇄ 2 NO2(g)
apresenta uma constante de equilíbrio Kc = 1,0.
Analise os dados abaixo, relativos a duas misturas
gasosas sob essa mesma temperatura, e decida em
qual delas os gases estão em equilíbrio. Indique os
cálculos que você utilizou.
Mistura
I
II
[NO2]
-1
1,0 x 10
-2
1,0 x 10
[N2O4]
-3
1,0 x 10
-4
1,0 x 10
12. (UFGO) 200 ml de solução de ácido acético contêm
3,0 g do ácido puro. Essa solução foi transferida
totalmente para um balão volumétrico aferido de 500
ml de capacidade. Em seguida, completou-se o
volume com água destilada até o traço de aferição.
Sabendo que, na solução preparada (500 ml), o
ácido acético está 1,3% ionizado, calcule sua
constante de ionização. (Massas molares, em g/mol:
H=1; C=12; O=16)
13. (UNICAMP-SP) A metilamina, H3C – NH2, proveniente da decomposição de certas proteínas e
responsável pelo desagradável cheiro de peixe, é
uma substância gasosa, solúvel em água. Em
soluções aquosas de metilamina ocorre o equilíbrio:
H3C–NH2(aq) + H2O(l) ⇄ H3C–NH3 (aq) + OH (aq)
a) O pH de uma solução aquosa de metilamina será
maior, menor ou igual a 7? Justifique sua resposta.
b) Por que o limão ou vinagre (soluções ácidas)
diminuem o cheiro de peixe?
+
-
14. (FUVEST-SP) Considere os seguintes equilíbrios:
+
Ag
+ Cℓ (aq) ⇄ AgCℓ(s)
-
(aq)
K = 6,0 x 10
9
Ag (aq) + I (aq) ⇄ AgI(s)
K = 1,0 x 10
a) Qual dos sais de prata é mais solúvel? Justifique.
+
b) Calcule a concentração de íons Ag (aq) numa
solução saturada de AgI.
+
-
16
15. (ENEM-MEC) Suponha que um agricultor esteja
interessado em fazer uma plantação de girassóis.
Procurando
informação,
leu
a
seguinte
reportagem:
Solo ácido não favorece plantio
Alguns cuidados devem ser tomados por quem
decide iniciar o cultivo de girassol. A oleaginosa
deve ser plantada em solos descompactados, com
pH acima de 5,2 (que indica menor acidez da
terra). Conforme as recomendações da Embrapa,
o agricultor deve colocar, por hectare, 40 kg a 60
kg de nitrogênio, 40 kg a 80 kg de potássio e 40
kg a 80 kg de fósforo.
O pH do solo, na região do agricultor, é de 4,8.
Dessa forma, o agricultor deverá fazer a
“calagem”.
(Folha de São Paulo, 25/09/1996)
Suponha que o agricultor vá fazer calagem
(aumento do pH do solo por adição de cal virgem
– CaO). De maneira simplificada, a diminuição da
acidez se dá pela interação da cal (CaO) com a
água presente no solo, gerando hidróxido de
+
cálcio (Ca(OH)2), que reage com os íons H (dos
ácidos), ocorrendo, então, a formação de água e
2+
deixando os íons Ca no solo.
Considere as seguintes equações:
I. CaO + 2 H2O → Ca(OH)3
II. CaO + H2O → Ca(OH)2
+
2+
III. Ca(OH)2 + 2 H → Ca + 2 H2O
+
IV. Ca(OH)2 + H → CaO + H2O
O processo de calagem descrito acima pode ser
representado pelas equações:
a) I e II
b) I e IV
c) II e III
d) II e IV
e) III e IV












