NOME:___________________________________________________________N.º____TURMAS 301
QUÍMICA - PROFESSOR LUIZ ANTÔNIO
AS FUNÇÕES ORGÂNICAS: GRUPOS FUNCIONAIS
Vimos que há uma enorme quantidade de compostos orgânicos. Existem muito
mais compostos orgânicos do que inorgânicos. Estudá-los individualmente é praticamente
impossível. Uma saída é agrupá-los de acordo com propriedades químicas semelhantes.
Cada um desses grupos é dito função orgânica. Estudos demonstram que tais
propriedades semelhantes são devidas a átomos ou grupos de átomos presentes na
molécula e são denominados grupos funcionais.
A função orgânica, considerada mais simples, formada exclusivamente por
átomos de carbono e hidrogênio é chamada hidrocarbonetos. Veja exemplos:
H
I
Ex.1:
H–C–H
I
H
metano
(gás dos pântanos)
H H
I I
Ex.2: H –C–C–H
I I
H H
etano
(componente do gás natural)
Por outro lado, se substituirmos um átomo de hidrogênio apenas por um grupo
chamado oxidrila (–OH), não temos mais a função hidrocarboneto e sim função álcool.
H
I
Ex.1:
H–C–H
I
OH
metanol
(álcool de madeira)
H H
I I
Ex.2: H –C–C–H
I I
H OH
etanol
(álcool comum)
Como se vê a raiz é a mesma (hidrocarbonetos) e perceberemos que as várias
funções orgânicas são obtidas da mesma forma. Isso reforça o que já havíamos estudado
a respeito da importância do petróleo (basicamente mistura de hidrocarbonetos) como a
principal fonte de compostos orgânicos.
Quanto aos hidrocarbonetos, queremos ressaltar ainda que, dependendo do tipo
de cadeia carbônica (saturada ou insaturada, cíclica ou acíclica), são divididos em
subclasses: alcanos, alcenos, alcinos, ciclanos, aromáticos.
2
Nos quadros que seguem, resumimos as principais funções orgânicas. Fique
atento aos grupos funcionais. São eles que caracterizam cada função orgânica. Como
sempre dizemos, não é preciso decorá-las, mas manuseá-las corretamente. Com a
prática, vamos gravando as mais importantes.
1. Funções não oxigenadas
2. Funções oxigenadas
3
3. Funções nitrogenadas
4. Funções sulfuradas
4
Existem compostos mais complexos que não apresentem único grupo funcional.
São compostos com funções mistas. A IUPAC recomenda, nesses casos, que uma das
funções seja considerada a principal. A preferência na escolha da função principal é a
seguinte:
Exemplos:
EXERCÍCIOS
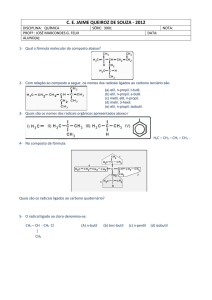
1. Dadas as fórmulas estruturais planas, escrevas as fórmulas moleculares:
a)
c)
b)
d)
5
2. Utilizando o quadro de funções, identifique grupo funcional e cada uma das
funções orgânicas a seguir:
FÓRMULA ESTRUTURAL PLANA
GRUPO
FUNCIONAL
FUNÇÃO
ORGÂNICA
6
Continuação . . .
7
AS FUNÇÕES ORGÂNICAS: NOMENCLATURA 1
A nomenclatura de todos os compostos orgânicos tem como base a
nomenclatura dos hidrocarbonetos. Será, portanto, a abordagem dessa última nosso
ponto de partida. Utilizaremos a nomenclatura oficial, isto é, aquela adotada pela IUPAC.
Isso não impede que, eventualmente façamos referência à nomenclatura usual de certos
compostos em especial presentes em nosso cotidiano.
Nos compostos ditos hidrocarbonetos, o nome é formado unindo-se três
segmentos:
PREFIXO + INFIXO + SUFIXO
O prefixo (antes) indica o número de carbonos presentes na molécula, ou melhor,
na cadeia principal (maior número de carbonos, lembra?), conforme tabela:
PREFIXO
Met
Et
Prop
But
Pent
Hex
Hept
Oct
Non
Dec
NÚMERO DE CABONOS
1
2
3
4
5
6
7
8
9
10
O infixo(intermediário) indica o tipo de ligação (simples, dupla, tripla) entre
átomos de carbono:
INTERMEDIÁRIO
an
en
in
LIGAÇÃO
simples
dupla
tripla
O sufixo (final) será o para hidrocarbonetos. Outros compostos serão abordados
oportunamente. Cada função orgânica tem seu sufixo próprio. Por exemplo, a função
álcool tem sufixo ol.
8
Exemplos:
1.
Este composto é chamado eteno. Por quê?
Prefixo: et, pois tem dois carbonos;
Intermediário: en, pois tem ligação dupla;
Sufixo: o, pois é hidrocarboneto.
ET + EN + O
=
ETENO
2.
Este composto é chamado etanol. Por quê?
Prefixo: et, pois tem dois carbonos;
Intermediário: an, pois tem ligação simples;
Sufixo: ol, pois é álcool.
ET + AN + OL
=
ETANOL
DETALHANDO A NOMENCLATURA DOS HIDROCARBONETOS
Já vimos, através do exemplo, que ao fazer a nomenclatura dos hidrocarbonetos,
basta unir prefixo + infixo + sufixo. Às vezes, porém, devido à complexidade, é preciso
detalhar essa nomenclatura. É que, com o aumento da cadeia carbônica, a posição da
insaturação (dupla ou tripla) deve ser indicada. Por exemplo, há duas possibilidades para
o buteno. Veja:
H
H H
I
I I
H – C = C – C – C–H 1-buteno
I
I
I I
H H H H
H
H
I
I
H – C – C = C – C–H 2-buteno
I
I
I
I
H H H H
Perceba que é indispensável indicar a posição da ligação dupla. O mesmo vale
para ligação tripla.
9
Outra abordagem necessária ao fazer a nomenclatura química dos
hidrocarbonetos (também válida para os outros compostos orgânicos) é indicar o tipo e
posição dos chamados radicais. Mas o que são esses radicais? São grupos orgânicos em
que pelo menos uma das ligações do carbono se encontra incompleta. Valem os mesmos
prefixos e infixos para os hidrocarbonetos, traçando-se apenas o sufixo “o” por “il”. Em
nosso presente estudo, apenas alguns radicais serão utilizados.
FÓRMULA
NOME
CH3 –
Metil
CH3–CH2–
Etil
CH3–CH2–CH2–
n–propil ou
normal-propil
CH3–CH2–CH2–CH2–
n-butil
fenil
Há muitos outros radicais orgânicos. Optamos pelos radicais acima por serem
mais comuns.
Com base no que foi dito, repare como fica a nomenclatura do alcano a seguir:
1
2
3 4
5
6
CH3–CH–CH–CH– CH2–CH3
I
I
I
CH3 CH2 CH3
I
CH3
2,4-dimetil-3-etil-hexano
10
Outro exemplo:
5
4
3
2
1
CH3–CH2–CH2–CH–CH3
I
CH3
2-metil-pentano
Repare que a contagem da cadeia começa pelo carbono mais próximo da
ramificação. Isso significa que 4-metil-pentano é incorreto.
Mais um exemplo. Agora, com insaturação:
6
5 4
3 2
1
CH3–CH–CH2–CH=CH –CH3
I
CH3
5-metil-2-hexeno
Nesse exemplo a contagem dos carbonos da cadeia principal também é feita da
esquerda para a direita. Prevalece a posição da ligação dupla sobre a posição da
ramificação. Note que a cadeia principal deverá conter a insaturação.
Por enquanto, é isso em termos de nomenclatura de hidrocarbonetos. No próximo
encontro veremos como é feita a nomenclatura dos demais compostos orgânicos. Iremos
notar que é muito semelhante ao que acabamos de estudar.
EXERCÍCIOS:
1. Escreva fórmulas dos radicais:
a) metil
b) n-butil
c) fenil
d) n-propil
e) terc-butil
11
2. Escreva as fórmulas dos compostos:
a) 2- metil-hexano
b) n-butano
c) 3-fenil-2-heptetno
d) 2-pentino
e) 3,4-dietil-nonano
3. Quais os nomes dos hidrocarbonetos?
a) CH3–CH2–CH2–CH=CH –CH2–CH3
I
CH3
b) CH3–CH2–CH2–CH–CH –CH2
I
CH3
c) CH2=CH–CH2–CH2–CH2–CH2–CH2–CH3
I
I
CH3
CH3
d) CH2–CH–CH=CH2
I
CH2
I
CH3
e) CH2–CH–CH=CH2–CH2–CH3
I
I
CH2
CH3
I
CH3