Aula: 04
Temática: Ozônio e Nitrogênio.
Vamos aprender nesta aula sobre ozônio e nitrogênio. Siga!
OZÔNIO
O Ozônio (O3) é uma variedade alotrópica do elemento oxigênio (O), que, ao
invés de dois, contém três átomos. Sua coloração é azul pálida. Este gás é
extremamente oxidante e reativo, capaz de oxidar metais como ferro, chumbo e
arsênico, e ocorre naturalmente na estratosfera.
Ocorrência
Na atmosfera, a maior ocorrência de ozônio natural se dá entre trinta e
cinqüenta quilômetros de altitude. No final do século XX, foram constatadas
formações e ampliações de buracos na camada de ozônio, principalmente
sobre o Pólo Sul. Acredita-se que grande parte do aumento do buraco da
camada de Ozônio ocorra devido ao uso descontrolado de produtos à base
clorofluorcarbonos (CFCs) e hidrocarbonetos alifáticos halogenados (halons),
que liberam gases destruidores do Ozônio.
Obtenção
O processo para produzir o ozônio artificialmente se dá com a passagem de
um arco voltaico com descargas elétricas de alta tensão por meio de uma
corrente de Oxigênio ou ar seco. A composição química do Ozônio foi
estabelecida em 1872 que, naquela época se descobriu, é cinqüenta por cento
mais denso que o oxigênio. O gás se liquefaz à temperatura de -112° C, seu
ponto de congelamento se dá a -251,4° C e sua decomposição ocorre acima de
100° C ou em temperatura ambiente quando usados catalisadores. Após a
liquefação, sua coloração torna-se azul-escura.
Existem vários métodos para a obtenção do Ozônio industrial. Um deles é a
liquefação, em que se utiliza uma mistura de Oxigênio-Ozônio no qual ocorre a
QUÍMICA INORGÂNICA
separação em duas camadas. A mais densa contém cerca de 75% de Ozônio.
Devido à sua extrema instabilidade e reatividade, os processos de produção
são extremamente delicados e trabalhosos. Misturas gasosas com baixas
concentrações de O3 podem ser obtidas irradiando-se O2 com luz ultravioleta
(UV). Isso ocorre na atmosfera quando há formação de “smog” fotoquímico
sobre as cidades.
Estrutura
A estrutura do O3 é angular, com um ângulo de ligação O-O-O de 116º 48´
suas duas ligações O-O têm comprimento de 1,25 ângstron (Figura 1). O
átomo central tem um par eletrônico isolado, enquanto os átomos de O das
extremidades têm dois pares isolados. Com isso, haverá quatro elétrons para
formar ligações π.
Figura 1 – Representação do
ozônio, com três moléculas de
oxigênio.
Propriedades
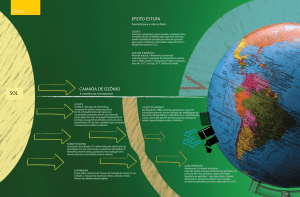
Na região da atmosfera, situada entre 30 e 50 km de altitude, a camada é tão
rarefeita que, se fosse comprimida à pressão atmosférica ao nível do mar, sua
espessura não ultrapassaria a três milímetros. Esta camada tem a propriedade
de absorver a radiação ultravioleta do Sol. Por este motivo, sem a proteção do
Ozônio, as radiações causam graves danos aos organismos vivos que habitam
a superfície do planeta Terra.
O ozônio é um gás tóxico e instável que decompõe-se a O2. Possui reação de
decomposição exotérmica, e é catalisado por diversos materiais. O sólido e o
QUÍMICA INORGÂNICA
líquido geralmente se decompõem de maneira explosiva. O gás se decompõe
lentamente, mesmo quando aquecido moderadamente, desde que não esteja
na presença de catalisadores ou luz UV. O ozônio é um agente oxidante e
extremamente forte, por isso é mais reativo que o gás oxigênio. O O3 absorve
fortemente na região do UV (λ 255nm).
Aplicações
Na indústria, o ozônio é utilizado em misturas com outros gases devido à sua
poderosa capacidade como agente oxidante, sobretudo na transformação de
alcenos em aldeídos, cetonas ou ácidos carboxílicos. Também é um poderoso
germicida, empregado na esterilização de água potável e na remoção de
sabores e odores indesejáveis. Também serve como agente branqueador para
compostos orgânicos.
NITROGÊNIO
Ocorrência, Obtenção e Aplicação.
O nitrogênio é um gás incolor, inodoro, insípido e mais leve que o ar, é o
componente principal da atmosfera terrestre (78,1% em volume), obtido para
usos industriais. Está presente também em produtos de excreção de animais
como o guano, o qual é encontrado na forma de uréia e ácido úrico.
Tem-se observado composto que contêm nitrogênio no espaço exterior, como
o isótopo N-14 que se cria nos processos de fusão nuclear das estrelas.
A mais importante aplicação comercial do nitrogênio é na obtenção do gás
amoníaco pelo processo Haber. O amoníaco é usado, posteriormente, para a
fabricação de fertilizantes e ácido nítrico. Devido à sua baixa reatividade, é
usado em tanques de armazenamento de líquidos explosivos durante a
fabricação
de
componentes
eletrônicos
(transistores,
diodos,
circuitos
integrados etc.) e na fabricação do aço inoxidável. Outra aplicação importante é
o seu uso como refrigerante, para o congelamento e transporte de alimentos,
QUÍMICA INORGÂNICA
conservação de corpos e células, reprodutivos sexuais e femininos ou
quaisquer outras amostras biológicas.
Entre os sais do ácido nítrico estão inclusos importantes compostos como o
nitrato de potássio (salitre empregado na fabricação de pólvora) e o nitrato de
amônio como fertilizante.
Os compostos orgânicos de nitrogênio como a nitroglicerina e o Trinitrotolueno
(TNT) são muito explosivos. A hidrazina e seus derivados são usados como
combustível em foguetes. O Nitrogênio-13, radioativo com emissão de pósitron
também é usado no exame PET em medicina nuclear.
B
A
Figura 2 – Composição química da (A) nitroglicerina e (B) Trinitrotolueno
Pequenas
quantidades
de
N2
puro
podem
ser
obtidas
aquecendo
cuidadosamente o nitreto de sódio (NaN3,) a 300ºC. A decomposição térmica
do NaN3 é usada para inflar os colchões de ar, empregados como dispositivo
de segurança em veículos (air-bags).
2NaN3 → 3N2 + 2Na
(300ºC)
Estrutura
A molécula de N2 contém uma ligação tripla N≡N curta com comprimento de
1,09 ângstron. Essa ligação é muito estável e consequentemente sua energia
de dissociação é muito alta (945,4 kJ/mol). Portanto, o N2 é estável a
temperatura ambiente, embora possa reagir com lítio formando o nitreto de lítio,
(Li3N). Outras espécies isoeletrônicas, tais como CO, CN-, NO+, são muito mais
reativas que o N2, pois suas ligações são polares, enquanto o N2 é apolar. Em
QUÍMICA INORGÂNICA
Formatado: Fonte: Negrito,
Cor da fonte: Cor Personalizada
(RGB(214;0;147))
Formatado: Fonte: Negrito,
Cor da fonte: Cor Personalizada
(RGB(214;0;147))
temperaturas elevadas, a reatividade do N2 aumenta gradativamente, o que o
faz reagir diretamente com elementos dos Grupos 2, 13 e 14, com hidrogênio e
com alguns metais de transição.
Propriedades
Possui uma elevada eletronegatividade (3 na escala de Pauling), 5 elétrons no
nível mais externo (camada de valência), e comporta-se como trivalente na
maioria dos compostos que forma.
Com hidrogênio, o nitrogênio forma amoníaco líquido que atua como uma base
em solução aquosa e forma íons de amônio (NH4+) que se comporta como um
ácido na ausência de água, cedendo um próton a uma base e dando lugar ao
ânion amida (NH2-). Também são conhecidas largas cadeias e compostos
cíclicos de nitrogênio, porém, são muito instáveis.
Com o oxigênio formam-se vários óxidos, como o óxido nitroso (N2O) ou gás
hilariante, o óxido nítrico (NO) e o dióxido de nitrogênio (NO2), estes dois
últimos são representados genericamente por NOx e são produtos de
processos de combustão, que contribui para o aparecimento de contaminantes
(smog fotoquímico). Outros óxidos são o trióxido de dinitrogênio (N2O3) e o
pentóxido de dinitrogênio (N2O5). Ambos são muito instáveis e explosivos e
respectivos ácidos são o ácido nitroso ( HNO2 ) e o ácido nítrico ( HNO3 ) que,
por sua vez, formam os sais nitritos e nitratos.
O nitrogênio é o componente essencial dos aminoácidos e dos ácidos
nucléicos, vitais para os seres vivos. As leguminosas são capazes de fazer
simbiose com certas bactérias do solo chamadas de Rizóbios. Estas bactérias
absorvem o nitrogênio diretamente do ar, sendo este transformado em
amoníaco que logo é absorvido pela planta. Na planta, o amoníaco é reduzido
a nitrito pela enzima nitrito redutase. Logo, o nitrito, por ação das bactérias,
transforma-se em nitrato, que,
posteriormente, é utilizado pela planta para
formar o grupo amina dos aminoácidos os quais finalmente se incorporam à
cadeia trófica. Um bom exemplo deste processo é observado na soja, pois é
uma cultura que dispensa adubação nitrogenada.
QUÍMICA INORGÂNICA
Existem dois isótopos estáveis do nitrogênio, N-14 e N-15, sendo o primeiro —
produzido no ciclo carbono-nitrogênio das estrelas — o mais comum
(99,634%). Dos dez isótopos que foram sintetizados, um tem uma vida média
de nove minutos e os demais de segundos ou menos.
As reações biológicas de nitrificação e desnitrificação contribuem, de maneira
determinante, na dinâmica do nitrogênio no solo, quase sempre produzindo um
enriquecimento em N-15 do substrato. Os fertilizantes nitrogenados são uma
poderosa fonte de contaminação do solo e das águas. Os compostos que
contêm íons cianeto (CN-) formam sais extremadamente tóxicos e são mortais
para animais, dentre eles os mamíferos.
Nesta aula foi visto o Ozônio (ocorrência, obtenção, estrutura,
propriedades e aplicações). Na próxima aula veremos o Enxofre. Até lá.
QUÍMICA INORGÂNICA