Diretrizes
DIRETRIZES BRASILEIRAS PARA O MANEJO DA DPOC (ADAPTAÇÃO
PARA O BRASIL DO CONSENSO LATINO-AMERICANO DE DPOC)
Coordenadores: Roberto Stirbulov e Jose Roberto Jardim
Autores do Documento Original:
María Montes de Oca
, María Victorina López Varela.
Eduardo Schiavi. María Alejandra Rey.
Agustín Acuña,
José Roberto Jardim , Alejandro
Casas, Antonio Tokumoto, Carlos A. Torres Duque, Alejandra RamírezVenegas. Gabriel García. Roberto Stirbulov.
Aquiles Camelier.
Miguel Bergna. Mark Cohen. Santiago Guzmán. Efraín
Sánchez.
INTRODUÇÃO
A Doença Pulmonar Obstrutiva Crônica (DPOC) é um problema importante de
Saúde Pública por sua elevada prevalência e morbimortalidade, além de ser
frequentemente subdiagnosticada e inadequadamente conduzida.
Em 2004, a SBPT publicou sua primeira edição de um Consenso, com
recomendações para abordagem e manejo de pacientes com DPOC. A seção
de tratamento broncodilatador do documento foi atualizado em 2006 e em 2014
foram publicadas as orientações específicas para a exacerbação na DPOC.
O presente documento incorpora métodos que permitem catalogá-lo como
uma Diretriz de Prática Clínica (GPC). Para tanto, foram introduzidas
perguntas sob o formato PICO (Paciente, Intervenção, Comparação,
Outcome/Desfecho), que tem por objetivo esclarecer controvérsias. Para cada
pergunta se designa um grau de evidência para determinar a recomendação.
Aspectos específicos abordados nesta Diretrizestão relacionados com o
impacto sanitário do subdiagnóstico, abordagem diferenciada para as
mulheres, simplificação dos critérios de gravidade e análise detalhada do
tratamento.
Esta GPC deve ser atualizada a cada três anos. Está dirigida a
pneumologistas, generalistas e a todo o pessoal de saúde pública que toma
decisões relacionadas aos pacientes com DPOC (fisioterapeutas respiratórios,
enfermeiros, administradores de saúde, entidades governamentais e privadas)
.
Método de elaboração
Inicialmente foi elaborado um manual de procedimentos ou diretriz
metodológica, utilizando ferramentas provenientes de diferentes centros
dedicados à elaboração, à disseminação e à implementação de GPCs
Grupos de trabalho
Para organizar os grupos de trabalho foram convocados associados com
expertise na elaboração e/ou avaliação de Diretrizes. Os participantes foram
alocados
em
cinco
grupos:
1-
INTRODUÇÃO
E
MÉTODOS
DE
ELABORAÇÃO; 2- DEFINIÇÃO, EPIDEMIOLOGIA, FATORES DE RISCO E
PATOGENIA; 3- CURSO CLÍNICO, DIAGNÓSTICO, BUSCA DE CASOS E
CLASSIFICAÇÃO DE GRAVIDADE; 4- TRATAMENTO DA DPOC ESTÁVEL;
5- DEFINIÇÃO, DIAGNÓSTICO E TRATAMENTO DA EXACERBAÇÃO DA
DPOC (E-DPOC)
Cada sub-grupo elegeu um coordenador encarregado de estimular a tomada
de decisões por consenso. Para tanto, foram realizadas três reuniões
presenciais de treinamento e trabalho. Também, cada sub-grupo realizou
sessões plenárias para elaboração das perguntas PICO e encaminhamento
das estratégias de busca, seleção bibliográfica e recomendações.
Estrutura da diretriz e formulação de perguntas clínicas
Os grupos elaboraram perguntas de relevância clínica de acordo com a revisão
e
discussão
de
documentos
nacionais
previamente.
Foi
utilizado
formato
o
e
internacionais
PICO
(Paciente,
publicadas
Intervenção,
Comparação, Outcome/Desfecho) para o desenvolvimento das questões. (15)
Estratégia de busca
A bibliografia foi selecionada através de busca ativa no Tripdatabase e
PUBMED. O primeiro foi usado para hierarquizar as informações e responder
às perguntas PICO; o PUBMED, com a ferramenta MeSh, foi empregado para
a busca de controvérsias e completar a busca de respostas.
Foi dada prioridade a Diretrizes publicadas, evidências secundárias, ensaios
clínicos e investigações primárias identificadas no Tripdatabase através do uso
de palavras-chave. (6)
Elegibilidade
Para responder às perguntas PICO, foram priorizadas respostas com os mais
altos níveis de evidências. Quando o material disponível não respondia
completamente à questão, novas estratégias eram implementadas. Foi
seguida a recomendação algorítmica, especialmente para as perguntas
terapêuticas. Não foi estabelecido nenhum limite no número de publicações
por idioma, tendo sido considerados o espanhol, português e inglês. A data de
encerramento das buscas foi outubro de 2014.
Análise crítica e formulação de recomendações
Para a análise crítica das referências selecionadas foram usadas as
recomendações e planilhas propostas pela rede CASPE (www.redcaspe.org).
Além disso, foram seguidas as diretrizes do grupo GRADE (Grading of
Recommendations, Assessment, Development and Evaluation) para classificar
a qualidade da evidência e avaliar a força das recomendações relativas às
perguntas PICO. No processo de graduação da força das recomendações
foram considerados os seguintes fatores:
Comparação dos benefícios e riscos: foi considerado o risco basal da
população a qual a recomendação era dirigida e o efeito tanto relativo quanto
absoluto.
Qualidade da evidência científica: antes de considerar uma recomendação foi
necessário conhecer a segurança da estimativa do efeito observado. Se a
qualidade da evidência não é alta, apesar de que a magnitude seja importante,
deve-se diminuir a confiança e, portanto, a força da recomendação.
Custos: são muito variáveis com o tempo, com as geografias e em função de
outros diversos fatores.
Revisão externa
A Diretriz foi avaliada por cinco revisores externos com experiência em DPOC
e a versão final da Diretriz foi revisada e aceita pelos autores de cada capítulo
Perguntas PICO
Existem outros fatores de risco inalados além da fumaça de tabaco
relacionados com o surgimento da DPOC?
A DPOC em mulheres tem características epidemiológicas e clínicas
diferentes?
É justificada a busca ativa de casos da DPOC através de provas de função
pulmonar (espirometria) em sintomáticos respiratórios e em pessoas sem
sintomas respiratórios com fatores de risco?
Quais índices multidimensionais foram validados para predizer mortalidade em
DPOC?
Os agentes muscarínicos de ação prolongada (LAMA) proporcionam maiores
benefícios que os beta2 agonistas de ação prolongada (LABA) em pacientes
com DPOC?
A associação LABA+LAMA proporciona maiores benefícios do que a
monoterapia com LABA ou LAMA em pacientes com DPOC?
A terapia combinada (LABA/CI) proporciona maiores benefícios do que a
monoterapia com LAMA em pacientes com DPOC?
A combinação LABA/CI associada aotiotrópio (terapia tripla) proporciona
maiores benefícios quando comparada com monoterapia com tiotrópio,
combinação LABA/CI ou dupla terapia broncodilatadora (LABA+LAMA) em
pacientes com DPOC?
Está justificado o uso de imunizações e de produtos bacterianos em pacientes
com DPOC?
O uso profilático de antibióticos em pacientes com DPOC estável previne as
exacerbações?
Os antibióticos são efetivos em todas as exacerbações da DPOC?
Os corticosteroides sistêmicos (via oral ou parenteral) são efetivos no
tratamento das exacerbações da DPOC?
Nesse documento, que corresponde à adaptação das Diretrizes
Latinoamericanas para o Brasil, as citações de trabalhos publicados após
Outubro de 2014 e que, portanto, não foram considerados nas respostas das
perguntas PICO, foram referenciadas no próprio texto.
DEFINIÇÃO, EPIDEMIOLOGIA, FATORES DE RISCO E PATOGÊNESE
Pontos principais
A DPOC é uma doença frequente, prevenível e tratável, heterogênea em sua
apresentação clínica e evolução, caracterizada por obstrução ao fluxo de ar,
persistente e geralmente progressiva.
A espirometria é essencial para confirmar o diagnóstico.
O estudo epidemiológico PLATINO forneceu dados sobre a prevalência da
DPOC no Brasil.
É grande a prevalência de subdiagnóstico (64%) e também de erros de
diagnóstico (64%) relacionados a vários fatores, principalmente à baixa
utilização de espirometria (20%).
Definição
A DPOC é uma doença frequente, prevenível e tratável, heterogênea em sua
apresentação clínica e evolução.É caracterizada pela limitação crônica e
persistente ao fluxo de ar e geralmente progressiva, associada a uma reação
inflamatória pulmonar causada principalmente pela exposição à fumaça de
tabaco, exposição ocupacional e combustão de biomassa.
O conceito da DPOC como doença inexoravelmente progressiva está
mudando, pois o declínio da função pulmonar não acontece em todos os
pacientes.(7-9)
Para o diagnóstico da doença é essencial a realização da espirometria que
permitirá confirmar a obstrução ao fluxo de ar através do resultado da relação
entreo volume expiratório forçado no primeiro segundo (VEF1) e a
capacidadevitalforçada (CVF)inferior a 0,70após o uso de broncodilatador
inalatório(VEF1/CVF<0,70 pós-BD).
É uma doença heterogêneaem sua apresentaçãoe evolução, e pode ou nãoser
acompanhada
de
expectoração,exacerbações,
sintomascomo
manifestações
dispneia,
tosse
extra-pulmonares
e
e
comorbidades.(1,2,10)
Epidemiologia
A DPOC é uma das principais causas de morbidade e mortalidade, com
impacto sócio-econômico significativo e constitui um problema prioritário de
saúde pública,sendoreconhecida como a terceira principal causa de morte no
mundo.(11,12)
Tem sido postulado que dentre as doenças crônicas não transmissíveis, a
DPOC é a única cuja morbi-mortalidade mantém aumento constante.(13,14)
No entanto, estudos recentes indicam que as taxas de mortalidade têm
aumentado a um ritmo mais lento ou até mesmo diminuindo, especialmente
entre homens.(15-18)
Dados de estudos epidemiológicos de diferentes regiões permitirem estimar a
prevalência global da DPOC em 10%.(19-23) As estimativas mostram
considerável variabilidade entre as regiões, sugerindo que fatores de risco
podem afetar as populações de forma distinta.
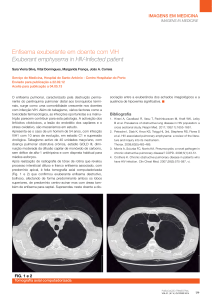
O estudo epidemiológico, Projeto Latinoamericano de Pesquisa em Obstrução
Pulmonar (PLATINO), forneceu informações sobre a prevalência da DPOC na
América Latina e no Brasil (Figura 1).(24)
O PLATINOavaliou a prevalência da DPOC em indivíduos ≥40 anos, tendo sido
realizado em cinco cidades da América Latina: Cidade do México (México),
São Paulo (Brasil), Montevidéu (Uruguai), Santiago (Chile) e Caracas
(Venezuela).
Usando o critério de diagnóstico do VEF1/CVF<0,70 pós-BD, aprevalência da
DPOC no Brasil foi de 15,8% (variando de 7,8% na Cidade do México até
19,7% em Montevidéu).(24,25) Usando o critério do limite inferior da
normalidade (LIN) da razão VEF1 /CVF pós-BD,a prevalência da DPOC no
Projeto PLATINO foi de 11,7%.(26) Na Região Metropolitana de São Paulo o
subdiagnóstico foi de 87,5% (Nascimento OA, Camelier A, Rosa FW, Menezes
AM, Pérez-Padilla R, Jardim JR; Latin American Project for the Investigation of
Obstructive Lung Disease (PLATINO) Group. Chronic obstructive pulmonary
disease is underdiagnosed and undertreated in São Paulo (Brazil): results of
the PLATINO study. Braz J Med Biol Res. 2007 Jul;40(7):887-95.). Apenas
20% dos indivíduos pesquisados no PLATINO haviam sido submetidos a
espirometria em algum momento de suas vidas.(27) Em outro estudo realizado
com pessoas que procuravam unidades de saúde da região metropolitana de
Goiânia (GO), entre aqueles com exposição ao tabagismo e/ou combustão de
biomassa foi identificado DPOC em 31,5%; adicionalmente, 71,4% não sabiam
do diagnóstico. (Queiroz MC, Moreira MA, Rabahi MF. Underdiagnosis of
COPD at primary health care clinics in the city of Aparecida de Goiânia, Brazil.J
Bras Pneumol. 2012 Nov-Dec;38(6):692-9.)
Fatores de risco
Pontos principais
Os principais fatores de risco são o tabagismo, a exposição ocupacional e a
combustão de biomassa.
Tabagismo
O principal fator de risco para a DPOC é o consumo de tabaco. De acordo com
levantamento doVigitel em 2013 (Vigilância de Fatores de Risco e Proteção
para Doenças Crônicas por Inquérito Telefônico), inquérito promovido pelo
Ministério da Saúde do Brasil anualmente, a parcela da população brasileira
fumante acima de 18 anos caiu 28 % nos últimos oito anos. A prevalência em
2015 foi de 10,5% de fumantes, enquanto em 2006 o índice era de 15,7%. A
frequência permanece maior entre os homens (14,4%) do que em mulheres
(8,6%). O percentual de fumantes passivos no domicílio passou de 12,7% em
2009 para 10,2% em 2015, e no local de trabalho passou de 12,1% para
9,8%%. (portalsaude.saude.gov.br/images/pdf/.../Lancamento-Vigitel-28-04ok.pdf)
Sabe-se que o risco para a DPOC é dependente da carga tabagística.
Pergunta: Há outros fatores de risco inalados que sejam diferentes ao da
fumaça do cigarro relacionada com o desenvolvimento da DPOC?
Resposta: Embora o consumo de tabaco seja o principal fator de risco para
a DPOC, há um número significativo de casos que não podem ser atribuídos
a essa exposição. Outros fatores de risco como a exposição à combustão de
biomassa, poeiras ocupacionais, gases e poluição do ar têm sido associados
à patogênese da doença. No entanto, o debate sobre a influência e
importância desses fatores persiste.
Seleção da busca bibliográfica
Foram analisadas 158 referências (MeSh: 114; Tripdatabase: 44) sendo 18
delas selecionadas (2 revisões sistemáticas, 3 estudos diagnósticos, 3 estudos
de caso-controle e 13 estudos de coorte)
Resumo da evidência
Em cerca de 50% dos lares em todo o mundo e em 90% das áreas rurais,a
combustão de biomassaé utilizada como a principal fonte de energia
doméstica. Os resultados de uma meta-análise indicam que, em geral, as
pessoas expostas à fumaça de biomassa tem 2,44 vezes mais chance (IC
95%: 1,9-3,33) de desenvolver DPOC em comparação com não expostos.(29)
Esta exposição foi identificada como fator de risco para homens e
mulheres.(30) Estudos latino-americanos confirmam esta relação, indicando
que os sintomas respiratórios ocorrem a partir de exposição à fumaça de
biomassa a partir de 100 horas/ano e limitaçãoao fluxo de ar a partir de 200
horas/ano, ou> 10 anos de exposição.(31) Estudo realizado em Goiânia
demonstrou que mulheres com DPOC, não fumantes e que apresentavam
história de exposição àfumaça de fogão a lenha apresentavam alterações na
tomografia
de
tórax
como
espessamento
das
paredes
brônquicas,
bronquiectasias, perfusão em mosaico, bandas parenquimatosas, padrão de
árvore em brotamento e atelectasias laminares; a extensão das alterações
apresentavam associação positiva com tempo de exposição à fumaça.
(Moreira MA, Barbosa MA, Queiroz MC, Teixeira KI, Torres PP, Santana Júnior
PJ, Montadon Júnior ME, Jardim JR. Pulmonary changes on HRCT scans in
nonsmoking females with COPD due to wood smoke exposure. J
BrasPneumol. 2013 Mar-Apr;39(2):155-63.)
Existem informações limitadas sobre a relação entre poluição do ar e o
desenvolvimento da DPOC. Estudos existentes sugerem a associação entre a
poluição ambiental e a perda da função pulmonar,(32,33) a redução dos
sintomas com a diminuição da exposição às partículas ambientais(34) e entre
o aumento de internações hospitalares com o aumento dos níveis de
poluição.(35-38)
Não existem dados suficientes para inferir uma relação causal entre a
exposição ocupacional e o desenvolvimento da DPOC. Este risco tem sido
demonstrado em mineradores de carvão,trabalhadores em escavações em
rocha, produtores de concreto, trabalhadores do agronegócio e expostos a
agentes químicos.(39-41) No entanto, não está claro o percentual de
indivíduos expostos que desenvolvem a doença.
Tem sido sugerido que a exposição passiva ao tabaco esteja associada
com risco aumentado da DPOC. Os resultados de um estudo transversal
indicam que a exposição durante mais de 20 horas por semana aumentou em
1,18 vezes a possibilidade de risco da DPOC (IC 95%: 1,0-1,4).(42)
Conclusões e recomendações
Existem outros fatores de risco de substâncias inaladas para
desenvolver DPOC diferentes da fumaça do tabaco, com várias evidências
para sugerir a associação da DPOC com a exposição ocupacional e biomassa,
com FORTE recomendação para explorar clínica e epidemiologicamente os
fatores de risco diferentes ao tabaco.
Histórico de tuberculose
Dados dos estudos PLATINO mostram maior prevalência da DPOC em
indivíduos com história de tuberculose em comparação com aqueles sem
história anterior.(25,43) É desconhecido se a perda da função pulmonar
relacionada à tuberculose é clinicamente semelhante à DPOC do fumante.(44)
Fatores genéticos
Deficiência da α-1-antitripsina
A deficiência de α-1-antitripsina (AAT) é uma doença hereditária associada
com baixos níveis da proteína AAT, o que leva a um desequilíbrio de proteaseantiprotease e maior risco de desenvolver DPOC. A prevalência dos genótipos
de AAT anormais associados com deficiência grave de AAT é maior entre as
populações de risco, tais como pessoas com DPOC, que é estimado em cerca
de 1-2%.(45,46) No Brasil, estudo recente que avaliou a prevalência de
deficiência de alfa 1 antitripsina (AAT) em pacientes com diagnóstico de DPOC
mostrou deficiência intermediária a grave em 2,8% dos pacientes e deficiência
grave (com fenótipo ZZ) em 0,8%. (Russo R e col. J Bras Pneumol.
2014;40:R1-R450 PE248)
Outros fatores genéticos
Outros fatores genéticos diferentes da deficiência da proteína AAT
provavelmente influenciam na variação da função pulmonar especialmenteem
pessoas não fumantes. Entretanto, os estudos atuais ainda não identificaram
os fatores genéticos que aumentam o risco de desenvolver DPOC.(47)
Pergunta: A DPOC em mulheres tem características clínicas e epidemiológicas
diferentes?
Resposta: A prevalência da DPOC em mulheres está aumentando. Isto poderia
ser explicado pelo aumento no consumo de tabaco e dificuldade em conseguir
a abstinência entre as mulheres. Existem controvérsias sobre possíveis
diferenças na expressão clínica da DPOC em mulheres referente ao impacto,
características clínicas, progressão e mortalidade.
Seleção da busca bibliográficas
Foram selecionadas 26 referências (MeSh: 4;Tripdatabase:22), sendo que 9
foram analisadas (6 estudos de coorte, 3 estudos de caso- controle)
Resumo da evidência
Perante a mesma exposição à fumaça do tabaco, as mulheres são mais
propensas a desenvolver DPOC em idade mais precoce, com maior
comprometimento da função pulmonar.(48,49)
Estudos na população geral e selecionada, mostram que as mulheres com
gravidade de obstrução semelhante aos homens apresentam maior grau de
dispneia, ansiedade e depressão, menos enfisema na radiologia, pior
qualidade de vida e menor sobrevida.(50-56)
Conclusões e recomendações
As evidências indicam que existem diferenças na epidemiologia e expressão
clínica da DPOC em mulheres. É importante considerar e identificar estas
manifestações e desenvolver estratégias adequadas para seu controle,
especialmente em casos de ansiedade e depressão.
Patogenia
Pontos principais
A DPOC é uma doença inflamatória que afeta as vias aéreas, os alvéolos e
acirculação pulmonar.
A inflamação crônica provoca espessamento da parede brônquica com
redução do tamanho e destruição alveolar com aumento dos espaços aéreos
e perda da arquitetura brônquica.
As consequências funcionais são a obstrução do fluxo de ar, colapso
expiratório da árvore brônquica e perda da elasticidade pulmonar.
A obstrução da via aérea possuicomponentes irreversíveis e
reversíveis, nos quais é possível a ação farmacológica.
A DPOC é provavelmente o resultado da interação de múltiplos genes,
alguns dos quais podem interagir com os fatores de risco ambientais,
principalmente o tabagismo.
A DPOC é uma doença inflamatória que afeta as vias aéreas em todas as suas
dimensões,
alvéolos
e
circulação
pulmonar.
O
principal
local
de
comprometimento são os brônquiosde diâmetro inferior a 2 mm e o
componente elástico dos pulmões.(57) O danonestas estruturas é precocena
evolução da doença e leva a todas as manifestações fisiológicas e clínicas no
sistema respiratório.Ao mesmo tempo, e por diferentes mecanismos, que
causam manifestações sistêmicas,
efeitos extra-pulmonares(58,59) são
ativados. A Figura 2 mostra as inter-relações entre a inflamação e DPOC.
Os mecanismos patogênicos mais bem estudados são causados pela fumaça
do tabaco. As substâncias inaladas desencadeiam um processo inflamatório
crônico persistente no tempo.(60)
A obstrução das vias aéreas possui componentes reversíveis e irreversíveis.
A inflamação danifica o epitélio respiratório, estimulando as fibras nervosas
expostas (fibras sensoriais C, receptores de adaptação rápida) liberando
neurocininas. Este mecanismo aumenta o estímulo do nervo aferente vagal
e,como
consequência,ocorre
a
resposta
do
nervo
eferente
com
broncoconstrição pelo aumento do tônus broncomotor.(61)
Este é o principal componente reversível da obstrução ao fluxo de ar e pode
ser tratado farmacologicamente.
Mecanismos dos reflexos vagais também aumentam a secreção de muco que
contribui para a obstrução brônquica.(62) Tanto a resposta constritora do
músculo liso, como a hipersecreção brônquica são reguladas pelo receptor
muscarínico M3.
A estimulação dos receptores muscarínicos atua sinergicamente com o fator
de crescimento epitelial (EGF) na ativação de células muco secretoras. O
mecanismo de secreção aumentado de acetilcolina pode intervir na hipertrofia
e hiperplasia de células caliciformes e glândulas submucosas contribuindo
para o remodelamento das paredes brônquicas.(63) Estas mudanças
estruturais são permanentes e difícilmente reversíveis.
O resultado final da inflamação crônica é o espessamento da parede brônquica
com a diminuição do calibre, destruição alveolar com aumento dos espaços
aéreos e perda da arquitetura pulmonar. As consequências funcionais são a
obstrução ao fluxo de ar, colapso expiratório da árvore brônquica e perda da
elasticidade pulmonar.
A inflamação é um mecanismo ativo e progressivo, com picos de aumento
durante as exacerbações.
A desativação deste mecanismo é mais difícil à medida que a doença progride
e os danos estruturais(64) estejam estabelecidos. O efeito da cessação do
tabagismo é mais eficaz nas fases iniciais da doença.(65-67)
Pacientes com DPOC apresentam evidências de inflamação sistêmica, com
aumento de citocinas no sangue (IL-8, IL-6, fator de necrose tumoral alfa, IL1β), quimiocinas (CXCL8), proteínas de fase aguda (proteína C-reactiva ),
neutrófilos, monócitos e linfócitos.(59,68,69) Não está bem estabelecida a
relação entre essas alterações com os efeitos extra-pulmonares.
Embora haja clara evidência da contribuição genética para a patogênese da
DPOC, poucos genes relacionados à doença foram identificados até
recentemente. A maior parte dos estudos realizados até há poucos anos teve
uma amostra muito pequena para detectar, com precisão adequada, genes
que pudessem ser implicados de maneira significativa com a doença.
A DPOC é provavelmente o resultado da interação de múltiplos genes, alguns
dos quais podem interagir com os fatores de risco ambientais, principalmente
o tabagismo.
Na DPOC, o estudo mais importante dedicado a desvendar os aspectos
genéticos relacionados à patogenia da doença é o COPDGene Study que
encontra-se em andamento desde 2010. O estudo foi delineado para identificar
os fatores genéticos na DPOC, para definir e caracterizar os fenótipos
relacionados à doença e para acessar a associação existente entre estes dois
componentes. (Reagan AR. Genetic Epidemiology of COPD (COPDGene)
Study Design.COPD: J COPD 2010; 7:32-43 )
Do ponto de vista prático, o COPDGene está em andamento, com os seguintes
objetivos:
1-Definir associações genéticas com os fenótipos da DPOC
2-Caracterizar os fenótipos da doença através da definição dos:
a-Aspectos fisiopatológicos
b-Fatores que controlam a expressão da doença
c-Fatores que influenciam a progressão da doença
d-Fatores que influenciam as respostas à terapia
O risco atribuível à população com história familiar para DPOC foi de 18,6%.
O estudo concluiu que história familiar da DPOC é um forte fator de risco para
o surgimento da DPOC, independentemente de história familiar de tabagismo,
história pessoal de tabagismo ou exposição à fumaça do cigarro durante a
infância. (Hersch CH. Family history is a risk factor for COPD. Chest 2012;
2:343-350)
O COPDGene, com sua grande população e foco nos aspectos clínicos,
funcionais, radiológicos e genéticos propõe definir os subtipos da DPOC que
podem refletir os efeitos de variantes genéticas específicas e, assim,
esclarecer muitas dúvidas que ainda persistem com relação à patogenia da
doença. Uma cuidadosa fenotipagem radiológica pode gerar biomarcadores
de imagem e permitir a identificação precoce de grupos de alto risco. O
diagnóstico precoce da doença, ainda assintomática, pode proporcionar
estratégias de prevenção e tratamento para limitar a progressão da doença.
As associações genéticas esperadas a partir dos estudos de varredura
genética ampla na grande coorte do COPDGeneStudy podem revelar novas
direções para definir a patogenia e os mecanismos da doença com o objetivo
de
prover
oportunidades
para
a
prevenção
e
o
tratamento.
(www.copdgene.org)
CURSO CLÍNICO, DIAGNÓSTICO, BUSCA DE CASOS E
ESTRATIFICAÇÃO DA GRAVIDADE
Curso clínico
Pontos principais
• O diagnóstico precoce da DPOC é importante porque permite alterar a
exposição a fatores de risco e melhorar o prognóstico.
Um terço dos pacientes com DPOC são assintomáticos.(70-72) A dispneia e
limitação ao exercício são os principais determinantes de incapacidade e
redução da qualidade de vida dos pacientes.(73)
A DPOC é uma doença heterogênea. Existe grande variação no declínio do
VEF1 e frequência das exacerbações entre pacientes.(7,9,74-76) Fatores
como a intensidade e continuidade da exposição ao tabaco, a frequência e a
gravidade das exacerbações e a extensão do enfisema têm sido associados
com o declínio acelerado da função pulmonar.(75-79) Os pacientes que param
de fumar mais precocemente retardam a queda do VEF1 e o risco de óbito.(80)
A heterogeneidade da DPOC permite identificar subgrupos de pacientes com
diferentes características clínicas. Alguns autores têm proposto agrupar os
fenótipos clínicos com desfechos relevantes, como a frequência e a gravidade
das exacerbações, a progressão da doença, a resposta ao tratamento e a
mortalidade. Os subgrupos clínicos mais estudados são: enfisemahiperinflação, bronquite crônica, exacerbador frequente e associação
asma/DPOC.(8,75,76,79,81-90) A diferenciação nesses fenótipos clínicos
além de descrever comportamento comum, pode levar a diferentes
abordagens diagnósticas e terapêuticas, com melhor acurácia da avaliação
clínica e do prognóstico. Porém, uma vez que esses fenótipos não foram
consistentemente
validados,
este
documento
não
propõe
nenhuma
categorização e tratamento de acordo com eles.
Diagnóstico
Pontos principais
• Todo indivíduo com 40 anos ou mais de idade e com história de exposição a
fatores de risco para a DPOC (tabaco, biomassa, vapores ou poeira
ocupacional), ainda que assintomático deve ser avaliado. Estudos em curso
estão avaliando se detecção precoce deve começar aos 30 ou 35 anos de
idade. Esses dados, entretanto, ainda carecem de validação.
• A presença de sinais ou sintomas clínicos sugere o diagnóstico da DPOC,
mas a sua ausência quando há fator de risco evidente não exclui a doença.
• Para estabelecer o diagnóstico da DPOC é necessária a realização de
espirometria, que haja a presença de obstrução ao fluxo de ar e que ela
persista após a administração de broncodilatador (VEF1 / CVF<0,70 pós-BD).
• Outras avaliações permitem afastar diagnósticos diferenciais, definir a
gravidade da doença e estabelecer o prognóstico.
Em qualquer adulto com 40 anos ou mais e história de exposição a fatores de
risco (tabaco, biomassa, vapores ou poeira ocupacional), com ou sem
sintomas respiratórios, deve-se considerar o diagnóstico da DPOC e solicitar
espirometria. Nestes indivíduos a presença de obstrução ao fluxo de ar pósbroncodilatador confirma o diagnóstico da DPOC. A gravidade da obstrução
combinada com o impacto da doença (dispneia e exacerbações) definem a
gravidade da DPOC e o nível de atenção médica necessária. O processo de
diagnóstico da DPOC inclui suspeita clínica, confirmação, avaliação da
gravidade e prognóstico.
Suspeita clinica
A suspeita da DPOC deve ser feita quando há história de exposição a fatores
de risco acompanhada ou não de sintomas respiratórios.
Avaliação dos fatores de risco
A avaliação dos fatores de risco deve ser realizada de rotina a investigação
sobre exposição ao tabaco, combustíveis de biomassa, vapores e outros
fumos e/ou poeiras de origem ocupacional. Os principais aspectos que devem
ser definidos são: duração, intensidade e continuidade da exposição. A partir
destes dados pode-se calcular o índice anos-maço (número médio de cigarros
fumados por dia, dividido por vinte, e multiplicado pelo número de anos que o
indivíduo fumou; também conhecido como índice maços/ano), o número de
horas-ano de exposição à fumaça de lenha (número médio de horas
cozinhando em fogão de lenha multiplicado pelo número de anos que cozinhou
com lenha). Um indivíduo com idade de 40 anos ou mais e carga tabagística
igual ou maior do que 10 anos-maço ou exposição à biomassa por mais de 200
horas-ano ou 10 anos tem risco elevado de desenvolver DPOC.(25)
Apesar do tabagismo ser um importante fator causal da obstrução ao fluxo de
ar, estima-se que somente 15% a 30% dos fumantes desenvolvam DPOC
(Celli BR, MacNee W, Force AET. Standards for the diagnosis and treatment
of patients with COPD: A summary of the ATS/ERS position paper. Eur Respir
J 2004;23:932-946.). Existe significativa variação dos efeitos do tabagismo e
da queima de biomassa sobre cada indivíduo. Entender a DPOC como doença
heterogênea de inúmeras facetas é um desafio real e torna-se fundamental a
compreensão que, apesar da clássica definição de ser uma doença presente
clinicamente em indivíduos acima de 40 anos, isto não implica que a doença
não possa ter sua origem na infância ou possuir outros mecanismos etiológicos
envolvidos em sua gênese que não os do cigarro e ou exposição à fumaça de
lenha.(Postma DS, Bush A, van den Berge M. Risk factors and early origins of
chronic obstructive pulmonary disease. Lancet 2015;385:899-909)
Reconhecer todos os possíveis fatores de risco para o desenvolvimento da
doença pulmonar obstrutiva crônica em diferentes estágios da vida (alterações
genéticas, obstrução ao fluxo de ar, tabagismo antes e ou durante a gestação,
história familiar de asma, hiperresponsividade brônquica, uso de antibióticos,
prematuridade, infecções respiratórias na infância) exige amplo conhecimento
dos mecanismos da doença e a investigação de todos os fatores envolvidos
para correta caracterização dos fenótipos.(2)
Síntomas: Cerca de 30% dos pacientes com DPOC são assintomáticos e
podem passar vários anos entre o aparecimento de limitação ao fluxo de ar e
o desenvolvimento de manifestações clínicas.(70-72) A dispneia, a tosse e a
expectoração são os principais sintomas da DPOC.
A dispneia de esforço é o sintoma mais frequente.(72,91,92) A percepção de
dispneia é variável entre os indivíduos e, por este motivo, recomenda-se que
sua avaliação seja padronizada com o uso da escala modificada do Medical
Research Council (mMRC) (Tabela 1).(93-96) A associação entre o escore de
dispneia e a gravidade da obstrução ao fluxo de ar é fraca visto que a dispneia
é multifatorial,,dependendo não apenas da obstrução ao fluxo de ar, mas
também de condicionamento, comorbidades e fatores psicoemocionais.(97101)
A tosse do paciente com DPOC é crônica, persistente ou episódica,
geralmente predomina no período matutino e, frequentemente, é produtiva
com expectoração mucosa.(102) O volume e a purulência da expectoração
aumentam durante as exacerbações da doença.(91,103) Volume mais
expressivo de expectoração sugere a presença de bronquiectasias.(104)
Confirmação diagnóstica
Espirometria após uso de broncodilatador. Para o diagnóstico da DPOC é
imprescindível realizar espirometria para confirmar a presença de obstrução
fixa ao fluxo de ar.
O parâmetro mais utilizado é a relação VEF1/CVF<0,70 após o uso de
broncodilatador, conforme foi preconizado inicialmente pela GOLD.
Este
critério, de fácil aplicação, tem sido um parâmetro bastante utilizado para o
diagnóstico da DPOC. Entretanto, pode estar associado à subdiagnóstico de
obstrução das vias aéreas em jovens expostos a fatores de risco e à
sobrediagnóstico em pessoas com idade acima de 65 anos sem exposição a
fatores de risco. Por isso, existem critérios diagnósticos alternativos, e mais
precisos, como o limite inferior da normalidade (LIN) da relação VEF1/CVF
(<percentil 5) ou a relação VEF1/VEF6<0,70, ambos após broncodilatador
(26,105), os quais deveriam preferencialmente ser utilizados.
Apesar do
conhecimento de que o uso da relação fixa VEF1/CVF<0,70 pode ser
inadequada, ela tem sido utilizada em vários estudos epidemiológicos para que
se possa comparar as prevalências de DPOC em distintas áreas.O VEF1,
expresso como porcentagem do valor previsto, é a variável que define a
gravidade da obstrução ao fluxo de ar (Tabela 2).
Reversibilidade
aguda
aos
broncodilatadores.
Considera-se
que
há
reversibilidade ao broncodilatador quando um dos seguintes parâmetros são
alcançados15 a 20 minutos depois do uso de 400 mcg de beta agonista de
curta ação.(72, 106):
1)
aumento do VEF1≥12% e ≥200 mL (GOLD 2015)
2)
aumento do VEF1 e/ou CVF ≥12% e ≥200 mL (ATS e ERS 2005)
3)
aumento do VEF1em 7% do previsto e/ou CVF≥ 350 mL e/ou CV ≥400
mL e/ou CI ≥ 300 mL (SBPT). (Soares ALP , Pereira CAC, Rodrigues SC Alterações espirométricas em doenças obstrutivas: afinal, o quanto é
relevante? J Bras Pneumol. 2013;39(1):56-62)
4)
aumento de 7% e 0,20 L para ambos, VEF1, e CVF e elevação de 0,30
L na capacidade inspiratória.
Estima-se que, aproximadamente, um terço dos pacientes com DPOC
apresentam reversibilidade ao exame de espirometria.(72,107-109) A taxa de
reversibilidade depende da dose e da medicação utilizada na espirometria
como broncodilatador. Acréscimo na broncodilatação pode ser obtido com a
associação de 160 mcg de brometo de ipratrópio. A presença de
reversibilidade aguda ao broncodilatador em teste de espirometria não permite
discriminar asma da DPOC.
Diagnóstico diferencial
Deve-se realizar diagnóstico diferencial com outras doenças respiratórias
como asma, sequela de tuberculose, pneumoconiose, bronquiectasias,
bronquiolite constrictiva ou obstrução de via aérea superior.
O diagnóstico diferencial com asma pode ser difícil e é importante porque há
diferenças no prognóstico e no manejo terapêutico. Geralmente, os sintomas
de asma se iniciam mais precocemente (antes dos 40 anos), são episódicos e
há predomínio de sibilos. Com frequência há sintomas alérgicos associados e
antecedentes pessoais ou familiares de manifestações atópicas. Como são
doenças prevalentes, não é raro que asma e DPOC coexistam.(83-85,110)
Busca ativa e oportuna de casos
A melhor forma de enfrentar o problema do subdiagnóstico, e também do
diagnóstico tardio na DPOC, ainda é controversa.
Pergunta:
A realização de espirometria em pacientes sintomáticos e assintomáticos
respiratórios, com fatores de risco pode ser justificada na busca ativa dos
casos da DPOC?
Justificativa:
O
subdiagnóstico
da
DPOC
é
um
problema
importante
e
conhecido.(25,27,70,111,112) O estudo PLATINO mostrou que os principais
fatores associados com o subdiagnóstico são: menor idade, menor gravidade
da obstrução e poucos sintomas respiratórios.(27) Estudos populacionais que
utilizaram métodos de busca ativa em instituições de atenção primária à saúde
mostram que um terço dos pacientes diagnosticados são assintomáticos, e
mais da metade tem manifestações leves.(79-72,113) Outro fator importante
observado é a existência de baixa percepção dos sintomas respiratórios na
fase pré-clinica, que contribui para o subdiagnóstico da DPOC.(27,111,112)
Nas etapas iniciais da DPOC as alterações dos valores na prova de função
pulmonar são frequentemente a única evidência da doença.(111,114) Continua
a ser tema de controvérsia a seleção da população e o momento de realizar a
espirometria para reduzir o subdiagnóstico da DPOC. A busca ativa com a
realização de espirometria em população geral e não selecionada (screening
ou rastreamento em massa) não mostra custo-efetividade favorável, uma vez
que a detecção dos casos é baixa se a população de alto risco não é
discriminada e não existem evidências sobre os benefícios do tratamento
medicamentoso em pacientes assintomáticos.(3,64,115,116)
Há controvérsias sobre o custo-efetividade da busca ativa da DPOC na
população exposta a fatores de risco por meio da realização de espirometria,
porque uma proporção significativa de indivíduos assintomáticos ou com
formas
leves
da
doença
não
se
beneficiariam
de
intervenções
medicamentosas.(3) No entanto, outros autores argumentam que o
diagnóstico da DPOC, nesta fase, permitiria intervir nos fatores de risco e
mudar o curso da doença.(64,67) A seleção da população em situação de risco
pode ser feito por simples interrogatório ou utilizando questionários
estruturados para identificar sintomas respiratórios crônicos e exposição a
fatores de risco.(117)
Referências selecionadas
Foram selecionadas 90 referências (MeSH: 58 e TripDatabase: 32), sendo que
26 foram analisadas (um artigo de revisão e 25 estudos com delineamento
transversal).
Evidências atuais
Todos os estudos analisados, fundamentalmente, avaliaram o desempenho
das estratégias de detecção dos casos em termos de prevalência, proporção
de novos casos e os custos da estratégia.(71,113,118-136) Nenhum estudo
analisa o desempenho em termos do impacto sobre o curso natural da doença
ou da morbimortalidade.
Para discriminar a população maior de 40 anos com fator de risco e justificar o
uso da espirometria, alguns estudos partem da história de exposição ao tabaco
e outros partem dos sintomas respiratórios e, ou da combinação entre eles.
Em todos os estudos, a aplicação de questionários, tanto para a população em
geral (busca ativa) como para a população que procurou o serviço de saúde
por qualquer causa (busca oportuna), permitiu selecionar a população com
maior risco para DPOC e melhorar o rendimento diagnóstico da
espirometria.(125,133) A discriminação do risco inicial pela presença de
sintomas respiratórios crônicos apresentou desempenho inferior ao do
histórico de exposição ao tabaco (10,8% vs. 36,3%).(135) Quando a
discriminação do risco inicial partiu da história de exposição, em particular ao
tabaco, a proporção de casos foi superior à prevalência da DPOC na
população geral.(130) A presença concomitante de sintomas em indivíduos
expostos aumenta a probabilidade do diagnóstico da DPOC. Um estudo
mostrou que a busca de casos da DPOC entre fumantes de clínica de
cessação do tabagismo, com ou sem sintomas respiratórios, pode ter melhor
desempenho do que entre os fumantes sintomáticos na população geral
(13,3% vs. 10,1%).(137) Entretanto, como a população de programas de
cessação do tabagismo tem geralmente maior exposição ao tabaco, este
rendimento não pode ser extrapolado na busca de casos da DPOC para outras
populações que procuram auxilio médico por qualquer motivo. O estudo CODE
realizado na Argentina desenvolveu um questionário de resposta binária para
identificar obstrução do fluxo de ar na população de fumantes com idade igual
ou maior do que 50 anos, história de tabagismo de ≥30 anos-maço, homem,
tosse crônica, expectoração crônica e dispnéia que apresenta a área sob a
curva ROC ( receiver operating characteristic) de 0,75. Miguel A. Bergna,
Gabriel R. García, Ramon Alchapar, Hector Altieri, Juan C. Figueroa Casas,
Luis Larrateguy, Luis J. Nannini, Daniel Pascansky, Pedro Grabre, Gustavo
Zabert and Marc Miravitlles. Development of a simple binary response
questionnaire to identify airflow obstruction in a smoking population in
Argentina. Eur Respir Rev 2015; 24: 320–326.
Recomendações e conclusões
Recomenda-se a realização da espirometria para detecção de casos da DPOC
na população igual ou acima de 40 anos de idade, exposta a fatores de risco
como tabagismo (≥ 10 anos/maço), exposição à fumaça de lenha (≥ 200
horas/ano ou ≥10 anos) ou exposição a fatores ocupacionais, com ou sem
sintomas respiratórios, tanto na população que não procura auxilio médico
(busca ativa de casos) como na população que realiza consulta médica por
qualquer motivo (busca oportuna de casos).
Assim, existe evidência fraca e recomendação forte para a realização de
espirometria na população exposta a fatores de risco com e sem sintomas
respiratórios.
Avaliação complementar
Uma vez confirmado o diagnóstico da DPOC recomenda-se as seguintes
avaliações:
•
Índice de massa corpórea (IMC=peso [kg]/altura [m]2). Na DPOC,
valores inferiores a 25kg / m2 estão associados com pior prognóstico (ERS
Task Force, Schols AM et al.A Nutritional assessment and therapy in COPD: a
European Respiratory Society Statement. Eur Respir J 2014; 44: 1504- 1520.)–
•
Gravidade, frequência das exacerbações e hospitalizações por DPOC
no ano anterior.(74,140)
•
Identificação de comorbidades (índice COTE). A explicação mais
pormenorizada deste índice está na secção comorbidades (Tabela 3).(138,139
,141)
•
A gravidade da dispneia por meio da escala mMRC (Tabela 1).
•
A oximetria de pulso (SpO2) em repouso e em ar ambiente serve como
triagem para o diagnóstico de insuficiência respiratória crônica. A presença de
dessaturação durante atividade (TC6M ou teste do degrau) está associada a
alteração da relação ventilação-perfusão. Entretanto, seu uso para indicar
suplementação de oxigênio ainda é controverso.
•
Radiograma de tórax. Recomenda-se na avaliação inicial para excluir
outras doenças como câncer de pulmão, tuberculose e doenças ocupacionais.
Em casos da DPOC moderada e grave pode-se encontrar sinais de
hiperinflação (retificação do diafragma, aumento de ar no espaço retrosternal,
aumento do diâmetro vertical do tórax entre outros) e sinais de hipertensão
pulmonar direita.
•
Hemoglobina e hematócrito para excluir policitemia associada à
hipoxemia.
•
Dosagem de alfa1-antitripsina. Segundo a Organização Mundial de
Saúde todos os pacientes com DPOC devem ter ao menos uma dosagem de
alfa1-antitripsina
•
Gasometria arterial. Recomenda-se na avaliação inicial de pacientes
com obstrução grave ou muito grave (VEF1<50% do previsto), saturação em
repouso<92% e naqueles com manifestações clínicas da hipoxemia (cianose,
cor pulmonale e hipertensão pulmonar) para determinar a necessidade de
oxigênio
ambulatorial.
Em
estádios
avançados
a
hipoxemia
freqentemente associada à hipercapnia, outro marcador de gravidade.
está
•
Teste de caminhada de seis minutos (TC6M). A distância percorrida em
metros reflete a capacidade funcional dos pacientes.(142-144) Este teste é
recomendado para avaliar a tolerância ao exercício, determinar o índice BODE,
medir o efeito do treinamento em programas de reabilitação pulmonar e outras
intervenções terapêuticas.(145-148)
•
Capacidade de difusão de monóxido de carbono (DLCO).
Diminuição da DLCO se correlaciona com a gravidade do enfisema medida por
tomografia computadorizada com alta resolução (TCAR). A sua medição pode
ser útil para o diagnóstico diferencial com asma. Alguns estudos têm mostrado
que, ao contrário da DPOC relacionada ao tabagismo, a DLCO na DPOC por
fumaça lenha é maior.(149,150) Este é o resultado de menor grau de enfisema
e maior comprometimento das vias aéreas na doença relacionada a este fator
de risco.(31,149-151)
•
Tomografia de tórax de alta resolução (TCAR). A TCAR é útil para
determinar os danos estruturais por DPOC, especialmente o grau de enfisema
e presença de bronquiectasia.(152,153) O grau de enfisema tem sido
associado com a gravidade, a progressão e o prognóstico da DPOC. No
entanto, as implicações clínicas da tomografia ainda são limitadas e não é
recomendada como exame de rotina em todos os pacientes diagnosticados.
•
Eletrocardiograma e ecocardiograma. São indicados se existe suspeita
clínica ou radiográfica de hipertensão pulmonar ou em casos em que a
dispneia seja desproporcional à função pulmonar e exista evidência ou
suspeita de doença cardiovascular.
•
Índice BODE. Este índice foi desenvolvido para ser um modelo
multidimensional de previsão de mortalidade na DPOC.(154) É um índice que
utiliza variáveis não invasivas, de fácil obtenção, baixo custo e com poder
prognóstico (dispnéia, VEF1, IMC e TC6M). Sua pontuação varia de 0 (melhor
prognóstico) a 10 (pior prognóstico) (Tabela 4). Aumento de um ponto eleva a
mortalidade por todas as causas e por causas respiratórias em 34% e 62%,
respectivamente.(154)
Estratificação da gravidade, comorbidade e avaliação prognóstica
A Figura 1 ilustra a proposta de estratificação da gravidade combinada da
DPOC com a avaliação de comorbidade e prognóstico. Uma abordagem
sequencial é proposta em quatro etapas:
• ETAPA 1 e 2 (estratificação da gravidade): impacto clínico, funcional e risco
de exacerbações ou hospitalizações por exacerbações.
• ETAPA 3: Avaliação de comorbidades.
• ETAPA 4: Estabelecimento de prognóstico.
Estadiamento da gravidade
O estadiamento da gravidade é baseado na intensidade da dispneia, no grau
de obstrução e na frequência de exacerbações ou hospitalizações associadas
às exacerbações no ano anterior. Estas variáveis são de fácil medição e podem
ser usadas em qualquer nível de atenção médica e representam diferentes
dimensões da doença.
Recomenda-se a Escala mMRC (Tabela 1) para avaliação da dispneia,
considerando-se os graus 0 e 1 como leve, 2 como moderada, 3 como intensa
e 4 como muito intensa. A gravidade da obstrução se determina com o VEF1%
pós-BD (Tabela 2). O risco de exacerbação se avalia pela história de
exacerbações ou hospitalizações no último ano (≥2 exacerbações ou ≥1
hospitalizacão por exacerbação como indicador de doença grave ou muito
grave). Se há discrepância entre a intensidade das variáveis deve-se usar para
definir a gravidade aquela com pontuação mais elevada. As áreas cinzas
escuro na Figura 1 e na Tabela 5 mostram os critérios de avaliação por
especialista.
Comorbidades
A DPOC associa-se a múltiplas doenças crônicas que podem agravar em seu
prognóstico.(155-159) A prevalência de comorbidades na DPOC é variável,
contudo os estudos mostram que elas são a regra e não a exceção nestes
pacientes.(156-161) A maioria dos pacientes tem ao menos uma comorbidade.
Pacientes com DPOC tem em média mais comorbidades do que os indivíduos
sem DPOC.(161,162)
Doenças cardiovasculares, diabetes, câncer de pulmão, osteoporose, artrite e
transtornos psiquiátricos (ansiedade e depressão) são comuns nos pacientes
com DPOC.(160,163-169)
Em uma coorte de pacientes identificaram-se 12 comorbidades associadas
com maior mortalidade na DPOC, elaborando-se com elas o índice COTE
(COmorbidade e TEste). O câncer (em particular do pulmão, esôfago,
pâncreas e mama), ansiedade, cirrose hepática, fibrilação atrial, diabetes,
fibrose pulmonar, insuficiência cardíaca, úlcera gastroduodenal e doença
coronariana se associaram com maior mortalidade (Tabela 4).(141) Este índice
pode ser utilizado para quantificar o impacto da comorbidade na DPOC e é
uma forma de prevero risco de morte que complementa o prognóstico do índice
BODE. Pontuação do índice ≥4 pontos aumenta em 2,2 vezes o risco de morte
em todos os quartís do índice BODE.(141)
Avaliação prognóstica
O desenvolvimento do índice BODE(154) gerou a proposta de novos índices
prognósticos na DPOC que utilizam diferentes variáveis.
Pergunta: Quais os índices multidimensionais que tem sido validados para
prever a mortalidade na DPOC?
Justificativa
Apesar do conhecimento que a deterioração da função pulmonar está
relacionada com a morbimortalidade na DPOC, a natureza heterogênea da
doença obriga a buscare validar marcadores prognósticos de caráter
multidimensional.(170-175) Algumas variáveis como a gravidade da dispneia,
idade, capacidade de exercício, IMC, exacerbações e qualidade de vida têm
sido utilizadas individualmente como preditoras de mortalidade por todas as
causas. Uma visão mais integral da DPOC deve envolver escalas
multidimensionais que apóiem o clínico na tomada de decisões e na avaliação
do prognóstico. Têm-se propostos vários índices para definir prognóstico na
DPOC. Contudo, persiste a controvérsia sobre quais destes índices preveem
com mais acurácia a mortalidade.
Seleção da busca
Foram obtidas 192 referências (MeSh: 192), sendo que 7 foram selecionadas
para análise (1 revisão sistemática e 6 estudos de coorte).
Resumo da evidência
Uma revisão sistemática(176) descreve a capacidade de predizer mortalidade
de
oito
índices:
ADO
(Age-idade,
Dyspnea-dispneia,
Obstruction-
obstrução),(171,177) BODE (Bodymass index-IMC, Obstruction-obstrução
Dyspnea-dispneia, Exercise-exercício),(154) HADO (Health-saúde, Activityatividade, Dyspnea-dispneia, Obstruction-obstrução),(178) DOREMI BOX
(Dyspnea-dispneia, Obstruction-obstrução, Rate ofExacerbation-taxa de
exacerbação, Movement ExerciseIntolerance-intolerância ao movimento no
exercício, Body Mass Index-IMC, Ox-bloodoxygendisturbances-alterações do
oxigênio sanguíneo),(179) PILE (Predicted FEV1-VEF1 previsto, IL-6 e
KneeExtensor
Strength-fôrça
do
extensor
do
joelho),(180)
eBODE
(BODEplusexacerbations-BODE mais exacerbações) e BODex (Bodymass
index, ObstructionDyspnea, e Exacerbations-e exacerbações).(181)
Outros índices avaliados em ensaios clínicos são o DOSE (Dyspnea-dispneia,
Obstruction-obstrução, Smoking-tabagismo, Exacerbation-exacerbação),(182)
mBODE (VO2% esperado com ergômetro no lugar do teste da caminhada de
6 minutos,(183) mDOSE (DOSE modificado substitui exacerbações por um
questionário de qualidade de vida),(183) i-BODE (substitui o teste da
caminhada
de
6
minutos
pelo
teste
(ClassificationAndRegressionTree-algoritmo
shuttle),(184)
de
e
classificação
CART
e
regressão).(185)
Em pacientes com DPOC, todos estes índices tem capacidade de prever
mortalidade de forma similar ou superior ao VEF1. No estudo COCOMICS, ao
se ajustar por idade, o índice BODE e suas variantes (eBODE e BODEx)
mostram uma discreta superioridade em relação aos demais.(186)
Conclusões e recomendações
A evidência mostra que os índices multidimensionais têm capacidade superior
ao VEF1 isoladamente para prever mortalidade na DPOC.
Assim, temos evidência ALTA e recomendação FORTE para utilizar qualquer
índice como prognóstico, tendo em conta que nenhum deles demonstrou ser
amplamente superior ao outro. Na prática clínica, se recomenda o uso daquele
que melhor se adapte à capacidade de implementação de cada centro,
preferivelmente o BODE ou suas variantes (eBODE e BODEx).
Tabela 1 - Escala de dispneia do Medical Research Council modificada
(mMRC).
Pontuação
Atividade
0
Dispneia a exercícios intensos.
1
Dispneia andando rápido no plano ou subindo aclives leves
2
Andar mais lentamente que pessoas da mesma idade devido à dispneia ou parar para
respirar andando normalmente no plano.
3
Parar para respirar após caminhar uma quadra (90 a 120 metros) ou após poucos
minutos no plano.
4
Não sair de casa devido à dispneia ou dispneico ao vestir-se.
Tabela 2 - Gravidade da obstrução (VEF1/CVF < 0,70 pós-BD).
Gravidade
VEF1 (% previsto)
Leve
> 80%
Moderada
50 - 80%
Grave
30 –<50%
Muito grave
< 30%
Tabela 3 - Índice de comorbidade COTE
Comorbidade
Pontos
Câncer de pulmão, esôfago, pâncreas ou de mama *
6
Ansiedade*
6
Outros tipos de câncer
2
Cirrose hepática
2
Fibrilação atrial / Palpitação
2
Diabetes com neuropatia
2
Fibrose pulmonar
2
Insuficiência cardíaca congestiva
1
Úlcera gástrica/duodenal
1
Doença coronariana
1
*Válido apenas na população feminina.
Tabela 4 - Índice BODE: variáveis e pontuação
Variável / Pontos
0
1
B
Índice de massa corpórea (IMC)
> 21
≤ 21
O
VEF1 (%)
≥ 65
D
Dispneia (mMRC)
0-1
E
Teste de caminhada de 6 minutos (m)
≥ 350
2
3
50-64
36-49
≤ 35
2
3
4
250-349
150-249
≤ 149
Tabela 5 - Critérios para encaminhamento ao pneumologista.
Dúvida diagnóstica.
DPOC grave ou muito grave.
Presença de cor pulmonale.
Avaliação de candidatos a programas de reabilitação pulmonar.
Perda acelerada da função pulmonar (queda do VEF1> 50 mL/ano).
Pacientes com exacerbações frequentes e/ou uso intensivo de recursos de saúde.
Suspeita da DPOCemindivíduos jovens com perda de função pulmonar.
Diagnóstico diferencial com outras doenças respiratórias crônicas.
Sintomas desproporcionais à função pulmonar.
Suspeita de hipoventilação crônica e outros transtornos do sono associados.
Avaliação de incapacidade ocupacional.
Candidatos a tratamento cirúrgico ou endoscópico (redução de volume pulmonar).
Figura 1 - Estratificação combinada da gravidade da DPOC.
DPOC ESTÁVEL E FARMACOTERAPIA
O tratamento da DPOC deve ser individualizado de acordo com a gravidade e
modificado conforme a resposta. Deve abranger as medidas gerais, de
prevenção e farmacológicas.
Medidas gerais e de prevenção
Educação
A transmissão de conceitos sobre a doença para os pacientes e seus familiares
é parte do tratamento. Orientações quanto ao automanejo provavelmente
reduzem a probabilidade de internações.(187)
O conteúdo e a implementação dos programas de educação são
heterogêneos. Os temas mais frequentes são: cessação de tabagismo,
medicamentos,
uso
correto
de
dispositivos
inalatórios,
exercício,
reconhecimento de exacerbações, estratégias para minimizar a dispneia e
oestresse. O objetivo é que o paciente tenha o autocontrole de sua doença e
adequada adesão ao tratamento. Desta forma, se podemevitar as
exacerbações e identificar precocementeos sinais de alerta para avaliação e
tratamento precoces.(187)
Cessação de tabagismo
A DPOC é uma doença prevenível; deixar de fumar é a intervenção mais custoefetiva para a sua prevenção. É também a mais eficaz para retardar a
progressão da doença, aumentar a sobrevida e reduzir a morbidade. Uma
proporção significativa de pacientes, mesmo com doença grave, continuam a
fumar e requerem maior suporte farmacológico e não farmacológico para
abandono do hábito.(188-190)
Uma intervenção mínima, como a utilização de materiais de autoajudapode
aumentar em 1% a taxa de cessação.(191,192) Aconselhamento superior a 3
minutos por médicos ou enfermeiros aumenta esta taxa para 2,5%.(193,194)
O aconselhamento individual tem um efeito dose-resposta de acordo com o
número e duração das sessões.(194) O cenário ideal é de quatro sessões de
10-15 minutos durante os primeiros três meses, após o primeiro dia em que o
paciente para de fumar.(194) A intervenção deve incluir uma explicação do
porquêé necessário deixar de fumar, enfatizando que o tabagismo é uma
doença crônica condicionada pela dependência à nicotina.
As fármacos mais eficazes, com um perfil de segurança adequado, em
pacientes com dependência tabagística moderada incluem terapia de
reposição de nicotina (TRN), bupropiona e vareniclina.(193,194) Bupropiona e
TRN são igualmente eficazes.(193) A vareniclina é superior às formas
individuais de TRN (adesivos, goma, tablete ou pastilha) e à bupropiona. No
entanto, a combinação de dois TRN tem a mesma eficácia que a
vareniclina.(194) Em pacientes com DPOC a terapiafarmacológica combinada
com aconselhamento comportamental ou aconselhamento médico é mais bem
sucedida do que se feito separadamente.(195)
A Tabela 6 resume a dose, o modo de ação e os benefícios de medicamentos
de primeira linha para a cessação do tabagismo.
Exposição à fumaça de biomassa
A exposição à fumaça de biomassa deve ser evitada com a utilização de
exaustores ou cozinhando em ambientes ventilados. A cessação da exposição
à fumaça de lenha tem um impacto favorável sobre os sintomas respiratórios
e a perda de função pulmonar.(196)
Vacinação
Recomendações para o uso da vacina contra influenza e pneumococo são
abordadas na seção exacerbações.
Suporte nutricional
Alterações nutricionais, tanto o baixo índice de massa corpórea como o
sobrepeso ea obesidade são comuns em pacientes com DPOC.(197,198) A
presença de IMC baixo (<20 kg/m2) está associada com aumento da
mortalidade, enquanto que o sobrepeso ea obesidade parecem ter um efeito
protetor.(173,199-202) Descata-se que , de acordo com as recomendações da
Europen Respiratory Society, na DPOC, valores de IMC inferiores a 25kg / m2
estão associados com pior prognóstico.(ERS Task Force, Schols AM et al.A
Nutritional assessment and therapy in COPD: a European Respiratory Society
Statement. Eur Respir J 2014; 44: 1504- 1520)
Em pacientes com má nutrição, a utilização de suplementos nutricionais
promove o ganho significativo de peso, melhora a força dos músculos
respiratórios, a qualidade de vida, as taxas de massa gorda e massa magra, e
a distância no teste da caminhada de 6 minutos.(203-205)
Atividade física
Pacientes com DPOC têm atividade física diária menor que os indivíduos
saudáveis da mesma idade ou que fumantes sem DPOC. A gravidade da
doença não parece ser o principal determinante deste comportamento.(206211)
A medida objetiva da atividade física diária é um preditor independente de
mortalidade por todas as causas e de hospitalizações por exacerbação
grave.(212,213) A atividade física regular por,pelo menos, 30 minutos, três
vezes por semana, reduz o risco de hospitalizações e mortalidade.(214)
Farmacoterapia
A farmacoterapia tem como objetivo principal a redução dos sintomas, da
frequência e gravidade das exacerbações, e melhorar a qualidade de vida, a
função pulmonar e a tolerância ao exercício. A escolha do tratamento depende
da disponibilidade dos medicamentos, da gravidade da doença e da resposta
clínica.
A Tabela 7 mostra os tipos e as doses dosfármacos para o tratamento da
DPOC.
Broncodilatadores
Os broncodilatadores são a pedra angular da terapia medicamentosa. De
acordo com a duração do efeito são classificados como broncodilatadores de
curta ou longa duração de ação e quanto ao mecanismo de ação, em
antimuscarínicos e β2-agonistas. O tratamento regular com broncodilatadores
de longa duração é mais eficaz e conveniente do que com os de curta duração
de ação.(215-217)
Broncodilatadores de curta duração de ação
A duração do efeito de broncodilatadores de curta duração, tais como β2agonistas (salbutamol, fenoterol e terbutalino) e antimuscarínicos (ipratrópio) é
de 6-8 horas. Eles podem ser usados regularmente em caso de não
disponibilidade dos de ação prolongada.
O rápido início de ação permite a sua utilização como medicação de resgate,
mesmo se o paciente usar regularmente broncodilatadores de ação
prolongada. Esta recomendação não é baseada em evidências, por isso o uso
de altas doses de β2-agonistas de curta duração de ação não pode ser
recomendada.
Broncodilatadores de longa duração de ação
Em pacientes sintomáticos é recomendado o uso regular de broncodilatadores
de ação prolongada. Os β2-agonistas de ação prolongada (LABA pelo seu
nome Inglês, long-acting β2-agonists) e os antimuscarínicos de ação
prolongada (LAMA pelo seu nome Inglês, long-acting muscarinic antagonists)
demonstraram benefícios na qualidade de vida, dispneia, exacerbações e
função pulmonar, com um perfil de segurança adequado.(215,218-232)
β2-agonistas de longa duração de ação (LABA)
Estes fármacos estimulam os receptores β2-adrenérgicos e aumentam a
concentração intracelular de AMP-c, o que promove o relaxamento dos
músculos lisos das vias aéreas. Atualmente estão disponíveis LABA de 12
(salmeterol e formoterol) e 24 horas de ação (indacaterol, olodaterol,
vilanterol). A sua eficácia é decorrente de sua longa meia-vida e à maior
seletividade sobre os receptores β2.(233) Os LABA de administração em duas
doses por dia (salmeterol e formoterol) têm demonstrado eficácia no médio e
longo prazo sobre a qualidade de vida e reduçãodas exacerbações, incluindo
as
que
requerem
hospitalização,
com
um
perfil
de
segurança
adequado.(218,222,234) Foi demonstrado que o Indacaterol (LABA de 24
horas)
melhora a dispneia, a função pulmonar, a qualidade de vida e a
tolerância ao exercício.(224-226) A magnitude do benefício não diferiu entre
as doses de 150mcg e 300mcg.(225)
Novos LABA de 24 horas (olodaterol e vilanterol) já estão atualmente
disponíveis. Os estudos mostram um perfil adequado de eficácia, segurança e
tolerabilidade.(235-238)
Antimuscarinicos de ação prolongada (LAMA)
Estes fármacos induzem à broncodilatação por bloqueio dos receptores
muscarínicos das vias aéreas.
O tiotrópio tem uma meia-vida mais longa do que o ipratrópio, com ação
mantida por mais de 24 horas.(239) Melhora a qualidade de vida, reduz o risco
de exacerbações e das hospitalizações delas decorrentes.(228)
O tiotrópio, na dose de 18mcg na forma de pó ou 5mcg na forma líquida, tem
um perfil de segurança e de tolerância adequados.(215,228,229) Estudos de
longo prazo confirmam a segurança do tiotrópio em suas duas formas de
aplicação (HandiHaler e Respimat).(107,230) As informações sobre o perfil de
segurança dos LAMA em pacientes com comorbidade cardiovascular
significativa eram limitadas. .No entanto, o Estutdo Tiospir, com mais de 17 mil
pacientes, comparando 18mcg na forma em pó com o dispositivo Handihaler®
e 5mcg e 2,5mcg na forma de névoa com o dispositivo Respimat®, mostrou
segurança cardiovascular comparável entre eles.
Brometo de aclidínio é um novo LAMA, aprovado na Europa e nos Estados
Unidos. Uma dose de 400 mcg, duas vezes ao dia tem mostrado benefícios na
função pulmonar, dispneia e qualidade de vida, com perfil de ação de início
rápido.(240,241) Os benefícios destes resultados são semelhantes aos obtidos
com tiotrópio e glicopirrônio.(231,232)
O glicopirrônio na forma de pó e dose de 50mcg está disponível e tem perfil de
ação não inferior ao tiotrópio, porém com ação já aos cinco minutos, portanto
mais rápido do que o tiotrópio. Novos LAMA de 24 horas de ação, como o
umeclidínio, estão atualmente em desenvolvimento. Os primeiros estudos
mostram
um
perfil
adequado
de
eficácia,
segurança
e
tolerabilidade.(237,238,242,243)
Metilxantinas
A teofilina é um inibidor não específico da fosfodiesterase (PDE), que aumenta
o AMP-c intracelular, relaxando o músculo liso da via aérea. Tem um discreto
efeito
broncodilatador
em
concentrações
plasmáticasrelativamente
elevadas(10-20 mg/L).(244-246)
O limiar entre o nível terapêutico e o de toxicidade é muito estreito, por isso
seu uso é muito limitado. É recomendado monitorizar os níveis séricos de
teofilina e usar níveis inferiores aos aceitos como broncodilatadores (≤10
mg/L), que demonstraram um efeito de inibição sobre a inflamação das vias
aéreas com um melhor perfil de segurança.(247-250)
Inibidor da fosfodiesterase-4: roflumilaste
As PDEs são enzimas localizadas por todo o corpo, cuja função é a de
hidrolisar o AMP-c. A ação deste segundo mensageiro,reconhecido pelos seus
efeitos anti-inflamatórios em células pró-inflamatórias e imunocompetentes,
pode ser incrementadapela inibição da fosfodiesterase. Esta ação provocaria
um efeito anti-inflamatório.(251) A PDE4 é uma das 11 isoformas da enzima e
poderia ser importante neste mecanismo. O roflumilaste, um inibidor específico
da PDE4, é considerado um antiinflamatório de segunda linha de potencial
utilidade em pacientes com DPOC. O fármaco melhora a função pulmonar e
reduz a probabilidade de exacerbações, com pouco impacto na qualidade de
vida ou sobre os sintomas.(252) Alguns efeitos adversos gastrointestinais
(diarreia, náuseas) e perda de peso são comuns. Os dados de segurança
apresentados à FDA também levantaram preocupações sobre efeitos
colaterais psiquiátricos.(252) Roflumilaste, na dose de 500 mg, por via oral,
pode ser útil como terapia adjuvante para reduzir o número de exacerbações
em pacientes com sintomas de bronquite crônica (tosse e expectoração
broncodilatadores de longa ação. Ele tem ação em pacientes com DPOC em
uso ou não de corticosteroide inalatório (ESTUDO REACT). Martinez FJ et.
Effect of roflumilast on excacerbations in patients with severe chronic
obstructive pulmonary disease uncontrolled by combination therapy (REACT):
a multicentric randomized controlled trial. Lancet. 2015;385(9971):857–866.
Corticosteroides inalados (CI)
O efeito dos CI sobre a inflamação pulmonar e sistêmica em pacientes com
DPOC tem sido motivo de controvérsia. O benefício terapêutico destes
fármacos seria através da diminuição de citoquinas, proteína C reativa e de
células inflamatórias.
Diversos estudos avaliaram o uso dos CI isolados ou combinados com LABA
na DPOC.(253-255) Os potenciais benefícios do CI na DPOC (diminuição da
frequência das exacerbações e redução da deterioração da qualidade de vida),
devem ser avaliados em relação aos efeitos adversos, como candidíase
orofaríngea, disfonia e aumento do risco de pneumonia.(253,256)
A monoterapia a longo prazo com CI não é recomendada em pacientes com
DPOC porque é menos eficaz do que a monoterapia com LABA ou combinação
LABA/CI e aumenta o risco de pneumonia.(257,258)
O uso de corticosteroides sistêmicos em pacientes com DPOC é indicado
apenas durante as exacerbações.
Modalidades terapêuticas
Broncodilatador em monoterapia (LABA ou LAMA)
•A
monoterapia
comum
broncodilatadora,
de
preferência
de
ação
prolongada,está indicada nos pacientes sintomáticos que necessitam de
tratamento regular.
• A seleção inicial do broncodilatador levará em conta a condição particular do
paciente e a disponibilidade local.
Pergunta: Os antimuscarínicos de longa duração de ação proporcionam
pacientes com DPOC?
Justificativa
Os broncodilatadores de longa duração de ação são a base do tratamento da
DPOC estável. Tanto os LAMA quanto os LABA demonstraram benefícios
significativos em alguns desfechos, com um perfil de segurança adequado. Ao
dispor dos dois fármacos, surge a questão se há diferenças em termos de
eficácia e segurança entre eles.
Seleção de busca
Foram encontradas 142 referências (MeSh:
114; Tripdatabase: 28),
sendoselecionadas 4 para análise (2 revisões sistemáticas e dois ensaios
clínicos aleatorizados).
Resumo da evidência
Em termos de eficácia, duas revisões sistemáticas mostraram que a melhora
na qualidade de vida, da intensidade da dispneia, das atividades de vida diária
e
da
função
pulmonar
foi
semelhante
nas
duas
opções
de
tratamento.(219,220) No entanto, o tiotrópio foi superior aos LABA como um
grupo (indacaterol, salmeterol ou formoterol) na reduçãodo número de
exacerbações e hospitalizações relacionadas à DPOC, embora não tenham
sido observadas diferenças significativas na frequência de hospitalizações em
geral (por qualquer causa) e mortalidade.(219,220) Quanto à segurança, uma
revisão sistemática da Cochrane de ensaios clínicos sugere ocorrência inferior
de eventos adversos sérios e abandonos de tratamento com o uso de tiotrópio
em comparação com os LABA.(219)
Um ensaio clínico controlado comparou a eficácia e segurança do indacaterol
e do tiotrópio em pacientes com DPOC grave, indicando que ambas as opções
terapêuticas melhoram a função pulmonar com perfil de segurança
semelhante.(221) O grupo tratado com tiotrópio teve maiores benefícios na
prevenção de exacerbações.
No passado o aumento da mortalidade cardiovascular do tiotrópio administrado
com o dispositivo Respimat®foi tema de controvérsia. Uma revisão sistemática
na qual foram incluídos dois estudos com tiotrópio Respimat® relatou aumento
do risco de mortalidade geral e cardiovascular no grupo em que foi
administrado Respimat® e redução de ambos desfechos com a terapia
combinada salmeterol/fluticasona.(259) No entanto, o estudo de segurança
TioSpir com mais de 17 mil pacientes, no qual o desfecho primário foi
mortalidade, concluiu que a mortalidade global do tiotrópio com o dispositivo
Respimat® (nas doses de 5 mcg ou 2,5 mcg uma vez por dia) foi semelhante
ao tiotrópio com o dispositivo HandiHaler (18 mcg na forma de pó).(230) Neste
estudo foram excluídos pacientes com história de infarto do miocárdio nos
últimos 6 meses, hospitalização prévia por insuficiência cardíaca classe III-IV,
ou arritmia instável ou potencialmente fatal requerendo tratamento nos 12
meses anteriores, mas 10% dos pacientes eram cardiopatas e não houve
diferença na mortalidade.
Não foram encontrados estudos comparativos entre o indacaterol e os novos
LAMA, como glicopirrôneo, aclidinío ou umeclidínio.
Conclusões e recomendações
As evidências indicam que os LAMA e os LABA são igualmente eficazes
quanto à sua ação sobre a dispneia, função pulmonar e qualidade de vida. No,
entanto, estudos de comparação com o tiotrópio mostraram ser ele mais
eficaz do que os LABA para reduzir a frequência das exacerbações. O perfil
de segurança entre as duas opções de tratamento é semelhante.
Em relação ao desfecho avaliado
Evidência
ALTA
e
Recomendação
FORTE
pela
semelhança
dos
broncodilatadores (LABA ou LAMA) em termos de melhora da dispneia,
qualidade de vida e função pulmonar.
Evidência ALTA e Recomendação FORTE para o uso de tiotrópio em relação
aos LABA em pacientes com exacerbações frequentes.
Terapia dupla: associação de dois broncodilatadores de longa duração
ou de um LABA com um corticoide inalatório
Associação de dois broncodilatadores de longa duração com diferentes modos
de ação (LABA + LAMA)
Pergunta: A terapia combinada LABA + LAMA proporciona maiores benefícios
do que LAMA ou LABA em monoterapia em pacientes com DPOC?
Justificativa
Diversos estudos avaliaram a eficácia e segurança da terapia broncodilatadora
dupla (LABA + LAMA), em comparação com LAMA ou LABA em monoterapia.
Em geral, considera-se que a adição de um segundo broncodilatador de longa
duração com um mecanismo de ação diferente aumenta os benefícios sobre
diferentes desfechos. Com base nessas premissas, surge a questão se há
justificativa em acrescentar um segundo broncodilatador a pacientes que
permanecem sintomáticos com broncodilatadoresem monoterapia (LAMA ou
LABA).
Seleção de busca
Foram encontradas 174 referências (MeSh:
70; Tripdatabase: 104) e
selecionadas 6 para análise (3 revisões sistemáticas e 3 ensaios clínicos
aleatorizados).
Resumo da evidência
Em termos de eficácia uma revisão sistemática mostrou discreta melhora na
qualidade de vida com a combinação de tiotrópio e LABA em comparação com
monoterapia com tiotrópio em pacientes com DPOC moderada a grave.(260)
Não foram observadas diferenças em outros desfechos (internações,
mortalidade, função pulmonar, exacerbações e escores de sintomas). Nesta
revisão não foram incluídos estudos que examinaram a eficácia comparativa
da dupla broncodilatação em relação à monoterapia com LABA. É importante
assinalar que o tempo de seguimento dos diferentes estudos incluídos nesta
revisão foi inferior a um ano.
Outra revisão sistemática em pacientes com DPOC moderada a muito grave,
que incluiu estudos com duração inferior a seis meses, indicou maior benefício
da broncodilatação dupla em relação à monoterapia (tiotrópio vs tiotrópio +
LABA) na qualidade de vida, dispneia e função pulmonar, mas não na redução
do risco de exacerbações.(261)
A revisão sistemática realizada por Wang J. et al. em pacientes com DPOC
moderada a grave mostra melhora na função pulmonar e sintomas com
tiotrópio + formoterol em comparação ao tiotrópio isolado.(223) É importante
ressaltar que 7 dos 8 estudos nesta revisão incluíram pacientes em uso de CI,
razão pela qual as conclusões sobre as vantagens da dupla terapia
broncodilatadora em relação à monoterapia não são sustentáveis.
Os resultados de um ensaio clínico aleatorizado comparando tiotrópio +
indacaterol vs tiotrópio em pacientes com DPOC moderada a grave
demonstraram melhora na função pulmonar com a dupla broncodilatação em
um seguimento de 12 semanas.(262) Outro ensaio clínico aleatorizado
comparou indacaterol + glicopirrônio vs glicopirrônio ou tiotrópio em pacientes
comDPOC grave ou muito grave, seguidos por 64 semanas.(263) A terapia
broncodilatadora dupla mostrou maiores benefícios na função pulmonar e
qualidade de vida e maior redução na frequência global de exacerbações em
comparação com os dois fármacos em monoterapia. No entanto, ao analisar
separadamente os tipos de exacerbações, não foram observadas diferenças
na frequência de exacerbações moderadas e graves. Por outro lado, Bateman
et al. compararam a terapia broncodilatadora dupla glicopirrônio + indacaterol
vs placebo, tiotrópio, glicopirrônio e indacaterol (isolados) por seis meses em
pacientes
com
broncodilatadores
DPOC
moderada
obteve
a
resultados
grave.(264)
superiores
A
em
associação
dos
comparação
à
monoterapia com indacaterol, glicoporrônio e tiotrópio quanto à função
pulmonar, dispneia e qualidade de vida.
Quanto à segurança, a frequência de efeitos adversos entre a terapia
broncodilatadora
dupla
e
a
monoterapia
LABA
ou
LAMA
foi
semelhante.(107,262,263)
Conclusões e recomendações
A evidência indica que, em termos de eficácia, a terapia broncodilatadora dupla
tem vantagens em comparação com a monoterapia em pacientes com DPOC
de moderada a muito grave, analisada pela melhora da dispneia, da função
pulmonar e da qualidade de vida, mas não sobre o número de exacerbações.
O perfil de segurança é semelhante em ambas as opções de tratamento.
Evidência ALTA e Recomendação FORTE para o uso de broncodilatação
dupla (LABA + LAMA) vs LAMA ou LABA em pacientes com DPOC moderada
a muito grave, que permanecem sintomáticos ou qualidade de vida muito
comprometida quando medicados com broncodilatadores em monoterapia.
Associação de um LABA com corticoides inalatórios (LABA/CI)
Pergunta: A terapia combinada (LABA/CI) proporciona maiores benefícios do
que LAMA em monoterapia em pacientes com DPOC?
Justificativa
A utilização da associação LABA/CI ou de um LAMA em monoterapia é
frequente em pacientes com DPOC.O tiotrópio é eficaz melhorando a dispneia
e a qualidade de vida, e reduzindo a frequência das exacerbações e
hospitalizações.(107) A associação LABA/CI também reduz o número de
exacerbações, melhora a qualidade de vida e a função pulmonar.(265)
Partindo da premissa das duas opções terapêuticas estarem disponíveis surge
a questão de saber se existem diferenças em termos de eficácia e segurança
entre estes tratamentos.
Seleção de busca
Foram encontradas 32 referências (MeSh: 24; Tripdatabase: 8) e selecionadas
quatro para análise (3 revisões sistemáticas e 1 ensaio clínico aleatorizado).
Resumo da evidência
Em termos de eficácia, a revisão sistemática da Cochrane mostra resultados
semelhantes na frequência das exacerbações, internações hospitalares por
exacerbações e qualidade de vida entre as duas opções de tratamento.(266268) No entanto, o número de desistências em um dos estudos incluídos foi
alta. Como não houve acompanhamento dos pacientes após o abandono,
gerou-se um desequilíbrio entre os grupos, o que limita parcialmente a
aplicabilidade dos resultados.(269)
Outra revisão sistemática e um ensaio clínico aleatorizado mostrou eficácia
semelhante quanto à melhora do VEF1, uso de medicação de resgate, melhora
da qualidade de vida e dispneia.(261,268)
No que diz respeito à segurança, a revisão sistemática da Cochrane mostra
aumento do risco de pneumonia com a combinação salmeterol / fluticasona em
comparação com o tiotrópio. Não foram encontrados estudos que tenham
comparado outras combinações LABA/CI além de salmeterol / fluticasona vs
tiotrópio ou outros LAMA.
Conclusões e recomendações
A evidência indica quea eficácia de LAMA em monoterapia e da terapia
combinada LABA / CI é semelhante. No que diz respeito à segurança, há
evidências de aumento do risco de pneumonia com a associação LABA / CI.
Evidência ALTA para o uso de
tiotrópio ou da combinação (LABA / CI).
Recomendação FRACA em preferir a combinação LABA/CI, devido ao
aumento do risco de pneumonia.
Terapia tripla: Associação de LABA, corticoides inalatórios e tiotrópio.
Pergunta: A associação LABA/CI+ tiotrópio (terapia tripla) oferece maiores
benefícios em comparação com a monoterapia com tiotrópio, a associação
LABA/IC ou a terapia broncodilatadora dupla (LABA + LAMA) em pacientes
com DPOC?
Justificativa
Foi sugerido que a adição de tiotrópio à combinação LABA/CI pode ser
benéfica, reduzindo as exacerbações, as hospitalizações e os custos de saúde
em pacientes com DPOC de moderada a grave. No entanto, persiste a
controvérsia sobre o perfil de eficácia e segurança daterapia tripla (LABA/CI+
tiotrópio) em comparação com a monoterapia (tiotrópio) ou terapia
broncodilatadora dupla (LABA + LAMA).
Seleção de busca
Foram encontradas 32 referências (MeSh: 24; Tripdatabase: 8) e selecionadas
quatro para análise (3 revisões sistemáticas e 1 ensaio clínico aleatorizado).
Resumo da evidência
Uma revisão sistemática encontrou apenas um estudo comparando a terapia
tripla (LABA/CI + tiotrópio) vs a terapia broncodilatadora dupla (LABA + LAMA)
enão mostrou diferenças de eficácia, quanto à qualidade de vida, função
pulmonar,
mortalidade
hospitalizações.(269)
por
Também
qualquer
não
foram
causa,
exacerbações
observadas
diferenças
e
na
frequência de pneumonia e outros eventos adversos. Embora o método
empregado no estudo tenha sido adequado, a frequência alta e irregular de
abandono (26% na terapia tripla e 46% na dupla) tornam os resultados
inconclusivos.
Uma segunda revisão sistemática da Cochrane comparando a terapia tripla
(LABA/CI+ tiotrópio), a terapia combinada (LABA/CI) e a monoterapia
(tiotrópio) indica melhora na qualidade de vida relacionada à saúde e à função
pulmonar com terapia tripla.(270) No entanto, os benefícios sobre a
mortalidade,frequência de internações e exacerbações e risco de pneumonia
em longo prazo com a terapia tripla são incertos.
Outra revisão sistemática comparando a terapia tripla vstiotrópio em
monoterapia mostrou superioridade da terapia tripla em relação à melhora de
função pulmonar e qualidade de vida, sem diferença na taxa de exacerbações,
dispneia, pneumonia, eventos adversos graves e abandonos.(261) Os
resultados de um estudo aberto aleatorizado comparando a terapia tripla vs
monoterapia com tiotrópio mostrou maior eficicáciada terapia tripla sobre a
função pulmonar ea qualidade de vida em pacientes com DPOC (VEF1≤ 65%),
sem diferenças na frequência depneumonia eeventos adversos.(271)
Conclusões e recomendações
A evidência indica que, em termos de eficácia, a terapia tripla tem discreto
benefício sobre a função pulmonar e a qualidade de vida em pacientes com
DPOC moderada a grave, com perfil de segurança comparável a outras
opções de tratamento.
Evidência ALTA e Recomendação FRACA para o uso de terapia tripla em
pacientes com DPOC moderada a grave (VEF1 ≤65%) que persistem com
comprometimento da qualidade de vida apesar de broncodilatação dupla
(LABA + LAMA) ou terapia combinada (LABA/CI).
Esquema de tratamento farmacológico da DPOC estável
Pontos principais
• A monoterapia com LABA ou LAMA é equivalente e pode ser usada
indistintamente para o tratamento da dispneia, melhorar a qualidade de vida e
a função pulmonar de pacientes com DPOC. Recomenda-se o uso de tiotrópio
em pacientes com exacerbações frequentes.
• Recomenda-se a broncodilatação dupla (LABA + LAMA) em pacientes com
DPOC moderada a muito grave que permanecem sintomáticos e com a
qualidade de vida muito comprometida apesar de monoterapia com
broncodilatadores.
• Em termos de eficácia,a monoterapia com LAMA e a terapia combinada
(LABA/CI) são semelhantes. No que diz respeito à segurança, há evidências
de aumento do risco de pneumonia com a terapia combinada (LABA/CI).
• Recomenda-se a terapia tripla (LABA/CI+LAMA) em pacientes com doença
moderada a muito grave, que persistamcom comprometimento da qualidade
de vida apesar de broncodilatação dupla (LABA + LAMA) ou terapia combinada
(LABA/CI).
O tratamento farmacológico da DPOC é feito de forma gradual e escalonada
de acordo com a gravidade da doença (dispneia, obstrução e exacerbações) e
pode ser modificado, dependendo da resposta. A Figura 5 mostra o esquema
geral de tratamento de acordo com a gravidade da DPOC. As medidas gerais
de prevenção e tratamento devem ser aplicadas em todos os pacientes,
independentemente da gravidade.
Em pacientes com indicadores de gravidade leve a moderada (mMRC 0-2 ou
VEF1> 50% pós-BD) é recomendado iniciar o tratamento com monoterapia
broncodilatadora com LAMA ou LABA.
Na doença grave (mMRC 3-4 ou VEF1<50%) ou em pacientes que
permanecem sintomáticos ou com qualidade de vida afetada apesar da
monoterapia,recomenda-se broncodilatação dupla (LABA + LAMA). Em
pacientes com doença grave a muito grave (mMRC 3-4 ou VEF1<50%) que
permaneçam com a qualidade de vida prejudicada apesar de broncodilatação
dupla, recomenda-se a terapia tripla (LABA/CI + LAMA).
Em pacientes com duas ou mais exacerbações ou uma ou maishospitalizações
por exacerbação (DPOC grave a muito grave), com dispneia ou obstrução leve
a moderada (mMRC 0-2 ou VEF1> 50% pós BD) recomenda-semonoterapia
com LAMA, terapia combinada (LABA/CI) ou terapia broncodilatadora dupla,
enquanto que naqueles com mMRC 3-4 ou VEF1<50% recomenda-se terapia
tripla (LABA/CI + LAMA) e considerar a associação com roflumilaste.
Outros tratamentos farmacológicos
O uso de agentes mucolíticos em pacientes com bronquite crônica ou DPOC
está associada com uma pequena redução das exacerbações, mas com
grande heterogeneidade na resposta e sem efeitos na função pulmonar ou na
qualidade de vida dos pacientes.(272)
A administração de N-acetilcisteína pode diminuir a frequência das
exacerbações apenas em pacientes com grau moderado de gravidade que
estejam ou não em uso de CI.(273).A atualização da Estratégia GOLD 2015
recomenda a utilização da N-acetilcisteína para redução da taxa de
exacerbações
em
pacientes
com
DPOC
com
grau
moderado
(www.goldcopd.org – último acesso 20 de agosto de 2015) .
Tratamento não-farmacológico
Oxigenoterapia
Embora a qualidade da evidência seja baixa, postulou-se que o tratamento
com oxigenoterapia prolongada (OP) em média 15 horas/dia reduz a
mortalidade global em pacientes co
insuficiência cardíaca.(274) Em pacientes com hipoxemia moderada (PaO2
entre 59-65mmHg) não se demonstrou qualquer efeito benéfico da OP sobre
a mortalidade por todas as causas.(274) A Tabela 8 apresenta as indicações
de OP em pacientes com DPOC.
Reabilitação pulmonar
A reabilitação pulmonar (RP) é uma intervenção multiprofissional, baseada em
evidências, destinada a reduzir os sintomas, otimizar o estado funcional,
melhorar a qualidade de vida e reduzir os custos de saúde. É definida como
uma intervenção baseada em uma avaliação completa do paciente, seguida
de um tratamento individualizado que inclui treinamento físico, educação e
mudança de comportamento.(275)
Foram publicadas recentemente diretrizes sobre os efeitos, indicações e
componentes desta modalidade terapêutica.(275,276)
Foram também avaliados os efeitos de programas de RP domiciliar como uma
alternativa à RP realizada em hospital, com resultados positivos.(277,278)
Cirurgia de redução de volume e transplante de pulmão
A cirurgia de redução do volume do pulmão é considerada uma alternativa útil
para um subgrupo de pacientes com DPOC grave, já com
a terapia
farmacológica otimizada, antes de oferecer o transplante. Este procedimento
cirúrgico consistena ressecção de áreas com predomínio de enfisema e
aprisionamento aéreo. O objetivo é melhorar o recolhimento elástico, o
funcionamento dos músculos respiratórios, reduzir a hiperinsuflação pulmonar
e o trabalho respiratório, e recuperar áreas de tecido pulmonar funcional.
Estudos observacionais e aleatorizados sugerem que a cirurgia de redução de
volume pulmonar melhora a função pulmonar, a tolerância ao exercício, a
qualidade de vida e a sobrevida em um subgrupo de pacientes com enfisema
adequadamente selecionado (enfisema heterogêneo predominantemente nos
lobos superiores, com VEF1 e DLCO> 20%). Atualmente, esta cirurgia ainda é
uma terapia subutilizada e seu lugar como um tratamento potencialmente
modificador
do
enfisema
grave
ainda
não
está
adequadamente
reconhecida.(279-281)
Várias estratégias broncoscópicas de redução do volume pulmonar foram
introduzidas numa tentativa de reduzir os riscos e custos. Em pacientes com
DPOC grave (VEF1<40%, hiperinsuflação pulmonar e enfisema heterogêneo)
a redução de volume pulmonar mediante a colocação endobrônquica de
válvulas unidirecionais nos segmentos pulmonares afetados não mostrou
efeitos benéficos sobre os desfechos principais, como a mortalidade, e tem
efeitos limitados sobre a função pulmonar, a capacidade de exercício e os
sintomas, com aumento do número de exacerbações, pneumonias e
hemoptise. As informações disponíveis não são suficientes para recomendar
a utilização destas estratégias broncoscópicas.(282,283)
Em pacientes selecionados, o transplante de pulmão produz melhora
significativa da função pulmonar, das trocas gasosas, da tolerância ao
exercício e da qualidade de vida. Recomenda-se considerar o transplante de
pulmão em pacientes que continuam a deteriorar apesar de receber tratamento
médico máximo. Os critérios padrão de indicação de transplante pulmonar na
DPOC incluem: índice BODE de 7 a 10, internações repetidas devido a
exacerbações, hipercapnia (PaCO2> 55 mmHg), distribuição homogênea de
apesar de oxigenoterapia.(284) A sobrevida referida em centros de referência
é de 80% no primeiro ano, 50% em 5 anos e 35% em 10 anos.(285)
Ventilação domiciliar não-invasiva (VNI) no paciente estável
A VNI domiciliar não melhora a mortalidade, a função pulmonar, a tolerância
ao exercício, a qualidade de vida, a força muscular respiratória ou a eficiência
do sono em pacientes com DPOC hipercápnica estável.(286,287) Persiste a
dúvida em relação a potenciais benefícios nas trocas gasosas. Os resultados
de estudos a longo prazo não mostram melhorias significativas nos gases
sanguíneos, na qualidade de vida e na função pulmonar após 12 meses de
VNI domiciliar.(286) No entanto, as pequenas casuísticas desses estudos não
permitem uma conclusão definitiva.
Com base nas informações disponíveis não se pode recomendar de forma
generalizada o uso de VNI em pacientes com DPOC grave estável.
Recomenda-se utilizar este procedimento com precaução em DPOC e apenas
considerar o seu uso em pacientes com hipóxia crônica grave e hipercapnia
que desenvolvam uma condição respiratória instável determinada clinicamente
e confirmada por uma piora progressiva da gasometria arterial.
Cuidados paliativos nos estádios finais da doença
A implementação e o conhecimento dos cuidados paliativos em pacientes com
DPOC grave são muito limitados.(288-290) As recomendações sobre como
abordar o final de vida foram recentemente revistas.(289) As principais
barreiras à sua implementação são: o prognóstico incerto da doença, a atitude
fatalista de alguns profissionais e comunicação ineficaz entre o médico, o
paciente ea família.(291,292)
Esta intervenção deve ser considerada em pacientes com pior prognóstico.
Alguns critérios para identificar esses pacientes são: idade avançada, VEF1<
30%, dispneia intensa (mMRC 3-4), limitação significativa das atividades de
vida diária, depressão, grande utilização de recursos de saúde (exacerbações
frequentes, atendimentos de emergência e/ou internações ), índice BODE de
7 a 10 e índice COTE ≥4.
A abordagem terapêutica nas fases finais da vida deve prestar especial
atenção para o alívio da dispneia, bem como o impacto da ansiedade e da
depressão.(292)
Tabela 6 - Tratamento farmacológico para cessação do tabagismo.
Tipo de
medicamentos
Vareniclina
Bupropiona
Nicotina
(adesivos)
Nicotina
(goma de mascar)
Nicotina
(aerossol nasal
Mecanismo de
ação
Agonista parcial
de receptores
nicotínicos α4β2
Aumenta a
concentração de
dopamina no
cérebro. Atua
nolocus ceruleus.
Atuasobre os
receptores
nicotínicos do
SNC.
Atua sobre os
receptores
nicotínicos do
SNC.
Atua nos
receptores
nicotínicos do
SNC.
Dose
* Día 1-3 (0,5 mg
c/24 h).
*Día 4-7 (0,5 mg
c/12 h).
*Día 8-Sem. 12 (1
mg c/12 h).
*150 mg/dia x 3
días.
*No 4º día 150mg
c/12 h por 7-12
semanas.
Apresentações de
21, 14 e 7 mg
Dose:
21 mg x 4 sem.
14 mg x 2 sem.
7 mg x 2 sem.
Apresentações de
2 e 4 mg.
Dose:
*Até 20 gomas por
dia (4 mg) x 8-12
sem.
Apresentação e
pó de 0,5 mg
Dose:
Iniciar com 2
aplicações por
hora.
Dose máxima 5
aplicações por
hora ou 40 lpor
día.
Contraindicações
Alergia ao
fármaco,
tendências
suicidas,
depressão.
Crises convulsivas,
traumatismos
craneoencefálicos.
Infarto do
miocárdio no mês
prévio,
reação local.
Infarto do
miocárdiono mês
prévio,
problemas de
articulação
mandibular.
Infarto do
miocárdio um m
antes; reação
local.
Tabela 7 - Duração e doses dos broncodilatadores e corticoides inalatórios no
tratamento da DPOC.
Tipo
Apresentação
(μg por inalalação)
Dose média
(μg)
Duração de ação (h)
Neb,100 μg/in
Neb, 20 μg/in
200 μg c/4-6 h
40-80 μg c/6-8 h
4–6
6–8
Broncodilatador de curta ação
Salbutamol
Ipratrópio
Broncodilatador de longa duração de ação
Formoterol
Salmeterol
IPS,4.5-12 μg/in
IPS, 25-50 μg/inh
9-12 μg c/12 h
50 μg c/12 h
+12
+12
Indacaterol
Tiotrópio Respimat
IPS, 150-300 μg/inh
2.5 μg/in
150-300 μg c/24 h
5 μg/in c/24 h
+24
+24
Glicopirrônio
IPS, 50 μg/inh
50 μg c/24 h
+24
IPS,4.5/160 μg/ inh
IPS, 9/320 μg/inh
IDM, 4.5/160 μg/inh
IDM, 9/320 μg/inh
9/320 μg c/12 h
+12
Salmeterol/Fluticasona
IPS, 50/100 μg/inh
IPS, 50/250 μg/inh
IPS, 50/500 μg/inh
IDM, 25/50 μg/inh
IDM, 25/125 μg/inh
IDM, 25/250 μg/inh
50/250-500 μg c/12 h
+12
Formoterol/Beclometasona
IDM 6/100 μg/inh
6/100 μg c/12 h
12
Combinação LABA/CI
Formoterol/Budesonida
Neb: Nebulímetro ou aerossol; IPS: inalador de pó seco; LABA: β2-agonistas de longa duração de
ação; CI: Corticoide inalatório.
Tabela 8 - Recomendações de oxigenoterapia prolongada ao nível do mar.
PaO2≤ 55 mmHg ou SpO2≤ 88% com ou sem hipercapnia.
PaO2 56-59 mmHg ou SpO2 89% associada a: hipertensão pulmonar, e/ou edema periférico,
sugestivo de insuficiência cardíaca congestiva, ou policitemia (hematócrito >55%).
Avaliar a indicação de oxigenoterapia em todo paciente com doença grave.
O objetivo é o de aumentar a PaO2 no mínimo a 60 mmHg e/ou a SpO2 ≥ 90% em repouso ao nível
do mar. É recomendada a utilização por ≥ 15 horas por dia.
Pode-se utilizar a oximetria de pulso para excluir hipoxemia e ajustar os fluxos de O 2.
A avaliação inicial para indicação de oxigenoterapia deve ser realizada em condições estáveis, sob
tratamento otimizado. É necessária a coleta de gasometria arterial, em ar ambiente por 30 minutos,
para medida da PaO2.
Figura 4 - Esquema geral de tratamento de acordo com o nível de gravidade
da DPOC.
DEFINIÇÃO, DIAGNÓSTICO E TRATAMENTO DA EXACERBAÇÃO DA
DPOC
Pontos-chave
• A exacerbação da DPOC é um evento agudo caracterizado por piora da
dispneia , aumento da tosse e / ou expectoração (volume ou purulência).
• Exacerbações pioram o curso natural da doença.
• A principal causa da exacerbação é a infecção respiratória.
• Diagnósticos diferenciais devem ser excluídos antes de iniciar o tratamento
Definição e impacto
A exacerbação da DPOC (E-DPOC) é um evento agudo na evolução da
doença caracterizada por piora da dispneia, aumento da tosse e / ou
expectoração (volume e / ou purulência)
além da variabilidade diária o
suficiente para exigir a modificação do tratamento regular.(293-295)
As E-DPOC são de grande importância devido aos seus efeitos negativos a
longo prazo na função pulmonar, qualidade de vida, piora dos sintomas,
aumento da mortalidade e custos de cuidados de saúde.(140,296-304)
A mortalidade intra-hospitalar durante a E-DPOC varia entre 3,6 e 11%. O risco
de hospitalização pode aumentar de 23 a 43% durante o ano seguinte à
hospitalização.Em pacientes internados em unidade de terapia intensiva (UTI),
a mortalidade hospitalar é de 24%, chegando a 42% no decorrer de um
ano.(305,306) A fatalidade calculada (excesso de mortalidade em comparação
com DPOC estável) é de 15,6%, o que realça a importância das medidas de
prevenção de exacerbações.(307)
Fatores associados com mau prognóstico no E-DPOC são hipoxemia,
hipercapnia, hipoalbuminemia (<2,5 g / dl), IMC <20 kg / m2), história de
exacerbações anteriores, uso prolongado de corticosteroides orais e presença
de hipertensão pulmonar.(74,308 -311)
Diagnóstico
Atualmente, o diagnóstico de E-DPOC baseia-se unicamente na apresentação
clínica (sintomas respiratórios). Não há nenhum biomarcador ou conjunto deles
para confirmar ou excluir o diagnóstico de E-DPOC, pois este é um diagnóstico
de exclusão. A apresentação é variável e pode ser aguda ou progressiva desde
o início. Além disso, a resolução pode ser rápida ou lenta.(312) Levando-se
em conta a frequência das exacerbações,os pacientes podem ser classificados
em exacerbadores frequentes ou infrequentes(76):
Exacerbador frequente: são aqueles indivíduos com 2 ou mais exacerbações
por ano; cada uma separada por, pelo menos, 4 semanas após o fim do
tratamento da exacerbação anterior ou 6 semanas a partir do início do evento
em casos que não tenham sido tratados.
Exacerbador infrequente: são aqueles com uma ou nenhuma exacerbação por
ano. A história de exacerbações no ano anterior é o melhor preditor de
exacerbações futuras.(76,313)
Prevenção
A prevenção da E-DPOC é considerada um objetivo clínico muito importante.
A cessação do tabagismo reduz o risco de exacerbações em 20-30%,
especialmente em pacientes com maior duração da abstinência.(314,315)
Adesão adequada ao tratamento e o uso correto da terapia inalatória reduz o
risco de exacerbações.(316) Os programas de auto-manejo também são
benéficos
para
reduzir
o
risco
de
hospitalização.(317,318)
Os
broncodilatadores de longa duração e a terapia combinada (LABA / CI)
demonstraram eficácia na redução do número de exacerbações e
hospitalizações
relacionadas
à
doença.(215,218,228,229,234,255,257,263,266)
Pergunta: É justificável a aplicação de vacinas e lisados bacterianos em
pacientes com DPOC?
Justificativa
A maioria das diretrizes de tratamento da DPOC recomendam a aplicação
regular de imunizações contra a gripe e vacinas pneumocócicas para a
prevenção das exacerbações. Esse comportamento pode envolver custo mais
elevado e possíveis efeitos colaterais. Não há evidências para a utilização de
lisados bacterianos por via oral (ou sublingual) para impedir as exacerbações.
Portanto, justifica-se a busca de evidências para apoiar essas intervenções na
prevenção das exacerbações em pacientes com DPOC.
Seleção de busca
Foram encontradas 112 referências (15 Tripdatabase e 97 MeSH) sendo 5
selecionadas para análise ( 4 revisões sistemáticas e 1 meta-análise )
Resumo das evidências
Em termos de eficácia os resultados de uma avaliação de evidência indicam
que, em geral, a probabilidade de não adquirir episódios de infecções
respiratórias agudas associadas com a influenza em indivíduos vacinados
contra a influenza (trivalente, vírus fragmentado e inativado) é de 76%.(319)
Para DPOC leve, moderada ou grave, a eficácia da vacina foi de 84%, 45% e
85%, respectivamente.(319) Não foram observadas diferenças no número de
hospitalizações por episódios de infecções respiratórias agudas relacionadas
com a gripe e a necessidade de ventilação mecânica entre os pacientes
vacinados e do grupo placebo.(319) Resultados similares foram relatados em
outra revisão sistemática.(320) Em termos de segurança, existem diferenças
significativas em comparação com placebo no número de eventos adversos
locais (prurido ou inflamação), mas não na frequencia de reações sistêmicas
(dor de cabeça, mialgia, febre e exantema).(319,320)
Uma revisão sistemática que incluiu estudos com vacinas contra o
pneumococo (polissacarídeo purificado sorotipos 14 e 23) em pacientes com
DPOC não mostrou redução na probabilidade de desenvolvimento de
pneumonia pneumocócica e mortalidade cardiovascular ou por qualquer outra
causa.(321) Também não se
observou redução
na frequencia
de
exacerbações, internações e atendimentos de emergência. No entanto, a
análise de um ensaio clínico em subgrupos de pacientes indicou que a eficácia
na prevenção da pneumonia (pneumocócica e de etiologia desconhecida) em
pacientes com DPOC com idade inferior a 65 anos foi de 76% e de 48%
naqueles com obstrução grave (VEF1<40%).(322) Com relação a segurança,
os efeitos locais e sistêmicos foram comparáveis aos do placebo.(321)
Quanto ao uso de lisados bacterianos obtidos através de proteólise (OM-85
BV) na prevenção da E-DPOC, os resultados de uma meta-análise e revisão
sistemática
não
mostraram
efeitos
sobre
a
prevenção
das
exacerbações.(323,324) Os eventos adversos urológicos e de pele foram
comuns em pacientes que receberam este tratamento.
Conclusões e recomendações
Evidência ALTA e recomendação FORTE para o uso anual da vacina contra
influenza em todos os pacientes com DPOC.
Evidência ALTA e
recomendação
FORTE para o
uso da vacina
antipneumocócica em pacientes com DPOC com menos de 65 anos e / ou com
obstrução grave (VEF1 <40%). Não recomendamos o uso de imunização
generalizada em pacientes com DPOC.
Evidenciar ALTA e recomendação FORTE contra o uso de lisados bacterianos
orais em pacientes com DPOC.
Roflumilaste reduz o número de exacerbações moderadas em pacientes com
doença grave (VEF1<50%), exacerbações frequentes, tosse crônica e
expectoração, sem efeito sobre hospitalizações ou mortalidade.(325,326)
Em pacientes com bronquite crônica, o tratamento continuado com mucolíticos
(N-acetil-cisteína, carbocisteína, ambroxol) pode levar à discreta redução do
número de exacerbações.(272,327) Metanálise recente mostra que o uso d Nacetil-cisteína na dose de 1200 mcg ao dia (600 mcg duas vezes) reduz as
exacerbações em pacientes com obstrução das vias aéreas(328); em
pacientes com bronquite crônica, mas sem obstrução brônquica, o tratamento
regular com 600 mcg ao dia pode ser suficiente.O Documento GOLD 2015
recomenda o seu uso. Mario Cazzola, Luigino Calzetta, Clive Page, Josè
Jardim, Alexander G. Chuchalin, Paola Rogliani, Maria Gabriella Matera,
Influence of low- and high-doses of N-acetylcysteine on chronic bronchitis or
chronic obstructive pulmonary disease exacerbations: a meta-analysis. Eur
Respir Rev 2015.
Os pacientes cujo VEF1 aumenta mais de 200mL aos seis meses da cirurgia
de redução de volume pulmonar tem menor número de exacerbações
comparados com os que receberam somente tratamento clínico.(329,330)
Profilaxia
Pergunta: O uso profilático de antibióticos em pacientes com DPOC estável,
previne exacerbações?
Justificativa:
Há vários anos a possibilidade de reduzir a frequência de exacerbações da
DPOC tem sido avaliada com uso de antibioticoterapia profilática. Os primeiros
estudos demonstraram redução no número de dias, porém, sem mudança na
frequência das exacerbações, mas com surgimento de eventos adversos e
desenvolvimento de resistência bacteriana.(331)
Estudos mais recentes têm investigado a utilização de diferentes esquemas de
tratamento com antibióticos intermitentes a longo prazo, cuja análise dos
desfechos pudessemgerar uma recomendação sobre a sua utilização na
prevenção da E-DPOC.
Seleção de busca
Cento e vinte e três referências (MeSH: 46: Tripdatabase: 77), selecionandose cinco para análise (2 metanálises e 3 ensaios clínicos).
Resumo das evidências
Os resultados das metanálises que avaliaram a prevenção das exacerbações
com uso de macrolídeos mostraram redução da frequência das exacerbações
nos pacientes que receberam estes fármacos profiláticos por ao menos
seismeses.(332,333) É importante destacar a heterogeneidade nos esquemas
dos antibióticos dos estudos incluídos nas metanálises. Também se observou
heterogeneidade no tratamento inalado de manutenção (<50% dos pacientes
recebiam terapia inalatória dupla ou tripla).
Dois ensaios clínicos haviam avaliado a eficácia dos macrolídeos na
prevenção das exacerbações. O uso de 250mg de eritromicina a cada 12 horas
durante 1 ano reduziu as exacerbações moderadas e graves em pacientes
com DPOC moderado a grave.(334) De forma similar, o uso de 250 mg de
azitromicina uma vez ao dia durante 1 ano, diminuiu a frequência das
exacerbações e melhorou a qualidade de vida.(335)
Quanto à segurança, o uso de azitromicina se associou a maior resistência aos
macrolídeos e deterioração auditiva. Nesse estudo não se incluíram pacientes
com taquicardia de repouso, ou risco de intervalo QT prolongado corrigido,
persistindo a controvérsia sobre o risco cardiovascular.(335)
Moxifloxacino (400mg/dia, durante 5 dias) em pulsos a cada 8 semanas por 48
semanas, não modificou a frequência das exacerbações, nem outros
desfechos de importância, tais como, hospitalizações, mortalidade e qualidade
de vida.(336) No entanto, num subgrupo de pacientes com expectoração
purulenta,
omoxifloxacinoreduziu
exacerbações.
significativamente
o
número
de
Os principais eventos adversos associados ao uso do moxifloxacino foram
náuseas, vômitos e diarreia.
Conclusões e recomendações
As evidências mostram que em pacientes com DPOC e risco elevado de
exacerbações, apesar do tratamento com broncodilatadores e CI, o uso de
antibióticos profiláticos pode diminuir a frequência das exacerbações. No
entanto, a presença de efeitos adversos, a possibilidade de favorecer a
resistência bacteriana e a ausência de informações para prolongar estes
esquemas por mais de um ano, impedem de fazer uma recomendação geral
para o seu uso.
Evidência ALTA e recomendação FORTE contra o uso regular de antibióticos
profiláticos na DPOC.
Etiologia
As E-DPOC podem ser desencadeadas por diferentes fatores etiológicos. A
principal causa são as infecções respiratórias por vírus ou bacterianas (Tabela
9).(337,338)
Fatores ambientais como exposições ao dióxido de enxofre, ozônio e outras
partículas tóxicas, assim como as baixas temperaturas são também fatores
desencadeantes.(339,340) Em alguns casos não é possível identificar a
causa.(337)
Diagnóstico diferencial
Manifestações clínicas de E-DPOC podem ser confundidas com as de outras
afecções concomitantes que podem, inclusive, agravar a exacerbação..
Devem ser consideradas no diagnóstico diferencial:
•
Enfermidades pulmonares: pneumonia, derrame pleural, pneumotórax,
tromboembolismo pulmonar, obstrução da via aérea alta e aspiração
recorrente do conteúdo gástrico;
•
Enfermidades não pulmonares: arritmias cardíacas, cardiopatia
isquêmica, insuficiência cardíaca, transtornos da ansiedade ou pânico;
•
Outras: uso de drogas, como os bloqueadores beta-adrenérgicos não
seletivos e sedativos.
Não havendo contraindicações recomenda-se realizar tromboprofilaxia em
pacientes hospitalizados, seguir as medidas para a prevenção de infecção
hospitalar e continuar com o tratamento das comorbidades.
Classificação de gravidade da E-DPOC
Pontos-chave
•
Recomenda-se estratificar segundo o nível de atenção requerida para
seu tratamento e a utilização de recursos terapêuticos: ambulatório,
hospitalizado em enfermaria ou em UTI.
Não existe um critério absoluto para classificar a gravidade das E-DPOC. Uma
forma prática é utilizar o nível de atenção requerida pelo paciente: ambulatório,
hospitalizado em enfermaria ou na UTI, assim como o tratamento
requerido.(341,342) Recomendamos classificar as E-DPOC em leves,
moderadas, graves e muito graves de acordo com os seguintes critérios:
Exacerbação leve: piora dos sintomas que requerem aumento do uso de
broncodilatadores de ação curta em relação às doses habituais (3 ou mais jatos
adicionais por 2 dias consecutivos); tratamento ambulatorial.
Exacerbação moderada: piora dos sintomas que requerem uso de
corticosteroides e/ou antibióticos por via oral; tratamento ambulatorial ou breve
tratamento no serviço de emergência.
Exacerbação grave:
piora dos sintomas que requerem o uso de
corticosteroides e/ou antibióticos por via oral ou endovenoso; tratamento
hospitalizado em enfermaria.
Exacerbação muito grave: piora dos sintomas que põem em perigo a vida do
paciente e que
requer o uso de corticosteroide e/ou antibióticos por via
endovenosa e por vezes ventilação mecânica; tratamento hospitalizado em
UTI.
Tem sido desenvolvidos questionários visando a padronização da avaliação da
gravidade da E-DPOC, citando-se, dentre eles, o EXACT-PRO. Até o
momento, o seu uso está limitado a estudos clínicos, pelo que não se
recomenda seu emprego rotineiro na prática diária.(343)
Fatores a considerar para decisão de hospitalização
A Tabela 10 lista os fatores a serem considerados quando da decisão da
escolha do local de tratamento de pacientes com E-DPOC. Não é necessário
que todos estejam presentes, devendo a decisão ser individualizada. A
ausência dos mesmos define o tratamento ambulatorial.
Tratamento da exacerbação da DPOC
Os objetivos do tratamento da E-DPOC incluem minimizar o impacto da
agudização atual e prevenir o desenvolvimento de exacerbações futuras. Os
medicamentos utilizados no tratamento da E-DPOC são os broncodilatadores,
corticosteroides sistêmicos e antibióticos.
Pergunta: Os antibióticos são eficazes em todas as exacerbações da DPOC?
Justificativa
As infecções respiratórias são as causas mais comuns de E-DPOC e
representam aproximadamente 80% dos casos (50-70% de origem
bacteriana). Por outro lado recomenda-se classificar a gravidade da E-DPOC
de acordo com o local necessário para o tratamento: ambulatório, internação
em enfermaria ou em UTI. Há controvérsia acerca da indicação rotineira de
antibióticos em todos os níveis de gravidade da E-DPOC.
Seleção de pesquisa
Foram identificadas 93 referências (MeSh: 57; Tripdatabase: 35) selecionandose 2 para análise (1 revisão sistemática e 1 ensaio clínico aleatorizado).
Resumo da evidência
Uma revisão sistemática, em termos de eficácia, mostra benefícios
consistentes do uso de antibióticos sobre o risco de fracasso de tratamento,
internação hospitalar e mortalidade nos pacientes com E-DPOC internados em
UTI (344). Em pacientes com exacerbação grave e hospitalizados fora do
ambiente de UTI,o uso de antibióticos reduziu as falhas de tratamento embora
não tenha alteradoa duração da hospitalização e nem a mortalidade. Persiste
a incerteza acerca dos benefícios dos antibióticos na E-DPOC de tratamento
ambulatorial. Não foram observadas diferenças nafalha de tratamento,
reinternação e tempo até a próxima exacerbação quando se comparou
tratamento de curta duração (5-7 dias) com tratamento prolongado (10-14
dias).(344)
Um ensaio clínico aleatorizado que avaliou preditores de desfecho em EDPOC leves e moderadas verificou que a taxa de fracasso clínico sem uso de
antibióticos foi significativamente superior (19,9%) quando comparadacom a
dogrupo que recebeu amoxicilina/ácido.clavulânico (9,5%).(345) Os principais
fatores associados com o aumento do risco de fracasso sem antibióticos foram
a purulência do catarro (OR=6,1, IC95%:1,5-25; p=0,005) e nível de PCR
≥40mg/L (OR=13,4, IC95%: 4,6-38,8; p<0,001). Quando ambos fatores
estavam presentes, a probabilidade de fracasso sem antibióticos foi de
63,7%.(345)
Conclusões e recomendações
A evidência indica que está justificado o uso de antibiótico nasE-DPOC que
requerem hospitalização, particularmente nos pacientes que internam na UTI.
Na E-DPOC leve e moderada recomenda-se considerar o uso de antibiótico
nos pacientes com expectoração purulenta e/ou elevado nível de PCR.
Evidência ALTA e recomendação FORTE para o uso de antibiótico em
exacerbações graves e muito graves.
Evidência ALTA e recomendação FRACA em exacerbações leves e
moderadas com expectoração purulenta e/ou nível elevado de PCR.
Pergunta: Os corticosteroides sistêmicos (via oral ou parenteral) são eficazes
no tratamento das E-DPOC?
Justificativa
Os corticosteroides sistêmicos têm sido utilizados no tratamento
ambulatorial e hospitalar da E-DPOC. Existem evidências que respaldam seu
uso. Entretanto, persistem controvérsias sobre dose, risco de efeitos adversos,
vias de administração e duração do tratamento.
Seleção de pesquisa
Foram selecionadas 36 referências (MeSh: 24;Tripdatabase:36) escolhendose 7 para as análises (3 revisões sistemáticas e 4 ensaios clínicos
aleatorizados).
Resumo da evidência
Duas revisões sistemáticas mostraram benefícios consistentes com o uso de
corticosteróides sistêmicos (oral ou parenteralna redução do risco de falha
terapêutica, duração do tempo de internação, recorrências e readmissões em
30 dias, melhora do VEF1, gases arteriais e dispneia em pacientes com EDPOC tratados em ambulatório ou internados.(346,347) Os estudos incluem
poucos pacientes tratados em ambulatórios, por isso, as recomendações
nestes casos devem ser avaliadas com cautela.
Os resultados de três revisões sistemáticas e dois ensaios clínicos
aleatorizados apoiam o uso da prednisona por via oral como primeira escolha
(30-60 mg/dia) durante 5 a 14 dias ou metilprednisolona em doses
equivalentes.(348-351) As evidências indicam igual efeito sobre os desfechos
clínicos quando são comparados esquemas de tratamento de 5 dias versus 14
dias com prednisona oral na dose de 40 mg/dia. Há evidências que
demonstram que os esquemas de tratamento de curta duração (5-7 dias) são
tão eficazes quanto os de longa duração (10-14 dias). Entretanto, com os
esquemas de curta duração observa-se menor frequência de efeitos adversos
como hiperglicemia e infecções respiratórias.
Em relação à via de administração, em termos de eficácia, não há diferença
entre a via intravenosa ou oral, entretanto, a via parenteral se associa com
maior custo e complicações locais.(348,350) Em termos de segurança o
evento adverso mais frequente é a hiperglicemia transitória. Naqueles
pacientes exacerbadores frequentes que necessitam múltiplos ciclos de
corticosteroides, a dose acumulada aumenta o risco de diabetes, osteoporose,
fraturas, ganho de peso, insônia e complicações oculares.(351)
Conclusões e recomendações
A evidência indica que o uso de corticosteroides sistêmicos, preferencialmente
por via oral na dose equivalente de 40 mg/dia de prednisona por 5-10 dias, é
eficaz e seguro no tratamento das exacerbações. Recomenda-se o uso por via
oral devendo-se evitar a via parenteral.
Evidência ALTA e recomendação FORTE a favor do uso de
corticosteroides sistêmicos orais em exacerbações que requerem tratamento
ambulatorial ou hospitalar.
E-DPOC de tratamento ambulatorial
Condições gerais dos pacientes
•
A intensidade dos sintomas não apresenta riscos para a vida do
paciente.
•
Ausência de enfermidade concomitante ou a mesma encontra-se bem
controlada.
•
Ausência dehospitalização por E-DPOC nos seis meses anteriores.
•
Ter apoio domiciliar adequado.
•
Tolerar bem via oral.
Sobre o tratamento ambulatorial
•
O reconhecimento dos sintomas de exacerbação e o tratamento
precoce associam-se com o período de recuperação mais curto, melhora na
qualidade de vida, redução dos riscos de hospitalização, fracasso terapêutico
e de recorrência.(352)
•
Recomenda-se
realizar
um
interrogatório
e
exame
físico
minuciosospara descartar os diagnósticos diferenciais.
•
Não se recomenda realizar estudo bacteriológico de rotina. A Tabela 11
mostra os fatores de risco de infecção por Pseudomonas aeruginosa.(353)
•
Recomenda-se a manutenção do tratamento com broncodilatadores de
ação prolongada e aumentar a frequência dos broncodilatadores de ação curta
(salbutamol, ipratrópio ou combinação de ambos) via aerossol pressurizado ou
nebulizadores. Não existe evidência da superioridade deste último sistema.
•
A Tabela 12 mostra as doses recomendadas dos broncodilatadores de
açãocurta para o tratamento da E-DPOC.
•
Recomenda-se considerar o uso de antibiótico em pacientes com
expectoração purulenta e/ou nível de PCR elevado.
Tempo de monitoramento e recuperação
Há uma grande variabilidade quanto à história natural, frequência e período de
recuperação de exacerbações entre os pacientes. O tempo de recuperação
dos sintomas e da função pulmonar após uma exacerbação da DPOC também
é variável e pode ser superior a um mês em alguns casos.(312,352,354)
A E-DPOC pode se apresentar de duas formas: uma de aparecimento súbito
e outra de início gradual (início dos sintomas cerca de 4 dias).(312) A E-DPOC
de início súbito está associada com o aumento da gravidade dos sintomas
respiratórios e período de recuperação mais curto, enquanto a de início gradual
associa-se com um período de recuperação mais longo. Outros fatores
associados à recuperação tardia (≥ 8 dias) são idade avançada, história de
exacerbações
frequentes,
internações
anteriores
e
comorbidade
cardíaca.(355)
No acompanhamento da E-DPOC é importante orientar o paciente a retornar
à consulta caso não obtenha melhora no prazo de 72 horas. Recomenda-se
uma consulta de controle no prazo de 15 dias para detectar ou prevenir a
recorrência de exacerbações.
Tratamento hospitalar E-DPOC
Critérios de avaliação e internação do paciente
História médica. Para avaliar e descartar diagnósticos diferenciais e
determinar o local da internação: enfermaria geral ou UTI.
Gasometria arterial. Está indicada na presença de SpO2<90% em ar
ambiente, história ou suspeita clínica de hipercapnia, ou critérios de admissão
na UTI (Tabela 10). É útil para o diagnóstico e avaliação da insuficiência
respiratória e para determinar a necessidade de suporte ventilatório.
Radiograma do tórax. Necessária para o diagnóstico diferencial com
outras doenças respiratórias (pneumotórax, pneumonia, edema pulmonar e
derrame pleural).
Eletrocardiograma. Importante para avaliar arritmias, distúrbios de
condução e doença cardíaca isquêmica aguda.
Cultura de escarro. Indicada no caso de pacientes com exacerbação
muito grave ou doentes em risco de infecção por Pseudomonas aeruginosa
(Tabela 11) ou bactéria hospitalar.(356)
Avaliação de comorbidades. É importante avaliar o estado de controle
das
comorbidades,
especialmente
diabetes
mellitus
e
doenças
cardiovasculares
Estudo prospectivo com mais de 300 pacientes mostrou que manter os
broncodilatadores de longa duração reduz o uso de broncodilatadores de curta
ação e o tempo de permanência hospitalar de 6 para 5 dias. A broncodilatação
é semelhante ao se utilizar salbutamol 800mcg em dose acumulativa/dia ou
formoterol 48mcg em dose acumulativa/dia no tratamento da exacerbação.
(Cazzola M, D'Amato M, Califano C, Di Perna F, Calderaro E, Matera MG,
D'Amato G. Formoterol as dry powder oral inhalation compared with salbutamol
metered-dose inhaler in acute exacerbations of chronic obstructive pulmonary
disease. Clin Ther. 2002 Apr;24(4):595-604).
Recomendações para o tratamento hospitalar E-DPOC
Poucos estudos existem sobre o efeito dos broncodilatadores de longa
ação durante a exacerbação.
•
Na exacerbação, as medicações utilizadas pelo paciente devem ser
mantidas. (Puhan MA, Bachmann LM, Kleijnen J, Ter Riet G, Kessels AG.
Inhaled drugs to reduce exacerbations in patients with chronic obstructive
pulmonary disease: a network meta-analysis. BMC Med. 2009 Jan 14;7:2). Os
broncodilatadores de curta duração sob a forma de inaladores dosimetrados
ou nebulizadores devem ser iniciados. (Wise R a, Anzueto A, Cotton D, Dahl
R, Devins T, Disse B, et al. Tiotropium Respimat inhaler and the risk of death
in COPD. N Engl J Med. 2013 369(16):1491–501; Ram FS, Brocklebank DM,
Muers M, Wright J, Jones PW. Pressurised metered-dose inhalers versus all
other hand-held inhalers devices to deliver bronchodilators for chronic
obstructive
pulmonary
disease.
Cochrane
Database
Syst
Rev.
2002;(1):CD002170. PMID 11869627; Brocklebank D, Ram F, Wright J, Barry
P, Cates C, Davies L, Douglas G, Muers M, Smith D, White J. Comparison of
the effectiveness of inhaler devices in asthma and chronic obstructive airways
disease: a systematic review of the literature. Health Technol Assess.
2001;5(26):1-149. Review.
•
O uso de metilxantinas deve ser excluído do tratamento da
exacerbação. (Drescher GS, Carnathan BJ, Imus S, Colice GL. Incorporating
tiotropium into a respiratory therapist-directed bronchodilator protocol for
managing in-patients with COPD exacerbations decreases bronchodilator
costs. Respir Care. 2008 Dec;53(12):1678-84; Barr RG, Rowe BH, Camargo
CA Jr. Methylxanthines for exacerbations of chronic obstructive pulmonary
disease: meta-analysis of randomized trials. BMJ. 2003 20;327 (7416):643.
Erratum in: BMJ. 2003 Oct 18;327(7420):919
•
Nos
pacientes
sob
ventilação
mecânica
a
administração
de
broncodilatadores deve ser realizada com inaladores dosimetrados através do
circuito inspiratório do ventilador, mantendo-se as mesmas doses dos
medicamentos. Yang SC, Yang SP, Lee TS. Nebulized ipratropium bromide in
ventilator-assisted
patients
with
chronic
bronchitis.
Chest.
1994
May;105(5):1511-5; Malliotakis P, Mouloudi E, Prinianakis G, Kondili E,
Georgopoulos D. Influence of respiratory efforts on b2-agonist induced
bronchodilation in mechanically ventilated COPD patients: a prospective
clinical study. Respir Med. 2007 101(2):300-7,; Dhand R, Tobin MJ.
Bronchodilator delivery with metered-dose inhalers in mechanically-ventilated
patients. Eur Respir J. 1996 Mar;9(3):585-95)
A Sociedade Brasileira de Pneumologia e Tisologia recomenda-se não
suspender o tratamento com broncodilatadores de longa duração e iniciar o
tratamento com broncodilatadores de curta duração (salbutamol, ipratrópio ou
sua combinação), em nebulização ou spray (Tabela 12), devendo dar-se
atenção no sentido de prevenir-se sobredose e efeitos colaterais , advindos do
uso excessivo de broncodilatadores
Iniciar
antibióticos
intravenosos,
considerando
os
padrões
de
resistência locais. A forma de seleção inicial do antibiótico está descrita na
Figura 6. Em caso de exacerbações muito graves são recomendadas o uso de
antibióticos endovensos – betalactâmicos ativos contra Pseudomonas
aeruginosa ( cefepima 2 g / 8 horas, 2 g de ceftazidima a cada 8 horas,
piperacilina-tazobactam 4,5 g a cada 6 horas, imipenem 0,5-1 gr a cada 6-8
horas ou meropenem 0,5-1 gr a cada 6-8 horas), isoladamente ou em
combinação com um aminoglicosídeo (tobramicina ou amicacina) durante os
primeiros 3 a 5 dias. A levofloxacina (750 mg IV / 24 horas) ou ciprofloxacina
(400 mg IV c / 8 horas) pode substituir aminoglicosídeos no caso de
contraindicações para a utilização destes e desde que a cepa seja
sensível.(357)
O uso de corticosteróides orais ou intravenosos em exacerbações
graves segue o mesmo padrão de tratamento ambulatorial, mas recomendase administrar as primeiras doses por via endovenosa (metilprednisolona 1020 mg a cada 8 horas ou hidrocortisona 25-50 mg a cada 6 horas) seguida pela
via oral (prednisona 40 mg / dia). Em caso de intolerância à utilização de
medicamentos por via oral, recomenda-se manter a via intravenosa e fazer a
troca por prednisona oral assim que possível, completando-se 5-10 dias de
tratamento.(346-350)
Iniciar oxigenoterapia no caso de SpO2 <90% ou PaO2<60 mmHg (ver
recomendações da oxigenoterapia).
Iniciar ventilação não invasiva (VNI) em pacientes com insuficiência
respiratória que não respondam à terapia convencional (pH> 7,25 e <7,35).
A eficácia clínica da budesonida nebulizada (1-2 mg cada 6 horas) sobre a
função pulmonar e gasometria arterial é comparável à da prednisona por via
oral (40 mg / dia),mas com menor risco de hiperglicemia e com custo mais
elevado e uma maior complexidade na administração.(358-360) Não se
recomenda o uso de corticosteroides nebulizados no tratamento de
exacerbações moderadas a graves que necessitem de hospitalização,
particularmente aqueles suficientemente graves com indicação de UTI. Esta
modalidade terapêutica só deve ser considerada em pacientes diabéticos ou
aqueles exacerbadores frequentes, visando a redução da dose cumulativa de
esteroides.
O uso de metilxantinas (teofilina ou aminofilina) na E-DPOC não melhora os
sintomas, função pulmonar e evolução hospitalar.(361) Os pacientes tratados
com metilxantinas relatam significativamente mais náuseas e vômitos e uma
maior tendência a tremores, palpitações e arritmias. Não se recomenda o uso
desses medicamentos no tratamento da E-DPOC.
Oxigenoterapia
A administração de oxigênio visa corrigir a hipoxemia e prevenir complicações
como a insuficiência respiratória com necessidade de ventilação mecânica e a
mortalidade. Não há evidência suficiente que apoiem o uso de modalidades
diferentes de administração de oxigênio no tratamento pré-hospitalar da EDPOC.(362,363) No entanto, tem sido sugerido que o uso de oxigênio na
ambulância para manter uma SpO2 entre 88-92% está associada à redução
da mortalidade e da incidência de acidose hipercápnica, sem efeito sobre a
necessidade de ventilação mecânica ou de hospitalização. Recomenda-se as
seguintes diretrizes para a terapia de oxigênio, tanto na fase pré-hospitalar
como na hospitalar:
Titular a oferta de oxigênio através de uma cânula nasal (começar com
2 litros por minuto) ou máscara de Venturi (FiO2 0,24-0,28) para manter uma
SpO2> 88% ou PaO2> 60 mmHg, sem causar acidose respiratória (pH <7,30).
Avaliar os gases sanguíneos30 minutos após o início da terapia. Usar ar
comprimido e não oxigênio na nebulização para evitar elevação da PaCO2 e
acidose respiratória em pacientes com hipercapnia prévia.
No caso de pacientes com hipoxemia persistente, considerar a
administração de FiO2 mais altas, desde que não cause acidose respiratória,
e/ou iniciar suporte ventilatório.
Ventilação mecânica não invasiva (VNI)
Indicada em pacientes com insuficiência respiratória sem resposta à
terapia convencional. Nesses pacientes recomenda-se o uso de VNI como
uma primeira linha de tratamento.
Avaliar as alterações na frequência respiratória, PCO2, pH e escala de
Glasgow no momento e duas horas após o início da VNI. Se o paciente não
melhorar, prosseguir com intubação orotraqueal e ventilação mecânica
invasiva.
A VNI é um método de fornecimento de ventilação sem intubação
endotraqueal. Recomenda-se como primeira escolha na E-DPOC com
insuficiência respiratória devendo ser utilizada em centros onde este modo de
ventilação esteja disponível e operado com uma equipe de profissionais
experientes. Os critérios de inclusão e contraindicações relativas são descritas
na Tabela 13.
Estudos com VNI em E-DPOC demonstraram diminuição do trabalho
respiratório, acidose respiratória, mortalidade, necessidade de intubação,
tempo de internação e complicações.(364-366) A relação custo-efetividade do
seu uso é superior á das estratégias-padrão e onde há uma equipe de
profissionais experientes e cujo tratamento posa ser realizado fora da UTI.
Ventilação mecânica invasiva
Pacientes com exacerbações graves ou não responsivos à VNI devem ser
intubados e conectados à ventilação mecânica invasiva. Os critérios de
intubação e ventilação mecânica invasiva estão na Tabela 14. A decisão de
intubação e ventilação mecânica deve ser compartilhada entre o médico, o
paciente e sua família, levando-se também em consideração a opinião do
paciente..
Critérios de alta
A alta hospitalar deve ser considerada quando houver estabilidade clínica e
gasométrica que possibilitem que o paciente controle a sua doença em casa,
ainda que persista uma hipoxemia leve e/ou hipercapnia sem alteração do
pH.(367,368) Aconselha-se uma visita ao médico dentro de duas semanas
após a alta, uma vez que neste período cerca de um quarto dos pacientes
podem apresentar agravamento com aumento do risco de reinternações.(369371)
Reabilitação pulmonar (RP) em pacientes com E-DPOC
A RP pode ser realizada com segurança durante a E-DPOC desde que a
condição do paciente o permita.(372-374) Alguns estudos sugerem que a RP
é segura e eficaz para reduzir internações, morte e melhora da qualidade de
vida
em
pacientes
com
DPOC
que
recentemente
tiveram
uma
exacerbação.(375)
Não há diferenças entre a RP precoce e tardia ou em diferentes níveis de
intensidade devendo-se indicá-la de acordo com as possibilidades de cada
paciente.(372,376,377) O treinamento de resistência do quadríceps e
mobilização precoce dos pacientes mostraram benefícios mensuráveis nos
testes de função pulmonar e um impacto favorável sobre a RP pósexacerbação.(373,378,379)
Tabela 10 - Critérios de hospitalização na E-EPOC
Paciente sem capacidade de autocuidado
Dispneia intensa: mMRC 4
Dispneia grave que não melhora com tratamento otimizado*
Fracasso do tratamento ambulatorial
Comorbidades significativas (diabetes ou cardiovasculares)
Antecedente de três ou mais exacerbações/hospitalizações no último ano
Taquipneia (FR >30)
Estado de consciência alterado*
Uso de músculos ventilatórios acessórios
Respiração paradoxical*
Instabilidade hemodinámica*
Aumento de edema periférico
Hipoxemia grave (SpO2<90%)
Hipercapnia com acidose respiratória*
Tabela 11 - Fatores de risco para infecções por Pseudomonas aeruginosa.
Deterioração da função pulmonar (VEF1< 30% do esperado)
Bronquiectasias
Isolamento de Pseudomonas aeruginosa em exacerbação prévia
Colonização brônquica por Pseudomonas aeruginosa
Tratamento antibiótico nos três meses anteriores ou mais do que 4 cursos por ano
Hospitalização recente
Uso de corticosteroide oral (prednisona>10 mg/día) nas últimas 2 semanas
Tabela 12 - Broncodilatadores para o tratamento da DPOC.
Terapia Broncodilatadora
Ipratrópio
Fenoterol + Ipratrópio
Salbutamol + Ipratrópio
Fenoterol + Ipratrópio
Inalador dosimetrado
(Aerosol)
Iniciar 200-400 mcg c/30 min.
(até 3 vezes)
Manutenção:
200-400 mcg c/4-6 h.
40-80 mcg c/6-8 h.
100-200 + 40-80 mcg c/4-6 h.
200-400 + 40-80 mcg c/4-6 h
100-200 + 40-80 mcg c/4-6 h.
Salbutamol + Ipratrópio
200-400 + 40-80 mcg c/4-6 h
Salbutamol
Nebulização em 3 ml de soro
fisiológico
Iniciar 2,5 - 5 mg c/30 min. (até
3 vezes)
0,25-0,5 mg c/4-6 h.
0,5 + 0,25 mcg c/4-6 h.
5 + 0,25 mcg c/4-6 h
2,5 mg+ 5,0 mg +0, 25 mg –
0,50mgc/4-6 h.
2,5 mg+ 5,0 mg + 0,25mg c/4-6
h
Tabela 13 - Seleção de pacientes para ventilação mecânica não invasiva.
Critérios de Inclusão
Dispneia moderada a grave
Taquipneia > 30 rpm
Paciente capaz de manter via aérea permeável
pH > 7.25 e < 7-35; PaCO2> 50
PaO2< 60 o PaO2/FiO2< 200
Sem pneumotórax ao Rx de tórax
Glasgow > 11pontos
APACHE II < 29
Recusa do paciente
Contraindicações
Parada cardiorrespiratória
Cardiopatía isquêmica ou arritmia cardíaca
instável
Instabilidade hemodinâmica
(PAS < 90 mmHg)
Apneia
Obstrução de via aérea alta
Trauma ou queimadura de face
Hemorragia digestiva alta
Glasgow < 11 pontos
Tabela 14 - Critérios de intubação e ventilação invasiva.
Parada respiratória
Sinais de insuficiência respiratória progressiva
Coma ou agravamento do estado de consciência
Instabilidade hemodinâmica
Deterioração da troca gasosa apesar do manejo médico máximo e adequado
Falha terapêutica ou intolerância à VNI
Referências Bibliográficas
1. Vestbo J, Hurd SS, Agustí AG, Jones PW, Vogelmeier C, Anzueto A, et al.
Global strategy for the diagnosis, management, and prevention of chronic
obstructive pulmonary disease: GOLD executive summary. Am J Respir Crit
Care Med. 2013;187(4):347–65.
2. Miravitlles M, Soler-Cataluña JJ, Calle M, Molina J, Almagro P, Quintano JA,
et al. Guía Española de la EPOC(GesEPOC): Tratamiento farmacológico de la
EPOC estable. Arch Bronconeumol. 2012. ;48(7):247–57.
3. Qaseem A, Wilt TJ, Weinberger SE, Hanania NA, Criner G, van der Molen
T, et al. Diagnosis and management of stable chronic obstructive pulmonary
disease: a clinical practice guideline update from the American College of
Physicians, American College of Chest Physicians, American Thoracic Society,
and European Respiratory Society. Ann Intern Med. 2011;155(3):179–91.
4. Marciniuk DD, Goodridge D, Hernandez P, Rocker G, Balter M, Bailey P, et
al. Managing dyspnea in patients with advanced chronic obstructive pulmonary
disease: a Canadian Thoracic Society clinical practice guideline. Can Respir J.
2011;18(2):69–78.
5. Fervers B, Burgers JS, Haugh MC, Latreille J, Mlika-Cabanne N, Paquet L,
et al. Adaptation of clinical guidelines: literature review and proposition for a
framework and procedure. Int J Qual Health Care. 2006;18(3):167–76.
6. Glasziou P, Del Mar CH SJ. Evidence-based Medicine Workbook. Finding
and applying the best evidence to improve patient care. BMJ Publishing Group;
2003.
7. Casanova C, de Torres JP, Aguirre-Jaíme A, Pinto-Plata V, Marin JM,
Cordoba E, et al. The progression of chronic obstructive pulmonary disease is
heterogeneous: the experience of the BODE cohort. Am J Respir Crit Care
Med. 2011;184(9):1015–21.
8. Nishimura M, Makita H, Nagai K, Konno S, Nasuhara Y, Hasegawa M, et al.
Annual change in pulmonary function and clinical phenotype in chronic
obstructive pulmonary disease. Am J Respir Crit Care Med. 2012;185(1):44–
52.
9. Vestbo J, Edwards LD, Scanlon PD, Yates JC, Agusti A, Bakke P, et al.
Changes in forced expiratory volume in 1 second over time in COPD. N Engl J
Med. 2011;365(13):1184–92.
10. Celli BR, MacNee W. Standards for the diagnosis and treatment of patients
with COPD: a summary of the ATS/ERS position paper. Eur Respir J.
2004;23(6):932–46.
11. Hurd SS, Lenfant C. COPD: good lung health is the key. Lancet.
2005;366(9500):1832–4.
12. Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, et al.
Global and regional mortality from 235 causes of death for 20 age groups in
1990 and 2010: a systematic analysis for the Global Burden of Disease Study
2010. Lancet. 2012;380(9859):2095–128.
13. Bousquet J, Kiley J, Bateman ED, Viegi G, Cruz a a, Khaltaev N, et al.
Prioritised research agenda for prevention and control of chronic respiratory
diseases. Eur Respir J. 2010;36:995–1001.
14. Mannino DM, Buist AS. Global burden of COPD: risk factors, prevalence,
and future trends. Lancet. 2007;370:765–73.
15. Ford ES, Croft JB, Mannino DM, Wheaton AG, Zhang X, Giles WH. COPD
surveillance--United States, 1999-2011. Chest. 2013;144(1):284–305.
16. Rycroft CE, Heyes A, Lanza L, Becker K. Epidemiology of chronic
obstructive pulmonary disease: a literature review. Int J Chron Obstruct Pulmon
Dis. 2012;7:457–94.
17. Ford ES, Mannino DM, Zhao G, Li C, Croft JB. Changes in mortality among
US adults with COPD in two national cohorts recruited from 1971-1975 and
1988-1994. Chest. 2012;141(1):101–10.
18. Gershon AS, Wang C, Wilton AS, Raut R, To T. Trends in chronic
obstructive pulmonary disease prevalence, incidence, and mortality in ontario,
Canada, 1996 to 2007: a population-based study. Arch Intern Med.
2010;170(6):560–5.
19. Mannino DM, Gagnon RC, Petty TL, Lydick E. Obstructive lung disease and
low lung function in adults in the United States: data from the National Health
and
Nutrition
Examination
2000;160(11):1683–9.
Survey,
1988-1994.
Arch
Intern
Med.
20. Peña VS, Miravitlles M, Gabriel R, Jiménez-Ruiz CA, Villasante C, Masa
JF, et al. Geographic variations in prevalence and underdiagnosis of COPD:
results
of
the
IBERPOC
multicentre
epidemiological
study.
Chest.
2000;118(4):981–9.
21. Zhong N, Wang C, Yao W, Chen P, Kang J, Huang S, et al. Prevalence of
chronic obstructive pulmonary disease in China: a large, population-based
survey. Am J Respir Crit Care Med. 2007;176(8):753–60.
22. Buist AS, McBurnie MA, Vollmer WM, Gillespie S, Burney P, Mannino DM,
et al. International variation in the prevalence of COPD (the BOLD Study): a
population-based prevalence study. Lancet. 2007;370(9589):741–50.
23. Halbert RJ, Natoli JL, Gano A, Badamgarav E, Buist AS, Mannino DM.
Global burden of COPD: systematic review and meta-analysis. Eur Respir J.
2006;28(3):523–32.
24. Menezes AMB, Perez-Padilla R, Jardim JRB, Muiño A, Lopez MV, Valdivia
G, et al. Chronic obstructive pulmonary disease in five Latin American cities
(the PLATINO study): a prevalence study. Lancet. 2005;366(9500):1875–81.
25. Caballero A, Torres-Duque CA, Jaramillo C, Bolívar F, Sanabria F, Osorio
P, et al. Prevalence of COPD in five Colombian cities situated at low, medium,
and high altitude (PREPOCOL study). Chest. 2008;133(2):343–9.
26. Pérez-Padilla R, Hallal PC, Vázquez-García JC, Muiño A, Máquez M,
López MV, et al. Impact of bronchodilator use on the prevalence of COPD in
population-based samples. COPD. 2007;4(2):113–20.
27. Tálamo C, de Oca MM, Halbert R, Perez-Padilla R, Jardim JR, Muiño A, et
al. Diagnostic labeling of COPD in five Latin American cities. Chest.
2007;131(1):60–7.
28. Perez-Padilla R, Wehrmeister FC, Celli BR, Lopez-Varela MV, Montes de
Oca M, Muiño A, et al. Reliability of FEV1/FEV6 to diagnose airflow obstruction
compared with FEV1/FVC: the PLATINO longitudinal study. PLoS One.
2013;8(8):e67960.
29. Menezes AM, Lopez M V, Hallal PC, Muiño A, Perez-Padilla R, Jardim JR,
et al. Prevalence of smoking and incidence of initiation in the Latin American
adult population: the PLATINO study. BMC Public Health. 2009;9:151.
30. Hu G, Zhou Y, Tian J, Yao W, Li J, Li B, et al. Risk of COPD from exposure
to biomass smoke: a metaanalysis. Chest. 2010;138(1):20–31.
31. Regalado J, Pérez-Padilla R, Sansores R, Páramo Ramirez JI, Brauer M,
Paré P, et al. The effect of biomass burning on respiratory symptoms and lung
function in rural Mexican women. Am J Respir Crit Care Med. 2006;174(8):901–
5.
32. Ackermann-Liebrich U, Leuenberger P, Schwartz J, Schindler C, Monn C,
Bolognini G, et al. Lung function and long term exposure to air pollutants in
Switzerland. Study on Air Pollution and Lung Diseases in Adults (SAPALDIA)
Team. Am J Respir Crit Care Med. 1997;155(1):122–9.
33. Downs SH, Schindler C, Liu L-JS, Keidel D, Bayer-Oglesby L, Brutsche MH,
et al. Reduced exposure to PM10 and attenuated age-related decline in lung
function. N Engl J Med. 2007;357(23):2338–47.
34. Schindler C, Künzli N, Bongard JP, Leuenberger P, Karrer W, Rapp R, et
al. Short-term variation in air pollution and in average lung function among
never-smokers. The Swiss Study on Air Pollution and Lung Diseases in Adults
(SAPALDIA). Am J Respir Crit Care Med. 2001;163(2):356–61.
35. Anderson HR, Spix C, Medina S, Schouten JP, Castellsague J, Rossi G, et
al. Air pollution and daily admissions for chronic obstructive pulmonary disease
in 6 European cities: results from the APHEA project. Eur Respir J.
1997;10(5):1064–71.
36. Schwartz J. Air pollution and hospital admissions for the elderly in Detroit,
Michigan. Am J Respir Crit Care Med. 1994 150(3):648–55.
37. Burnett RT, Dales R, Krewski D, Vincent R, Dann T, Brook JR. Associations
between ambient particulate sulfate and admissions to Ontario hospitals for
cardiac and respiratory diseases. Am J Epidemiol. 1995;142(1):15–22.
38. Salvi SS, Barnes PJ. Chronic obstructive pulmonary disease in nonsmokers. Lancet. Elsevier Ltd; 2009;374(9691):733–43.
39. Lindberg A, Jonsson A-C, Rönmark E, Lundgren R, Larsson L-G, Lundbäck
B. Ten-year cumulative incidence of COPD and risk factors for incident disease
in a symptomatic cohort. Chest. 2005;127(5):1544–52.
40. Lamprecht B, McBurnie MA, Vollmer WM, Gudmundsson G, Welte T,
Nizankowska-Mogilnicka E, et al. COPD in never smokers: results from the
population-based
burden
2011;139(4):752–63.
of
obstructive
lung
disease
study.
Chest.
41. Po JY, FitzGerald JM, Carlsten C. Respiratory disease associated with solid
biomass fuel exposure in rural women and children: systematic review and
meta-analysis. Thorax. 2011;66(3):232–9.
42. Jordan RE, Cheng KK, Miller MR, Adab P. Passive smoking and chronic
obstructive pulmonary disease: cross-sectional analysis of data from the Health
Survey for England. BMJ Open. 2011;1(2):e000153.
43. Menezes AMB, Hallal PC, Perez-Padilla R, Jardim JRB, Muiño A, Lopez M
V, et al. Tuberculosis and airflow obstruction: evidence from the PLATINO
study in Latin America. Eur Respir J. 2007;30(6):1180–5.
44. Ehrlich RI, Adams S, Baatjies R, Jeebhay MF. Chronic airflow obstruction
and respiratory symptoms following tuberculosis: a review of South African
studies. Int J Tuberc Lung Dis. 2011;15(7):886–91.
45. Silverman EK, Miletich JP, Pierce JA, Sherman LA, Endicott SK, Broze GJ,
et al. Alpha-1-antitrypsin deficiency. High prevalence in the St. Louis area
determined
by
direct
population
screening.
Am
Rev
Respir
Dis.
1989;140(4):961–6.
46. Campos M, Shmuels D, Walsh J. Detection of alpha-1 antitrypsin deficiency
in the US. Am J Med. 2012;125(7):623–4.
47. Eisner MD, Anthonisen N, Coultas D, Kuenzli N, Perez-Padilla R, Postma
D, et al. An official American Thoracic Society public policy statement: Novel
risk factors and the global burden of chronic obstructive pulmonary disease.
Am J Respir Crit Care Med. 2010;182(5):693–718.
48. Han MK, Postma D, Mannino DM, Giardino ND, Buist S, Curtis JL, et al.
Gender and chronic obstructive pulmonary disease: why it matters. Am J Respir
Crit Care Med. 2007;176(12):1179–84.
49. Sørheim I-C, Johannessen A, Gulsvik A, Bakke PS, Silverman EK, DeMeo
DL. Gender differences in COPD: are women more susceptible to smoking
effects than men? Thorax. 2010;65(6):480–5.
50. Lopez Varela M V, Montes de Oca M, Halbert RJ, Muiño a, Perez-Padilla
R, Tálamo C, et al. Sex-related differences in COPD in five Latin American
cities: the PLATINO study. Eur Respir J. 2010;36(5):1034–41.
51. De Torres JP, Casanova C, Hernández C, Abreu J, Aguirre-Jaime A, Celli
BR. Gender and COPD in patients attending a pulmonary clinic. Chest. 2005
Oct;128(4):2012–6.
52. De Torres JP, Cote CG, López M V, Casanova C, Díaz O, Marin JM, et al.
Sex differences in mortality in patients with COPD. Eur Respir J.
2009;33(3):528–35.
53. Martinez FJ, Curtis JL, Sciurba F, Mumford J, Giardino ND, Weinmann G,
et al. Sex differences in severe pulmonary emphysema. Am J Respir Crit Care
Med. 2007;176(3):243–52.
54. Dransfield MT, Washko GR, Foreman MG, Estepar RSJ, Reilly J, Bailey
WC. Gender differences in the severity of CT emphysema in COPD. Chest.
2007;132(2):464–70.
55. Celli B, Vestbo J, Jenkins CR, Jones PW, Ferguson GT, Calverley PM a, et
al. Sex differences in mortality and clinical expressions of patients with chronic
obstructive pulmonary disease. The TORCH experience. Am J Respir Crit Care
Med. 2011;183(3):317–22.
56. Gonzalez A V, Suissa S, Ernst P. Gender differences in survival following
hospitalisation for COPD. Thorax. 2011;66(1):38–42.
57. Hogg JC, Chu F, Utokaparch S, Woods R, Elliott WM, Buzatu L, et al. The
nature of small-airway obstruction in chronic obstructive pulmonary disease. N
Engl J Med. 2004;350(26):2645–53.
58. Cosio MG, Saetta M, Agusti A. Immunologic aspects of chronic obstructive
pulmonary disease. N Engl J Med. 2009;360(23):2445–54.
59. Barnes PJ, Celli BR. Systemic manifestations and comorbidities of COPD.
Eur Respir J. 2009;33(5):1165–85.
60. Macnee W. Pathogenesis of chronic obstructive pulmonary disease. Clin
Chest Med. 2007;28(3):479–513, v.
61. Gosens R, Zaagsma J, Meurs H, Halayko AJ. Muscarinic receptor signaling
in the pathophysiology of asthma and COPD. Respir Res. 2006;7:73.
62. Cortijo J, Mata M, Milara J, Donet E, Gavaldà A, Miralpeix M, et al.
Aclidinium inhibits cholinergic and tobacco smoke-induced MUC5AC in human
airways. Eur Respir J. 2011;37(2):244–54.
63. Iwase N, Sasaki T, Oshiro T, Tamada T, Nara M, Sasamori K, et al.
Differential effect of epidermal growth factor on serous and mucous cells in
porcine airway submucosal gland. Respir Physiol Neurobiol. 2002;132(3):307–
19.
64. Scanlon PD, Connett JE, Waller LA, Altose MD, Bailey WC, Buist AS, et al.
Smoking cessation and lung function in mild-to-moderate chronic obstructive
pulmonary disease. The Lung Health Study. Am J Respir Crit Care Med.
2000;161(2 Pt 1):381–90.
65. Gamble E, Grootendorst DC, Hattotuwa K, O’Shaughnessy T, Ram FS, Qiu
Y, et al. Airway mucosal inflammation in COPD is similar in smokers and exsmokers: a pooled analysis. Eur Respir J. 2007;30(3):467–71.
66. Godtfredsen NS, Lam TH, Hansel TT, Leon ME, Gray N, Dresler C, et al.
COPD-related morbidity and mortality after smoking cessation: status of the
evidence. Eur Respir J. 2008;32(4):844–53.
67. Kohansal R, Martinez-Camblor P, Agustí A, Buist AS, Mannino DM, Soriano
JB. The natural history of chronic airflow obstruction revisited: an analysis of
the Framingham offspring cohort. Am J Respir Crit Care Med. 2009;180(1):3–
10.
68. Pinto-Plata V, Casanova C, Müllerova H, de Torres JP, Corado H, Varo N,
et al. Inflammatory and repair serum biomarker pattern: association to clinical
outcomes in COPD. Respir Res. 2012;13:71.
69. Celli BR, Locantore N, Yates J, Tal-Singer R, Miller BE, Bakke P, et al.
Inflammatory biomarkers improve clinical prediction of mortality in chronic
obstructive
pulmonary
disease.
Am
J
Respir
Crit
Care
Med.
2012;185(10):1065–72.
70. Murphy DE, Panos RJ. Diagnosis of COPD and clinical course in patients
with unrecognized airflow limitation. Int J Chron Obstruct Pulmon Dis.
2013;8:199–208.
71. Lu M, Yao W, Zhong N, Zhou Y, Wang C, Chen P, et al. Asymptomatic
patients of chronic obstructive pulmonary disease in China. Chin Med J (Engl).
2010;123(12):1494–9.
72. Montes de Oca M, Perez-Padilla R, Tálamo C, Halbert RJ, Moreno D, Lopez
MV, et al. Acute bronchodilator responsiveness in subjects with and without
airflow obstruction in five Latin American cities: the PLATINO study. Pulm
Pharmacol Ther. 2010;23(1):29–35.
73. Tsiligianni I, Kocks J, Tzanakis N, Siafakas N, van der Molen T. Factors
that influence disease-specific quality of life or health status in patients with
COPD: a review and meta-analysis of Pearson correlations. Prim Care Respir
J. 2011;20(3):257–68.
74. Suissa S, Dell’Aniello S, Ernst P. Long-term natural history of chronic
obstructive pulmonary disease: severe exacerbations and mortality. Thorax.
2012;67(11):957–63.
75. Wedzicha JA, Brill SE, Allinson JP, Donaldson GC. Mechanisms and impact
of the frequent exacerbator phenotype in chronic obstructive pulmonary
disease. BMC Med. 2013;11:181.
76. Hurst JR, Vestbo J, Anzueto A, Locantore N, Müllerova H, Tal-Singer R, et
al. Susceptibility to exacerbation in chronic obstructive pulmonary disease. N
Engl J Med. 2010;363(12):1128–38.
77. Postma DS, Anzueto AR, Jenkins C, Make BJ, Similowski T, Östlund O, et
al. Factor analysis in predominantly severe COPD: identification of disease
heterogeneity
by
easily
measurable
characteristics.
Respir
Med.
2013;107(12):1939–47.
78. Castaldi PJ, San José Estépar R, Mendoza CS, Hersh CP, Laird N, Crapo
JD, et al. Distinct quantitative computed tomography emphysema patterns are
associated with physiology and function in smokers. Am J Respir Crit Care
Med. 2013;188(9):1083–90.
79. Han MK, Kazerooni EA, Lynch DA, Liu LX, Murray S, Curtis JL, et al.
Chronic obstructive pulmonary disease exacerbations in the COPDGene study:
associated radiologic phenotypes. Radiology. 2011;261(1):274–82.
80. Anthonisen NR, Skeans MA, Wise RA, Manfreda J, Kanner RE, Connett
JE. The effects of a smoking cessation intervention on 14.5-year mortality: a
randomized clinical trial. Ann Intern Med. 2005;142(4):233–9.
81. Han MK, Agusti A, Calverley PM, Celli BR, Criner G, Curtis JL, et al. Chronic
obstructive pulmonary disease phenotypes: the future of COPD. Am J Respir
Crit Care Med. 2010;182:598–604.
82. Dirksen A, MacNee W. The search for distinct and clinically useful
phenotypes in chronic obstructive pulmonary disease. Am J Respir Crit Care
Med. 2013;188(9):1045–6.
83. De Marco R, Pesce G, Marcon A, Accordini S, Antonicelli L, Bugiani M, et
al. The coexistence of asthma and chronic obstructive pulmonary disease
(COPD): prevalence and risk factors in young, middle-aged and elderly people
from the general population. PLoS One. 2013;8(5):e62985.
84. Hardin M, Silverman EK, Barr RG, Hansel NN, Schroeder JD, Make BJ, et
al. The clinical features of the overlap between COPD and asthma. Respir Res.
2011;12:127.
85. Miravitlles M, Soriano JB, Ancochea J, Muñoz L, Duran-Tauleria E,
Sánchez G, et al. Characterisation of the overlap COPD-asthma phenotype.
Focus on physical activity and health status. Respir Med. 2013;107(7):1053–
60.
86. Kim V, Han MK, Vance GB, Make BJ, Newell JD, Hokanson JE, et al. The
chronic bronchitic phenotype of COPD: an analysis of the COPDGene Study.
Chest. 2011;140(3):626–33.
87. Lu M, Yao W, Zhong N, Zhou Y, Wang C, Chen P, et al. Chronic obstructive
pulmonary disease in the absence of chronic bronchitis in China. Respirology.
2010;15(7):1072–8.
88. De Oca MM, Halbert RJ, Lopez MV, Perez-Padilla R, Tálamo C, Moreno D,
et al. The chronic bronchitis phenotype in subjects with and without COPD: the
PLATINO study. Eur Respir J. 2012;40(1):28–36.
89. Ekberg-Aronsson M, Pehrsson K, Nilsson J-A, Nilsson PM, Löfdahl C-G.
Mortality in GOLD stages of COPD and its dependence on symptoms of chronic
bronchitis. Respir Res. 2005;6:98.
90. Burgel P-R, Nesme-Meyer P, Chanez P, Caillaud D, Carré P, Perez T, et
al. Cough and sputum production are associated with frequent exacerbations
and hospitalizations in COPD subjects. Chest. 2009;135(4):975–82.
91. Kessler R, Partridge MR, Miravitlles M, Cazzola M, Vogelmeier C, Leynaud
D, et al. Symptom variability in patients with severe COPD: a pan-European
cross-sectional study. Eur Respir J. 2011;37(2):264–72.
92. O’Donnell DE, Guenette JA, Maltais F, Webb KA. Decline of resting
inspiratory capacity in COPD: the impact on breathing pattern, dyspnea, and
ventilatory capacity during exercise. Chest. 2012;141(3):753–62.
93. Bestall JC, Paul EA, Garrod R, Garnham R, Jones PW, Wedzicha JA.
Usefulness of the Medical Research Council (MRC) dyspnoea scale as a
measure of disability in patients with chronic obstructive pulmonary disease.
Thorax. 1999;54(7):581–6.
94. Kesten S, Chapman KR. Physician perceptions and management of COPD.
Chest. 1993;104(1):254–8.
95. Gallego MC, Samaniego J, Alonso J, Sánchez A, Carrizo S, Marín JM.
Disnea en la EPOC:Relación entre la escala MRC con la disnea inducida por
la prueba de marcha y el ejercicio cardiopulmonar máximo. Arch
Bronconeumol. 2002;38(3):112–6.
96. Serrano J, De Jesús-Berríos Y, Santos RA, Dexter D, Nazario CM,
Montalvo F. Adaptation of the Medical Research Council Dyspnea Scale and
the Oxygen Cost Diagram for its use in Puerto Rico. P R Health Sci J.
2007;26(2):135–40.
97. Agusti A, Calverley PMA, Celli B, Coxson HO, Edwards LD, Lomas DA, et
al. Characterisation of COPD heterogeneity in the ECLIPSE cohort. Respir
Res. 2010;11:122.
98. Mahler DA, Ward J, Waterman LA, Baird JC. Longitudinal changes in
patient-reported dyspnea in patients with COPD. COPD. 2012;9(5):522–7.
99. Mahler DA, Ward J, Waterman LA, McCusker C, Zuwallack R, Baird JC.
Patient-reported dyspnea in COPD reliability and association with stage of
disease. Chest. 2009;136(6):1473–9.
100. Oga T, Nishimura K, Tsukino M, Sato S, Hajiro T, Mishima M. Longitudinal
deteriorations in patient reported outcomes in patients with COPD. Respir Med.
2007;101(1):146–53.
101. Oga T, Tsukino M, Hajiro T, Ikeda A, Nishimura K. Analysis of longitudinal
changes in dyspnea of patients with chronic obstructive pulmonary disease: an
observational study. Respir Res. 2012;13:85.
102. Roche N, Chavannes NH, Miravitlles M. COPD symptoms in the morning:
impact, evaluation and management. Respir Res. 2013;14:112.
103. Miravitlles M. Cough and sputum production as risk factors for poor
outcomes in patients with COPD. Respir Med. 2011;105(8):1118–28.
104. Novosad SA, Barker AF. Chronic obstructive pulmonary disease and
bronchiectasis. Curr Opin Pulm Med. 2013;19(2):133–9.
105. Swanney MP, Ruppel G, Enright PL, Pedersen OF, Crapo RO, Miller MR,
et al. Using the lower limit of normal for the FEV1/FVC ratio reduces the
misclassification of airway obstruction. Thorax. 2008;63(12):1046–51.
106. Pellegrino R, Viegi G, Brusasco V, Crapo RO, Burgos F, Casaburi R, et
al.
Interpretative
strategies
for
lung
function
tests.
Eur
Respir
J.
2005;26(5):948–68.
107. Tashkin DP, Celli B, Senn S, Burkhart D, Kesten S, Menjoge S, et al. A 4year trial of tiotropium in chronic obstructive pulmonary disease. N Engl J Med.
2008;359(15):1543–54.
108. Anthonisen NR, Lindgren PG, Tashkin DP, Kanner RE, Scanlon PD,
Connett JE. Bronchodilator response in the lung health study over 11 yrs. Eur
Respir J. 2005;26(1):45–51.
109. Ben Saad H, Préfaut C, Tabka Z, Zbidi A, Hayot M. The forgotten message
from gold: FVC is a primary clinical outcome measure of bronchodilator
reversibility in COPD. Pulm Pharmacol Ther. 2008;21(5):767–73.
110. Gibson PG, Simpson JL. The overlap syndrome of asthma and COPD:
what are its features and how important is it? Thorax. 2009;64(8):728–35.
111. Price D, Freeman D, Cleland J, Kaplan A, Cerasoli F. Earlier diagnosis
and earlier treatment of COPD in primary care. Prim Care Respir J.
2011;20(1):15–22.
112. Soriano JB, Zielinski J, Price D. Screening for and early detection of
chronic obstructive pulmonary disease. Lancet. 2009;374(9691):721–32.
113. Bednarek M, Maciejewski J, Wozniak M, Kuca P, Zielinski J. Prevalence,
severity and underdiagnosis of COPD in the primary care setting. Thorax.
2008;63(5):402–7.
114. Price D, Crockett A, Arne M, Garbe B, Jones RCM, Kaplan A, et al.
Spirometry in primary care case-identification, diagnosis and management of
COPD. Prim Care Respir J. 2009;18(3):216–23.
115. Scanlon PD, Connett JE, Waller LA, Altose MD, Bailey WC, Buist AS, et
al. Smoking cessation and lung function in mild-to-moderate chronic obstructive
pulmonary disease. The Lung Health Study. Am J Respir Crit Care Med.
2000;161(2 Pt 1):381–90.
116. Lin K, Watkins B, Johnson T, Rodriguez JA, Barton MB. Screening for
chronic obstructive pulmonary disease using spirometry: summary of the
evidence for the U.S. Preventive Services Task Force. Ann Intern Med.
2008;148(7):535–43.
117. Price DB, Tinkelman DG, Nordyke RJ, Isonaka S, Halbert RJ. Scoring
system and clinical application of COPD diagnostic questionnaires. Chest.
2006;129(6):1531–9.
118. Zieliñski J, Bednarek M. Early detection of COPD in a high-risk population
using spirometric screening. Chest. 2001;119(3):731–6.
119. Haroon S, Adab P, Griffin C, Jordan R. Case finding for chronic obstructive
pulmonary disease in primary care: a pilot randomised controlled trial. Br J Gen
Pract. 2013;63(606):e55–62.
120. Jithoo A, Enright PL, Burney P, Buist a S, Bateman ED, Tan WC, et al.
Case-finding options for COPD: results from the Burden of Obstructive Lung
Disease study. Eur Respir J. 2013;41(3):548–55.
121. Bunker J, Hermiz O, Zwar N, Dennis SM, Vagholkar S, Crockett A, et al.
Feasibility and efficacy of COPD case finding by practice nurses. Aust Fam
Physician. 2009;38(10):826–30.
122. Schayck CP Van, Loozen JMC, Wagena E, Akkermans RP, Wesseling
GJ. Primary care. BMJ Prim Care. 2002;324(8):1–5.
123. Jordan RE, Lam KH, Cheng KK, Miller MR, Marsh JL, Ayres JG, et al.
Case finding for chronic obstructive pulmonary disease: a model for optimising
a targeted approach. Thorax. 2010;65(6):492–8.
124. Hamers R, Bontemps S, van den Akker M, Souza R, Penaforte J,
Chavannes N. Chronic obstructive pulmonary disease in Brazilian primary care:
Diagnostic competence and case-finding. Prim Care Respir J. 2006;15(5):299–
306.
125. Castillo D, Guayta R, Giner J, Burgos F, Capdevila C, Soriano JB, et al.
COPD case finding by spirometry in high-risk customers of urban community
pharmacies: a pilot study. Respir Med. 2009;103(6):839–45.
126. Løkke A, Ulrik CS, Dahl R, Plauborg L, Dollerup J, Kristiansen LC, et al.
Detection of previously undiagnosed cases of COPD in a high-risk population
identified in general practice. COPD. 2012;9(5):458–65.
127. Ulrik CS, Løkke A, Dahl R, Dollerup J, Hansen G, Cording PH, et al. Early
detection of COPD in general practice. Int J Chron Obstruct Pulmon Dis.
2011;6:123–7.
128. Vandevoorde J, Verbanck S, Gijssels L, Schuermans D, Devroey D, De
Backer J, et al. Early detection of COPD: a case finding study in general
practice. Respir Med. 2007;101(3):525–30.
129. Buffels J, Degryse J, Heyrman J, Decramer M. Office spirometry
significantly improves early detection of COPD in general practice: the
DIDASCO Study. Chest. 2004;125(4):1394–9.
130. Sansores RH, Ramírez-Venegas A, Hernández-Zenteno R, Mayar-Maya
ME, Pérez-Bautista OG, Velázquez Uncal M. Prevalence and diagnosis of
chronic obstructive pulmonary disease among smokers at risk. A comparative
study of case-finding vs. screening strategies. Respir Med. 2013;107(4):580–
6.
131. Hill K, Goldstein RS, Guyatt GH, Blouin M, Tan WC, Davis LL, et al.
Prevalence and underdiagnosis of chronic obstructive pulmonary disease
among patients at risk in primary care. CMAJ. 2010;182(7):673–8.
132. Takahashi T, Ichinose M, Inoue H, Shirato K, Hattori T, Takishima T.
Underdiagnosis and undertreatment of COPD in primary care settings.
Respirology. 2003;8(4):504–8.
133. Schirnhofer L, Lamprecht B, Firlei N, Kaiser B, Buist a S, Halbert RJ, et al.
Using targeted spirometry to reduce non-diagnosed chronic obstructive
pulmonary disease. Respiration. 2011;81(6):476–82.
134. Tinkelman DG, Price D, Nordyke RJ, Halbert RJ. COPD screening efforts
in primary care: what is the yield? Prim Care Respir J. 2007;16(1):41–8.
135. Konstantikaki V, Kostikas K, Minas M, Batavanis G, Daniil Z,
Gourgoulianis KI, et al. Comparison of a network of primary care physicians
and an open spirometry programme for COPD diagnosis. Respir Med. Elsevier
Ltd; 2011;105(2):274–81.
136. Cui J, Zhou Y, Tian J, Wang X, Zheng J, Zhong N, et al. A discriminant
function model as an alternative method to spirometry for COPD screening in
primary care settings in China. J Thorac Dis. 2012;4(6):594–600.
137. Kögler H, Metzdorf N, Glaab T, Welte T. Preselection of patients at risk for
COPD by two simple screening questions. Respir Med. 2010;104(7):1012–9.
138. Harik-Khan RI, Fleg JL, Wise RA. Body mass index and the risk of COPD.
Chest. 2002;121(2):370–6.
139. Saha A, Barma P, Biswas A, Ghosh S, Malik T, Mitra M, et al. A study of
correlation between body mass index and GOLD staging of chronic obstructive
pulmonary disease patients. J Assoc Chest Physicians. 2013;1(2):58.
140. Soler-Cataluña JJ, Martínez-García MA, Román Sánchez P, Salcedo E,
Navarro M, Ochando R. Severe acute exacerbations and mortality in patients
with chronic obstructive pulmonary disease. Thorax. 2005;60(11):925–31.
141. Divo M, Cote C, de Torres JP, Casanova C, Marin JM, Pinto-Plata V, et
al. Comorbidities and risk of mortality in patients with chronic obstructive
pulmonary disease. Am J Respir Crit Care Med. 2012;186(2):155–61.
142. Casas A, Vilaro J, Rabinovich R, Mayer A, Barberà JA, Rodriguez-Roisin
R, et al. Encouraged 6-min walking test indicates maximum sustainable
exercise in COPD patients. Chest. 2005;128(1):55–61.
143. Spruit MA, Watkins ML, Edwards LD, Vestbo J, Calverley PMA, PintoPlata V, et al. Determinants of poor 6-min walking distance in patients with
COPD: the ECLIPSE cohort. Respir Med. 2010;104(6):849–57.
144. Troosters T, Vilaro J, Rabinovich R, Casas A, Barberà JA, RodriguezRoisin R, et al. Physiological responses to the 6-min walk test in patients with
chronic obstructive pulmonary disease. Eur Respir J. 2002;20(3):564–9.
145. Cote CG, Pinto-Plata V, Kasprzyk K, Dordelly LJ, Celli BR. The 6-min walk
distance, peak oxygen uptake, and mortality in COPD. Chest;132(6):1778–85.
146. Casanova C, Celli BR, Barria P, Casas A, Cote C, de Torres JP, et al. The
6-min walk distance in healthy subjects: reference standards from seven
countries. Eur Respir J. 2011;37(1):150–6.
147. Casanova C, Cote C, Marin JM, Pinto-Plata V, de Torres JP, AguirreJaíme A, et al. Distance and oxygen desaturation during the 6-min walk test as
predictors
of
long-term
mortality
in
patients
with
COPD.
Chest.
2008;134(4):746–52.
148. Pinto-Plata VM, Cote C, Cabral H, Taylor J, Celli BR. The 6-min walk
distance: change over time and value as a predictor of survival in severe COPD.
Eur Respir J. 2004;23(1):28–33.
149. González-García M, Maldonado Gomez D, Torres-Duque CA, Barrero M,
Jaramillo Villegas C, Pérez JM, et al. Tomographic and functional findings in
severe COPD: comparison between the wood smoke-related and smokingrelated disease. J Bras Pneumol. 2013;39(2):147–54.
150. González M, Páez S, Jaramillo C, Barrero M MD. Enfermedad pulmonar
obstructiva crónica (EPOC) por humo de leña en mujeres. Comparación con la
EPOC por cigarrillo. Acta Med Colomb. 2004;29:17–25.
151. Moreira MA, Barbosa MA, Queiroz MC, Antonelli M, Teixeira K, Torres PP,
et al. Pulmonary changes on HRCT scans in nonsmoking females with COPD
due to wood smoke exposure. J Bras Pneumol. 2013;39(2):155–63.
152. Schroeder JD, McKenzie AS, Zach JA, Wilson CG, Curran-Everett D,
Stinson DS, et al. Relationships between airflow obstruction and quantitative
CT measurements of emphysema, air trapping, and airways in subjects with
and without chronic obstructive pulmonary disease. Am J Roentgenol.
2013;201(3):W460–70.
153. Xie X, de Jong PA, Oudkerk M, Wang Y, Ten Hacken NHT, Miao J, et al.
Morphological measurements in computed tomography correlate with airflow
obstruction in chronic obstructive pulmonary disease: systematic review and
meta-analysis. Eur Radiol. 2012;22(10):2085–93.
154. Celli BR, Cote CG, Marin JM, Casanova C, Montes de Oca M, Mendez
RA, et al. The body-mass index, airflow obstruction, dyspnea, and exercise
capacity index in chronic obstructive pulmonary disease. N Engl J Med.
2004;350(10):1005–12.
155. Sin DD, Anthonisen NR, Soriano JB, Agusti AG. Mortality in COPD: Role
of comorbidities. Eur Respir J. 2006;28(6):1245–57.
156. Agusti A, Sobradillo P, Celli B. Addressing the complexity of chronic
obstructive pulmonary disease: from phenotypes and biomarkers to scale-free
networks, systems biology, and P4 medicine. Am J Respir Crit Care Med.
2011;183(9):1129–37.
157. Patel ARC, Hurst JR. Extrapulmonary comorbidities in chronic obstructive
pulmonary disease: state of the art. Expert Rev Respir Med. 2011;5(5):647–62.
158. Holguin F, Folch E, Redd SC, Mannino DM. Comorbidity and mortality in
COPD-related hospitalizations in the United States, 1979 to 2001. Chest.
2005;128(4):2005–11.
159. Burgel P-R, Escamilla R, Perez T, Carré P, Caillaud D, Chanez P, et al.
Impact of comorbidities on COPD-specific health-related quality of life. Respir
Med. 2013;107(2):233–41.
160. Schnell K, Weiss CO, Lee T, Krishnan JA, Leff B, Wolff JL, et al. The
prevalence of clinically-relevant comorbid conditions in patients with physiciandiagnosed COPD: a cross-sectional study using data from NHANES 19992008. BMC Pulm Med. 2012;12:26.
161. Baty F, Putora PM, Isenring B, Blum T, Brutsche M. Comorbidities and
burden of COPD: a population based case-control study. PLoS One.
2013;8(5):e63285.
162. Vanfleteren LEGW, Spruit MA, Groenen M, Gaffron S, van Empel VPM,
Bruijnzeel PLB, et al. Clusters of comorbidities based on validated objective
measurements and systemic inflammation in patients with chronic obstructive
pulmonary disease. Am J Respir Crit Care Med. 2013;187(7):728–35.
163. López Varela MV, Montes de Oca M, Halbert R, Muiño A, Tálamo C,
Pérez-Padilla R, et al. Comorbilidades y estado de salud en individuos con o
sin EPOC en 5 ciudades de América Latina: Estudio PLATINO. Arch
Bronconemol. 2013;49(11):468–74.
164. Sidney S, Sorel M, Quesenberry CP, DeLuise C, Lanes S, Eisner MD.
COPD and incident cardiovascular disease hospitalizations and mortality:
Kaiser Permanente Medical Care Program. Chest. 2005;128(4):2068–75.
165. Müllerova H, Agusti A, Erqou S, Mapel DW. Cardiovascular comorbidity in
COPD: systematic literature review. Chest. 2013;144(4):1163–78.
166. Lee CT-C, Mao I-C, Lin C-H, Lin S-H, Hsieh M-C. Chronic obstructive
pulmonary disease: a risk factor for type 2 diabetes: a nationwide populationbased study. Eur J Clin Invest. 2013;43(11):1113–9.
167. Powell HA, Iyen-Omofoman B, Baldwin DR, Hubbard RB, Tata LJ. Chronic
obstructive pulmonary disease and risk of lung cancer: the importance of
smoking and timing of diagnosis. J Thorac Oncol. 2013;8(1):6–11.
168. Romme EAPM, Smeenk FWJM, Rutten EPA, Wouters EFM. Osteoporosis
in chronic obstructive pulmonary disease. Expert Rev Respir Med.
2013;7(4):397–410.
169. Putman-Casdorph H, McCrone S. Chronic obstructive pulmonary disease,
anxiety, and depression: state of the science. Heart Lung. 2009;38(1):34–47.
170. Nishimura K, Izumi T, Tsukino M, Oga T. Dyspnea is a better predictor of
5-year survival than airway obstruction in patients with COPD. Chest.
2002;121(5):1434–40.
171. Puhan MA, Garcia-Aymerich J, Frey M, ter Riet G, Antó JM, Agustí AG, et
al. Expansion of the prognostic assessment of patients with chronic obstructive
pulmonary disease: the updated BODE index and the ADO index. Lancet.
2009;374(9691):704–11.
172. Oga T, Nishimura K, Tsukino M, Sato S, Hajiro T. Analysis of the factors
related to mortality in chronic obstructive pulmonary disease: role of exercise
capacity and health status. Am J Respir Crit Care Med. 2003;167(4):544–9.
173. Landbo C, Prescott E, Lange P, Vestbo J, Almdal TP. Prognostic value of
nutritional status in chronic obstructive pulmonary disease. Am J Respir Crit
Care Med. 1999;160(6):1856–61.
174. Fan VS, Curtis JR, Tu S-P, McDonell MB, Fihn SD. Using quality of life to
predict hospitalization and mortality in patients with obstructive lung diseases.
Chest. 2002;122(2):429–36.
175. Mannino DM, Reichert MM, Davis KJ. Lung function decline and outcomes
in an adult population. Am J Respir Crit Care Med. 2006;173(9):985–90.
176. Dijk WD Van, Bemt L Van Den, Haak-Rongen S Van Den, Bischoff E,
Weel C Van, Veen JCCM in ’T, et al. Multidimensional prognostic indices for
use in COPD patient care. A systematic review. Respir Res. 2011;12(1):151.
177. Puhan M a, Hansel NN, Sobradillo P, Enright P, Lange P, Hickson D, et
al. Large-scale international validation of the ADO index in subjects with COPD:
an individual subject data analysis of 10 cohorts. BMJ Open. 2012;2(6).
178. Esteban C, Quintana JM, Aburto M, Moraza J, Capelastegui A. A simple
score for assessing stable chronic obstructive pulmonary disease. QJM.
2006;99(11):751–9.
179. Kostianev SS, Hodgev VA, Iluchev DH. Multidimensional system for
assessment of COPD patients. Comparison with BODE index. Folia Med
(Plovdiv). 2008;50(4):29–38.
180. Mehrotra N, Freire AX, Bauer DC, Harris TB, Newman AB, Kritchevsky
SB, et al. Predictors of mortality in elderly subjects with obstructive airway
disease: the PILE score. Ann Epidemiol. 2010;20(3):223–32.
181. Soler-Cataluña JJ, Martínez-García MA, Sánchez LS, Tordera MP,
Sánchez PR. Severe exacerbations and BODE index: two independent risk
factors for death in male COPD patients. Respir Med. 2009;103(5):692–9.
182. Sundh J, Janson C, Lisspers K, Ställberg B, Montgomery S. The
Dyspnoea , Obstruction , Smoking , Exacerbation ( DOSE ) index is predictive
of mortality in COPD. Prim Care Respir J. 2012;21(3):295–301.
183. Oga T, Tsukino M, Hajiro T, Ikeda A, Nishimura K. Predictive properties of
different multidimensional staging systems in patients with chronic obstructive
pulmonary disease. Int J Chron Obstruct Pulmon Dis. 2011;6:521–6.
184. Williams JE a, Green RH, Warrington V, Steiner MC, Morgan MDL, Singh
SJ. Development of the i-BODE: validation of the incremental shuttle walking
test within the BODE index. Respir Med. 2012;106(3):390–6.
185. Esteban C, Arostegui I, Moraza J, Aburto M, Quintana JM, PérezIzquierdo J, et al. Development of a decision tree to assess the severity and
prognosis of stable COPD. Eur Respir J. 2011;38(6):1294–300.
186. Marin JM, Alfageme I, Almagro P, Casanova C, Esteban C, SolerCataluña JJ, et al. Multicomponent indices to predict survival in COPD: the
COCOMICS study. Eur Respir J. 2013;42(2):323–32.
187. Effing T, Monninkhof EM, van der Valk PDLPM, van der Palen J, van
Herwaarden CLA, Partidge MR, et al. Self-management education for patients
with chronic obstructive pulmonary disease. Cochrane Database of Systematic
Review. 2007;(4):CD002990.
188. Warnier MJ, van Riet EES, Rutten FH, De Bruin ML, Sachs APE. Smoking
cessation strategies in patients with COPD. Eur Respir J. 2013;41(3):727–34.
189. Jiménez-Ruiz CA, Riesco Miranda JA, Altet Gómez N, Lorza Blasco JJ,
Signes-Costa Miñana J, Solano Reina S, et al. Tratamiento del tabaquismo en
fumadores con Enfermedad Pulmonar Obstructiva Crónica. Sociedad
Española de Neumología y Cirugía Torácica (SEPAR). Arch Bronconeumol.
2013;49(8):354–63.
190. Jiménez Ruiz CA, Ramos Pinedo A, Cicero Guerrero A, Mayayo Ulibarri
M, Cristobal Fernández M, Lopez Gonzalez G. Characteristics of COPD
smokers and effectiveness and safety of smoking cessation medications.
Nicotine Tob Res. 2012;14(9):1035–9.
191. Aveyard P, Begh R, Parsons A, West R. Brief opportunistic smoking
cessation interventions: a systematic review and meta-analysis to compare
advice to quit and offer of assistance. Addiction. 2012;107(6):1066–73.
192. Tønnesen P. Smoking cessation and COPD. Eur Respir Rev.
2013;22(127):37–43.
193. Cahill K, Stevens S, Perera R, Lancaster T. Pharmacological interventions
for smoking cessation: an overview and network meta-analysis. Cochrane
Database of Systematic Review 2013;5:CD009329.
194. Cahill K, Stead LF, Lancaster T. Nicotine receptor partial agonists for
smoking
cessation.
Cochrane
Database
of
Systematic
Review.
2012;4:CD006103.
195. Strassmann R, Bausch B, Spaar A, Kleijnen J, Braendli O, Puhan MA.
Smoking cessation interventions in COPD: a network meta-analysis of
randomised trials. Eur Respir J. 2009;34(3):634–40.
196. Romieu I, Riojas-Rodríguez H, Marrón-Mares AT, Schilmann A, PerezPadilla R, Masera O. Improved biomass stove intervention in rural Mexico:
impact on the respiratory health of women. Am J Respir Crit Care Med.
2009;180(7):649–56.
197. Vermeeren MA, Creutzberg EC, Schols AM, Postma DS, Pieters WR,
Roldaan AC, et al. Prevalence of nutritional depletion in a large out-patient
population of patients with COPD. Respir Med. 2006;100(8):1349–55.
198. Montes de Oca M, Tálamo C, Perez-Padilla R, Jardim JRB, Muiño A,
Lopez MV, et al. Chronic obstructive pulmonary disease and body mass index
in five Latin America cities: the PLATINO study. Respir Med. 2008;102(5):642–
50.
199. Schols AM, Slangen J, Volovics L, Wouters EF. Weight loss is a reversible
factor in the prognosis of chronic obstructive pulmonary disease. Am J Respir
Crit Care Med. 1998;157(6 Pt 1):1791–7.
200. Vestbo J, Prescott E, Almdal T, Dahl M, Nordestgaard BG, Andersen T, et
al. Body mass, fat-free body mass, and prognosis in patients with chronic
obstructive pulmonary disease from a random population sample: findings from
the Copenhagen City Heart Study. Am J Respir Crit Care Med.
2006;173(1):79–83.
201. Chailleux E, Laaban J-P, Veale D. Prognostic value of nutritional depletion
in patients with COPD treated by long-term oxygen therapy: data from the
ANTADIR observatory. Chest. 2003;123(5):1460–6.
202. Cao C, Wang R, Wang J, Bunjhoo H, Xu Y, Xiong W. Body mass index
and mortality in chronic obstructive pulmonary disease: a meta-analysis. PLoS
One. 2012;7(8):e43892.
203. Ferreira IM, Brooks D, White J, Goldstein R. Nutritional supplementation
for stable chronic obstructive pulmonary disease. Cochrane Database of
Systematic Review. 2012;12:CD000998.
204. Collins PF, Stratton RJ, Elia M. Nutritional support in chronic obstructive
pulmonary disease: a systematic review and meta-analysis. Am J Clin Nutr.
2012;95(6):1385–95.
205. Collins PF, Elia M, Stratton RJ. Nutritional support and functional capacity
in chronic obstructive pulmonary disease: a systematic review and metaanalysis. Respirology. 2013;18(4):616–29.
206. Vorrink SNW, Kort HSM, Troosters T, Lammers J-WJ. Level of daily
physical activity in individuals with COPD compared with healthy controls.
Respir Res. 2011;12:33.
207. Van Remoortel H, Hornikx M, Demeyer H, Langer D, Burtin C, Decramer
M, et al. Daily physical activity in subjects with newly diagnosed COPD. Thorax.
2013;68(10):962–3.
208. Park SK, Richardson CR, Holleman RG, Larson JL. Physical activity in
people with COPD, using the National Health and Nutrition Evaluation Survey
dataset (2003-2006). Heart Lung. 2013;42(4):235–40.
209. Garcia-Rio F, Lores V, Mediano O, Rojo B, Hernanz A, López-Collazo E,
et al. Daily physical activity in patients with chronic obstructive pulmonary
disease is mainly associated with dynamic hyperinflation. Am J Respir Crit Care
Med. 2009;180(6):506–12.
210. Pitta F, Takaki MY, Oliveira NH de, Sant’anna TJP, Fontana AD, Kovelis
D, et al. Relationship between pulmonary function and physical activity in daily
life in patients with COPD. Respir Med. 2008;102(8):1203–7.
211. Bossenbroek L, de Greef MHG, Wempe JB, Krijnen WP, Ten Hacken
NHT. Daily physical activity in patients with chronic obstructive pulmonary
disease: a systematic review. COPD. 2011;8(4):306–19.
212. Waschki B, Kirsten A, Holz O, Müller K-C, Meyer T, Watz H, et al. Physical
activity is the strongest predictor of all-cause mortality in patients with COPD:
a prospective cohort study. Chest. 2011;140(2):331–42.
213. Garcia-Rio F, Rojo B, Casitas R, Lores V, Madero R, Romero D, et al.
Prognostic value of the objective measurement of daily physical activity in
patients with COPD. Chest. 2012;142(2):338–46.
214. Garcia-Aymerich J, Lange P, Benet M, Schnohr P, Antó JM. Regular
physical activity reduces hospital admission and mortality in chronic obstructive
pulmonary disease: a population based cohort study. Thorax. 2006;61(9):772–
8.
215. Cheyne L, Irvin-Sellers MJ, White J. Tiotropium versus ipratropium
bromide for chronic obstructive pulmonary disease. Cochrane Database of
Systematic Review. 2013;9:CD009552.
216. Beeh KM, Beier J. The short, the long and the “ultra-long”: why duration of
bronchodilator action matters in chronic obstructive pulmonary disease. Adv
Ther. 2010;27(3):150–9.
217. Appleton S, Jones T, Poole P, Pilotto L, Adams R, Lasserson TJ, et al.
Ipratropium bromide versus long-acting beta-2 agonists for stable chronic
obstructive pulmonary disease. Cochrane Database of Systematic Review.
2006;(3):CD006101.
218. Kew KM, Mavergames C, Walters JAE. Long-acting beta2-agonists for
chronic obstructive pulmonary disease. Cochrane Database of Systematic
Review. 2013;10:CD010177.
219. Chong J, Karner C, Poole P. Tiotropium versus long-acting beta-agonists
for stable chronic obstructive pulmonary disease. Cochrane Database of
Systematic Review. 2012;(9):008567
220. Rodrigo GJ, Neffen H. Comparison of indacaterol with tiotropium or twicedaily long-acting β -agonists for stable COPD: a systematic review. Chest.
2012;142(5):1104–10.
221. Decramer ML, Chapman KR, Dahl R, Frith P, Devouassoux G, Fritscher
C, et al. Once-daily indacaterol versus tiotropium for patients with severe
chronic obstructive pulmonary disease (INVIGORATE): a randomised, blinded,
parallel-group study. Lancet Respir Med. 2013;1(7):524–33.
222. Decramer ML, Hanania NA, Lötvall JO, Yawn BP. The safety of long-acting
β2-agonists in the treatment of stable chronic obstructive pulmonary disease.
Int J Chron Obstruct Pulmon Dis. 2013;8:53–64.
223. Wang J, Jin D, Zuo P, Wang T, Xu Y, Xiong W. Comparison of tiotropium
plus formoterol to tiotropium alone in stable chronic obstructive pulmonary
disease: a meta-analysis. Respirology. 2011;16(2):350–8.
224. Han J, Dai L, Zhong N. Indacaterol on dyspnea in chronic obstructive
pulmonary disease: a systematic review and meta-analysis of randomized
placebo-controlled trials. BMC Pulm Med. 2013;13:26.
225. Chung VCH, Ma PHX, Hui DSC, Tam WWS, Tang JL. Indacaterol for
chronic obstructive pulmonary disease: systematic review and meta-analysis.
PLoS One. 2013;8(8):e70784.
226. Jiang F-M, Liang Z-A, Zheng Q-L, Wang R-C, Luo J, Li C-T. Safety and
efficacy of 12-week or longer indacaterol treatment in moderate-to-severe
COPD patients: a systematic review. Lung. 2013;191(2):135–46.
227. Cope S, Donohue JF, Jansen JP, Kraemer M, Capkun-Niggli G, Baldwin
M, et al. Comparative efficacy of long-acting bronchodilators for COPD--a
network meta-analysis. Respir Res. 2013;14:100.
228. Karner C, Chong J, Poole P. Tiotropium versus placebo for chronic
obstructive pulmonary disease. Cochrane Database of Systematic Review.
2012;7:CD009285.
229. Yohannes AM, Willgoss TG, Vestbo J. Tiotropium for treatment of stable
COPD: a meta-analysis of clinically relevant outcomes. Respir Care.
2011;56(4):477–87.
230. Wise RA, Anzueto A, Cotton D, Dahl R, Devins T, Disse B, et al. Tiotropium
Respimat inhaler and the risk of death in COPD. N Engl J Med.
2013;369(16):1491–501.
231. Karabis A, Lindner L, Mocarski M, Huisman E, Greening A. Comparative
efficacy of aclidinium versus glycopyrronium and tiotropium, as maintenance
treatment of moderate to severe COPD patients: a systematic review and
network meta-analysis. Int J Chron Obstruct Pulmon Dis. 2013;8:405–23.
232. Fuhr R, Magnussen H, Sarem K, Llovera AR, Kirsten A-M, Falqués M, et
al. Efficacy of aclidinium bromide 400 μg twice daily compared with placebo
and tiotropium in patients with moderate to severe COPD. Chest.
2012;141(3):745–52.
233. Cazzola M, Page CP, Rogliani P, Matera MG. β2-agonist therapy in lung
disease. Am J Respir Crit Care Med. 2013;187(7):690–6.
234. Wang J, Nie B, Xiong W, Xu Y. Effect of long-acting beta-agonists on the
frequency of COPD exacerbations: a meta-analysis. J Clin Pharm Ther.
2012;37(2):204–11.
235. Van Noord JA, Smeets JJ, Drenth BM, Rascher J, Pivovarova A, Hamilton
AL, et al. 24-hour bronchodilation following a single dose of the novel β(2)agonist olodaterol in COPD. Pulm Pharmacol Ther. 2011;24(6):666–72.
236. Hanania NA, Feldman G, Zachgo W, Shim J-J, Crim C, Sanford L, et al.
The efficacy and safety of the novel long-acting β2 agonist vilanterol in patients
with COPD: a randomized placebo-controlled trial. Chest. 2012;142(1):119–27.
237. Feldman G, Walker RR, Brooks J, Mehta R, Crater G. 28-Day safety and
tolerability of umeclidinium in combination with vilanterol in COPD: a
randomized placebo-controlled trial. Pulm Pharmacol Ther. 2012;25(6):465–
71.
238. Donohue JF, Maleki-Yazdi MR, Kilbride S, Mehta R, Kalberg C, Church a.
Efficacy and safety of once-daily umeclidinium/vilanterol 62.5/25 mcg in COPD.
Respir Med. 2013;107(10):1538–46.
239. Littner MR, Ilowite JS, Tashkin DP, Friedman M, Serby CW, Menjoge SS,
et al. Long-acting bronchodilation with once-daily dosing of tiotropium (Spiriva)
in stable chronic obstructive pulmonary disease. Am J Respir Crit Care Med.
2000;161(4 Pt 1):1136–42.
240. Jones PW, Singh D, Bateman ED, Agusti A, Lamarca R, de Miquel G, et
al. Efficacy and safety of twice-daily aclidinium bromide in COPD patients: the
ATTAIN study. Eur Respir J. 2012;40(4):830–6.
241. Woods JA, Nealy KL, Barrons RW. Aclidinium bromide: an alternative
long-acting inhaled anticholinergic in the management of chronic obstructive
pulmonary disease. Ann Pharmacother. 2013;47(7-8):1017–28.
242. D’Urzo A, Ferguson GT, van Noord J a, Hirata K, Martin C, Horton R, et
al. Efficacy and safety of once-daily NVA237 in patients with moderate-tosevere COPD: the GLOW1 trial. Respir Res. 2011. 12(1):156.
243. Tal-Singer R, Cahn A, Mehta R, Preece A, Crater G, Kelleher D, et al.
Initial assessment of single and repeat doses of inhaled umeclidinium in
patients with chronic obstructive pulmonary disease: two randomised studies.
Eur J Pharmacol. 2013;701(1-3):40–8.
244. Ram FSF, Jardin JR, Atallah A, Castro AA, Mazzini R, Goldstein R, et al.
Efficacy of theophylline in people with stable chronic obstructive pulmonary
disease: a systematic review and meta-analysis. Respir Med. 2005;99(2):135–
44.
245. Ram FS, Jones PW, Castro AA, De Brito JA, Atallah AN, Lacasse Y, et al.
Oral theophylline for chronic obstructive pulmonary disease. Cochrane
Database of Systematic Review. 2002;(4):CD003902.
246. Molfino NA, Zhang P. A meta-analysis on the efficacy of oral theophylline
in patients with stable COPD. Int J Chron Obstruct Pulmon Dis. 2006;1(3):261–
6.
247. Hirano T, Yamagata T, Gohda M, Yamagata Y, Ichikawa T, Yanagisawa
S, et al. Inhibition of reactive nitrogen species production in COPD airways:
comparison
of
inhaled
corticosteroid
and
oral
theophylline.
Thorax.
2006;61(9):761–6.
248. Culpitt S V, de Matos C, Russell RE, Donnelly LE, Rogers DF, Barnes PJ.
Effect of theophylline on induced sputum inflammatory indices and neutrophil
chemotaxis in chronic obstructive pulmonary disease. Am J Respir Crit Care
Med. 2002;165(10):1371–6.
249. Kobayashi M, Nasuhara Y, Betsuyaku T, Shibuya E, Tanino Y, Tanino M,
et al. Effect of low-dose theophylline on airway inflammation in COPD.
Respirology. 2004;9(2):249–54.
250. Barnes PJ. Theophylline for COPD. Thorax. 2006;61(9):742–4.
251. Gamble E, Grootendorst DC, Brightling CE, Troy S, Qiu Y, Zhu J, et al.
Antiinflammatory effects of the phosphodiesterase-4 inhibitor cilomilast (Ariflo)
in chronic obstructive pulmonary disease. Am J Respir Crit Care Med.
2003;168(8):976–82.
252. Chong J, Poole P, Leung B, Black PN. Phosphodiesterase 4 inhibitors for
chronic obstructive pulmonary disease. Cochrane Database of Systematic
Review. 2011;(5):CD002309.
253. Yang IA, Clarke MS, Sim EHA, Fong KM. Inhaled corticosteroids for stable
chronic obstructive pulmonary disease. Cochrane Database of Systematic
Review. 2012;7:CD002991.
254. De Coster DA, Jones M, Thakrar N. Beclometasone for chronic obstructive
pulmonary
disease.
Cochrane
Database
of
Systematic
Review.
2013;10:CD009769.
255. Nannini LJ, Poole P, Milan SJ, Holmes R, Normansell R. Combined
corticosteroid and long-acting beta₂-agonist in one inhaler versus placebo for
chronic obstructive pulmonary disease. Cochrane Database of Systematic
Review. 2013;11:CD003794.
256. Suissa S, Patenaude V, Lapi F, Ernst P. Inhaled corticosteroids in COPD
and the risk of serious pneumonia. Thorax. 2013;68(11):1029–36.
257. Nannini LJ, Lasserson TJ, Poole P. Combined corticosteroid and longacting beta(2)-agonist in one inhaler versus long-acting beta(2)-agonists for
chronic obstructive pulmonary disease. Cochrane Database of Systematic
Review. 2012;9:CD006829.
258. Spencer S, Karner C, Cates CJ, Evans DJ. Inhaled corticosteroids versus
long-acting beta(2)-agonists for chronic obstructive pulmonary disease.
Cochrane Database of Systematic Review. 2011;(12):CD007033.
259. Dong Y-H, Lin H-H, Shau W-Y, Wu Y-C, Chang C-H, Lai M-S.
Comparative safety of inhaled medications in patients with chronic obstructive
pulmonary disease: systematic review and mixed treatment comparison metaanalysis of randomised controlled trials. Thorax. 2013;68(1):48–56.
260. Karner C, Cates C. Long-acting beta 2 -agonist in addition to tiotropium
versus either tiotropium or long-acting beta 2 -agonist alone for chronic
obstructive pulmonary disease. Cochrane Database of Systematic Review.
2012;(4):006215
261. Rodrigo GJ, Plaza V, Castro-Rodríguez JA. Comparison of three
combined pharmacological approaches with tiotropium monotherapy in stable
moderate to severe COPD: a systematic review. Pulm Pharmacol Ther.
2012;25(1):40–7.
262. Mahler DA, D’Urzo A, Bateman ED, Ozkan SA, White T, Peckitt C, et al.
Concurrent use of indacaterol plus tiotropium in patients with COPD provides
superior bronchodilation compared with tiotropium alone: a randomised,
double-blind comparison. Thorax. 2012;67(9):781–8.
263. Wedzicha JA, Decramer M, Ficker JH, Niewoehner DE, Sandström T,
Taylor AF, et al. Analysis of chronic obstructive pulmonary disease
exacerbations with the dual bronchodilator QVA149 compared with
glycopyrronium and tiotropium (SPARK): a randomised, double-blind, parallelgroup study. lancet Respir Med. 2013;1(3):199–209.
264. Bateman ED, Ferguson GT, Barnes N, Gallagher N, Green Y, Henley M,
et al. Dual bronchodilation with QVA149 versus single bronchodilator therapy:
the SHINE study. Eur Respir J. 2013;42(6):1484–94.
265. Calverley PMA, Anderson JA, Celli B, Ferguson GT, Jenkins C, Jones PW,
et al. Salmeterol and fluticasone propionate and survival in chronic obstructive
pulmonary disease. N Engl J Med. 2007;356(8):775–89.
266. Welsh EJ, Cates CJ, Poole P. Combination inhaled steroid and long-acting
beta2-agonist versus tiotropium for chronic obstructive pulmonary disease.
Cochrane database Syst Rev. 2013 Jan;5:CD007891.
267. Wedzicha JA, Calverley PMA, Seemungal TA, Hagan G, Ansari Z,
Stockley RA. The prevention of chronic obstructive pulmonary disease
exacerbations by salmeterol/fluticasone propionate or tiotropium bromide. Am
J Respir Crit Care Med. 2008 Jan 1;177(1):19–26.
268. Bateman ED, van Dyk M, Sagriotis A. Comparable spirometric efficacy of
tiotropium compared with salmeterol plus fluticasone in patients with COPD: a
pilot study. Pulm Pharmacol Ther. 2008 Jan;21(1):20–5.
269. Karner C, Cj C. Combination inhaled steroid and long-acting beta 2 agonist in addition to tiotropium versus tiotropium or combination alone for
chronic obstructive pulmonary disease Cochrane Database Syst Rev. 2011;(3).
270. Karner C, Cj C. The effect of adding inhaled corticosteroids to tiotropium
and long-acting beta 2 -agonists for chronic obstructive pulmonary disease
Cochrane Database Syst Rev. 2011 ;(9).
271. Jung KS, Park HY, Park SY, Kim SK, Kim Y-K, Shim J-J, et al. Comparison
of tiotropium plus fluticasone propionate/salmeterol with tiotropium in COPD: a
randomized controlled study. Respir Med. 2012 Mar;106(3):382–9.
272. Poole P, Black PN, Cates CJ. Mucolytic agents for chronic bronchitis or
chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2012;(8)
.
273. Decramer M, Rutten-van Mölken M, Dekhuijzen PNR, Troosters T, van
Herwaarden C, Pellegrino R, et al. Effects of N-acetylcysteine on outcomes in
chronic obstructive pulmonary disease (Bronchitis Randomized on NAC CostUtility Study, BRONCUS): a randomised placebo-controlled trial. Lancet.
365(9470):1552–60.
274. COPD Working Group. Long-term oxygen therapy for patients with chronic
obstructive pulmonary disease (COPD): an evidence-based analysis. Ont
Health Technol Assess Ser. 2012;12(7):1–64.
275. Spruit MA, Singh SJ, Garvey C, ZuWallack R, Nici L, Rochester C, et al.
An official American Thoracic Society/European Respiratory Society statement:
key concepts and advances in pulmonary rehabilitation. Am J Respir Crit Care
Med. 2013;188(8):e13–64.
276. Bolton CE, Bevan-Smith EF, Blakey JD, Crowe P, Elkin SL, Garrod R, et
al. British Thoracic Society guideline on pulmonary rehabilitation in adults.
Thorax. 2013;68 Suppl 2:ii1–30.
277. Mendes de Oliveira JC, Studart Leitão Filho FS, Malosa Sampaio LM,
Negrinho de Oliveira AC, Hirata RP, Costa D, et al. Outpatient vs. home-based
pulmonary rehabilitation in COPD: a randomized controlled trial. Multidiscip
Respir Med. 2010;5(6):401–8.
278. Dias FD, Sampaio LMM, da Silva GA, Gomes ÉLFD, do Nascimento ESP,
Alves VLS, et al. Home-based pulmonary rehabilitation in patients with chronic
obstructive pulmonary disease: a randomized clinical trial. Int J Chron Obstruct
Pulmon Dis. 2013;8:537–44.
279. Tiong LU, Davies R, Gibson PG, Hensley MJ, Hepworth R, Lasserson TJ,
et al. Lung volume reduction surgery for diffuse emphysema. Cochrane
Database of Systematic Review. 2006;(4):CD001001.
280. Huang W, Wang WR, Deng B, Tan YQ, Jiang GY, Zhou HJ, et al. Several
clinical interests regarding lung volume reduction surgery for severe
emphysema: meta-analysis and systematic review of randomized controlled
trials. J Cardiothorac Surg. 2011;6:148.
281. Criner GJ, Cordova F, Sternberg AL, Martinez FJ. The National
Emphysema Treatment Trial (NETT) Part II: Lessons learned about lung
volume reduction surgery. Am J Respir Crit Care Med. 2011;184(8):881–93.
282. Sciurba FC, Ernst A, Herth FJF, Strange C, Criner GJ, Marquette CH, et
al. A randomized study of endobronchial valves for advanced emphysema. N
Engl J Med. 2010;363(13):1233–44.
283. Berger RL, Decamp MM, Criner GJ, Celli BR. Lung volume reduction
therapies for advanced emphysema: an update. Chest. 2010;138(2):407–17.
284. Román A, Ussetti P, Solé A, Zurbano F, Borro JM, Vaquero JM, et al.
Normativa para la selección de pacientes candidatos a transplante pulmonar..
Arch Bronconeumol. 2011;47(6):303–9.
285. Christie JD, Edwards LB, Kucheryavaya AY, Benden C, Dobbels F, Kirk
R, et al. The Registry of the International Society for Heart and Lung
Transplantation: Twenty-eighth Adult Lung and Heart-Lung Transplant Report-2011. J Heart Lung Transplant. 2011;30(10):1104–22.
286. Struik FM, Lacasse Y, Goldstein R, Kerstjens HM, Wijkstra PJ. Nocturnal
non-invasive positive pressure ventilation for stable chronic obstructive
pulmonary
disease.
Cochrane
Database
of
Systematic
Review.
2013;6:CD002878.
287. Shi J, Xu J, Sun W, Su X, Zhang Y, Shi Y. Effect of noninvasive, positive
pressure ventilation on patients with severe, stable chronic obstructive
pulmonary disease: a meta-analysis. Chin Med J (Engl). 2013;126(1):140–6.
288. Janssen DJA, Curtis JR, Au DH, Spruit MA, Downey L, Schols JMGA, et
al. Patient-clinician communication about end-of-life care for Dutch and US
patients with COPD. Eur Respir J. 2011;38(2):268–76.
289. Momen N, Hadfield P, Kuhn I, Smith E, Barclay S. Discussing an uncertain
future: end-of-life care conversations in chronic obstructive pulmonary disease.
A systematic literature review and narrative synthesis. Thorax. 2012;67(9):777–
80.
290. Fahim A, Kastelik JA. Palliative care understanding and end-of-life
decisions in chronic obstructive pulmonary disease. Clin Respir J. 2013 Nov 5;
291. Lanken PN, Terry PB, Delisser HM, Fahy BF, Hansen-Flaschen J, Heffner
JE, et al. An official American Thoracic Society clinical policy statement:
palliative care for patients with respiratory diseases and critical illnesses. Am J
Respir Crit Care Med. 2008;177(8):912–27.
292.
Escarrabill
J,
Soler
Cataluña
JJ,
Hernández
C,
Servera
E.
Recomendaciones para los cuidados al final de la vida de pacientes con EPOC.
Arch Bronconeumol. 2009;45(6):297–303.
293. Burge S, Wedzicha JA. COPD exacerbations: definitions and
classifications. Eur Respir J Suppl. 2003;41:46–53.
294. Celli BR, Barnes PJ. Exacerbations of chronic obstructive pulmonary
disease. Eur Respir J. 2007;29(6):1224–38.
295. Rodriguez-Roisin R. Toward a consensus definition for COPD
exacerbations. Chest. 2000;117:398S–401S.
296. Donaldson G, Seemungal T, Bhowmik a, Wedzicha J. Relationship
between exacerbation frequency and lung function decline in chronic
obstructive pulmonary disease. Thorax. 2002;57:847–52.
297. Halpin DMG, Decramer M, Celli B, Kesten S, Liu D, Tashkin DP.
Exacerbation frequency and course of COPD. Int J Chron Obstruct Pulmon Dis.
2012;7:653–61.
298. Miravitlles M, Ferrer M, Pont A, Zalacain R, Alvarez-Sala JL, Masa F, et
al. Effect of exacerbations on quality of life in patients with chronic obstructive
pulmonary disease: a 2 year follow up study. Thorax. 2004;59(5):387–95.
299. Seemungal TA, Donaldson GC, Paul EA, Bestall JC, Jeffries DJ,
Wedzicha JA. Effect of exacerbation on quality of life in patients with chronic
obstructive pulmonary disease. Am J Respir Crit Care Med. 1998;157(5 Pt
1):1418–22.
300. Spencer S, Calverley PMA, Burge PS, Jones PW. Impact of preventing
exacerbations on deterioration of health status in COPD. Eur Respir J.
2004;23(5):698–702.
301. Andersson F, Borg S, Jansson SA, Jonsson AC, Ericsson A, Prütz C, et
al. The costs of exacerbations in chronic obstructive pulmonary disease
(COPD). Respir Med. 2002;96(9):700–8.
302. Miravitlles M, Murio C, Guerrero T, Gisbert R. Pharmacoeconomic
evaluation of acute exacerbations of chronic bronchitis and COPD. Chest.
2002;121(5):1449–55.
303. Oostenbrink JB, Rutten-van Mölken MPMH. Resource use and risk factors
in high-cost exacerbations of COPD. Respir Med. 2004;98(9):883–91.
304. O’Reilly JF, Williams AE, Rice L. Health status impairment and costs
associated with COPD exacerbation managed in hospital. Int J Clin Pract.
2007;61(7):1112–20.
305. Ai-Ping C, Lee K-H, Lim T-K. In-hospital and 5-year mortality of patients
treated in the ICU for acute exacerbation of COPD: a retrospective study.
Chest. 2005;128(2):518–24.
306. Seneff MG, Wagner DP, Wagner RP, Zimmerman JE, Knaus WA. Hospital
and 1-year survival of patients admitted to intensive care units with acute
exacerbation
of
chronic
obstructive
pulmonary
disease.
JAMA.
1995;274(23):1852–7.
307. Hoogendoorn M, Hoogenveen RT, Rutten-van Mölken MP, Vestbo J,
Feenstra TL. Case fatality of COPD exacerbations: a meta-analysis and
statistical modelling approach. Eur Respir J. 2011;37(3):508–15.
308. Groenewegen KH, Schols AMWJ, Wouters EFM. Mortality and mortalityrelated factors after hospitalization for acute exacerbation of COPD. Chest.
2003;124(2):459–67.
309. Gunen H, Hacievliyagil SS, Kosar F, Mutlu LC, Gulbas G, Pehlivan E, et
al. Factors affecting survival of hospitalised patients with COPD. Eur Respir J.
2005;26(2):234–41.
310. McGhan R, Radcliff T, Fish R, Sutherland ER, Welsh C, Make B.
Predictors of rehospitalization and death after a severe exacerbation of COPD.
Chest. 2007;132(6):1748–55.
311. Connors AF, Dawson N V, Thomas C, Harrell FE, Desbiens N, Fulkerson
WJ, et al. Outcomes following acute exacerbation of severe chronic obstructive
lung disease. The SUPPORT investigators (Study to Understand Prognoses
and Preferences for Outcomes and Risks of Treatments). Am J Respir Crit Care
Med. 1996;154(4 Pt 1):959–67.
312. Aaron SD, Donaldson GC, Whitmore GA, Hurst JR, Ramsay T, Wedzicha
JA. Time course and pattern of COPD exacerbation onset. Thorax.
2012;67(3):238–43.
313. Soler-Cataluña JJ, Rodriguez-Roisin R. Frequent chronic obstructive
pulmonary disease exacerbators: how much real, how much fictitious? COPD.
2010;7(4):276–84.
314. Au DH, Bryson CL, Chien JW, Sun H, Udris EM, Evans LE, et al. The
effects of smoking cessation on the risk of chronic obstructive pulmonary
disease exacerbations. J Gen Intern Med. 2009;24(4):457–63.
315. Miravitlles M. Epidemiology of Chronic Obstructive Pulmonary Disease
Exacerbations. Clin Pulm Med. 2002;9(4):191–7.
316. Vestbo J, Anderson JA, Calverley PMA, Celli B, Ferguson GT, Jenkins C,
et al. Adherence to inhaled therapy, mortality and hospital admission in COPD.
Thorax. 2009;64(11):939–43.
317. Casas A, Troosters T, Garcia-Aymerich J, Roca J, Hernández C, Alonso
A, et al. Integrated care prevents hospitalisations for exacerbations in COPD
patients. Eur Respir J. 2006;28(1):123–30.
318. Bourbeau J, Nault D. Self-management strategies in chronic obstructive
pulmonary disease. Clin Chest Med. 2007;28(3):617–28, vii.
319. Sehatzadeh S. Influenza and pneumococcal vaccinations for patients with
chronic obstructive pulmonary disease (COPD): an evidence-based review.
Ont Health Technol Assess Ser. 2012;12(3):1–64.
320. Poole PJ, Chacko E, Wood-Baker RWB, Cates CJ. Influenza vaccine for
patients with chronic obstructive pulmonary disease. Cochrane Database of
Systematic Review. 2006;(1):CD002733.
321. Walters JA, Smith S, Poole P, Granger RH, Wood-Baker R. Injectable
vaccines for preventing pneumococcal infection in patients with chronic
obstructive pulmonary disease. Cochrane Database of Systematic Review.
2010;(11):CD001390.
322. Alfageme I, Vazquez R, Reyes N, Muñoz J, Fernández A, Hernandez M,
et al. Clinical efficacy of anti-pneumococcal vaccination in patients with COPD.
Thorax. 2006;61(3):189–95.
323. Cazzola M, Anapurapu S, Page CP. Polyvalent mechanical bacterial
lysate for the prevention of recurrent respiratory infections: a meta-analysis.
Pulm Pharmacol Ther. 2012;25(1):62–8.
324. Steurer-Stey C, Bachmann LM, Steurer J, Tramèr MR. Oral purified
bacterial extracts in chronic bronchitis and COPD: systematic review. Chest.
2004;126(5):1645–55.
325. Oba Y, Lone NA. Efficacy and safety of roflumilast in patients with chronic
obstructive pulmonary disease: a systematic review and meta-analysis. Ther
Adv Respir Dis. 2013;7(1):13–24.
326. Wedzicha JA, Rabe KF, Martinez FJ, Bredenbröker D, Brose M, Goehring
U-M, et al. Efficacy of roflumilast in the COPD frequent exacerbator phenotype.
Chest. 2013;143(5):1302–11.
327. Tse HN, Raiteri L, Wong KY, Yee KS, Ng LY, Wai KY, et al. High-dose Nacetylcysteine in stable COPD: the 1-year, double-blind, randomized, placebocontrolled HIACE study. Chest. 2013;144(1):106–18.
328. Zheng J-P, Wen F-Q, Bai C-X, Wan H-Y, Kang J, Chen P, et al. High-dose
N-acetylcysteine in the prevention of COPD exacerbations: rationale and
design of the PANTHEON Study. COPD. 2013;10(2):164–71.
329. Fishman A, Martinez F, Naunheim K, Piantadosi S, Wise R, Ries A, et al.
A randomized trial comparing lung-volume-reduction surgery with medical
therapy for severe emphysema. N Engl J Med. 2003;348(21):2059–73.
330. Washko GR, Fan VS, Ramsey SD, Mohsenifar Z, Martinez F, Make BJ, et
al. The effect of lung volume reduction surgery on chronic obstructive
pulmonary
disease
exacerbations.
Am
J
Respir
Crit
Care
Med.
2008;177(2):164–9.
331. Staykova T, Pn B, Ee C, Poole P. Prophylactic antibiotic therapy for
chronic
bronchitis.
Cochrane
Database
of
Systematic
Review.
2011;(11):CD004105.
332. Yao G-Y, Ma Y-L, Zhang M-Q, Gao Z-C. Macrolide therapy decreases
chronic obstructive pulmonary disease exacerbation: a meta-analysis.
Respiration. 2013;86(3):254–60.
333. Donath E, Chaudhry A, Hernandez-Aya LF, Lit L. A meta-analysis on the
prophylactic use of macrolide antibiotics for the prevention of disease
exacerbations in patients with Chronic Obstructive Pulmonary Disease. Respir
Med. 2013;107(9):1385–92.
334. Seemungal TAR, Wilkinson TMA, Hurst JR, Perera WR, Sapsford RJ,
Wedzicha JA. Long-term erythromycin therapy is associated with decreased
chronic obstructive pulmonary disease exacerbations. Am J Respir Crit Care
Med. 2008;178(11):1139–47.
335. Albert RK, Connett J, Bailey WC, Casaburi R, Cooper JAD, Criner GJ, et
al. Azithromycin for prevention of exacerbations of COPD. N Engl J Med.
2011;365(8):689–98.
336. Sethi S, Jones PW, Theron MS, Miravitlles M, Rubinstein E, Wedzicha J
a, et al. Pulsed moxifloxacin for the prevention of exacerbations of chronic
obstructive pulmonary disease: a randomized controlled trial. Respir Res.
2010;11:10.
337. Papi A, Bellettato CM, Braccioni F, Romagnoli M, Casolari P, Caramori G,
et al. Infections and airway inflammation in chronic obstructive pulmonary
disease
severe
exacerbations.
Am
J
Respir
Crit
Care
Med.
2006;173(10):1114–21.
338. Sethi S, Murphy TF. Infection in the pathogenesis and course of chronic
obstructive pulmonary disease. N Engl J Med. 2008;359(22):2355–65.
339. Anderson HR, Spix C, Medina S, Schouten JP, Castellsague J, Rossi G,
et al. Air pollution and daily admissions for chronic obstructive pulmonary
disease in 6 European cities: results from the APHEA project. Eur Respir J.
1997;10(5):1064–71.
340. Donaldson GC, Seemungal T, Jeffries DJ, Wedzicha JA. Effect of
temperature on lung function and symptoms in chronic obstructive pulmonary
disease. Eur Respir J. 1999,13(4):844–9.
341. Jones P, Higenbottam T. Quantifying of severity of exacerbations in
chronic obstructive pulmonary disease: adaptations to the definition to allow
quantification. Proc Am Thorac Soc. 2007;4(8):597–601.
342. Effing TW, Kerstjens HAM, Monninkhof EM, van der Valk PDLPM,
Wouters EF, Postma DS, et al. Definitions of exacerbations: does it really
matter in clinical trials on COPD? Chest. 2009;136(3):918–23.
343. Leidy NK, Wilcox TK, Jones PW, Roberts L, Powers JH, Sethi S.
Standardizing measurement of chronic obstructive pulmonary disease
exacerbations. Reliability and validity of a patient-reported diary. Am J Respir
Crit Care Med. 2011 Mar 1;183(3):323–9.
344. Vollenweider DJ, Jarrett H,Steurer-Stey CA,Puhan MA. Antibiotics for
exacerbations of chronic obstructive pulmonary disease.Cochrane Database of
Systematic Review. 2012;(12).
345. Miravitlles M, Moragas A, Hernández S, Bayona C, Llor C. Is it possible to
identify exacerbations of mild to moderate COPD that do not require antibiotic
treatment? Chest. 2013;144(5):1571–7.
346. Singh JM, Palda V a, Stanbrook MB, Chapman KR. Corticosteroid therapy
for patients with acute exacerbations of chronic obstructive pulmonary disease:
a systematic review. Arch Intern Med. 2013;162(22):2527–36.
347. Walters J, Wang W, Morley C, Soltani A. Different durations of
corticosteroid therapy for exacerbations of chronic obstructive pulmonary
disease.Cochrane Database of Systematic Review . 2012;(3).
348. De Jong YP, Uil SM, Grotjohan HP, Postma DS, Kerstjens H a M, van den
Berg JWK. Oral or IV prednisolone in the treatment of COPD exacerbations: a
randomized, controlled, double-blind study. Chest. 2007;132(6):1741–7.
349. Leuppi JD, Schuetz P, Bingisser R, Bodmer M, Briel M, Drescher T, et al.
Short-term vs conventional glucocorticoid therapy in acute exacerbations of
chronic obstructive pulmonary disease: the REDUCE randomized clinical trial.
JAMA. 2013;309(21):2223–31.
350. Walters J, Gibson PG, Hannay M, Walters E. Systemic corticosteroids for
acute exacerbations of chronic obstructive pulmonary disease. Cochrane
Database of Systematic Review. 2009;(1).
351. Niewoehner DE, Erbland ML, Deupree RH, Collins D, Gross NJ, Light RW,
et al. Effect of systemic glucocorticoids on exacerbations of chronic obstructive
pulmonary disease. Department of Veterans Affairs Cooperative Study Group.
N Engl J Med. 1999;340(25):1941–7.
352. Wilkinson TMA, Donaldson GC, Hurst JR, Seemungal TAR, Wedzicha JA.
Early therapy improves outcomes of exacerbations of chronic obstructive
pulmonary disease. Am J Respir Crit Care Med. 2004;169(12):1298–303.
353. Woodhead M, Blasi F, Ewig S, Huchon G, Ieven M, Leven M, et al.
Guidelines for the management of adult lower respiratory tract infections. Eur
Respir J. 2005;26(6):1138–80.
354. Parker CM, Voduc N, Aaron SD, Webb KA, O’Donnell DE. Physiological
changes during symptom recovery from moderate exacerbations of COPD. Eur
Respir J. 2005;26(3):420–8.
355. Anzueto A, Miravitlles M, Ewig S, Legnani D, Heldner S, Stauch K.
Identifying patients at risk of late recovery (≥ 8 days) from acute exacerbation
of chronic bronchitis and COPD. Respir Med. 2012;106(9):1258–67.
356. Pérez-Trallero E, García-de-la-Fuente C, García-Rey C, Baquero F,
Aguilar L, Dal-Ré R, et al. Geographical and ecological analysis of resistance,
coresistance, and coupled resistance to antimicrobials in respiratory
pathogenic bacteria in Spain. Antimicrob Agents Chemother. 2005;49(5):1965–
72.
357. Miravitlles M, Monsó E, Mensa J, Aguarón Pérez J, Barberán J, Bárcena
Caamaño M, et al. Tratamiento antimicrobiano de la agudización de la
EPOC:Documento de Consenso 2007. Arch Bronconeumol. 2008;44(2):100–
8.
358. Gunen H, Hacievliyagil SS, Yetkin O, Gulbas G, Mutlu LC, In E. The role
of nebulised budesonide in the treatment of exacerbations of COPD. Eur Respir
J. 2007;29(4):660–7.
359. Maltais F, Ostinelli J, Bourbeau J, Tonnel AB, Jacquemet N, Haddon J, et
al. Comparison of nebulized budesonide and oral prednisolone with placebo in
the treatment of acute exacerbations of chronic obstructive pulmonary disease:
a randomized controlled trial. Am J Respir Crit Care Med. 2002;165(5):698–
703.
360. Gaude GS, Nadagouda S. Nebulized corticosteroids in the management
of acute exacerbation of COPD. Lung India. 2010;27(4):230–5.
361. Barr RG, Rowe BH, Camargo CA. Methylxanthines for exacerbations of
chronic obstructive pulmonary disease. Cochrane Database of Systematic
Review. 2003;(2):CD002168.
362. Austin M, Wood-Baker R. Oxygen therapy in the pre-hospital setting for
acute exacerbations of chronic obstructive pulmonary disease. Cochrane
Database of Systematic Review. 2006 Jan;(3):CD005534.
363. Austin MA, Wills KE, Blizzard L, Walters EH, Wood-Baker R. Effect of high
flow oxygen on mortality in chronic obstructive pulmonary disease patients in
prehospital setting: randomised controlled trial. BMJ. 2010;341:c5462.
364. Ram FSF, Picot J, Lightowler J, Wedzicha JA. Non-invasive positive
pressure ventilation for treatment of respiratory failure due to exacerbations of
chronic obstructive pulmonary disease. Cochrane Database of Systematic
Review. 2004;(3):CD004104.
365. Keenan SP, Mehta S. Noninvasive ventilation for patients presenting with
acute respiratory failure: the randomized controlled trials. Respir Care.
2009;54(1):116–26.
366. Keenan SP, Sinuff T, Cook DJ, Hill NS. Which patients with acute
exacerbation of chronic obstructive pulmonary disease benefit from
noninvasive positive-pressure ventilation? A systematic review of the literature.
Ann Intern Med. 2003;138(11):861–70.
367. Skwarska E, Cohen G, Skwarski KM, Lamb C, Bushell D, Parker S, et al.
Randomized controlled trial of supported discharge in patients with
exacerbations
of
chronic
obstructive
pulmonary
disease.
Thorax.
2000;55(11):907–12.
368. Postma DS. When can an exacerbation of COPD be treated at home?
Lancet. 1998;351(9119):1827–8.
369. Sala E, Alegre L, Carrera M, Ibars M, Orriols FJ, Blanco ML, et al.
Supported discharge shortens hospital stay in patients hospitalized because of
an exacerbation of COPD. Eur Respir J. 2001;17(6):1138–42.
370. Hernandez C, Casas A, Escarrabill J, Alonso J, Puig-Junoy J, Farrero E,
et al. Home hospitalisation of exacerbated chronic obstructive pulmonary
disease patients. Eur Respir J. 2003;21(1):58–67.
371. Sin DD, Bell NR, Svenson LW, Man SFP. The impact of follow-up
physician visits on emergency readmissions for patients with asthma and
chronic obstructive pulmonary disease: a population-based study. Am J Med.
2002;112(2):120–5.
372. Puhan M a, Spaar A, Frey M, Turk A, Brändli O, Ritscher D, et al. Early
versus late pulmonary rehabilitation in chronic obstructive pulmonary disease
patients
with
acute
exacerbations:
a
randomized
trial.
Respiration.
2012;83(6):499–506.
373. Troosters T, Probst VS, Crul T, Pitta F, Gayan-Ramirez G, Decramer M,
et al. Resistance training prevents deterioration in quadriceps muscle function
during acute exacerbations of chronic obstructive pulmonary disease. Am J
Respir Crit Care Med. 2010;181(10):1072–7.
374. Eaton T, Young P, Fergusson W, Moodie L, Zeng I, O’Kane F, et al. Does
early pulmonary rehabilitation reduce acute health-care utilization in COPD
patients admitted with an exacerbation? A randomized controlled study.
Respirology. 2009;14(2):230–8.
375. Puhan MA, Gimeno-Santos E, Scharplatz M, Troosters T, Walters EH,
Steurer J. Pulmonary rehabilitation following exacerbations of chronic
obstructive pulmonary disease. Cochrane Database of Systematic Review.
2011;(10):CD005305.
376. Tang CY, Blackstock FC, Clarence M, Taylor NF. Early rehabilitation
exercise program for inpatients during an acute exacerbation of chronic
obstructive pulmonary disease: a randomized controlled trial. J Cardiopulm
Rehabil Prev. 2012;32(3):163–9.
377. Burtin C, Decramer M, Gosselink R, Janssens W, Troosters T.
Rehabilitation and acute exacerbations. Eur Respir J. 2011;38(3):702–12.
378. Saey D, Ribeiro F. Resistance training preserves skeletal muscle function
in patients with COPD who are hospitalised with an acute exacerbation. J
Physiother. 2011;57(3):194.
379. Reid WD, Yamabayashi C, Goodridge D, Chung F, Hunt M a, Marciniuk
DD, et al. Exercise prescription for hospitalized people with chronic obstructive
pulmonary disease and comorbidities: a synthesis of systematic reviews. Int J
Chron Obstruct Pulmon Dis. 2012;7:297–320.