1
Estudo Químico-Quântico de Espécies Precursoras de Filmes
Nanoestruturados
B. Caleffi1, V. C. Fernandes2, K. Capelle3 e P. Homem-de-Mello1
1
CCNH, Universidade Federal do ABC;
IQSC, Universidade de São Paulo, S. Carlos, SP, Brasil;
3
IFSC, Universidade de São Paulo, S. Carlos, SP, Brasil
2
Filmes nanoestruturados podem ser formados, por exemplo, com o uso de azocorantes (com aplicações em armazenamento óptico,
chaves ópticas, hologramas, grades de relevo superficiais e alinhamento de cristais líquidos). Neste trabalho, são estudadas moléculas
utilizadas na composição de alguns materiais nanoestruturados: azocorantes (Sudan 3, Sudan 4, Sudan Red, Orange G e Sunset
Yellow), utilizando a Teoria do Funcional da Densidade e o método de solvatação Integral Equation Formulation of Polarizable
Continuum Model.
Palavras chave — Diazocorantes, Filmes Nanoestruturados, DFT, IEFPCM.
I. INTRODUÇÃO
A
tualmente, a nanotecnologia e as nanociências vêm
dando um grande impulso à inovação e à evolução do
conhecimento, sendo hoje uma das áreas mais atraentes e
promissoras da ciência. Este fato pode ser verificado ao
observar o aumento expressivo nos números de trabalhos na
área, publicados em importantes revistas científicas da
atualidade. [1] Neste contexto, uma importante área de estudo
é a de materiais nanoestruturados. Esses materiais apresentam
características estruturais bem definidas, e suas propriedades
físicas e químicas são de crescente importância para futuras
aplicações tecnológicas. [2] Essas propriedades (magnética,
óptica, ponto de fusão, calor específico, reatividade de
superfície, dentre outras) podem ser afetadas pelo tamanho de
partícula e ser de interesse para diversas aplicações como
células solares, lasers, análises biológicas, catalisadores,
spintrônica e computação quântica. A seguir, são apresentados
compostos
utilizados
na
produção
de
materiais
nanoestruturados, com diferentes aplicações tecnológicas, que
têm sido objeto de estudo deste trabalho.
Atualmente, existem diversos grupos cromóforos utilizados
na síntese de corantes. Dentre eles, cerca de 60% pertencem à
família dos azocorantes, que se caracterizam por apresentarem
um ou mais agrupamentos –N=N– ligados a sistemas
aromáticos [3], vide Figuras 1 e 2.
Fig. 2. Estrutura geral para os azocorantes: Orange G: R1=H, R2=SO3;
Sunset Yellow: R1=SO3, R2=H.
Outra área de interesse para a aplicação desses filmes é no
alinhamento de cristais líquidos, resultando em processos
considerados “limpos“, sem contato mecânico na preparação
de substrato, ao contrário do processo de esfregamento de uma
superfície polimérica, que pode introduzir impurezas e
depositar cargas na superfície, prejudicando o bom
desempenho dos dispositivos. [4] Além disso, esses filmes
podem ser usados na produção de microtexturas que
possibilitam o controle local do alinhamento do cristal líquido
possibilitando sua aplicação para gravação a de informações,
tais como as memórias ópticas. [5]
Pelo fato destes materiais serem hoje estudados para
estas e diversas outras aplicações, neste trabalho foi realizado
o estudo químico–quântico de alguns diazocorantes em
diferentes conformações geométricas.
II. OBJETIVOS
Fig. 1 Estrutura geral para os diazocorantes estudados: Sudan III:
R1=R2=H; Sudan IV: R1=CH3, R2=H; Sudan Red: R1=H, R2=CH3.
Estudar, por meio de métodos de química-quântica,
moléculas precursoras de filmes nanoestruturados. Foram
estudados dois tipos de compostos: azo e diazocorantes,
utilizando-se o método DFT. Foi dada especial atenção à
inclusão do solvente, utilizando-se o IEFPCM (Integral
Equation Formulation of Polarizable Continuum Model).
2
III. METODOLOGIA
Foram estudados os diazocorantes Sudan 3, Sudan 4,
Sudan Red (Figura 1) e os azocorantes Orange G e Sunset
Yellow (Figura 2). Para tanto, foi utilizada a Teoria do
Funcional de Densidade (DFT), um método de Mecânica
Quântica, que tem sido utilizado intensamente no auxílio da
interpretação de resultados experimentais, bem como no
estudo de caminhos de reações, de barreiras de reação, da
influência de ligantes em compostos de coordenação, em
espectroscopia, etc. De acordo com Kohn et al. [6], a DFT é
uma linguagem conveniente e universal para a teoria de
estrutura eletrônica, que ajuda a unificar a química orgânica, a
inorgânica, química de superfície e a ciência dos materiais.
Com o avanço computacional, a DFT vem ocupando um
espaço ainda maior, tornando-se também uma ferramenta de
grande utilidade no estudo de sistemas bioquímicos, como as
interações fármaco-receptor e mecanismos de atividade
biológica. [7]
Foram feitas otimizações de geometria e cálculos de
propriedades eletrônicas, utilizando os funcionais B3LYP e
LSDA, base DGDZVP, no vácuo e em solução aquosa
(simulada com IEFPCM [8]), conforme implementados no
programa Gaussian 03 [9], sendo os inputs construídos com o
programa GaussView03 [10]. Para garantir que todas as
estruturas se tratassem de mínimos na superfície de energia,
foram realizados, também, cálculos de freqüência. [12]
Os azo e diazocorantes foram estudados em diferentes
conformações envolvendo o estereoisomerismo E-Z destes
compostos. Para o estudo do equilíbrio tautomérico, presente
nessas espécies, foram realizadas otimizações geométricas
partindo de dois ângulos H-O-C diferentes com a finalidade de
comparar o efeito deste tipo de interação nas propriedades dos
compostos estudados. Primeiro foram estudadas moléculas
com ângulos H-O-C de 109,5° que após a otimização
assumem valores em média de 106°. Essas moléculas
otimizadas servem como ponto de partida para novas
geometrias após a alteração no diedro H-O-C-C, o ângulo HO-C passa a ser aproximadamente 254°, após a otimização de
geometria temos ângulos de aproximadamente 265°. Os dois
ângulos obtidos estão representados na figura 4.
Figura 4: Ângulos H-O-C obtidos.
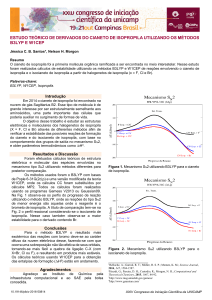
Os espectros teóricos de absorção foram obtidos pelo
método ZINDO a partir das estruturas com geometrias
otimizadas em fase gasosa.
IV. RESULTADOS E DISCUSSÃO
Os valores de energa total e espectro de absorção teórico,
obtidos para os azo e diazocorantes com ângulos H-O-C de
265° no vácuo são apresentados nas Tabelas 1, 2, 3 e 4. De
maneira geral, o estereoisômero E possui uma geometria mais
plana e menores valores de energia total, o que indica que é
uma estrutura de maior estabilidade.
Para os dois azocorantes: Orange G e Sunset Yellow, não
foi encontrado com o funcional B3LYP, nenhum ponto de
mínimo com ângulo H-O-C=106°, em ambos os casos durante
a otimização de geometria, houve rotação no diedro H-O-C-C
que resultou em uma molécula de ângulo H-O-C=265°.
As conformações EZ e ZE dos diazocorantes possuem
valores próximos de energia, com a forma ZE ligeiramente
mais estável em ângulos H-O-C=106°. Para ângulos H-OC=265°, a interação de hidrogênio favorece uma maior
diminuição na energia total nas conformações EZ, tornando-as
mais estáveis em comparação às conformações ZE.
Ângulos H-O-C=265° favorecem uma diminuição na
energia total devido a interação de hidrogênio e pode resultar
em tautomerismo. O equilíbrio tautomérico é estabelecido
pelo processo reversível da transferência do hidrogênio HO
para o nitrogênio β do grupo azila, formando uma ligação
(figura 5), e pode ser notado por valores na distância H-O
maiores que H-N.
Fig. 3. Equilíbrio tautomérico indicado pela transferência do próton ligado ao
oxigênia para o nitrogênio β do grupo azila.
A transferência do H foi prevista apenas pelo funcional
LSDA. E ocorreu somente nas conformações EE e EZ.
Conformações ZE e ZZ possuem geometrias mais distorcidas
que apresentam maiores distâncias H-N que dificultam esse
tipo de interação.
Os espectros de absorção obtidos por métodos teóricos
foram comparados com os experimentais que apresentam duas
bandas: para o Sunset Yellow 315 e 480, para o Orange G 330
e 480 e para os Sudans em torno de 350 e 530 [11].
De maneira geral, os valores do espectro de absorção
obtidos com geometrias de ângulos C-O-H de 264° estão mais
próximo dos dados experimentais. Para os diazocorantes, o
funcional LSDA apresentou melhores resultados para as
conformações EE e EZ onde foram previstos o equilíbrio
tautomérico, e o funcional B3LYP para a formação ZZ. Nos
azocorantes os valores mais próximos dos experimentais
foram obtidos com o funcional B3LYP para a conformação E,
e LSDA para a conformação Z. Os estudos envolvendo os
efeitos da solvatação realizados para o Sunset Yellow, Orange
G são apresentados na tabela 5. Os resultados indicam que as
moléculas são estabilizadas pela interação com a água.
3
Tab.1. Energia total e espectro de absorção teórico para o Sudan III, ângulo H-O-C de 265°, no vácuo.
Sudan III
EE
EZ
ZE
ZZ
B3LYP
LSDA
B3LYP
LSDA
B3LYP
LSDA
B3LYP
LSDA
Et (ua)
-1.142,247
-1.135,960
-1.142,222
-1.135,938
-1.142,209
-1.135,916
-1.142,183
-1.135,894
λ (nm)
502,25
541,55
472,43
557,37
406,34
441,5
350,52
425,14
Tab.2. Energia total e espectro de absorção teórico para o Sudan IV, ângulo H-O-C de 265°, no vácuo.
Sudan IV
EE
EZ
ZE
ZZ
B3LYP
LSDA
B3LYP
LSDA
B3LYP
LSDA
B3LYP
LSDA
Et (ua)
-1.220,886
-1.214,174
-1.220,861
-1.214,130
-1.220,851
-1.214,130
-1.220,822
-1.214,112
λ (nm)
507,33
547,79
473,79
553,97
412,56
445,72
347,78
424,38
Tab.3. Energia total e espectro de absorção teórico para o Sudan Red, ângulo H-O-C de 265°, no vácuo.
Sudan Red
EE
EZ
ZE
ZZ
B3LYP
LSDA
B3LYP
LSDA
B3LYP
LSDA
B3LYP
LSDA
Et (ua)
-1.220,882
-1.214,164
-1.220,857
-1.214,136
-1.220,843
-1.214,121
-1.220,821
-1.213,850
λ (nm)
504,49
543,63
472,98
577,09
408,24
441,46
357,34
425,33
Tab . 4. Energia total e espectro de absorção teórico para os azocorantes Sunset Yellow e Orange G, ângulo H-O-C de 265°, no vácuo.
Sunset Yellow
Orange G
E
Z
E
Z
B3LYP
LSDA
B3LYP
LSDA
B3LYP
LSDA
B3LYP
LSDA
Et (ua)
-2048,272
-2039,729
-2048,233
-2039,684
-2048,225
-2039,695
-2048,184
-2039,646
λ (nm)
474.95
541.09
285.67
291.29
461.82
500.92
382.65
321.57
Tab . 5. Energia de solvatação para os azocorantes Sunset Yellow e Orange G.
Sunset Yellow
E
Et (ua)
Orange G
Z
E
Z
B3LYP
LSDA
B3LYP
LSDA
B3LYP
LSDA
B3LYP
LSDA
-0,228
-0,232
-0,240
-0,245
-0,271
-0,245
-0,283
-0,276
V. CONCLUSÕES
O estereoisômero E apresenta maior estabilidade, pois
possui uma geometria mais plana, com uma tensão menor
entre os ângulos de ligação que resulta em menores valores de
energia total em comparação com o isômero Z. A interação
entre o hidrogênio (HO) e o nitrogênio β do grupo azila
contribui para uma estabilização ainda maior dessas moléculas
com possibilidade de equilíbrio tautomérico, previsto apenas
pelo funcional LSDA e para porções do tipo E, em que há uma
menor distância entre o grupo hidroxila e o nitrogênio β. O
funcional B3LYP, de maneira geral, pode apresentar melhores
geometrias, porém, não prevê o tautomerismo melhor descrito
pelo funcional LSDA que apresentou melhores geometrias
para os isômeros EE e EZ dos diazocorantes.
Nos azocorantes o substituinte SO3 pode deslocalizar a
nuvem eletrônica para suas proximidades por efeito indutivo e
“dificultar” a estabilização da carga positiva e negativa
formada no oxigênio e no nitrogênio após a transferência de
próton. Neste caso onde não ocorreria tautomerismo o
funcional B3LYP apresentou melhores resultados (com
exceção para o Orange G na conformação Z).
REFERÊNCIAS BIBLIOGRÁFICAS
[1] H. E. Toma, Quim. Nova (Suplemento) 2005, 28, S48-S51.
[2] A. P. Maciel, E. Longo e R. Leite, Quim. Nova 2003, 6, 855.
[3] A. Kunz, P. Peralta-Zamora, S. G. de Moraes, N. Durán, Quim. Nova,
2002, 25,.1.
[4] I. H. Bechtold, Efeitos de Superfície e de Confinamento na Ordem
Orientacional de Cristais Líquidos, 2004, tese apresentada ao Instituto de
Física, Universidade de São Paulo, 23.
[5] I. H. Bechtold, B. Stiller,L. Brehmer, E. A. de Oliveira, Polímeros, 2006,
16, 4.
[6] W. Kohn, A.D. Becke, R.G. Parr, J. Phys. Chem. 1996, 100, 12974.
[7] H.A. Duarte, Quím. Nova 2001, 24(4), 501.
[8] (a) E. Cancès, B. Mennucci, J.J. Tomasi, Chem. Phys. 1997, 107, 3032;
(b) B. Mennucci, E. Cancès, J. Tomasi, J. Phys. Chem. B 1997, 101,
10506; (c) E. Cancès, B. Mennucci, J. Math. Chem. 1998, 23, 309.
[9] Gaussian 03, Revision D.01, M. J. Frisch et al., Gaussian, Inc.,
Wallingford CT, 2004.
[10] GaussView, Version 4.1, Roy Dennington II, Todd Keith and John
Millam, Semichem, Inc., Shawnee Mission, KS, 2007.
[11] A.A. Andrade, S.B. Yamaki, L. Misoguti, S.C. Zilio, Teresa D.Z. Atvars,
O.N. Oliveira Jr., C.R. Mendonça Optical Materials, 2004, 27, 441.
[12] J. Silva; N. DeSouza, V. Fernandes, P. Homem-de-Mello, O.N. Oliveira
Jr. J. Colloid and Interf. Sci. 2008, 327, 31.
AGRADECIMENTOS: PIC/UFABC, FAPESP.