Síntese – Módulo Inicial
1. Materiais
O Homem dispõe de uma grande diversidade de matérias. Uns são de origem natural – dos
quais o Homem se serve tal e qual como os extrai -, e outros de origem sintética. Nos materiais
de origem natural incluem-se também os materiais manufaturados, que, apesar de serem
modificados pelo homem, são de origem natural.
Define-se matéria por aquilo que tem volume e ocupa espaço (é formado por átomos) e
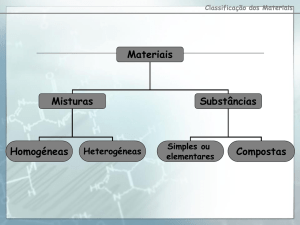
classifica-se em substâncias ou misturas de substâncias.
Substâncias: O material tem apenas uma componente/substância. Também é
denominada como substância pura. Uma substância é uma porção de matéria com
propriedades bem definidas e que lhe são características (densidade, ponto de
ebulição e fusão, cor, cheiro, …). A sua composição é fixa.
o Elementares: são sustâncias constituídas por átomos do mesmo elemento.
o Compostas: são substâncias constituídas por átomos de diferentes elementos.
Misturas: O material tem mais que uma componente, é uma mistura de substâncias.
o Heterogéneas: material em que se distinguem diferentes fases, não tendo por
isso um aspeto uniforme, á vista desarmada.
o Homogéneas: material em que não se distinguem diferentes fases, ou seja,
tem um aspeto uniforme e as diferentes substâncias que o compõem são
indistinguíveis, á vista desarmada.
Ao misturar-se substâncias diferentes, as propriedades de cada uma delas não se alteram pelo
facto de estas se encontrarem misturadas. É possível separar os constituintes de uma mistura
por processos físicos
As propriedades de uma mistura dependem dos seus constituintes, das suas propriedades e
das proporções em que estes se encontram.
As substâncias podem ter como unidades estruturais átomos (metais ou gases nobres),
moléculas (não metais) ou iões (metais e não metais), podendo ser representadas pelas suas
respetivas fórmulas químicas. No entanto, considera-se que toda a matéria é formada por
átomos, já que as moléculas são agregados de átomos e os iões provêm de um excesso carga
positiva ou negativa de um átomo.
Os estados de agregação da matéria resultam da combinação de duas forças opostas: as forças
de coesão de partículas (que tendem a dar um arranjo ordenado ao conjunto) e os
movimentos dessas partículas (que tendem a desfazer esse arranjo):
Estado sólido: as forças de atração sobrepõem-se aos movimentos das partículas.
o Energia crescente – fusão; energia decrescente: solidificação.
1
Síntese – Módulo Inicial
Estado líquido: as forças de coesão estão equilibradas com o movimento das
partículas.
o Energia crescente – vaporização; energia decrescente – condensação.
Estado gasoso: o movimento das partículas é mais evidente do que as forças de
coesão.
o A passagem direta do estado sólido para o gasoso e vice-versa denomina-se
sublimação (ex.. naftalina).
A mudança de estado físico não provoca alteração das unidades estruturais (com raras
exceções, como por exemplo o açúcar, que passa a sacarose).
Há casos em que as forças de coesão são tão fracas que se liquefazem a temperaturas muito
baixas e nunca solidificam, como o hélio.
O tamanho de um átomo depende fundamentalmente do tamanho da sua nuvem eletrónica,
já que o raio do núcleo é muito menor ao raio atómico. No entanto, a massa do mesmo átomo
depende fundamentalmente aos neutrões (protões e neutrões), que são as partículas
subatómicas do átomo mais pesadas.
Os átomos são eletricamente neutrões já que a sua carga nuclear (carga positiva proveniente
dos protões) simetriza-se com a carga dos eletrões (carga negativa).
Por vezes, os átomos perdem alguns eletrões, transformando-se em estruturas mais estáveis,
já que preenchem o último nível de energia, perdendo ou ganhando eletrões.
Quando o átomo atinge a sua estabilidade perdendo eletrões de valência, transformase num ião positivo ou catião, com excesso de carga positiva.
Quando o átomo atinge a sua estabilidade ganhando eletrões de valência, transformase num ião negativo ou anião, com excesso de carga negativa.
A massa de um ião é praticamente igual á massa do átomo do qual ele teve origem.
2
Síntese – Módulo Inicial
2. Soluções
Uma solução é uma mistura homogénea de duas ou mais substâncias.
Existem:
Soluções sólidas
Soluções gasosas
Soluções líquidas. Estas podem ser obtidas através de:
o Junção de líquidos miscíveis
o Dissolução de gases em líquidos
o Dissolução de sólidos em líquidos
Uma das substâncias da mistura denomina-se solvente e todas as outras são solutos. O
solvente é aquele que se encontra no mesmo estado físico que a solução, sendo considerado o
que está em maior quantidade, no caso de haver mais de uma substância no mesmo estado
físico que a solução. No entanto, caso as quantidades sejam as mesma, passa-se a consideram
como solvente a substância o componente mais volátil.
A concentração mássica de uma solução é a massa de um soluto existente em cada unidade de
volume de uma solução e obtém-se:
𝐶𝑚 =
𝑚
𝑣
, com:
Cm – concentração mássica
o Kg 𝑚−3 ou Kg/𝑚3 ( g 𝑑𝑚−3 ou g 𝐿−1)
m – massa do soluto
o Kg (g)
v – volume da solução
o 𝑚3 (𝑑𝑚3 )
3
Síntese – Módulo Inicial
3. Elementos Químicos
Cada elemento identifica-se pelo seu símbolo químico (X) e pelo seu respetivo número
atómico (Z):
𝑧𝑋
O número atómico (Z) indica o número de protões que o núcleo de determinado átomo de
determinado elemento (X) tem. O número de eletrões que o mesmo elemento (X) tem em
redor do seu núcleo também é deduzível a partir do seu número atómico (Z), já que os átomos
têm o mesmo número de protões e eletrões.
Os átomos do mesmo elemento podem apresentar, no entanto, diferentes números de massa,
isto é diferentes números de nucleões (A) – protões e neutrões, sendo que o número de
protões é constante e representado pelo número atómico (Z):
𝐴
𝑍𝑋
O número de neutrões (N) presente no núcleo de um átomo obtém-se então subtraindo ao
número de massa (A), o número de protões – número de protões (Z):
𝑁 =𝐴−𝑍
Existem átomos do mesmo elemento (com o mesmo número atómico), com diferentes
números de massa (nucleões). Esta variação é devida aos números de neutrões. Os átomos do
mesmo elemento que possuem um número diferente de nucleões são denominados isótopos.
Por exemplo:
12
6𝐶
13
6𝐶
14
6𝐶
A massa atómica (Ar) relativa de um elemento químico obtém-se efetuando uma média
pesada, já que temos de ter em conta a abundancia relativa de cada um dos isótopos desse
elemento e as respetivas massas (massas isotópicas):
𝐴𝑟 =
(𝑋1 ×𝐴𝑟1 )+(𝑋2 ×𝐴𝑟2 )
, com:
100
Ar – massa atómica relativa
𝐴𝑟1 – massa isotópica do isótopo 1
𝐴𝑟2 – massa isotópica do isótopo 2
𝑋1 – abundância relativa do isótopo 1
𝑋2 – abundância relativa do isótopo 2
4
Síntese – Módulo Inicial
A Tabela Periódica dos elementos tem 18 períodos (linhas) e 7 grupos (colunas) e está
organizada da esquerda para a direita e de cima para baixo por ordem crescente dos números
atómicos dos diferentes elementos químicos. A cada casa da Tabela Periódica corresponde um
átomo.
No mesmo grupo situam-se elementos com o mesmo número de eletrões de valência,
de maneira a que têm comportamentos químicos semelhantes.
o Os elementos que se situam nos grupos 1, 2, 13, 14, 15, 16, 17 e 18
denominam-se elementos representativos. (Os restantes elementos
denominam-se elementos de transição e não serão objeto de estudo direto).
Grupo 1 – metais alcalinos.
Grupo 2 – metais alcalino-terrosos.
Grupo 16 – calcogénios.
Grupo 17 – halogéneos.
Grupo 18 – gases nobres/raros/inertes
No mesmo período situam-se elementos com distribuição eletrónica semelhante. Cada
um dos períodos, com exceção do primeiro, inicia-se com um metal-alcalino e termina
com um gás nobre.
A Tabela periódica contém ainda uma linha quebrada que se inicia no Boro e que separa os
metais dos não-metais. No entanto alguns dos elementos que se encontram anexos a essa
linha podem comportar-se nalgumas situações como não-metais e noutras como metais.
A fórmula química de uma substância indica-nos a sua composição qualitativa (elementos
presentes) e a sua composição quantitativa (proporção de combinação dos elementos
presentes).
Na escrita de fórmulas químicas:
Representam-se em primeiro lugar os elementos metálicos e só depois os nãometálicos.
Os compostos moleculares (não metálicos) devem ser escritos segundo uma
determinada ordem.
o B
o C
o P
o N
o H
o S
o I
o Br
o Cl
o O
o F
5
Síntese – Módulo Inicial
Nos compostos iónicos, por convenção, representa-se em primeiro lugar os iões
positivos e depois os iões negativos, ainda que se escreva o nome dos aniões antes do
nome dos catiões.
o No caso dos compostos iónicos serem compostos dois elementos, recorre-se
às seguintes proporções:
1:1 se as combinações são entre elementos dos grupos 1 e 17 ou 2 e
16.
2:1 se as combinações são entre elementos dos grupos 1 e 16.
1:2 se as combinações são entre elementos dos grupos 2 e 17.
As substâncias iónicas que têm incorporadas na sua rede cristalina moléculas de água
(água de cristalização), dizem-se sais hidratados. Os que não têm dizem-se sais anidros.
Na fórmula química dos sais hidratados indica-se a proporção das moléculas de água:
CuSO4 .5H2 O
As massas moleculares relativas (Mr) obtém-se somando as massas atómicas relativas de cada
um dos elementos das moléculas (composição qualitativa), nas devidas proporções
(composição quantitativa).
6