UNIVERSIDADE FEDERAL DE OURO PRETO
PRÉ-VESTIBULAR RUMO À UNIVERSIDADE
CAMPUS JOÃO MONLEVADE
QUÍMICA AMBIENTAL
ORIENTADORA: PROF.ª DRA. KARLA VIEIRA
PROF. LUCAS SIQUEIRA
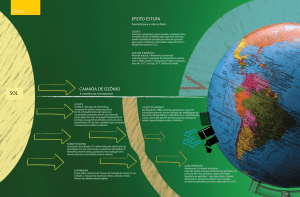
CAMADA DE OZÔNIO (I)
• A camada de ozônio situa-se na estratosfera e é
uma região que apresenta uma concentração
maior de Ozônio (O3) na atmosfera;
• O ozônio é formado pela fotodecomposição do
Oxigênio (O2) que atinge a estratosfera, originando
radicais livres;
• Esses radicais livres, muito instáveis, reagem com
moléculas de oxigênio, formando ozônio;
• A molécula de ozônio formada encontra-se em um
estado excitado de energia, no qual os
movimentos vibracionais de seus átomos levam à
sua decomposição;
CAMADA DE OZÔNIO (II)
• Entretanto, quando essa molécula excitada se
colide com outra partícula, ocorre transferência de
energia excedente, e é formado então Ozônio (O3)
em seu estado fundamental (estável);
• Nessas etapas anteriores, ocorre a absorção da
radiação UV e transformação em energia térmica,
tornando a temperatura da estratosfera maior que
a da atmosfera;
• Por outro lado, as moléculas de Ozônio (O3) sofrem
fotodecomposição, sendo transformadas em O2 e
o radical O;
CAMADA DE OZÔNIO (III)
• Esse radical oxigênio, ao atacar uma molécula de
gás oxigênio, origina o ozônio, estabelecendo
então um equilíbrio dinâmico que faz com que a
concentração de Ozônio (O3) na atmosfera seja
praticamente constante.
• Equações:
DESTRUIÇÃO DA CAMADA DE OZÔNIO (I)
• Estudos na década de 1970 revelaram que o NO e
o NO2 catalisavam o processo de decomposição
do Ozônio;
• O NO e o NO2 são formados naturalmente em uma
descarga elétrica:
• A ação catalítica desses gases na degradação da
camada de ozônio ocorre da seguinte forma:
DESTRUIÇÃO DA CAMADA DE OZÔNIO (II)
• Posteriormente, foi descoberto que algumas
moléculas de água que atingem a estratosfera
colidem com oxigênios excitados, originando
radicais livres hidroxila;
DESTRUIÇÃO DA CAMADA DE OZÔNIO (III)
• Os radicais hidroxila catalisam a decomposição do
ozônio:
• Estudos posteriores revelaram que os CFC’s
(Clorofluorcarbonetos, também conhecidos como
gases freons) eram nocivos a camada de ozônio.
DESTRUIÇÃO DA CAMADA DE OZÔNIO (IV)
• Os CFC’s foram muito utilizados no século passado
na indústria como propelentes em aerossois, gases
de expansão de polímeros e gases refrigeradores
em geladeira e aparelhos de ar condicionado,
devido aos CFC’s:
•
•
•
•
Não oxidarem metais;
Não serem combustíveis;
Não serem tóxicos;
Não apresentarem cheiro.
DESTRUIÇÃO DA CAMADA DE OZÔNIO (V)
• Devido a sua alta estabilidade e grande inércia
química, esses gases atingem a estratosfera, se
fragmentam em presença de radiação UV e
originam o radical livre Cloro, que é catalisador
potencial da decomposição do Ozônio.
BURACO NA CAMADA DE OZÔNIO (I)
• Na primavera antártica (de setembro à novembro)
ocorre uma grande diminuição na concentração
do ozônio estratosférico, o que chamamos de
buraco na camada de ozônio;
• O fenômeno causador é o vortex, um vento polar
que se caracteriza como um ciclone de grande
duração e extensão, que atrai para o Polo Sul
diversos gases, entre eles os catalisadores da
decomposição da camada de ozônio, no inverno.
Esses catalisadores ficam presos em cristais de gelo.
BURACO NA CAMADA DE OZÔNIO (II)
• Com a chegada da primavera, ocorre o
desaparecimento do vortex polar, o derretimento
dos cristais de gelo, e a liberação dos gases
aprisionados, o que provoca o aumento da
concentração de gases nocivos à camada de
ozônio;
• Esses gases potencializam a rarefação da camada
de ozônio até ao final de novembro, período que o
ar é renovado devido aos movimentos nas
correntes de ar e o buraco é fechado.
POLUIÇÃO DOS SOLOS (I)
• O solo constitui a camada superficial da crosta
terrestre. Ele funciona como uma espécie de filtro,
que impede a passagem de alguns compostos
químicos para a água subterrânea;
• A poluição do solo consiste no depósito de
substâncias nocivas em sua superfície ou em seu
interior,
capazes
de
provocar
mudanças
significativas em sua estrutura e composição
natural.
POLUIÇÃO DOS SOLOS (II)
• As principais atividades antropogênicas que levam
à sua destruição são:
• Utilização de fertilizantes e agrotóxicos na agricultura;
• Descarte de resíduos da produção industrial e vazamentos
de matéria-prima ou produtos finais;
• Estocagem e distribuição de combustíveis e lubrificantes;
• Utilização de substâncias tóxicas na extração de minérios;
• Acidentes nucleares envolvendo vazamento dos produtos
radioativos;
• Deposição de lixo sem tratamento, não reuso ou não
reciclagem de materiais;
• Despejo de esgoto sem tratamento ou de resíduos de seu
tratamento.
POLUIÇÃO DOS SOLOS (III)
CONSTRUÇÃO DE ATERROS
SANITÁRIOS (I)
CONSTRUÇÃO DE ATERROS
SANITÁRIOS (II)
CONSTRUÇÃO DE ATERROS
SANITÁRIOS (III)
POLUIÇÃO DAS ÁGUAS
• O lançamento de substâncias orgânicas, tóxicas, o
descarte inadequado de poluentes ou a infiltração
de líquidos poluentes nos lençóis freáticos gera um
enorme desequilíbrio nos ecossistemas aquáticos.
• Entre as principais formas de poluição, estão:
•
•
•
•
•
•
Poluição por fertilizantes e agrotóxicos;
Poluição pela exploração do petróleo;
Poluição por esgotos domésticos;
Poluição por fosfatos;
Poluição por dióxido de enxofre e de nitrogênio;
Poluição por mercúrio e chumbo.
OBRIGADO PELA ATENÇÃO!
PROF. LUCAS SIQUEIRA