O Ca2+ no Músculo Liso Unitário
A membrana da célula muscular lisa
possui muito mais canais de Ca2+
dependentes da voltagem do que o
músculo esquelético, e possui
correspondentemente muitos menos canais
de Na+ dependentes da voltagem.
Portanto, o Na+ participa pouco na geração
do potencial de acção no músculo liso. O
fluxo de iões Ca2+ para o interior da fibra
é responsável pela geração do potencial de acção. Isto ocorre da mesma forma
auto-regenerativa como ocorre para os canais de Na+ nas fibras musculares
esqueléticas.
Assim, o Ca2+ é não só responsável pela despolarização como também é responsável
pela activação do processo de contracção por interacção com a calmodulina. No
entanto, os canais de Ca2+ abrem mais lentamente que os canais de Na+ e
permanecem abertos mais tempo. Isto é dá origem aos prolongados potenciais de
acção característicos do músculo liso.
15
Potenciais no Músculo Liso Unitário
No estado de repouso, o potencial intracelular
da célula muscular lisa é de cerca de –50 a
–60 mV, ou seja, cerca de –30 mV menos
negativo que o da célula muscular
esquelética.
Os potenciais de acção no músculo liso
unitário ocorrem em duas formas:
A e B. Potencial em ponta (Spike Potentials)
Este tipo de potenciais, que são similares aos
que se observam no músculo esquelético,
ocorrem na maioria das células do músculo
liso unitário. Duram de cerca de 10 a 50 ms.
Podem ser estimuladas de várias maneiras, por
exemplo, por estimulação eléctrica, por acção
de hormonas no músculo liso, por acção
de neurotransmissores libertados pelas fibras nervosas, por estiramento, e ainda, como
resultado da despolarização da fibra muscular mediada pelas células intersticiais de
Cajal (células pacemaker).
16
Potenciais no Músculo Liso Unitário
B. Potencial de onda lenta (Slow Wave
Potentials).
O potencial de alguns tecidos musculares lisos
oscila, formando uma onda lenta na zona
adjacente à membrana plasmática, especialmente
nos músculos lisos da parede dos intestinos. Esta
onda lenta é produzida por uma rede especializada
de células não musculares: as células intersticiais
de Cajal que comunicam com o músculo liso
através de junções de hiato. A onda lenta não é um
potencial de acção. Ou seja, não é um processo
auto-regenerativo que se propaga ao longo da
fibra muscular. Mas quando a onda lenta é
suficientemente positiva pode iniciar potenciais de
acção no músculo liso, mediados pela abertura de
canais iónicos de Ca2+ dependentes da voltagem.
As ondas lentas são também conhecidas por ondas
marca-passo (pacemaker waves).
17
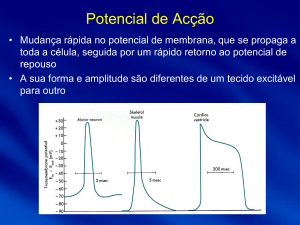
Potenciais no Músculo Liso Unitário
Figura do livro Integrative Action of the Autonomic Nervous System: Neurobiology of Homeostasis (2006) By Wilfrid
Jänig, Cambridge University Press.
Potenciais no Músculo Liso Unitário
C. Potencial de acção com plateau (Action
Potentials with Plateaus)
O começo deste tipo de potencial é similar ao
potencial em ponta. No entanto, em vez de
ocorrer uma rápida repolarização da célula, a
repolarização atrasa-se várias centenas de ms
(atraso que pode chegar até 1000 ms). Este
plateau pode explicar as contracções
prolongadas que ocorrem em alguns tipos de
músculo liso, tal como o ureter, o útero e
alguns tipos de músculos lisos vasculares.
19
Potenciais no Músculo Liso Multiunitário
As fibras musculares lisas multiunitárias contraem-se normalmente somente em
resposta a estímulos nervosos (sistema nervoso autónomo).
Não se desenvolvem tipicamente potenciais de acção. Isto deve-se ao facto das fibras
serem constituídas por células muito pequenas que não estão conectadas umas às
outras (o número de junções de hiato é muito reduzido ou nulo), pelo que cada célula
contrái independentemente das restantes.
O tempo requerido para
activação da fibra é de cerca de
200 a 300 ms, e chama-se
período latente, que decorre
antes da contracção começar.
Este período latente é cerca de
50× maior do que o período
latente do músculo esquelético.
20
Acção do Sistema Nervoso Autónomo no Músculo Liso
As fibras nervosas do sistema nervoso
autónomo que inervam o músculo liso
geralmente ramificam-se duma forma difusa no
topo da camada de fibras musculares lisas.
Na maioria dos casos, as fibras nervosas não
fazem contacto directo com as fibras musculares
lisas, formando junções difusas que secretam o
seu neurotransmissor na matriz que rodeia o
músculo liso, a alguns nm a µm das fibras. O
neurotransmissor difunde-se até às células
musculares.
Quando existem muitas camadas de células musculares lisas, só a camada externa é que
é inervada. A excitação muscular propaga-se entre as camadas por propagação interna
do potencial de acção de uma célula muscular para outra e ainda por difusão externa do
neurotransmissor.
Os botões terminais das fibras nervosas têm múltiplas varicosidades distribuídas ao
longo dos seus eixos. Nestes pontos, não existem células de Schwann, permitindo a
secreção de NT através das paredes das varicosidades.
21
Acção do Sistema Nervoso Autónomo no Músculo Liso
Em algumas situações, especialmente no músculo
liso multiunitário, as varicosidades encontram-se
directamente sobre a membrana da fibra
muscular, separados desta membrana por cerca
de 20 a 30 nm, a mesma espessura da fenda
sináptica da junção neuromuscular. Estas zonas
designam-se junções de contacto e funcionam da
mesma forma que no músculo esquelético. Como
consequência estas fibras contraem-se mais
rapidamente do que as fibras estimuladas pelas
junções difusas.
Os neurotransmissores mais importantes secretados pelas fibras nervosas do
sistema nervoso autónomo são a acetilcolina e a norepinefrina. Nunca são
secretadas pelas mesmas fibras nervosas. A acetilcolina e a norepinefrina são
substâncias excitatórias em alguns órgãos e inibitórias noutros órgãos.
22
Acção do Sistema Nervoso Autónomo no Músculo Liso
Quando a acetilcolina excita uma fibra muscular, a
norepinefrina tipicamente inibi-a, e vice-versa.
Isto acontece porque a acetilcoolina e a
norepinefrina actuam sobre as fibras musculares
lisas por interacção com receptores proteicos
membranares. Alguns destes receptores são
excitatórios, enquanto que outros são inibitórios.
Todos eles conduzem à activação de segundos
mensageiros metabotrópicos.
Exemplos da actuação de receptores muscarínicos
(acetilcolina) (Eglen, 2006, Autonomic & Autacoid Pharmacology, 26: 219–233): M3 medeia a contracção de
inúmeros músculos lisos nos tractos respiratório, gastrointestinal e genito-urinário; M1
e M3 medeiam a relaxação do músculo liso vascular.
Exemplos da actuação de receptores adrenérgicos (norepinefrina). Receptores α1,
excitatórios, envolvidos na contracção do músculo liso vascular, tracto genito-urinário e
esfíncteres e os receptores β2, com efeitos relaxantes no músculo liso dos tractos
respiratório, gastrointestinal, e genito-urinário (Kandel et al, 2001, Principles of Neuroscience, NY: MacGrawHill).
23
Estimulação mediada por hormonas
Cerca de metade das contracções do músculo liso são iniciadas por factores
estimulatórios que actuam directamente sobre a maquinaria de contracção do
músculo liso, sem recurso a potenciais de acção. Os factores mais frequentemente
envolvidos neste processo são: (1) hormonas e (2) agentes químicos locais.
Muitas das hormonas em circulação no
organismo afectam a contracção do músculo liso,
em maior ou menor grau. São elas a
norepinefrina, epinefrina, acetilcolina,
angiotensina, endotelina, vasopressina, oxitocina,
serotonina e histamina. Estas hormonas irão
provocar excitação ou inibição da fibra muscular
lisa dependendo da acção do receptor a que se
ligam na célula.
Os receptores hormonais apresentam dois tipos de resposta: (1) Alteram o
potencial da célula, aumentam ou diminuem o potencial, por abertura e/ou fecho
selectivo de canais iónicos; (2) Não alteram o potencial da célula, promovendo,
por exemplo, a libertação de Ca2+ do retículo sarcoplasmático (excitatório) ou a
activação das Ca2+ Mg-ATPase que bombeiam iões cálcio para o retículo
24
sarcoplasmático e espaço extracelular (inibitório).
Estimulação do músculo liso por neurotransmissores e hormonas
Hilgers et al, 2005, Exp Biol Med, 230: 829-835.
25
Relaxamento do músculo liso por neurotransmissores e hormonas
Yuan et al, 2007, BMC Pregnancy and Childbirth, 7(Suppl 1):S10.
26
Estimulação mediada por agentes químicos locais
A contracção das arteríolas,
metarteríolas e esfíncteres précapilares, é mediada pelo
músculo liso. Estes pequenos
vasos tem pouco ou nenhum
controlo nervoso. No entanto,
respondem rapidamente a
alterações nas condições
químicas locais do fluído
intersticial. Alguns dos agentes
químicos locais de controlo são:
(1) O2 - diminuição da concentração do O2 nos tecidos locais faz com que o
músculo liso relaxe, e portanto provoca vasodilatação.
(2) CO2 - excesso de CO2 também provoca vasodilatação.
(3) H+ - aumento da concentração de H+ também provoca vasodilatação.
O aumento da concentração em adenosina, ácido láctico, iões K+, a diminuição da
concentração em iões Ca2+ e o aumento da temperatura corporal também
provocam vasodilatação.
27
Estimulação mediada por estiramento das membranas
Quando o músculo liso é suficientemente estirado, gera potenciais de acção
espontaneamente. Eles resultam duma combinação de: (1) potenciais de onda
lenta e (2) despolarização membranar devida ao estiramento. Este tipo de
resposta permite que os músculos lisos do intestino, quando suficientemente
esticados por alimentos, se contraiam automática e ritmicamente.
Nota: Esta imagem é
ilustrativa da acção do
SNA e do estiramento
nos movimentos
peristálticos do
intestino.
http://www.mfi.ku.dk/ppaulev/chapter22/kap%2022.htm
28
Comparação dos mecanismos de contracção dos músculos
esquelético e liso
Para além dos aspectos, já referidos, sobre a acção do complexo Ca2+- calmodulina,
da miosina cinase e da miosina fosfafatase no processo de contracção muscular,
existem outras diferenças nos dois mecanismos de contracção muscular.
A velocidade do ciclo das cabeças cruzadas é muito menor no músculo liso, cerca
de 1/10 a 1/300 da frequência com que ocorre no músculo esquelético. Uma das razões
para esta lentidão é a lenta actividade ATPásica das cabeças de miosina, que afecta a
velocidade de degradação do ATP e consequentemente a velocidade de colocação das
cabeças de miosina num estado conformacional de alta-energia. Por outro lado, a
fracção de tempo em que as cabeças de miosina permanecem ligadas à actina é maior
no músculo liso.
A energia requerida para suster a contracção do músculo liso é cerca de 1/10 a 1/300
da energia necessária para suster a mesma tensão de contracção no músculo
esquelético. Pensa-se que isto resulta da lenta velocidade do ciclo das cabeças
cruzadas e do facto de só se despender 1 molécula de ATP por ciclo,
independentemente da sua duração. Este baixo dispêndio de energia é importante
porque órgãos como os intestinos, a bexiga, a vesícula biliar, e outras vísceras mantém
um estado de contracção tónica quase indefinidamente.
29
Comparação dos mecanismos de contracção dos músculos
esqueléticos e liso
O começo da contracção e a duração total da contracção demoram em média
mais tempo no músculo liso. O músculo liso começa a contrair cerca de 50 a 100
ms após ter sido excitado, atinge a força máxima cerca de 500 ms depois,
declinando de seguida até ao repouso em 1 a 2 s. O tempo total de contracção é de
1 a 3 segs. Isto é em média 30× mais lento do que uma contracção dum músculo
esquelético. Devido à grande variedade de músculos lisos, a contracção pode durar
tão pouco como 0.2 segs ou tanto como 30 segs. São duas as razões para esta
lentidão: (1) a baixa velocidade do ciclo das cabeças cruzadas; (2) a baixa
velocidade do processo de iniciação da contracção.
A força de contracção muscular é em média maior do que a do músculo
esquelético – 4 a 6 Kg/cm2 em comparação com o 3 a 4 Kg/cm2 do músculo
esquelético. Esta grande força de contracção resulta do período prolongado de
ligação das cabeças cruzadas de miosina aos filamentos de actina.
30
Comparação dos mecanismos de contracção dos músculos
esqueléticos e liso
O mecanismo latch permite que o
músculo liso permaneça em contracção
tónica durante horas, com pouco
consumo de energia ou necessidade de
sinais excitatórios.
Quando a estimulação é persistente e
os níveis citosólicos de Ca2+
permanecem relativamente elevados,
a velocidade de hidrólise do ATP no
ciclo das pontes cruzadas diminui.
Nestas circunstâncias, a desfosforilação, mediada pela miosina fosfatase, das unidades
regulatórias da miosina dá-se, mesmo com a miosina ligada à actina. As miosinas assim
desfosforiladas permanecem muito mais tempo agarradas à actina, atrasando o ciclo da
cabeças cruzadas enquanto mantém a tensão muscular. Como consequência, o número
de cabeças ligadas aos filamentos de actina num dado momento permanece elevado,
mantendo a contracção. Pouca energia está a ser utilizada nestas circunstâncias (cerca
de 1/300 da energia que é utilizada para manter a contracção no músculo esquelético)
porque o ATP não é degradado a ADP (Widmaier et al, 2006, Vander´s Human Physiology, McGraw-Hill
31).
Bibliografia
• Crimi E, Taccone FS, Infante T, Scolletta S, Crudele V, Napoli C (2012) Effects
of intracellular acidosis on endothelial function: an overview J Crit Care 27: 108118• Guyton & Hall, 2005, Textbook of Medical Physiology, Pennsylvania: Elsevier.
• Widmaier et al, 2006, Vander´s Human Physiology: The Mechanisms of Body
Funcion, NY: McGraw-Hill.
• Hilgers et al, 2005, Molecular Aspects of Arterial Smooth Muscle Contraction:
Focus on Rho, Exp Biol Med, 230: 829-835.
• Gunst, 2000, The contractile apparatus and mechanical properties of airway
smooth muscle, Eur Respir J, 15: 600-616.
32