Universidade de São Paulo
Faculdade de Medicina de Ribeirão Preto
Programa de Pós-Graduação em Imunologia Básica e Aplicada
Autores: Gislane Lelis Vilela de Oliveira e Bernardo Pereira Moreira
Compartimentos da Resposta Imune
Os órgãos e tecidos linfóides podem, didaticamente, ser divididos em órgãos linfóides
primários (medula óssea e timo) e órgãos linfóides secundários (sistema linfático, linfonodos e
baço).
A medula óssea é constituída por tecido esponjoso com função principal de realizar a
hematopoese, que ocorre no interior dos ossos chatos (esterno, vértebras, ílio, costelas, dentre
outros). As principais células do sistema imunológico, os linfócitos B e T, têm origem em
progenitor linfóide comum e seu desenvolvimento, e ainda, a
maturação funcional ocorrem na medula óssea, para o
linfócito B e, no timo para os linfócitos T.
O timo está localizado atrás do osso esterno e é
formado por uma cápsula de tecido conjuntivo. Está dividido
em lobos esquerdo e direito e subdividido em lóbulos. Cada
um desses lóbulos contém um córtex externo e uma medula
interna. Os linfócitos T, durante sua maturação, são chamados
de timócitos, passando por dois processos de maturação
importantes, a seleção positiva, que ocorre no córtex, e ainda,
a seleção negativa que ocorre na medula. No processo de
seleção positiva, somente são selecionados os timócitos que
apresentam interação adequada do TCR com a molécula do
MHC. Na seleção negativa, são delidos os linfócitos com alta afinidade pelos antígenos próprios
(link Tolerância).
Os órgãos linfóides secundários são os locais onde as respostas imunes são iniciadas.
Antígenos com porta de entrada nos tecidos são conduzidos aos linfonodos drenantes pelas células
dendríticas, carregados pela linfa por intermédio dos vasos linfáticos, enquanto antígenos
introduzidos diretamente na corrente sanguínea são conduzidos ao baço.
Os linfonodos estão localizados ao longo dos vasos linfáticos e são pequenos órgãos
envoltos em cápsula fibrosa, perfurada por um vaso linfático aferente, por onde a linfa adentra ao
linfonodo e um vaso eferente, de saída do liquido “filtrado”. Os linfonodos são constituídos por
córtex e medula interna. A camada mais externa do córtex contém os folículos primários ou zona de
células B e, na região parafolicular, a zona de células T.
Após os respectivos processos de maturação no timo ou medula óssea, os linfócitos entram
na circulação sanguínea, povoando os órgãos linfóides secundários. Ao migrarem para os
linfonodos, os linfócitos B e T naive atingem o estroma do córtex pelas vênulas de endotélio alto
(HEV – high endothelial venules), havendo interação da selectina (CD62L), presente nos linfócitos
T e B, com o ligante dessa molécula expresso nas HEVs. Uma vez dentro do linfonodo, ocorre
segregação anatômica dessas células, que expressam receptores que se ligam a quimiocinas
específicas presentes em diferentes locais do linfonodo. Assim, as quimiocinas CCL19 e CCL21
são produzidas pelas células estromais da região parafolicular, atraindo para essa região linfócitos T
e células dendríticas que expressam CCR7 (receptor específico para CCL19 e CCL21). A
quimiocina CXCL13 é produzida pelas células foliculares e atrai os linfócitos B naive para os
folículos primários, por meio da expressão do receptor CXCR5.
Uma vez que haja o encontro da célula dendrítica com o antígeno nos tecidos, essas células
migram para os vasos linfáticos por onde são
levadas até aos linfonodos onde se inicia a
resposta que envolve a interação de linfócitos
T e B. Os linfócitos T CD4 auxiliares são
ativados
por
células
dendríticas
que
apresentam o antígeno peptídico e passam
então a expressar CD40 e CXCR5, migrando
assim em direção ao folículo. Já os linfócitos
B,
ativados
apresentados
pelo
na
antígeno
superfície
solúvel
de
ou
células
dendríticas foliculares, passam a expressar CD40L e CCR7, migrando assim em direção a zona de
células T. Dessa forma, as duas células entram em contato e a interação dos seus ligantes é essencial
na formação do centro germinativo ou folículo secundário, região de amplificação da resposta
imune. Após essa interação, os linfócitos B voltam a expressar CXCR5 e retornam ao folículo, onde
iniciam intensa proliferação. Depois disso, as células vão passar pelo processo de maturação de
afinidade e somente aquelas que mantiverem maior afinidade ao antígeno são selecionadas para
diferenciação em células secretoras de anticorpos e células B de memória (link Imunidade
Humoral). As células T e B ativadas nos linfonodos, por intermédio da mudança da expressão de
receptores, migram para o local da infecção, onde realizam sua função efetora.
Assim como os linfonodos filtram a linfa, o baço exerce sua função de filtrar o sangue,
eliminando antígenos veiculados diretamente pela corrente sanguínea. Este órgão envolto por uma
cápsula está localizado no quadrante superior esquerdo do abdômen e está subdivido, interiormente,
em polpa branca e polpa vermelha. A polpa branca é constituída principalmente por linfócitos T e
B, que também são segregados anatomicamente pela atração de quimiocinas, assim como nos
linfonodos, compreendendo as zonas de células B (folículos) e zonas de células T. Na polpa
vermelha, encontram-se grandes quantidades de eritrócitos, células dendríticas e macrófagos, que
desempenham papéis importantes na remoção de microrganismos opsonizados e hemácias
danificadas, modificadas ou senescentes.
Como parte dos órgãos linfóides secundários está o sistema imunológico cutâneo e o
associado às mucosas. O sistema imunológico cutâneo é constituído pela pele, como a principal
barreira física, sendo os queratinócitos, células de Langerhans e linfócitos intra-epiteliais os
constituintes da primeira barreira de vigilância. Na derme, estão macrófagos e linfócitos T (tanto
CD4+ quanto CD8+) e essas células podem entrar nos vasos linfáticos e iniciar a resposta imune
nos linfonodos.
O sistema imunológico associado às mucosas, por outro lado, é constituído principalmente
pelas mucosas dos tratos gastrintestinal e respiratório. Estes ambientes são colonizados por
linfócitos e APCs e podem, rapidamente, migrar para os linfonodos para iniciar a resposta imune.
Como principal constituinte do sistema imunológico associado às mucosas, estão as Placas de
Peyer, que são conjuntos organizados de linfócitos, localizados logo abaixo do epitélio mucoso e
que podem rapidamente iniciar a resposta imune frente a um antígeno.
Esta organização dos tecidos linfóides está relacionada com a funcionalidade das células de
defesa que possuem a capacidade de vigiar todo o organismo e responder de forma efetiva em todos
os sítios de infecção. Para isso, o sistema deve ser capaz de responder a qualquer tipo de patógeno
que pode invadir qualquer lugar do organismo, mesmo levando-se em consideração que somente
poucos linfócitos são específicos para cada antígeno. Para isso, a rede de vasos sanguíneos e vasos
do sistema linfático proporcionam vias acessíveis para que os linfócitos vigiem o organismo e
facilitem a sua chegada aos sítios de infecção e exerçam seus mecanismos efetores. O movimento
dos linfócitos entre esses locais é chamado de recirculação linfocitária e o processo pelo qual as
diferentes populações de linfócitos entram em determinados tecidos em detrimento de outros, é
chamado de endereçamento linfocitário ou homing. Essa recirculação e migração de linfócitos são
mediadas por moléculas de adesão presentes nas superfícies dos linfócitos e das células endoteliais,
além de moléculas quimioatraentes produzidas por várias células (quimiocinas).
As moléculas de adesão e
quimiocinas
são
expressas
em
diferentes momentos nas células e
tecidos. Linfócitos naive ou inativos
expressam principalmente receptores
L-selectina, cujo principal ligante é
expresso na superfície de células
endoteliais e estão relacionados com
a adesão dos linfócitos às vênulas de
endotélio alto (HEVs) que chegam
aos linfonodos. Se não são ativadas
por
células
apresentadoras
de
antígenos, os linfócitos naive saem
dos linfonodos através dos vasos linfáticos eferentes e retornam à corrente sanguínea. Quando os
linfócitos que atingiram os linfonodos são ativados por células APCs (link Imunidade Celular) que
capturaram antígenos na periferia, eles passam a expressar um novo perfil de moléculas de
superfície e receptores, diferentes daqueles expressos em linfócitos naive. Então, ocorre aumento de
ligantes de selectinas –E e –P nas superfícies dos linfócitos ativados que se aderem ao endotélio de
capilares expressando selectinas –E e -P, nos locais de infecção. Integrinas de alta afinidade, como
LFA-1 (Lymphocyte function-associated antigen 1) e VLA-4 (Very Late Antigen-4) também são
expressas pelos linfócitos efetores que auxiliam na forte adesão destas células na parede dos
capilares e posterior migração para o tecido inflamado adjacente. Esta migração é dependente de
diferentes quimiocinas produzidas nos sítios de inflamação. Para cada tipo de tecido, são expressos
diferentes perfis de quimiocinas (ex: CCL25 na inflamação intestinal, CCL27 na inflamação
cutânea).
Os diferentes tipos celulares, em diferentes estágios de desenvolvimento e maturação,
expressam perfis específicos de moléculas de superfície e receptores, sendo responsáveis pelo
direcionamento dessas células para o seu local de ação. Todo esse mecanismo e as vias de
recirculação são fundamentais para o sucesso do sistema imunológico em combater as infecções e
manter a homeostase do organismo.
Implicações Clínicas
Uma vez perdida a homeostase no organismo, surgem alterações na função ou na arquitetura
dos órgãos linfóides primários ou secundários. No entanto, algumas alterações podem ser
congênitas ou de origem genética como veremos a seguir.
Algumas alterações na medula óssea podem ocorrer por insuficiência desse tecido, como
ocorre na anemia aplásica, ou por interferências na composição celular da medula, como ocorre nas
leucemias, em que as células neoplásicas infiltram esse tecido. O paciente com anemia aplásica
possui medula óssea hipocelular e o seu desenvolvimento está associado com exposições a drogas,
radiação ionizante, agentes químicos e infecções virais. Por outro lado, pacientes com leucemia
mielóide aguda apresentam a medula óssea infiltrada por blastos que sofreram transformação
neoplásica e prejudicam a produção de células sanguíneas (hematopoese).
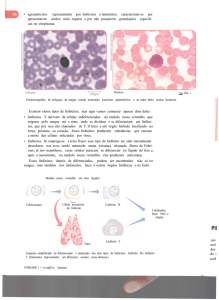
Medula óssea hipocelular (aplasia de medula) e composição celular de medula óssea saudável.
Fonte: Zago, MA; Falcão, RP; Pasquini, R. Hematologia, fundamentos e prática.
Medula óssea infiltrada por blastos mielóides em pacientes com leucemia mielíde aguda. Fonte:
http://anatpat.unicamp.br/lamhemo4.html.
A ausência congênita do timo, conhecida como síndrome de DiGeorge, é caracterizada pelo
numero reduzido de células T maduras na circulação sanguínea e nos órgãos linfóides periféricos,
ocasionando deficiência na imunidade mediada por linfócitos T.
Com relação aos órgãos linfóides secundários, algumas alterações podem ocorrer nos
linfonodos, como aumento de tamanho (adenomegalia) nos linfomas e alterações na arquitetura,
como ocorre na leucemia linfóide crônica. Os linfomas compreendem um conjunto de alterações,
em que ocorre transformação neoplásica dos linfócitos, infiltrando os linfonodos (principalmente os
axilares), formando massas tumorais linfáticas e prejudicando o funcionamento das respostas
imunes. Na leucemia linfóide crônica, ocorre alteração da arquitetura dos linfonodos, com
comprometimento das zonas cortical e medular e desaparecimento dos folículos devido à infiltração
por linfócitos em todo o órgão, incluindo a região do hilo.
Biópsia do linfonodo evidenciando todo comprometimento da arquitetura do órgão. Ausência de
diferenciação das zonas cortical e medular e ausência de folículos. Fonte:
http://anatpat.unicamp.br/lamhemo7.html.
Com relação ao baço, algumas doenças podem apresentar aumento deste órgão
(esplenomegalia), como ocorre em algumas doenças hematológicas (alguns tipos de anemias) e
infecciosas. O baço também participa na eliminação de hemácias defeituosas ou senescentes,
eliminando da circulação as células com alterações de forma, como os eritrócitos falciformes na
anemia falciforme ou as hemácias esféricas na esferocitose hereditária. Por outro lado, a retirada
deste órgão linfóide, seja por falência como consequência de doenças ou por acidentes, prejudica
gravemente o processo de fagocitose de bactérias encapsuladas, deixando estas pessoas suscetíveis
a infecções por tais bactérias.
Hemácias normais bicôncavas, esferócitos e hemácia falciforme em microscopia eletrônica de
varredura.
Fonte:
Página
da
Academia
de
Ciência
e
Tecnologia
(http://www.ciencianews.com.br/perguntas/perguntas-index.htm).
Microscopia eletrônica de varredura mostrando um macrófago, fagocitando um esferócito no baço.
Fonte:
Página
da
Academia
de
Ciência
e
Tecnologia
(http://www.ciencianews.com.br/perguntas/perguntas-index.htm).