Ciclo de Krebs ou do ácido cítrico; Rui Fontes
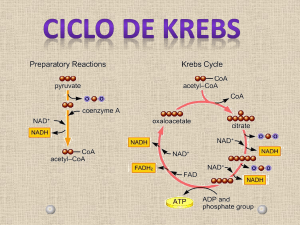
O ciclo de Krebs ou do ácido cítrico
1-
Por ação das enzimas da glicólise a glicose é, no citoplasma das células, parcialmente oxidada a piruvato. O
piruvato entra para a mitocôndria e, através da ação catalítica da desidrogénase do piruvato, dá origem a
acetil-CoA (ver Equação 1). No catabolismo dos aminoácidos, dos ácidos gordos e do etanol também se
forma acetil-CoA. O ciclo de Krebs (também designado do citrato ou dos ácidos tricarboxílicos) é uma via
metabólica central no metabolismo dos nutrientes pois permite a oxidação do grupo acetilo da acetil-CoA
(a CO2) com a concomitante redução do NAD+ e do FAD a NADH e FADH2 que são intermediários no
processo de redução do O2 (a H2O). A importância do ciclo de Krebs no metabolismo e na sobrevivência
dos seres vivos fica evidenciada pela extrema raridade das doenças congénitas em que há defeitos na
atividade de enzimas deste ciclo [1].
Equação 1
2-
piruvato + NAD+ + CoA → acetil-CoA + NADH + CO2
As enzimas envolvidas nas reações do ciclo de Krebs estão todas dentro da mitocôndria e são as seguintes:
síntase do citrato (Equação 2), aconitase (Equação 3), desidrogénase do isocitrato (Equação 4),
desidrogénase do α-cetoglutarato (Equação 5), sintétase de succinil-CoA (Equação 6), desidrogénase
do succinato1 (Equação 7), fumárase (Equação 8) e desidrogénase do malato (Equação 9). A sintétase de
succinil-CoA é o nome atribuído a duas isoenzimas distintas mas com atividades semelhantes: uma tem
maior afinidade para o GDP e leva à formação de GTP enquanto a outra tem maior afinidade para o ADP e
leva à formação direta de ATP.
Equação 2
Equação 3
Equação 4
Equação 5
Equação 6
Equação 7
Equação 8
Equação 9
acetil-CoA + oxalacetato + H2O → citrato + CoA
citrato ↔ isocitrato
isocitrato + NAD+ → α-cetoglutarato + CO2 + NADH
α-cetoglutarato + NAD+ + CoA → succinil-CoA + NADH + CO2
succinil-CoA + GDP (ou ADP) + Pi ↔ succinato + CoA + GTP (ou ATP)
succinato + FAD → fumarato + FADH2 (ver nota de rodapé nº 1)
fumarato + H2O ↔ malato
malato + NAD+ ↔ oxalacetato + NADH
Se ignorarmos momentaneamente a formação de NADH, FADH2, ATP (ou GTP), CO2 e CoA poderemos
escrever a seguinte sequência de transformações: oxalacetato [4C] (+ acetil-CoA [2C no resíduo acetilo])
→ citrato [6C] → isocitrato [6C] → α-cetoglutarato [5C] → succinil-CoA [4C no resíduo de succinilo]→
succinato [4C] → fumarato [4C] → malato [4C] → oxalacetato [4C]. O facto de iniciarmos e terminarmos a
listagem com o mesmo composto (o oxalacetato) evidencia o caráter cíclico do processo. A diminuição do
número de carbonos nos passos isocitrato [6C] → α-cetoglutarato [5C] e α-cetoglutarato [5C] → succinilCoA [4C no resíduo de succinilo] explica-se pela libertação simultânea de CO2 (ver Equação 4 e Equação
5).
3-
A sintétase de succinil-CoA (Equação 6) existe na forma de duas isoenzimas. Uma das isoenzimas tem
maior especificidade para o ADP e a outra maior especificidade para o GDP mas, em ambos os casos, a
reação pode ser entendida como correspondendo à rotura de uma ligação “rica em energia” e formação de
outra ligação “rica em energia”. No sentido succinil-CoA → succinato rompe-se uma ligação tioéster e
forma-se uma ligação anidrido entre os fosfato β e γ; num dos casos do ATP e no outro do GTP. No
1
A desidrogénase do succinato é, entre as enzimas “do ciclo de Krebs”, a única que está na membrana interna da
mitocôndria. Sendo constituída por várias subunidades é também conhecida como complexo II. O FAD não é o aceitador
último dos eletrões no processo catalisado pela desidrogénase do succinato mas sim o grupo prostético que aceita
diretamente os eletrões (ou os “hidrogénios”) quando o succinato se oxida. Nas células, o aceitador último dos eletrões na
ação catalítica da desidrogénase do succinato é a ubiquinona (ou coenzima Q) mas, tradicionalmente, quando se discute o
ciclo de Krebs, aponta-se o FAD como o oxidante do succinato. Curiosamente, quando se discute o papel catalítico da
desidrogénase do succinato no contexto do estudo da fosforilação oxidativa já é a ubiquinona que é, tradicionalmente,
apontado como o oxidante. Uma visão global da atividade catalítica da enzima permite compreender que a redução da
ubiquinona (a ubiquinol) pelo FADH2 também faz parte da sua atividade global e que a esta é melhor expressa pela equação
seguinte:
succinato + ubiquinona (ou coenzima Q) → fumarato + ubiquinol (ou coenzima QH2).
Estas idissincrasias têm origem na história da investigação da desidrogénase do succinato e das vias metabólicas onde pode
ser integrada.
Página 1 de 5
Ciclo de Krebs ou do ácido cítrico; Rui Fontes
entanto, em última análise, se também considerarmos a atividade da cínase dos nucleosídeos-difosfatos
(ver Equação 10) pode admitir-se que, na célula, o que se forma é ATP. Esta cínase não é, tradicionalmente,
considerada uma enzima do ciclo de Krebs, mas tem um papel importante neste contexto já que permite a
transferência do fosfato terminal do GTP (formado pela ação de uma das isoenzimas da sintétase do
succinil-CoA) para o ADP e, consequentemente, a formação de ATP. Assim, mesmo que se admita que,
num dado órgão, a isoenzima com maior atividade seja, a que tem maior afinidade para o GDP, o somatório
da sua atividade (ver Equação 6; com GDP como substrato) com a da cínase dos nucleosídeos difosfatos
(ver Equação 10) é a Equação 11. Por contraponto com a formação de ATP na fosforilação oxidativa, a
fosforilação do ADP (catalisada pela isoenzima que tem como substrato o ADP ou pelo somatório das duas
atividades atrás referidas) diz-se que ocorre “ao nível do substrato”.
Equação 10
Equação 11
GTP + ADP ↔ GDP + ATP
succinil-CoA + ADP + Pi ↔ succinato + CoA + ATP
4-
A fase preparatória da oxidação do grupo acetilo da acetil-CoA a CO2 começa com a sua ligação ao
oxalacetato por ação da síntase do citrato. Os passos oxidativos em que ocorre a redução do NAD+ e do
FAD são os catalisados pelas desidrogénases do isocitrato, do α-cetoglutarato, do malato (NAD+ a
NADH) e do succinato (FAD a FADH2). O NAD+ existe nas células em concentrações de ordem μM e a
oxidação da glicose, dos ácidos gordos e dos aminoácidos (que são ingeridos em quantidades de alguns
moles por dia) só pode ocorrer se o NADH formado aquando das reações expressas pela Equações 4, 5 e 9
for imediatamente reoxidado a NAD+. Algo de muito semelhante pode ser dito do FAD com a
particularidade de o FAD ser um dos grupos prostéticos da desidrogénase do succinato (ver nota de rodapé
nº 1). A regeneração do NAD+ e do FAD é indispensável para que o processo oxidativo possa prosseguir e,
na mitocôndria, o único processo que permite reoxidar o NADH e o FADH2 é desempenhado pelos
complexos da cadeia respiratória sendo que o oxidante final é o O2: ao contrário do que acontece no caso da
glicólise não existe “ciclo de Krebs anaeróbio”. As descarboxilações (libertação de CO2) ocorrem durante
as ações catalíticas da desidrogénase do isocitrato (ver Equação 4) e da desidrogénase do α-cetoglutarato
(ver Equação 5) e, tal como no caso da desidrogénase do piruvato (ver Equação 1), as reações que estas
duas desidrogénases catalisam são frequentemente referidas como oxidações-descarboxilativas. Juntamente
com a desidrogénase do piruvato, as desidrogénases do isocitrato e do α-cetoglutarato são responsáveis pela
esmagadora maioria das moléculas de CO2 que os animais produzem.
5-
A Equação 12 descreve o somatório das reações que constituem o ciclo de Krebs (Equações 2-9) e a
catalisada pela cínase dos nucleosídeos-difosfatos (Equação 10):
Equação 12
CH3CO-CoA + 2 H2O + 3 NAD+ + FAD + ADP + Pi →
2 CO2 + CoA + 3 NADH + FADH2 + ATP
Esta equação mostra que, conceptualmente, a ação do conjunto das enzimas referidas pode ser entendida
como um somatório de três processos: (12a) a hidrólise da acetil-CoA, (12b) a oxidação do resíduo de
acetato a CO2 com a concomitante redução do FAD e do NAD+ e (12c) a síntese de ATP (a partir de ADP +
Pi).
Equação 12a
Equação 12b
Equação 12c
CH3CO-CoA + H2O → CoA + CH3COOH
CH3COOH + 2 H2O + 3 NAD+ + FAD → 2 CO2 + 3 NADH + FADH2
ADP + Pi → ATP + H2O
Os processos 12a e 12b são exergónicos enquanto o 12c é endergónico e só ocorre porque está acoplado
com os dois primeiros. Vistos como um todo, o somatório das reações é, obviamente, um processo
exergónico; de contrário, a reação expressa pela Equação 12 não poderia ocorrer no sentido indicado.
6-
Em todos os tecidos e, particularmente, nos músculos, o principal papel das enzimas do ciclo de Krebs é, tal
como indica a Equação 12, catalisar a oxidação completa do resíduo acetilo do acetil-CoA formado durante
o catabolismo da glicose, ácidos gordos e aminoácidos. Nas reações em que intervêm catalisadores, porque
estes não se consomem nem se formam durante o processo reativo, o catalisador não aparece na equação
final. O mesmo acontece no caso dos intermediários do ciclo de Krebs: quando se somam as equações que
expressam a atividade de cada uma das enzimas os intermediários desaparecem da equação. Em cada uma
das reações um intermediário converte-se no seguinte e o “último” (o oxalacetato) converte-se no
“primeiro” (o citrato). Por isso, não é de estranhar que seja costume dizer-se que, no processo de oxidação
do grupo acetilo da acetil-CoA, os intermediários do ciclo de Krebs têm um papel catalítico.
Página 2 de 5
Ciclo de Krebs ou do ácido cítrico; Rui Fontes
7-
Nos músculos, a velocidade com que ocorrem as reações catalisadas pelas enzimas do ciclo de Krebs é
proporcional à despesa energética: a velocidade com que ocorrem as reações do ciclo de Krebs (a
oxidação do acetil-CoA a CO2) aumenta quando, como acontece durante o exercício físico, aumenta a
velocidade de hidrólise do ATP. As enzimas que catalisam reações fisiologicamente irreversíveis são as
catalisadas pela síntase do citrato e pelas desidrogénases do isocitrato e do α-cetoglutarato. Estas
enzimas são, in vitro, inibidas pelo ATP e estimuladas pelo ADP; dado que o esforço muscular implica
aumento da velocidade da hidrólise do ATP (atividade das ATPases da actina-miosina, do Ca2+ e do
Na+/K+) pensou-se durante muito tempo que ocorria diminuição da concentração de ATP e aumento da de
ADP durante o trabalho muscular e que essas variações de concentração fossem a causa direta da ativação
destas enzimas e do ciclo de Krebs no seu conjunto. Contudo, in vivo, as variações de concentração do ATP
(mesmo quando o trabalho muscular é violento) são praticamente nulas e as do ADP são muito modestas;
por isso crê-se, atualmente, que o marcado aumento da atividade das enzimas do ciclo de Krebs e o
consequente aumento de produção de CO2 durante o esforço muscular só, em parte, pode ser causado pelo
aumento do ADP. Pensa-se atualmente que um dos fatores responsáveis pelo aumento da produção de CO2
durante o esforço poderá ser o ião Ca2+ que estimula as desidrogénases do isocitrato e do αcetoglutarato (ativação alostérica) e cuja concentração aumenta na célula (citoplasma e mitocôndria)
durante a atividade contráctil do músculo [2].
8-
É de notar que a acetil-CoA não estimula a atividade das enzimas do ciclo de Krebs; ou seja, não é de
esperar que a ingestão aumentada de glicose ou ácidos gordos leve, por si só, a um aumento da oxidação da
acetil-CoA formada a partir dos nutrientes. Os sistemas oxidativos e, em particular, o ciclo de Krebs têm
velocidades que permitem manter a concentração de ATP estacionária: só é possível aumentar a velocidade
de oxidação da acetil-CoA (e, em última análise, a da oxidação dos nutrientes) se aumentar a velocidade de
hidrólise do ATP. Ou seja, a velocidade de oxidação dos nutrientes aumenta quando um animal faz
exercício físico mas aumentar a ingestão de nutrientes não aumenta a velocidade da sua oxidação2.
9-
Para além do papel central no processo oxidativo dos nutrientes (catabolismo) as enzimas do ciclo de Krebs
também participam noutros processos metabólicos que podem ser vistos como anabólicos. Por isso se
costuma dizer que o ciclo de Krebs tem caráter anfibólico: os intermediários deste ciclo são intermediários
no catabolismo dos nutrientes mas também podem ser intermediários em processos anabólicos, como a
síntese de ácidos gordos a partir de glicose (lipogénese), a síntese de glicose (gliconeogénese) ou de
glicerol-3-P (gliceroneogénese) a partir de aminoácidos ou de lactato, a síntese de alguns aminoácidos a
partir de glicose assim como a síntese do heme da hemoglobina e de outras proteínas hemínicas. O papel
anabólico das enzimas do ciclo de Krebs tem particular relevância nos casos do fígado, rim e tecido
adiposo.
10- Quando um intermediário do ciclo de Krebs é convertido num outro composto que não o é, diz-se que
o processo é cataplerótico [3, 4]. As reações catapleróticas tenderiam a “esvaziar” o ciclo de Krebs, mas
um processo cataplerótico não pode ocorrer sem que, a uma velocidade semelhante, um outro composto
que não é intermediário do ciclo de Krebs origine um intermediário do ciclo. Os processos deste último
tipo chamam-se anapleróticos. É uma boa aproximação à realidade afirmar-se que os intermediários do
ciclo de Krebs mantêm concentrações estacionárias; em diferentes estados metabólicos, ou mesmo quando
um músculo passa do estado de repouso para o de trabalho mecânico, as concentrações dos intermediários
do ciclo de Krebs variam muito pouco [3-6].
11- Quando a glicemia desce depois de terminado o processo absortivo de uma refeição que continha glicose, o
fígado (e o rim) forma glicose usando oxalacetato do citoplasma ou da mitocôndria como percursores e ao
processo chama-se gliconeogénese. A reação em que o oxalacetato se consome na gliconeogénese é
catalisada pela carboxicínase do fosfoenolpiruvato de que existem duas isoenzimas, uma citoplasmática e
outra mitocondrial; em ambos os casos o oxalacetato converte-se em fosfoenolpiruvato (ver Equação 13). A
quantidade total de oxalacetato num homem é de alguns miligramas mas, na gliconeogénese, pode formarse cerca de 100 g de glicose por dia [7]. O consumo de oxalacetato citoplasmático é possível porque o
oxalacetato citoplasmático é formado a partir de malato (catálise pela desidrogénase do malato
citoplasmática: ver Equação 9) que saiu da mitocôndria. O consumo de oxalacetato mitocondrial
(intermediário do ciclo de Krebs) via ação catalítica da carboxicínase do fosfoenolpiruvato mitocondrial e a
transformação de malato mitocondrial (também intermediário do ciclo de Krebs) em oxalacetato
2
De facto, esta afirmação não é completamente verdadeira porque, quando se ingerem alimentos em excesso, ocorrem
fenómenos adaptativos que tendem a aumentar ligeiramente a velocidade de oxidação dos nutrientes. No entanto, é de
sublinhar que, num adulto, os nutrientes ingeridos que excedam os gastos energéticos de um dado indivíduo (nutrientes não
oxidados) acabam armazenados na forma de triacilgliceróis do tecido adiposo.
Página 3 de 5
Ciclo de Krebs ou do ácido cítrico; Rui Fontes
citoplasmático são processos catapleróticos. Estes processos catapleróticos só são sustentáveis porque
durante a gliconeogénese ocorrem simultaneamente processos anapleróticos que permitem formar
intermediários do ciclo de Krebs. Quando, num processo anaplerótico, se forma um qualquer intermediário
do ciclo de Krebs, esse intermediário pode, por ação das enzimas do ciclo de Krebs, substituir o malato ou o
oxalacetato mitocondriais que foram consumidos.
São exemplos de processos anapleróticos importantes durante a gliconeogénese:
(i) a conversão de lactato citoplasmático em oxalacetato mitocondrial [via ação sequenciada da
desidrogénase láctica (ver Equação 14), do transporte de piruvato para a mitocôndria e da ação da
carboxílase do piruvato (ver Equação 15)],
(ii) a conversão de glutamina, glutamato e outros aminoácidos em α-cetoglutarato mitocondrial e
(iii) a conversão de propionato em succinil-CoA mitocondrial.
Todas as substâncias que podem, direta ou indiretamente, ser substratos em processos anapleróticos dizemse também glicogénicas porque, no fígado e no rim, são substratos da gliconeogénese. Um exemplo de uma
reação anaplerótica é a catalisada pela desidrogénase do glutamato (ver Equação 16): nesta reação um
aminoácido (o glutamato) converte-se num intermediário do ciclo de Krebs (o α-cetoglutarato); o glutamato
é, por isso, um substrato da gliconeogénese.
Equação 13
Equação 14
Equação 15
Equação 16
oxalacetato + GTP → fosfoenolpiruvato + GDP + CO2
lactato + NAD+ → piruvato + NADH
piruvato + CO2 + ATP → oxalacetato + ADP + Pi
glutamato + NAD+ → α-cetoglutarato + NADH + NH4+
12- A acetil-CoA reage com um intermediário do ciclo de Krebs (o oxalacetato) formando citrato (síntase do
citrato: ver Equação 2). Nesta reação, ao contrário do que acontece no caso dos processos anapleróticos,
não há formação líquida de um intermediário do ciclo de Krebs a partir de um outro que o não é. A reação
catalisada pela síntase do citrato pode ser interpretada como a conversão de um intermediário do ciclo de
Krebs (o oxalacetato) noutro intermediário do ciclo de Krebs (o citrato): em termos líquidos não há nem
formação nem consumo dos intermediários do ciclo de Krebs entendidos como um todo. Por isto, a reação
catalisada pela síntase do citrato não é uma reação anaplerótica (nem cataplerótica). Por outro lado, a
conversão de acetil-CoA em oxalacetato via reversão da reação catalisada pela desidrogénase do piruvato (e
a subsequente carboxilação do piruvato a oxalacetato; ver Equação 15) também não é possível porque a
reação catalisada pela desidrogénase do piruvato é fisiologicamente irreversível (ver Equação 1). A acetilCoA não pode, por estes motivos, ser considerada um substrato da gliconeogénese3.
13- A esmagadora maioria dos ácidos gordos, quer os da dieta quer os que fazem parte da estrutura dos lipídeos
dos seres vivos, contém um número par de carbonos. Estes ácidos gordos geram, no seu catabolismo,
apenas acetil-CoA e não podem, portanto, contribuir para a formação de glicose: os ácidos gordos de
cadeia par não são glicogénicos. Pelo contrário, a glicose pode dar origem a ácidos gordos cuja síntese
ocorre no citoplasma partindo de acetil-CoA (lipogénese). A acetil-CoA excedentária relativamente às
necessidades energéticas da célula não pode ser oxidada a CO2 no ciclo de Krebs mas pode, pelo menos no
fígado e no tecido adiposo, ser convertida em ácidos gordos no citoplasma das células. No entanto, a acetilCoA não pode atravessar a membrana mitocondrial porque não existe transportador para esta substância. O
mecanismo que permite, de forma indireta, transportar acetil-CoA para o citoplasma é complexo e envolve
as atividades catalíticas da síntase do citrato dentro da mitocôndria (ver Equação 2), do transportador
para o citrato existente na membrana interna da mitocôndria (ver Equação 17) e, já no citoplasma, da líase
do ATP-citrato (ver Equação 18).
Equação 17
Equação 18
citrato mitocondrial → citrato citoplasmático
ATP + citrato + CoA → oxalacetato + ADP + Pi + acetil-CoA
O somatório das Equações 2, 17 e 18 (ver Equação 19) mostra que o transporte de acetil-CoA ocorre à custa
do gasto de uma “ligação rica em energia” do ATP:
3
Do mesmo modo, também as substâncias que geram apenas acetil-CoA no seu catabolismo também não são substratos da
gliconeogénese e, portanto, não geram glicose no organismo.
Página 4 de 5
Ciclo de Krebs ou do ácido cítrico; Rui Fontes
Equação 19
acetil-CoA (mit.) + oxalacetato (mit.) + ATP + H2O →
acetil-CoA (cit.) + oxalacetato (cit.) + ADP + Pi
O processo descrito pela Equação 19 é um processo cataplerótico e, na membrana interna da mitocôndria,
não existe transportador para o oxalacetato. Assim, o regresso do oxalacetato citoplasmático à matriz
mitocondrial é indireto e uma das vias possíveis envolve a sua redução a malato no citoplasma (via
desidrogénase do malato; ver Equação 9) e o transporte do malato formado para a mitocôndria.
14- Sendo o acetil-CoA citoplasmático um substrato para a formação endógena de ácidos gordos pode afirmarse que a fração da glicose ingerida que não é oxidada contribui para a formação dos triacilgliceróis que
formam as gotículas de gordura dos adipócitos e de outras células do organismo. No entanto, o contrário
não é verdadeiro: a maioria dos ácidos gordos que ingerimos são de cadeia par e, no seu catabolismo, geram
acetil-CoA que não pode converter-se em glicose.
1. Rustin, P., Bourgeron, T., Parfait, B., Chretien, D., Munnich, A. & Rotig, A. (1997) Inborn errors of the Krebs cycle: a group of
unusual mitochondrial diseases in human, Biochim Biophys Acta. 1361, 185-97.
2. Balaban, R. S. (2002) Cardiac energy metabolism homeostasis: role of cytosolic calcium, J Mol Cell Cardiol. 34, 1259-71.
3. Brunengraber, H. & Roe, C. R. (2006) Anaplerotic molecules: Current and future, J Inherit Metab Dis. 29, 327-31.
4. Owen, O. E., Kalhan, S. C. & Hanson, R. W. (2002) The key role of anaplerosis and cataplerosis for citric acid cycle function, J Biol
Chem. 277, 30409-12.
5. Brunengraber, H., Boutry, M. & Lowenstein, J. M. (1973) Fatty acid and 3- -hydroxysterol synthesis in the perfused rat liver.
Including measurements on the production of lactate, pyruvate, -hydroxy-butyrate, and acetoacetate by the fed liver, J Biol Chem. 248,
2656-69.
6. Sharma, N., Okere, I. C., Brunengraber, D. Z., McElfresh, T. A., King, K. L., Sterk, J. P., Huang, H., Chandler, M. P. & Stanley, W. C.
(2005) Regulation of pyruvate dehydrogenase activity and citric acid cycle intermediates during high cardiac power generation, J Physiol.
562, 593-603.
7. Bisschop, P. H., Pereira Arias, A. M., Ackermans, M. T., Endert, E., Pijl, H., Kuipers, F., Meijer, A. J., Sauerwein, H. P. & Romijn, J.
A. (2000) The effects of carbohydrate variation in isocaloric diets on glycogenolysis and gluconeogenesis in healthy men, J Clin
Endocrinol Metab. 85, 1963-7.
Página 5 de 5