Profa. Dra. Milena Araújo Tonon Corrêa
AS DROGAS E O
SISTEMA ENDÓCRINO
E METABÓLICO
O sistema endócrino é constituído por um grupo de órgãos (algumas
vezes referidos como glândulas de secreção interna) cuja função principal é
produzir e secretar hormônios diretamente no interior da corrente
sanguínea. Os hormônios atuam como mensageiros para coordenar
atividades de várias partes do corpo, função do tecido alvo.
GLANDULAS
(ORGÃOS)
SUBSTÂNCIAS
(HORMÔNIOS)
TECIDO ALVO
As glândulas endócrinas secretam substâncias particulares que provocam
no organismo funções biológicas de alta importância: os hormônios. As
principais glândulas endócrinas do organismo são o pâncreas, a tireóide, as
supra-renais, a hipófise e as gônadas
Alguns hormônios afetam somente um ou dois órgãos, enquanto
outros afetam todo o organismo.
Por exemplo, o hormônio estimulante da tireóide (TSH) é
produzida na hipófise e afeta apenas a tireóide.
Em contraste, o hormônio tireoidiano é produzido na tireóide,
mas afeta células de todo o organismo.A
insulina, produzida pelas células das ilhotas pancreáticas, afeta
o metabolismo da glicose, das proteínas e das gorduras em
todo o organismo.
Sistema endócrino:
• Hipotálamo,
• Hipófise ou Ptuitária,
• Tireóide,
• Paratireóide,
• Supra-Renais ou Adrenais,
• Pâncreas,
• Gonadas (Ovários e Testículos)
Os hormônios tróficos são hormônios que controlam outras glândulas e
são classificados em:
•Tireotrópicos: atuam sobre a tireóide.
•Adrenocorticotrópicos: atuam sobre o córtex da glândula adrenal
•Gonadotróficos: atuam sobre as gônadas masculinas e femininas.
•Somatotróficos: atuam no crescimento, promovendo o alongamento dos
ossos e estimulando a síntese de proteínas e o desenvolvimento da massa
muscular. Também eleva o consumo de gorduras e inibe a síntese de
insulina do pâncreas, aumentando a concentração de glicose no sangue.
Eixo hipotálamo-hipófise
As interações complexas entre o hipotálamo, a hipófise e as glândulas
endócrinas periféricas fornecem exemplos primorosos de regulação
integrada por retroalimentação. Anatomicamente a Hipófise é
constituída por dois órgãos associados: adeno-hipófise (hipófise
anterior) é a neurohipófise (hipófise posterior), sendo que o órgão
controlador dos dois órgãos é o hipotálamo. Este eixo é uma
importante ligação entre dois sistemas: nervoso e endócrino.
O hipotálamo atua como transdutor neuroendócrino, integrando sinais neurais
provenientes do cérebro e convertendo-os em mensagens químicas (em grande
parte, peptídeos) que regulam a secreção dos hormônios hipofisários.
Os
hormônios
hipofisários
alteram as atividades dos órgãos
endócrinos
periféricos.
O
controle hipotalâmico da adeno-
hipófise
secreção
ocorre
através
hipotalâmica
da
de
hormônios no sistema vascular
porta-hipotalâmico-hipofisário.
Existe uma conexão neural direta
entre o hipotálamo e a neuro-
hipófise
Eixo hipotálamo-hipófise
O hipotálamo está intimamente relacionado com a hipófise no
comando das atividades.
Localiza-se abaixo do tálamo, na região do diencéfalo.
Possui vias de ligação com todos os níveis do sistema límbico. Liga-se ao
Sistema Nervoso e ao Sistema Endócrino, controlando a maioria das
funções vegetativas, endócrinas, comportamentais e emocionais do corpo.
A hipófise é dividida em dois lados: o anterior (adenohipófise) e o
posterior (neurohipófise).
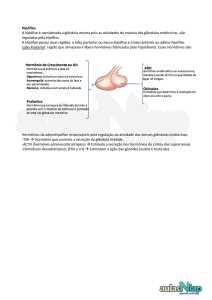
HORMÔNIOS DA HIPÓFISE E DO HIPOTÁLAMO
Os hormônios de liberação hipotalâmicos incluem:
Hormônio Liberador de Tireotropina (TRH),
Hormônio Liberador de Gonadotropina (GnRH),
Hormônio Liberador de Corticotropina (CRH),
Hormônio Liberador do Hormônio de Crescimento (GHRH),
Hormônio Inibidor do Hormônio do Crescimento (Somatostatina)
Fator Inibidor da Prolactina (PIF) - Dopamina.
A resposta da adeno-hipófise a um fator hipotalâmico é sinalizada através da
ligação do fator hipotalâmico a receptores específicos acoplados à proteína G, que
estão localizados na membrana plasmática do tipo celular apropriado da
adenohipófise. Esses receptores alteram, em sua maioria, os níveis intracelulares de
cAMP ou IP3 e de cálcio.
Os hormônios da hipófise posterior são também conhecidos como
hormônios neuro-hipofisários.
Ocitocina: principal h. estimulante da lactação e contração uterina. Promove
a ejeção do leite pela mama lactante, por estimular a contração das células
mioepiteliais que revestem os ductos mamários. Contração Uterina.
Estímulos para sua secreção: ato mamar, visão, som ou odor da criança,
dilatação da cérvice uterina.
Vasopressina(ADH) : h. antidiurético. Tem o papel de conservar a água
corporal e regular a tonicidade dos líquidos corporais. Tratamento da
diabetes insípido (síndrome clínica caracterizada pela incapacidade de
concentração do filtrado urinário, com consequente desenvolvimento de
urina hipotônica e aumento de volume urinário)
12
Os hormônios da hipófise anterior estimulam vários órgãos.
- Hôrmonio adenocorticotrófico (ACTH), corticotrofina- regula a
secreção de mais de 30 adrenocorticocosteróides. Hormônio
polipeptídio, cuja função é de regular o crescimento e a secreção do
córtex da supra-renal
- Hormônio lactogênio (PRL), prolactina – promove a secreção de leite.
Hormônio protéico participa na estimulação e desenvolvimento das
mamas e na produção do leite. Ocorre hiperplasia dos lactotrofos na
gravidez e lactação (resposta ao estrogênio). A prolactina inibe a
síntese e liberação GnRH (inibir a ovulação)
13
- Hormônio
do
crescimento
(GH),
somatotrofina
–
estimula
crescimento e regula muitos tecidos. Causa crescimento de todos os
tecidos capazes de crescer e promove o aumento do número de
células e o aumento das mesmas.
Efeitos do GH: Aumenta a síntese protéica em todas as células corporais, maior
mobilização de ácidos graxos a partir do tecido adiposo e sua maior utilização
para fins energéticos (lipolítico), redução da utilização da glicose em todo o
corpo, aumenta a reabsorção tubular de fosfato (aumentando a concentração
plasmática do fosfato), acelera a absorção de Cálcio pelo intestino, o GH induz a
produção hepática de diversas pequenas proteínas, somatomedinas, que agem
sobre as cartilagens e ossos promovendo o seu crescimento, o GH também
sensibiliza as gônadas ao LH e ao FSH e dessa forma promove a maturação sexual
puberal.
14
- Hormônio estimulante da tireóide (TSH), Tireotropina Glicoproteína cuja
função consiste em regular o crescimento e o metabolismo da tireóide e a
secreção de seus hormônios (Tiroxina:T4 e Triiodotironina:T3).
- Hormônio luteinizante (LH), lutrofina – estimula a ovulação promove a
secreção de progesterona e testosterona. Estimula as células intersticiais
ovarianas e as células de Leyding testiculares a secretarem testosterona e
outros produtos que desempenham papéis importantes na reprodução
- Hormônio folículo estimulante (FSH), folitrofina –Estimula as células da
granulosa ovariana e as células de Sertoli testiculares a sintetizarem e
secretarem estradiol e a diversos produtos protéicos essenciais a ovogênese
e a espermatogênese
15
HIPOTÁLAMO
HÍPÓFISE
GnRH( h. liberador de gonadotrofina) Hormônio
folículo-estimulante
(FSH):
estimula a formação do folículo de Graaf do ovário,
dos túbulos seminíferos do testículo e também
estimula a espermatogênes
TRH( h. liberador de tireotrofina)
Hormônio tirotrofina (TSH): estimula as
tireóides e a formação de tiroxina.
CRH( h. liberador de corticotrofina)
Hormônio adrenocorticotrópico (ACTH):
estimula a secreção dos hormônios córtico suprarenais.
GHRH( h. liberador de GH)
Hormônio somatotrofina (GH ou STH),
também denominado hormônio do crescimento:
atua sobre as cartilagens de crescimento dos ossos;
controla parte do metabolismo de gorduras,
proteínas e carboidratos
PRH( h. liberador de prolactina)
Hormônio prolactina: estabiliza a secreção do
estrogênio e progesterona e estimula a secreção de
leite
Fisiopatologia das doenças:
DISTÚRBIO NA HIPÓFISE
A hipófise controla muitas funções endócrinas, assim as patologias afetam
diversas funções orgânicas.
• Hipofunção da hipófise:
Motivo: lesão de massa-tumor, doença inflamatória (sarcoidose,) doença
infecciosa (tuberculose, sífiles), agressões físicas (traumas, cirurgia).
Tratamento: hormônio da tireoide, esteroides sexuais, glicocorticoides,
vasopressina e em alguns casos é preciso administrar também o hormônio
do crescimento.
Hiperprolactinemia:
As
ações
fisiológicas
da
prolactina
envolvem
a
regulação
do
desenvolvimento da glândula mamária e a biossíntese e secreção das
proteínas do leite. Ela é secretada pela adeno-hipófise. A síntese e a
secreção de prolactina na hipófise fetal começam durante as primeiras
semanas de gestação. Os níveis séricos de prolactina declinam logo após o
nascimento.
Enquanto os níveis séricos de prolactina permanecem baixos durante toda
a vida nos indivíduos normais do sexo masculino, apresentam-se
ligeiramente elevados nas mulheres com ciclos normais.
Os níveis de prolactina aumentam acentuadamente durante a gravidez,
atingem um valor máximo a termo e depois caem, a não ser que a mãe
amamente a criança.
Durante a lactação, a secreção de prolactina é estimulada pela sucção
ou pela manipulação da mama. Os níveis aumentados de prolactina
acabam suprimindo a síntese de estrógeno uma vez que a mesma
antagoniza a liberação de GnRH, como resultado há diminuição dos
hormônios LH e FSH, mecanismo este importante para inibir ovulação
da mulher enquanto estiver amamentando.
Fatores fisiológicos que influenciam a secreção de prolactina
assemelham-se aos que afetam a secreção de GH. Assim, o sono, o
estresse, a hipoglicemia, o exercício e o estrogênio aumentam a
secreção de ambos os hormônios.
A atividade das células lactrótoficas diminui em resposta à secreção
hipotalâmica de dopamina.
Hiperprolactinemia:
Motivo: compressão do tronco da hipófise (lesão de massa), estímulo físico
(amamentação), efeito hormonal (gravidez, terapia por estrogênios), drogas
(agentes antipsicóticos- antagonistas dopamina).
A dopamina inibe secreção de prolactina, assim agentes antipsicóticos que
inibem dopamina levam ao aumento de prolactina.
Prolactina em excesso é uma causa comum de infertilidade e galactorréia
Tratamento:
agonistas
dopaminérgicos
(Exemplos:
Cabergolina (Dostinex), Pergolida, Quinogolida.
Bromocriptina,
Anormalidade do eixo hormônio do crescimento - fator de crescimento:
O hormônio do crescimento é inicialmente expresso em altas concentrações
durante a puberdade; nessa ocasião, a secreção de hormônio do crescimento é
pulsátil, e os maiores pulsos são habitualmente observados à noite, durante o sono
A secreção de hormônio do
crescimento é intensificada
pelo GHRH e inibida pela
somatostatina.
A IGF1 é uma proteína produzida no fígado em resposta ao GH com papel importante no
crescimento, desenvolvimento da musculatura, reduz os níveis de glicose no sangue, reduz os
níveis de gordura corporal altera a oxidação lipídica e aumenta a síntese de proteínas
A incapacidade de secretar hormônio do crescimento ou de aumentar a
secreção de IGF-1 durante a puberdade resulta em retardo do
crescimento. A deficiência de hormônio do crescimento resulta mais
comumente da liberação hipotalâmica deficiente de GHRH ou de
insuficiência hipofisária.
Uma vez diagnosticado o retardo e a deficiência hormonal o tratamento
é em sua maioria por reposição hormonal através de hormônio de
crescimento
somatropina.
humano
recombinante
também
conhecido
como
A sermorrelina (GHRH sintético) pode ser administrada por via
parenteral para determinar a etiologia da doença. Se um paciente
apresenta uma liberação deficiente de GHRH pelo hipotálamo, porém
somatótrofos
da
adeno-hipófise
normalmente
funcionantes,
a
administração de GHRH exógeno resulta em liberação aumentada de GH.
Os casos de retardo do crescimento dependente de hormônio do
crescimento são tratados, em sua maioria, através de reposição com
hormônio do crescimento humano recombinante, designado pelo nome
genérico de somatropina. (Somatrem)
O IGF-1 recombinante, conhecido pelo nome genérico de mecasermina,
constitui um tratamento efetivo para pacientes com insensibilidade ao
hormônio do crescimento
- Deficiência H. Crescimento
Motivo: distúrbio comum que ocorre por motivos de genética (baixa
estatura familiar), condições endócrinas (deficiência do hormônio do
crescimento, resistência ao hormônio, síndromes genéticas)., doença
crônica, nanismo psicossocial, retardo intra-uterino do crescimento.
Tratamento : hormônio do crescimento recombinante humano - acelera o
crescimento esquelético linear, potencializa a mobilização de glicose e
ácido graxo, anabolismo em órgãos e tecidos moles.
Existem casos clínicos que resultam no excesso de hormônio do
crescimento.
Ocorre gigantismo quando o hormônio do crescimento é secretado em
níveis anormalmente altos antes do fechamento das epífise. O aumento dos
níveis de IGF-1 promove um crescimento longitudinal excessivo dos ossos.
A acromegalia ocorre quando o hormônio do crescimento é secretado em
níveis anormalmente alto após o fechamento das epífises. Neste caso
ocorre crescimento dos órgãos profundos e de extremidades.
O tratamento padrão para o adenoma de somatótrofos consiste na
remoção cirúrgica do tumor, porém será necessária terapia adjuvante que
pode ser com análogos da somatostatina, agonistas da dopamina e
antagonistas de receptores de GH.
- Excesso de hormônio crescimento (Acromegalia)
Hormônio do crescimento promove a síntese proteica e o crescimento
tecidual.
Motivo: distúrbio raro que ocorre principalmente devido a um adenoma na
hipófise.
Sinais e sintomas: em adultos ocorre o alargamento das extremidades
(mão, pé, queixo); e em crianças o gigantismo.
Tratamento: agonista de dopamina (inibe a secreção do hormônio do
crescimento)
DISTÚRBIO NA TIREOIDE
Situada na porção anterior do pescoço. A tireoide é regulada pelo
hormônio tireotrófico (TSH) da adeno-hipófise.
Os dois hormônios tireoidianos, tiroxina (T4) e triiodotironina (T3),
afetam a maioria dos órgãos, incluindo o coração, cérebro, fígado, rins e
pele, entre outros.
A regulação da secreção de hormônio tireoidiano pelo TSH está sob
controle por retroalimentação negativa (efeito feedback). O T3 e T4
circulantes agem na hipófise para diminuir a secreção de TSH; se os níveis
destes caírem, a secreção de TSH aumenta.
O T3 e T4 quando livres, e não as porções ligadas a proteínas regulam o
débito hipofisário de TSH.
A hipófise é capaz de desiodar T4 em T3, e este último age como efetor
final do bloqueio do TSH. Na circulação, a forma do hormônio em maior
quantidade é o T4, devido a sua menor velocidade de depuração
metabólica e renovação fracional em comparação à T3.
Distúrbio na tireoide
Hipertireoidismo
Com o funcionamento exagerado da tireoide, todo o metabolismo fica
acelerado. Levando ao batimento cardíaco acelerado, elevação da
temperatura do corporal, emagrecimento devido ao maior gasto calórico.
Esse quadro favorece o desenvolvimento de doenças cardíacas e
vasculares.
Causas: ingestão de hormônio, adenoma hiperfuncionante, tireoidite,
adenoma secretor de TSH, doença auto-imune (Graves- anticorpos ativam
receptores TSH)
Hipertireoidismo
Tratamento:
Metimazol e propiltiuracila - diminuem a produção do hormônio da tireoide
nos folículos tireoidianos.
Propiltiuracila também inibe formação de T3 a partir de T4.
Antagonistas B-adrenoceptores : antagonizam os efeitos dos hormônios nos
órgãos alvo. Exemplo: Propanolol, esmolol.
• Hipotireoidismo
O metabolismo se torna mais lento, algumas regiões do corpo ficam
inchadas, batimento cardíaco lento, o sangue circula mais lentamente,
menor gasto de energia, propensão à obesidade,.
Causas: destruição autoimune, inflamação, dano físico, deficiência de iodo,
doenças da hipófise.
Tratamento: levotiroxina sintética (1-T4); liotironina (hormonio sintético
da tireóide)
O pâncreas é um órgão glandular que contém tecido tanto exócrino
(apresenta um canal de excreção) quanto endócrino (lançados no sangue).
A porção exócrina — que constitui 99% da massa pancreática — secreta
bicarbonato e enzimas digestivas no trato gastrintestinal (GI).
Espalhadas dentro do tecido exócrino encontram-se pequenas ilhas de
tecido endócrino (ilhotas de Langerhans) que secretam hormônios
(glucagon, insulina, somatostatina, gastrina, polipeptídeo
pancreático)
diretamente no sangue e cujo número atinge quase um milhão.
A insulina promove a captação e o armazenamento da glicose e de outras
pequenas moléculas que contêm energia. Os hormônios “contrareguladores” — glucagon, catecolaminas, glicocorticoides (cortisol da supra
renal) e hormônio do crescimento (da hipófise) — antagonizam a ação da
insulina.
A regulação do pâncreas endócrino não se dá pelo eixo hipotalâmico hipofisária, ao contrário, o metabolismo dos lipídeos e carboidratos é
regulado por:
• Sinais do intestino (liberados pela distensão gástrica e pelo conteúdo
alimentar)
• Sinais da corrente circulatória (níveis circulantes de glicose)
• Sinais intracelulares (acúmulos energéticos intracelulares)
O nível de glicemia é facilmente medido e proporciona uma orientação
acurada sobre o equilíbrio da insulina e dos hormônios contra-reguladores.
Esse equilíbrio normalmente mantém os níveis de glicose dentro de uma
faixa estreita (70–120 mg/dL), independentemente da ingestão recente de
alimentos.
A hipoglicemia é perigosa, visto que os órgãos do corpo — particularmente
o cérebro — dependem de um suprimento constante de glicose para o seu
funcionamento apropriado. Por outro lado, a hiperglicemia crônica é tóxica
para numerosas células e tecidos.
A insulina é um hormônio produzido principalmente pela parte
endócrina do pâncreas (células de langerhans)
A estimulação dos receptores de insulina ativa os transportadores da
glicose na membrana plasmática de tecidos sensíveis a insulina, levando
a um aumento de absorção de glicose.
O controle dos transportadores de glicose nos tecidos periféricos é
essencial para a liberação energética, ao passo que nas células B
pancreáticas esse controle é essencial para o mecanismo de percepção
de glicose, que controla a liberação de insulina.
A liberação de insulina ocorre em resposta a um estímulo dependente de
alimento (glicose, aminoácido, hormônios do intestino).
Assim ocorre uma despolarização das células B pancreáticas (ilhotas de
Langerhans) e medeiam a exocitose mediada por Ca+2 da insulina para a
veia porta.
O potencial de repouso da membrana das células B é regulado por um
canal de potássio sensível a ATP. A inibição desse canal de K+ resulta na
despolarização e ativa canal de Ca+2 e libera mais insulina.
A glicose entra na célula B por difusão facilitada, é
metabolizada, produz ATP que inibe canal de K+ que ativa
Ca+2 e estimula a liberação de insulina.
A insulina estimula as células do fígado e dos músculos a
armazenar glicose em forma de glicogênio; estimula as células
adiposas a formar gorduras a partir de ácidos graxos e glicerol;
estimula as células do fígado e dos músculos a fazer proteínas a
partir de aminoácidos;
Quando está em jejum, o pâncreas libera glucagon para que seu
corpo possa produzir glicose. Este mobiliza glicose das reservas de
dentro do corpo e aumenta as concentrações de glicose na
corrente sanguínea.
Efeitos da insulina no metabolismo dos carboidratos:
• aumento no transporte de glicose através da membrana celular
• aumento na disponibilidade de glicose no líquido intracelular
• aumento na utilização de glicose pelas células
• aumento na glicogênese (polimerização de glicose, formando glicogênio),
principalmente no fígado e nos músculos •
aumento na transformação de glicose em gordura
Efeitos da insulina no metabolismo das proteínas:
• aumento no transporte de aminoácidos através da membrana celular
• maior disponibilidade de aminoácidos no líquido intracelular
• aumento na quantidade de RNA no líquido intracelular
• aumento na atividade dos ribossomas no interior das células
aumento na síntese protéica • redução na lise protéica
• aumento no crescimento
Efeitos da insulina no metabolismo das gorduras:
• aumento na transformação de glicose em gordura
• redução na mobilização de ácidos graxos dos tecidos adiposos
• redução na utilização de ácidos graxos pelas células
O glucagon é secretado pelas células alfa das ilhotas de Langerhans, é muito
importante principalmente para evitar que ocorra uma hipoglicemia acentuada
no organismo de uma pessoa. Quando a concentração de glicose no sangue
atinge valores baixos, as células alfa das ilhotas de Langerhans liberam uma
maior quantidade de glucagon. O glucagon, então, faz com que a glicose
sanguínea aumente e retorne aos valores aceitáveis como normal. Os principais
mecanismos através dos quais o glucagon faz aumentar a glicemia são:
• Aumento na glicogenólise (despolimerização do glicogênio armazenado nos
tecidos, liberando glicose para a circulação
• Aumento na gliconeogênese, através do qual elementos que não são
carboidratos (proteínas e glicerol) transformam-se em glicose
Diabetes melito tipo 1: agressão auto imune às células pancreáticas
(diabete melito juvenil). Ocasionado pela destruição da célula B do
pâncreas, em geral por decorrência de doença autoimune, levando a
deficiência absoluta de insulina.
Diabetes melito tipo 2: a insulina é secretada porém é ineficiente pra
normalizar a glicose plasmática. (resistência a insulina)
Diabetes na gravidez : os hormônios liberados durante a gravidez
pela placenta podem reduzir a sensibilidade das suas células e torná-las
mais resistentes à insulina. Assim, o corpo exige mais insulina para
controlar os seus níveis de açúcar no sangue.
Tratamento
• Insulina de curta ação (regula), ação intermediária e prolongada.
Insulina humana NPH e insulina humana regular – insulina regular
ou cristalina, de ação rápida, está indicada em cetoacidose,
gravidez e trabalho de parto, situações de emergência, em
combinação com insulinas de ação média ou prolongada, em bombas
de infusão subcutânea e em tratamento tipo bolo antes das
refeições.
A insulina isófana (NPH), de ação média, é usada em tratamento
de manutenção para controle glicêmico basal. As insulinas de
ação intermediária e prolongadas possuem uma manifestação mais
gradual devido a adição de um tampão, que altera a solubilidade
(lenta) ou adição de protamina às suspensões de insulina em Zn+2.
As insulinas de ação prolongada possuem o tampão e a suspensão
em Zn+2 para retardar ainda mais a absorção.
• Antidiabéticos orais:
Metformina (biguanida) constitui a primeira escolha no tratamento de
diabetes tipo 2 (resistência a insulina).
Esta aumenta os transportadores de glicose, aumenta a sensibilidade dos
tecidos a insulina, inibe gliconeogênese.
Vantagens: não causa ganho de peso, não causa hipoglicemia,
Glibenclamida e glicazina (sulfonilureias):
Estimulam liberação de insulina pelo pâncreas.
Bloqueia canais dependentes de K+
Efeito colateral: hipoglicemia
Repaglinida:
Estimulam liberação de insulina pelo pâncreas.
Bloqueia canais dependentes de K+
Efeito colateral: hipoglicemia
DISTÚRBIO DO METABOLISMO DOS LIPIDEOS
As hiperlipidemias são comuns e estão associadas com doenças
cardiovasculares (aumento LDL ou VLDL) .
As drogas redutoras de lipídeos atuam em múltiplas etapas da via
metabólica das lipoproteínas.
O tratamento inclui agentes que interferem na síntese do
colesterol, com as perdas de colesterol na bile e com o
metabolismo de LDL e VLDL.
As lipoproteínas se dividem segundo as suas dimensões e densidades
em:
lipoproteína de alta densidade (HDL);
lipoproteína de baixa densidade (LDL);
lipoproteína de densidade muito baixa (VLDL);
quilomicrons.
As lipoproteínas de maior interesse são a LDL, que transporta o
colesterol do fígado para os vasos sanguíneos e para o tecido adiposo
e muscular; e a HDL que é responsável pelo transporte de colesterol
dos tecidos periféricos de volta ao fígado.
TRATAMENTO:
Inibidores da HMG redutase
A HMG redutase libera ácido mevalônico que é um precursor do
colesterol. Desta forma as estatinas inibem etapas da via metabólica
das lipoproteínas. Reduzem o LDL e também o VLDL podendo
causar um pequeno aumento do HDL.
As estatinas possuem biodisponibilidade sistêmica limitada após
administração oral (metabolismo de 1ª passagem).
Ex pravastatina, fluvastatina, atorvastatina, cerivastatina.
A sinvastatina e a lovastatina são pró-fármacos.
Derivados do ácido fíbrico:
Ex gemfibrozil, fenofibrato, clofibrato
Esses potencializam a eliminação de VLDL. Os fibratos aumentam a
atividade da lipoproteína da lipase periférica e facilitam a transferência
dos ésteres de colesterol de VLDL para HDL (aumento HDL).
Niacina
Esta reduz o fluxo de ácidos graxos a partir do tecido adiposo. Reduz
produção de VLDL. Mecanismo pouco compreendido.
Resinas sequestradores dos ácidos biliares
Exemplos: colestiramina, colestipol, colesevelam
Essas inibem a reabsorção de ácidos biliares e combinados
com uma dieta mais pobre de colesterol podem ocasionar
concentrações plasmáticas menores de colesterol.
Ocorre assim um aumento da absorção hepática do colesterol do
sangue para compensar a síntese dos ácidos biliares do organismo.
Isso leva a uma diminuição de LDL.
EIXO HIPOTALÂMICO-HIPOFISÁRIO-SUPRARRENAL
Os neurônios do hipotálamo sintetizam e secretam o hormônio de liberação
da corticotropina (CRH).
O
CRH
estimula
a
síntese
e
a
liberação
do
hormônio
adrenocorticotrópico (ACTH). O ACTH é sintetizado como parte da
proopiomelanocortina (POMC), um polipeptídio precursor que é clivado em
múltiplas moléculas efetoras.
Além do ACTH, a clivagem da POMC produz : Hormônio melanócitoestimulante (MSH) (efeitos sobre a pigmentação da pele, o comportamento
alimentar e o peso corpora), a lipotropina e a endorfina.
Uma vez secretado, o ACTH liga-se a receptores de ACTH localizados
sobre células do córtex da supra-renal. O ACTH estimula a síntese e a
secreção
de
hormônios
esteróides
adrenocorticais, incluindo
glicocorticóides, androgênios e mineralocorticoides
Entre as células da adeno-hipófise, os gonadótrofos são singulares, uma
vez que secretam dois hormônios glicoprotéicos: o LH e o FSH. Esses
hormônios, em seu conjunto, são designados como gonadotropinas.
Uma vez secretadas, as gonadotropinas controlam a produção de
hormônios pelas gônadas, promovendo a síntese de androgênios e de
estrogênios. A seguir, os gonadótrofos são inibidos através de
retroalimentação pela testosterona e pelo estrogênio
As gonadotropinas estimulam o desenvolvimento do folículo.
O FSH é o principal hormônio que estimula a liberação de estrogênio.
O LH estimula a ovulação na metade do ciclo e constitui o principal
hormônio que controla a secreção subsequente de progesterona pelo corpo
lúteo.
O estrogênio controla a fase proliferativa do endométrio e exerce efeitos de
retroalimentação negativa sobre a adeno-hipófise.
A progesterona controla a fase secretária posterior e exerce efeitos de
retroalimentação negativa tanto no hipotálamo quanto na adeno-hipófise.
Se houver implantação de um óvulo fertilizado, o corpo lúteo continua
secretando progesterona. Após a implantação, a gonadotropina coriônica
humana (HCG) do córion toma-se importante, e, mais tarde, durante a
gravidez, a progesterona e outros hormônios são secretados pela placenta
SISTEMA REPRODUTOR
As adrenais e os testículos
produzem uma variedade de
compostos capazes de
estimular os receptores
androgênicos.
A diidrotestosterona e a
testosterona são os
principais exemplos de
hormônios que atuam nos
receptores androgênicos.
Andrógenos e anti-andrógenos
Andrógenos
Androstenodiona
Testosterona
(circulante)
Diidrotestoterona
(intracelular)
A glândula hipófise anterior secreta dois hormônios gonadotrópicos
principais: o hormônio folículo-estimulante (FSH) e o hormônio
luteinizante (LH). Ambos desempenham papéis importantes no
controle da função sexual masculina. O LH estimula as células
intersticiais de Leydig a produzirem testosterona.
A testosterona é responsável pelas características distintivas do corpo
masculino. Os testículos geralmente descem para o escroto durante os
últimos dois ou três meses de gravidez, quando estão secretando
quantidade adequada de testosterona.
Reposição com androgênios:
Reposição é indicada em casos de hipogonadismo masculino. A
reposição hormonal nesses pacientes melhora o desempenho físico, a
função sexual, o humor, a libido.
Em pacientes saudáveis, o emprego de altas doses de testosterona ou
andrógenos sintéticos produz pequeno aumento da massa muscular, mas
leva a um agravamento do perfil lipídico, humor agressivo.
A testosterona tem pouca biodisponibilidade em razão do metabolismo
hepático.
Devido a esse fator os análogos sintéticos são administrados através de
sistemas transdérmicos e formulações intramusculares.
Exemplos: enantato de testosterona, cipionato de testosterona,
proprionato de testosterona.
Cipionato de testosterona é um éster de testosterona que lhe confere
maior lipossolubilidade, permitindo que a solução oleosa seja
administrada por via intramuscular a cada 2 semanas em hipogonadismo
masculino.
Terapia com antiandrogênios e antagonistas de androgênos:
Hirsutismo, alopécia, acne, puberdade precoce em homens, tumores de
próstata benignos
Exemplos:
Finasterida: inibidor da 5-redutase tipo II
Tratamento de hiperplasia benigna
Reduz 80% DHT na próstata
Dutastarida:
inibidor da 5-redutase tipos I e II
Tratamento de hiperplasia benigna
Espironolactona:
Reduz síntese de testosterona, utilizada em mulheres para tratar
hirsutismo
Cetoconazol: reduz síntese de testosterona
Acetato de Mergestrol: progestágeno com atividade antiandrogênica
Utilizado em pacientes com anorexia/ caquexia por câncer
Tratamento de câncer de mama metastático em mulheres pós-menopausa
Flutamida, Nilutamida, Bicalutamida: antagonistas não-esteroidais.
Adjuvantes no tratamento de câncer de próstata
SISTEMA REPRODUTOR
17β- Estradiol: principal
estrógeno ovariano
Estriol: principal
estrógeno placentário
Estrona: metabólito do
17β- Estradiol, estrógeno
ovariano e pósmenopausa
Progesterona:
17α, 20α 20 βhidroxiprogesteronas
Estrógenos e
Progestágenos
O hormônio liberador de gonadotropina hipotalâmica (GnRH)
estimula a liberação do hormônio luteinizante (LH) e o
folículo
estimulante (FSH).
O LH e o FSH estimulam a esteroidogênese gonadal e a conversão
dos androgênios adrenais em testosterona e estrogênios nas
gônadas.
A enzima aromatase, nas gônadas e no tecido adiposo, converte os
androgênios em estrogênios. .
O LH aumenta a produção de androgênio e de progesterona
O FSH aumenta a produção de estrogênio a partir dos androgênios
Gonadotropinas: LH e FSH
Farmacologia Humana, 2006
Dia
Etapa do ciclo menstrual
1
Primeiro dia da menstruação –
epitélio uterino é liberado
3-5
epitélio uterino é liberado
6-13
Fase folicular ou proliferativa
14
Ovulação
15-30 Fase lútea ou secretora
Observação
Durante essa fase, os folículos desenvolvemse e produzem estradiol, que induz
proliferação do endométrio
INÍCIO DA MENSTRUAÇÃO:
Enquanto o endométrio descama, o FSH é secretado em maior quantidade
pela hipófise , fazendo com que se desenvolvam os folículos ovarianos
Perto do 7º dia do ciclo, o FSH começa a diminuir e, com a falta desse
hormônio, alguns folículos param de crescer e morrem.
Durante seu crescimento, o folículo ovariano produz quantidades de
estradiol, cada vez maiores. Esse hormônio produz aumento da espessura do
endométrio, preparando-o para receber o embrião.
Quando a quantidade de estradiol atinge seu máximo, é estimulada a
liberação de grande quantidade de hormônio luteinizante (LH) pela hipófise.
Algumas horas após, ocorre a ovulação.
Após a ovulação, o folículo se transforma numa estrutura chamada corpo
lúteo, e passa a fabricar, além do estradiol, o hormônio progesterona, que
prepara do endométrio para a implantação do embrião.
Se a concentração deste hormônio no sangue for baixa, o endométrio pode
ser não receptivo ao embrião e não ocorre gravidez.
Se não ocorre implantação, a progesterona e o estradiol param de ser
fabricados pelo corpo lúteo, seu nível diminui no sangue e se inicia outra
menstruação.
71
Os estrogênios regulação: Trato reprodutor, pituitária, mamas
Mediação das características sexuais femininas na puberdade: trompas, útero,
vagina, genitália externa, deposição de gordura, crescimento, fechamento
epífises ósseas, síntese e secreção de prolactina
Auxiliam na manutenção da massa óssea, influenciam na coagulação
sanguínea, aumentam HDL, inibem antitrombina III e LDL. Retenção de H2O
e sal (edema), reduzem a motilidade intestinal
Progesterona: expressão do receptor é dependente de estrógeno
(útero)
Preparação para implantação do embrião no útero
Manutenção da gestação, inibe contração uterina
Reduz HDL e aumenta LDL
Aumenta excreção de H2O e sódio
Desenvolvimento da glândula mamária
A terapia com estrogênios é utilizada para:
• Repor a produção hormonal normal nos quadros de deficiência
• Suprir a produção endógena de hormônios (contraceptivos)
• Tratar outras condições responsivas aos hormônios
Agonistas:
Tratamento menopausa
Contracepção
Antagonistas:
Tratamento da infertilidade: aumento de FSH leva
à ovulação
Tratamento de câncer de mama
Indução da Ovulação: (aumento de FSH)
É bloqueador de receptor estrogênico central, aumentando a
produção e a secreção de hormônio folículo-estimulante (FSH).
Ex: Citrato Clomifeno. Pode causar ovulações múltiplas
Menopausa: (Terapia de Reposição)
Ex :Raloxifeno: agonista ósseo
Possui efeitos de anti-reabsorção em mulheres no período pósmenopausa (importante na terapia da osteoporose)
Quimioterapia para o Câncer:
Ex: Tamoxifeno – antagonista do estrogênio no tecido mamário.
Efetivo em 30-40% dos casos de câncer de mama
Inibição da ovulação
Pílula Combinada:
Estrogênio (etinil estradiol, mestranol) +
Progesterona (norgestrel, levonorgestrel) sintéticos
20-21 dias com intervalo de 7-8 dias
Sangramento por suspensão
Os
progestogênios
suprem
o
ciclo
menstrual
por
efeitos
hipotalâmicos e hipofisários.
Os progestogênios tornam o muco cervical inóspito para os
espermatozóides
Os estrogênios regulam positivamente os receptores da progesterona
e potencializam a sensibilidade aos progestogênios
Os estrogênios contribuem para a retroalimentação negativa no
hipotálamo e na hipófise
Efeitos Adversos (Dependentes da dose)
Cardiovasculares
Efeitos endócrinos e metabólicos, câncer de mama
Riscos Mínimos nas atuais formulações (baixas doses)
Cardiovascular: pacientes com hipertensão e diabetes
Risco de tromboembolia
Câncer: não
Náuseas, edema, cefaléia
Levonorgestrel é progestogênio usado em contracepção de
emergência, ou seja, de 72 a 120 horas pós-coito não protegido ou
com baixa proteção, para a prevenção de gravidez não desejada. O
método tem eficácia inconteste e segurança aceitável. Entre as
principais indicações está a relação sexual sem uso de método
anticoncepcional, falha conhecida ou presumida do método em uso de
rotina, uso inadequado de anticoncepção e abuso sexual59. Quando
apropriadamente iniciada, até 72 horas depois de coito não protegido, a
contracepção de emergência prevenirá 80% das gravidezes em jovens e
adultas que estão no período fértil e, assim, sob risco.
A contracepção injetável está indicada em mulheres que desejam
contracepção prolongada e não querem aderir à tomada diária do
anticoncepcional oral ou que apresentem problemas de absorção
entérica (doença inflamatória no intestino). Pode ser feita somente
com progestogênio isolado ou a combinação de
estrogênio e
progestogênio. Esta permite diminuição de alguns efeitos adversos das
preparações injetáveis apenas com progestogênio.
Pós-menopausa: 10% da produção de estrogênios,
progesterona
Sintomas: sintomas vasomotores (“ondas de calor”),
osteoporose, atrofia urogenital, distúrbios psicológicos
Terapia de Reposição Hormonal:
estrógeno + progestágeno
A contracepção que envolvem a associação dos hormônios estrógeno
e progesterona são responsáveis em suprimir a secreção de GnRH,
FSH e LH e o desenvolvimento folicular, isto faz com haja inibição da
ovulação.
A associação das drogas também podem inibir mecanismos
secundários da gravidez incluindo alterações no peristaltismo das
tubas, na receptividade endometrial e na secreção de muco cervical.
Essas últimas ações poderiam, em seu conjunto, inibir o transporte
apropriado do óvulo e dos espermatozóides, mesmo se tivesse
ocorrido a ovulação.
Os contraceptivos podem ter várias apresentações como tratamentos
intradermicos, composições orais e até mesmo sendo incluso no anel vaginal
para sua liberação.
Os esquemas clássicos de anticoncepcionais orais combinados consistem em
sua administração durante 21 dias, seguidos de 7 dias de pílula placebo.
O período de 7 dias com placebo remove a estimulação hormonal exógena,
simulando a involução fisiológica do corpo lúteo que ocorre no final de um
ciclo menstrual normal.
A ausência de estrógeno e de progestina induz a descamação do endométrio,
resultando em menstruação. Como a administração de progestina durante
todo o ciclo inibe o crescimento proliferativo do endométrio, a maioria das
mulheres tem períodos menstruais menos intensos