MATERIAIS MESOPOROSOS A BASE DE SÍLICA OBTIDOS PELO
MÉTODO SOL-GEL: BIODISPOSITIVO PARA TRATAMENTO DE
INFECÇÃO ÓSSEA
Gracielle F. Andrade 1,2*; Armando S. Cunha1; Edésia M. B. Sousa2
1 Faculdade de Farmácia - Universidade Federal de Minas Gerais – UFMG
2 Centro de Desenvolvimento da Tecnologia Nuclear – CDTN/CNEN. Rua Professor
Mário Werneck, s/n. Campus Universitário – Belo Horizonte – MG, CEP 30.123-970 Brazil.
E-mail: [email protected]
Resumo. Várias sínteses de materiais mesoporosos à base de sílica são realizadas com o
objetivo de desenvolver dispositivos para aplicação biológica, devido as suas propriedades
bioativas e a sua biocompatibilidade. Materiais mesoporosos ordenados possuem uma rede
de canais e poros de tamanho bem definido na escala nanométrica, com diversidade
estrutural desses poros, elevada área superficial (400 – 1000 m2.g-1) e tamanho de poros
usualmente em torno de 2 a 30 nm. Essa estrutura de poros torna esses materiais apropriados
para incorporar e liberar uma grande variedade de moléculas na sua matriz. Dentre os
diversos tipos de materiais ordenados, o SBA-16 é considerado uma mesoestrutura muito
interessante devido ao fato de possuir um ordenamento de mesoporos cúbico tridimensional e
morfologia esférica, podendo ser um material promissor para uma gama de aplicações.
Dentre essas aplicações podemos citar o uso desses materiais como sistemas de liberação de
fármaco e sistemas osteogênicos para uso em tratamento ósseo. A efetiva presença de grupos
silanóis nas paredes da sílica mesoporosas fornece características e possibilidades diversas a
esse material incluindo a bioatividade, podendo ser uma escolha interessante como matriz de
fármacos utilizada como dispositivo implantável em tecidos ósseos. Esse trabalho teve como
objetivo sintetizar, caracterizar e avaliar preliminarmente esse material como para
tratamento de infecção óssea. As características estruturais do SBA-16 foram avaliadas por
espalhamento de raio X a baixo ângulo, adsorção de N2 e microscopia eletrônica de
varredura, e as características químicas foram obtidas por espectroscopia na região do
infravermelho com transformada de Fourier, análise térmica e análise elementar CHN,
espectroscopia de correlação de fótons e análise de potencial zeta. Ensaios preliminares de
incorporação e liberação in vitro foram realizados utilizando o fármaco ciprofloxacino,
tendo como objetivo o uso desse sistema para tratamento de infecção óssea.
Palavras-chave: SBA-16, Materiais mesoporosos, Liberação de fármaco.
1.
INTRODUÇÃO
Materiais mesoporosos são sistemas altamente ordenados com elevada área
superficial, diâmetro de poros bem definidos e um ordenamento de poros a longo alcance. O
SBA-16 é uma sílica mesoporosa que apresenta estas características e uma estrutura cúbica
ordenada tridimensional [MESA, 2008]. Para obtenção destas estruturas diferenciadas,
utilizam-se surfactantes que agem como direcionadores de rede. Esses materiais com maior
versatilidade associada às suas novas propriedades apresentam um grande potencial de
aplicações, tais como catálise, imobilização de enzimas, adsorção de metais pesados,
confecção de sistemas de liberação controlada de fármaco, entre outras [XUE,2004;
RYOO,2005; LIU,2003].
As duas principais aplicações dos materiais à base de sílica em medicina são como
dispositivo para reparo de ossos e como sistema de liberação de fármaco. Tanto a estrutura
quanto a composição química promovem características finais e propriedades interessantes
para esse tipo de aplicação. A combinação adequada das técnicas de síntese e a utilização de
diversificados tipos de direcionadores conduzem a um material que reuni um comportamento
bioativo com a capacidade de transporte de moléculas, inclusive fármacos. Esses materiais
também podem ser excelentes candidatos para o desenvolvimento de dispositivos para
engenharia de tecidos. Portanto, uma área bastante promissora para esse tipo de material é a
engenharia de tecidos. A engenharia de tecidos combina os princípios de materiais e
transplantes de células para desenvolver tecidos substitutos e/ou promover a regeneração
endógena. De outra forma, engenharia de tecidos in vivo tem por objetivo recriar um ambiente
biológico favorável ao tratamento ou regeneração de tecidos promovidos por aqueles
elementos biológicos que são fornecidos pelo corpo [VALLET-REGÍ,2008; COSTA,2010;
RÁMILA,2003]
O objetivo principal desse trabalho foi sintetizar e caracterizar uma sílica mesoporosa
com nanoestrutura ordenada, do tipo SBA-16, e avaliar a potencialidade deste sistema como
biodispositivo de liberação de fármaco para tratamento ósseo.
2.
MATERIAIS E MÉTODOS
A preparação iniciou-se com a dissolução do surfactante F127 (poli [(etileno oxido)bloco-poli(propileno oxido)bloco-poli(etileno oxido)] (ALDRICH)) em uma mistura de água
destilada, ácido e butanol mantida sob agitação por 30 minutos. A esta solução foi adicionado
tetraetilortossilicato (TEOS, Sigma-Adrich) sob agitação a temperatura constante de 45 ºC,
por 1 hora. Após este período a mistura foi envelhecida a 100 ºC. O material resultante foi
filtrado e seco a 37 ºC. A remoção do surfactante foi feita por calcinação sob atmosfera de
nitrogênio a uma taxa de 5 ºC por minuto até a temperatura de 550 ºC.
Os materiais obtidos foram caracterizados por adsorção de gases (BET) - NOVA 2200
Quantacrome, espectroscopia no infravermelho (FTIR), análise térmica (TG) e análise
elementar (CHN), Espectroscopia de correlação de fótons e análise de Potencial Zeta,
Espalhamento de raios X a baixos ângulos (SAXS) e microscopia eletrônica de varredura
(MEV).
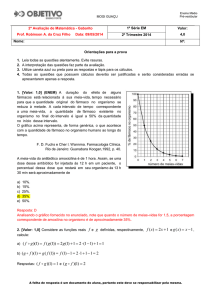
O fármaco do grupo das quinolonas denominado ciprofloxacino é um antibiótico de 2ª
geração desse grupo, Fig.1. Agentes à base de fluoroquinolonas tem sido cada vez mais
usados para tratamento de infecções no tecido ósseo. O ciprofloxacino apresenta um amplo
espectro de atividade antimicrobiana e uma boa penetração em muitos tecidos incluindo o
tecido ósseo. A concentração inibitória mínima da ciprofloxacino é baixa para Staphylococcus
aureus o qual é muito comum como patógeno em osteomielite. Ciprofloxacino também é
eficiente contra muitos microorganismos gram negativos, como as Enterobacteriaceas, que
são constantemente responsáveis por infecções ósseas, as quais requerem tratamento
prolongado com antibióticos [DÉSÉVAUXA, 2002; KAYSER, 1981]. Portanto, esse foi o
fármaco escolhido para o presente estudo.
Figura 1: Fórmula estrutural do fármaco Ciprofloxacino.
O processo de adsorção do fármaco ciprofloxacino na matriz do SBA-16 iniciou-se
com a adição de 100 mg da amostra em pó em uma solução do fármaco na concentração de
100 µg/mL, durante 48 horas, sob agitação, à temperatura média de 25°C. A solução de
ciprofloxacino foi submetida a uma variação de pH, para se obter a total solubilização do
fármaco. Inicialmente, o pH da solução foi reduzido a pH~2, utilizando ácido clorídrico 2M, e
posteriormente, foi elevado a pH~4, utilizando hidróxido de sódio 1M. O material final
incorporado com o fármaco foi denominado SBA-16-Cipro. Para os ensaios de liberação, as
amostras SBA-16-Cipro foram imersas em fluido corpóreo simulado (SBF) com pH~7,3, sob
agitação constante, e à temperatura média de 37 C. O perfil da liberação foi obtido medindose a concentração da droga em SBF, utilizando-se um espectrofotômetro na região de UV-Vis
(Shimadzu, UV-2550). A absorbância a 275 nm foi medida em intervalos de tempo de
aproximadamente 15 minutos no primeiro dia e em intervalos maiores nos demais.
3.
RESULTADOS E DISCUSSÃO
O espalhamento de raios X a baixo ângulo da amostra SBA-16 e SBA-16-Cipro está
representado no difratograma da Fig.2. O sinal de espalhamento correspondente ao plano
(hkl) de (110) está presente, correspondendo ao pico na região de 2θ entre 0,7 a 1,5º, com um
pico principal em torno de 2θ igual a 0,86°. Este sinal é característico de arranjo com simetria
tridimensional cúbica [ZHUY,2008]. É possível observar que após o processo de
incorporação o material mantém suas características estruturais, indicando que a presença do
fármaco não alterou o ordenamento da matriz.
SBA-16
SBA-16 cipro
Intensidade (u.a.)
(110)
1000
0,6
0,8
1,0
1,2
1,4
2 (Graus)
Figura 2: Espalhamento de raios X a baixo ângulo de SBA-16 e SBA-16 Cipro.
Os resultados das medidas de adsorção de N2 estão apresentados na Tab.1.
Material
SBA-16
SBA-16 Cipro
Tabela 1: Resultados da adsorção de nitrogênio.
Dp (nm)
SBET (m2/g)
Vp (cm³/g) x 10-³
3,6
3,6
499
500
405
415
As isotermas de adsorção de nitrogênio do SBA-16 e SBA-16-Cipro estão
apresentadas na Fig. 3. Essas isotermas apresentam histerese, fenômeno associado à presença
de mesoporos. Em ambos os casos, as isotermas são do tipo IV, características de materiais
mesoporosos e exibem histerese do tipo H2. Verifica-se que o perfil das isotermas não foi
alterado, preservando as características estruturais da matriz mesoporosa, mesmo após a
incorporação do fármaco. Uma análise qualitativa destas curvas indica que a quantidade de
fármaco incorporada foi relativamente baixa; o mesmo resultado pode ser percebido com os
dados da Tabela 1, uma vez que os valores da área superficial e do volume de nitrogênio
absorvido no SBA-16-Cipro não diferem da amostra pura.
260
3
-1
Volume Adsorvido (cm .g )
240
SBA-16
SBA-16
SBA-16 Cipro
SBA-16 Cipro
Desorçao
220
200
180
Adsorçao
160
140
120
0,2
0,4
0,6
0,8
1,0
P/P0
Figura 3: Isoterma de Adsorção de Nitrogênio de SBA-16 e SBA-16 cipro.
Na Fig. 4 estão apresentados os espectros de infravermelho das amostras pura e
incorporada com ciprofloxacino. Para ambas as amostras o espectro de infravermelho mostra
bandas de absorção referentes às vibrações fundamentais da rede de sílica, em torno de 460,
810, 960, 1080-1200, 3100-3700 cm-1. A banda entre 1080 e 1160 cm-1 é relativa ao
estiramento assimétrico das ligações Si-O-Si do SiO4. As bandas em 960 cm-1 e 1640 cm-1 são
atribuídas aos grupos silanóis existentes na estrutura do material. A banda em torno de 810
cm-1 é relativa ao estiramento simétrico da ligação Si-O-Si. A banda larga na região de 31003550 cm-1 relaciona-se ao grupo hidroxila da água e ao modo de vibração de deformação axial
de –OH do grupo Si-OH. No espectro do SBA-16-Cipro observa-se um estiramento
assimétrico da ligação CH em torno de 2900 cm-1 referente à cadeia de hidrocarbonetos do
fármaco incorporado. A banda em 1230 cm-1 é referente ao anel benzeno monofluorado. Essas
informações confirmam que existe uma incorporação do fármaco na matriz, embora os dados
estruturais da amostra SBA-16-Cipro obtidos por adsorção de N2 não indicaram tal resultado.
1,0
0,9
0,8
0,7
Transmitância (u.a.)
0,6
0,5
0,4
0,3
SBA-16 5.3
SBA-16 + Cipro 3
1,0
0,8
0,6
0,4
0,2
0,0
4000
Cipro
3500
3000
2500
2000
1500
1000
-1
Numero de onda (cm )
Figura 4: Espectro de FTIR do SBA-16 e SBA-16 cipro.
As curvas de TG do SBA-16 e SBA-16-cipro são apresentadas na Fig. 5. A perda de
massa no primeiro evento térmico das amostras, entre 25 e 150 ºC, é decorrente da dessorção
da água fisicamente adsorvida. Na amostra incorporada, observa-se uma maior perda de
massa entre 300 e 800 ºC que pode ser atribuída à degradação térmica do fármaco. Além desta
perda, pode se observar um ganho de massa entre 100-200°C. Esse evento pode ser atribuído
a alguma reação da sílica contendo o fármaco ciprofloxacino, com o meio, já que, a análise foi
realizada em atmosfera de nitrogênio.
Tabela 2: Perda de Massa em duas faixas de temperatura.
Amostra
Perda (% m/m)
Perda (% m/m)
Resíduos (%m/m)
25-150 ºC
300-800 ºC
>800 ºC
SBA-16
12,14
6,3
81,6
SBA-16 cipro
18,87
9,24
71,9
100
100
Ciprofloxacino
80
Perda de massa (%)
Perda de massa (%)
95
90
60
40
20
0
85
200
400
600
800
Temperatura (°C)
80
75
SBA-16
SBA-16 Cipro
200
400
600
800
Temperatura (°C)
Figura 5: Curva de TG do SBA-16 puro e SBA-16 cipro.
A microscopia eletrônica de varredura, Fig. 6, mostrou que o SBA-16 apresenta
partículas esféricas, resultado condizente com o descrito na literatura [ZHAO,2004]. Observase, porém, agregados de tamanhos variados, sugerindo que não há uniformidade de tamanho
das partículas obtidas.
Figura 6: Imagem de MEV SBA-16
Uma das evidências de que ocorreu a incorporação do fármaco ciprofloxacino na
amostra foi obtida pela técnica de análise elementar. Está técnica apontou o aumento na
variação das porcentagens do elemento carbono (C) na amostra em que ocorreu a
incorporação do fármaco. Na TAB. 3 encontram-se os valores desses elementos contidos na
amostra após incorporação. Os dados indicam que houve incorporação do ciprofloxacino na
estrutura do SBA-16. Entretanto, o percentual de carbono apresentado é muito baixo,
indicando uma pequena adsorção do fármaco. Vários fatores podem ser atribuídos a este
comportamento: a concentração inicial da solução de incorporação, o pH da solução, dentre
outros. Assim, para melhorar estes dados, estão sendo realizados estudos com algumas
alterações nas condições de incorporação.
Amostras
SBA-16
SBA16 cipro
100µg.mL-1
Tabela 3 – Porcentagem dos elementos C
C
%
mmol.g-1
0,01±0,015
0
1,14 ± 0,06
0,95
∆Cincor
mmol.g-1
0,95
∆Cincor = amostra antes de incorporar-amostra após incorporar
Com a técnica de espectroscopia de correlação de fótons foi possível avaliar o
tamanho médio das partículas de sílica, assim como, o seu índice de polidispersividade
(P.D.I), conforme apresentados na TAB. 4. O tamanho médio das partículas de SBA-16 se
encontra em torno de 1,2 µm. Entretanto, conforme percebido pelas imagens de MEV, a
variação do tamanho das partículas se apresenta em uma faixa relativamente larga, o que
reflete no índice de polidispersividade. O índice de polidispersividade (P.D.I) encontrado para
a amostra de SBA-16 foi de 0,46. Esse resultado indica que, embora o processo de sonicação
promova um sistema com uma razoável dispersividade, maiores investigações devem ser
feitas para melhorar a homogeneidade do tamanho das partículas.
Tabela 4- Espectroscopia de correlação de fóton e análise de potencial Zeta.
Tamanho médio
(nm)
Amostras
SBA-16
Índice de
Polidispersividade
ζ Potencial (mV)
0,46
-6,38
1284
O SBA-16 apresentou um potencial zeta negativo, com valor de -6,38 mV. O potencial
zeta pode indicar o comportamento das partículas nanoestruturas in vivo, no qual, a presença
de cargas minimizam os fenômenos de aglomeração e fusão.
Embora os dados de adsorção do fármaco tenham indicado uma baixa quantidade de
incorporação, a cinética de liberação in vitro de ciprofloxacino a partir do SBA-16 foi
estudada em função do tempo. A Fig. 7 mostra o perfil de liberação do fármaco
ciprofloxacino adsorvido na sílica mesoporosa. Esses resultados foram avaliados por um
modelo cinético matemático clássico, o modelo de Higuchi [SOUSA, 2006], onde se obtém
valores da taxa de liberação K, obtidos a partir da regressão linear dos dados de concentração
de ciprofloxacino liberada (ln Mt) em função do tempo ln (t). A análise mostra uma boa
correlação entre os dados, indicando que a liberação do fármaco ajusta-se ao mecanismo de
difusão, conforme Tab. 5.
Tabela 5- Parâmetros cinéticos
Amostras
K
SBA-16 Cipro
2,6
r2
0,98
24
22
% Massa Liberada
20
18
SBA-16 Cipro
16
14
12
10
8
6
0
500
1000
1500
2000
2500
3000
Tempo (min)
Figura 7: Perfil de liberação cumulativo de ciprofloxacino.
4.
CONCLUSÕES
A caracterização da sílica mesoporosa, SBA-16, foi realizada, assim como, essa matriz
após o processo de incorporação com o antibiótico ciprofloxacino. De acordo com as
informações fornecidas pelas análises de adsorção de nitrogênio, análise térmica (TG) e CHN
foi possível perceber que a quantidade de fármaco adsorvida na matriz de sílica foi muito
baixa. Essa baixa incorporação pode influenciar a velocidade e a quantidade de fármaco
liberada, podendo não ser satisfatória para o tratamento. Desta maneira, é necessário realizar
um estudo promovendo alterações para obter uma maior incorporação de ciprofloxacino no
material inorgânico. A modificação da superfície da sílica, a maior concentrações da solução
de incorporação do fármaco, a elevação da temperatura e a maior velocidade de agitação
durante o processo de incorporação são alternativas para se obter uma porcentagem de
incorporação mais elevada do fármaco. Ao analisar a cinética de liberação do fármaco foi
observada uma boa correlação entre os dados, indicando que a liberação do fármaco ajusta-se
ao mecanismo de difusão. Apesar da baixa incorporação os resultados indicaram que os
materiais mesoporosos apresentam potencialidade para serem utilizados como sistemas de
liberação de fármaco.
AGRADECIMENTOS: os autores agradecem o CNPq, CAPES e FAPEMIG pelo apoio
financeiro.
REFERÊNCIAS
1. COSTA, H. S., Síntese, caracterização e Avaliação do comportamento degradativo de híbridos porosos de
poli(álcool vinílico)/vidros bioativos, 2010, Teses de doutorado (Engenharia Metalúrgica e de Minas) –
Universidade Federal de Minas Gerais, Belo Horizonte, 2010.
2. DÉSÉVAUXA, C., et.al., Characterization of crosslinked high amylose starch matrix implants 2. In vivo
release of ciprofloxacin. Journal of Controlled Release, v. 82, p. 95–103, 2002.
3. KAYSER, F.H., EBERLE, H., Bacterial aspects of chronic post- traumatic osteomyelitis, in: J.G. van Rens,
F.H. Kayser (Eds.), Local Antibiotic Treatment in Osteomyelitis and Soft Tissue Infections, Excerpta Medica,
Amsterdam, pp 1–7, 1981.
4. LIU, Z. et al. Preparation of mesoporous MCM-41/poly(acrylic acid) composites using supercritical CO2 as a
solvent. Journal of Materials Chemistry, v. 13, p. 1373–1377, 2003.
5. MESA, M., SIERRA, L., GUTH, J.-L., Contribution to the study of the formation mechanism of mesoporous
SBA-15 and SBA-16 type silica particles in aqueous acid solutions, Microporous and Mesoporous Materials
v.112, p.338–350, 2008.
6. RÁMILA, A., MUÑOZ, B., PÉREZ-PARIENTE, J., VALLET-REGÍ, M.. Mesoporous MCM-41 as drug host
system. J. Sol-gel Sci. Techn. 26, 1199-1202. (2003).
7. RYOO, R. et al. Controlled polymerization in mesoporous silica toward the design of organic-inorganic
composite nanoporous materials. Journal of the American Chemical Society, v. 127, p. 1924-1932, 2005.
8. SOUSA, E. M. B. et.al., Funcionalization of mesoporous materials with long alkyl chains as a strategy for
controlling drug delivery pattern. Journal of Materials Chemistry, v. 16, p. 462-466, 2006.
9. VALLET-REGÍ, M. e BALAS, F. Silica Materials for Medical Applications The Open Biomedical
Engineering Journal, 2, 1-9, 2008.
10. XUE, J.M. & SHI, M. PLGA Mesoporous silica hybrid structure for controlled drug release. Journal of
Controlled Release, v. 98, p. 209 – 217, 2004.
11. ZHAO, D., et al. Synthesis and characterization of small pore thick-walled SBA-16 templated by oligomeric
surfactant with ultra-long hydrophilic chains, Microporous and Mesoporous Materials, v.67, p.135-141, 2004.
12. ZHU Y., et al. Highly Efficient VOx/SBA-16 Mesoporous Catalyst for Hydroxylation of Benzene Chin J
Catal, 29(11): 1067–1069, 2008.
MESOPOROUS MATERIALS BASED ON SILICA BY SOL-GEL :
DEVICE FOR BONE INFECTION TREATMENT
Gracielle F. Andrade 1,2*; Armando S. Cunha1; Edésia M. B. Sousa2
1 Faculdade de Farmácia - Universidade Federal de Minas Gerais – UFMG
2 Centro de Desenvolvimento da Tecnologia Nuclear – CDTN/CNEN. Rua Professor
Mário Werneck, s/n. Campus Universitário – Belo Horizonte – MG, CEP 30.123-970 Brazil.
E-mail: [email protected]
Abstract.Ordered mesoporous materials type SBA-16 have a cubic structure network of
channels and well defined pore size in nanometer scale. This porous structure makes these
materials appropriate to incorporate and release a large variety of molecules in the matrix and
it is considered a very interesting mesostructure due to the its 3D cubic arrangement of
mesopores corresponding to the Im3m space group, a promising material for a large range of
applications. In this work, mesoporous silica SBA-16 nanoparticles has been synthesized and
characterized by elemental analysis (CHN), Fourier Transform Infrared Spectroscopy (FTIR),
Nitrogen Adsorption, Scanning Electron Microscopy (SEM), Small Angle X Ray Scattering
(SAXS), Photon correlation spectroscopy and Zeta Potential analysis and Thermal Analysis.
The presence of the ciprofloxacin in the mesoporous material was confirmed by FTIR,
thermal analysis and CHN. The results obtained by SEM and SAXS for the samples reveal a
well-defined cubic arrangement of uniform spherical mesoporous structure, intrinsic
characteristic of these materials. The samples were charged with ciprofloxacin as a model
drug and in vitro release essays were carried out. The results indicated that SBA-16 would be
a potential to encapsulate bioactive molecules by utilizing ordered mesopores.
Keywords: SBA-16, mesoporous materials and drug delivery