e46
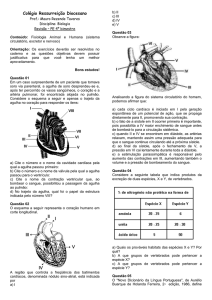
Nível das cristas ilíacas
Espaço intervertebral
de L3-L4
Técnica de Punção Lombar
Elizabeth Robbins
Stephen L. Hauser
EXAMES DE IMAGEM E ANÁLISES LABORATORIAIS ANTES DA PL
Os pacientes com alterações do nível de consciência, déficit neurológico focal, convulsão de início recente, papiledema ou imunossupressão encontram-se sob maior risco de desenvolver herniação cerebelar
ou tentorial potencialmente fatal depois da PL. Nesses casos, antes
da realização da PL, devem ser realizados exames neurológicos de
imagem para excluir lesão tumoral focal ou edema difuso. Os exames de imagens devem incluir a coluna vertebral dos pacientes com
sintomas sugestivos de compressão da medula espinal, inclusive dor
lombar, fraqueza dos membros inferiores, retenção urinária ou incontinência. Nos pacientes sob suspeita de meningite que precisarem
realizar exames neurológicos de imagem antes da PL com finalidade
diagnóstica, deverão ser administrados antibióticos antes dos exames, de preferência depois da coleta das amostras para hemocultura.
Os pacientes tratados com anticoagulantes ou que apresentam
distúrbios da coagulação (como trombocitopenia) também se encontram sob risco mais elevado de desenvolver hematomas subdurais ou
epidurais espinais depois da PL, podendo estas duas complicações
causar lesão das estruturas neurais e/ou paralisia irreversível. Se houver suspeita de distúrbio hemorrágico, a contagem das plaquetas, a
taxa normalizada internacional (INR) e o tempo de tromboplastina parcial deverão ser determinados antes da punção lombar. Hoje,
não existem dados disponíveis para avaliar a segurança da PL nos
pacientes com contagens das plaquetas baixas, mas as contagens <
20.000/L são consideradas contraindicações à PL. As complicações
hemorrágicas ocorrem raramente nos pacientes com contagens de
plaquetas ≥ 50.000/L e INR ≤ 1,5. Os pacientes tratados com heparina de baixo peso molecular têm risco aumentado de hematoma
epidural ou espinal depois da PL e as doses devem ser suspensas 24
horas antes do procedimento.
A PL não deve ser realizada na pele infectada porque os microrganismos podem ser introduzidos no espaço subaracnóideo (ESA).
ANALGESIA
A ansiedade e a dor podem ser atenuadas antes de iniciar o procedimento. A ansiedade é reduzida pela administração de 1 a 2 mg de
lorazepam* VO, 30 minutos antes do procedimento ou, por via IV, 5
minutos antes. A anestesia tópica pode ser conseguida pela aplicação
de um creme à base de lidocaína. A lidocaína a 4% é eficaz quando
aplicada 30 minutos antes do procedimento, enquanto a mistura de
lidocaína/prilocaína requer um intervalo de 60 a 120 minutos. O creme deve ser aplicado em uma camada espessa de forma a cobrir completamente a pele, sendo um curativo oclusivo aplicado para manter
o creme no local.
* N. de R.T.: No nosso meio, não existe lorazepan IV. Uma alternativa seria midazolan IV.
Figura e46.1 Posicionamento correto do paciente em decúbito lateral. Observe que os ombros e os quadris estão em um plano vertical e o dorso fica
perpendicular ao leito. (Segundo RP Simon et al. (eds.): Clinical Neurology, 7th ed.
New York, McGraw-Hill, 2009.)
POSICIONAMENTO
O posicionamento adequado do paciente é essencial. O procedimento deve ser efetuado em uma superfície firme e, se for necessário realizar a PL à beira do leito, o paciente deve ser posicionado na beira da
cama e não no meio. O paciente deve ser solicitado a deitar-se de lado
e de costas para o examinador, bem como a “enrolar-se como se fosse
uma bola”. O pescoço deve ser flexionado suavemente para frente e as
coxas devem ser puxadas na direção do abdome; os ombros e a pelve
devem ficar alinhados verticalmente, sem inclinação para frente ou
para trás (Fig. e46.1). A medula espinal termina em torno do nível
da vértebra L1 em 94% dos indivíduos. Nos casos restantes, o cone
da medula espinal estende-se até o espaço intervertebral de L2-L3.
Por essa razão, a PL deve ser realizada nesse espaço intervertebral
ou em L3-L4. Um parâmetro anatômico útil é uma linha traçada entre as cristas ilíacas posterossuperiores, que corresponde exatamente
ao nível do espaço intervertebral de L3-L4. O espaço intervertebral
é localizado depois da palpação suave para identificar os processos
espinhosos de cada vértebra.
Uma alternativa à posição de decúbito lateral é a posição sentada.
O paciente senta-se à beira do leito com os pés apoiados em uma
cadeira. Recebe instruções para flexionar o corpo para frente como
se tentasse tocar o umbigo com o nariz. É importante que o paciente
não se incline simplesmente para frente à beira do leito, pois esta não
é uma posição ideal para o afastamento dos processos espinhosos.
Em alguns casos, a PL dos pacientes obesos é realizada mais facilmente na posição sentada. Uma desvantagem dessa posição é que a
determinação da pressão de abertura pode não ser exata. Nos casos
em que a PL for difícil, tendo como base a palpação das marcas anatômicas, pode-se utilizar a ultrassonografia para orientar a introdução da agulha.
Técnica de Punção Lombar
Quando realizada por profissionais habilidosos, a punção lombar
(PL) geralmente é um procedimento seguro. As complicações significativas são extremamente raras, mas podem incluir herniação cerebral, lesão da medula espinal ou das raízes nervosas, hemorragia ou
infecção. As complicações brandas são mais comuns e podem incluir
dor lombar, cefaleia pós-PL e dor radicular ou dormência.
CAPÍTULO e46
CAPÍTULO
TÉCNICA
Quando o local desejado para a introdução da agulha está determinado, o examinador deve colocar luvas estéreis. Depois de limpar a pele
com iodo-povidona ou um desinfetante semelhante, a área deve ser
coberta com um campo estéril e o local escolhido para a introdução
da agulha deve ser enxugado com uma compressa de gaze estéril. A
desinfecção adequada da região reduz o risco de introduzir bactérias no ESA ou em outras estruturas. O anestésico local (geralmente
lidocaína a 1%, 3 a 5 mL no total) deve ser injetado no tecido subcutâneo – mas, nas situações que não constituem emergências, pode-se
aplicar um creme anestésico tópico (ver anteriormente). Quando há
tempo suficiente, a dor provocada pela injeção da lidocaína pode ser
atenuada pelas injeções repetidas e lentas, cada qual mais profunda
que a anterior, ao longo de um intervalo aproximado de 5 minutos.
Cerca de 0,5 a 1,0 mL da lidocaína é injetado de cada vez e geralmente a agulha não é retrocedida entre as injeções. Um intervalo de cerca
de 15 segundos entre as injeções ajuda a diminuir a dor da injeção
©2013, AMGH Editora Ltda. Todos os direitos reservados.
46-1
PARTE XVII
Distúrbios Neurológicos
46-2
subsequente. O objetivo é introduzir cada minidose do anestésico em
uma área já anestesiada pela injeção anterior. Cerca de 5 a 10 minidoses são injetadas, totalizando cerca de 5 mL de lidocaína.
Se for possível, a PL deverá ser postergada por 10 a 15 minutos
depois da conclusão das injeções do anestésico, porque isto reduz
significativamente e pode até eliminar a dor provocada pelo procedimento. Mesmo um intervalo de 5 minutos ajuda a atenuar a dor.
A agulha de PL (geralmente calibre 20 ou 22) é introduzida na
linha média a meia distância entre os processos espinhosos e é avançada lentamente. O bisel da agulha deve ser mantido em posição horizontal paralela à direção das fibras da dura-máter, com a porção
plana do bisel apontado para cima, o que reduz a lesão das fibras da
dura-máter à medida que são penetradas. Quando a punção lombar
é realizada nos pacientes sentados, o bisel deve ser mantido na posição vertical. Na maioria dos adultos, a agulha é avançada por 4 a 5
cm antes de atingir o ESA; o médico geralmente percebe que entrou
no espaço subdural pelo desaparecimento repentino da resistência
ou um estalido. Se não aparecer líquido apesar da posição aparentemente correta da agulha, esta poderá ser girada em 90 a 180o. Se
ainda assim não houver drenagem de líquido, o estilete deverá ser
reintroduzido e a agulha avançada ligeiramente. Alguns médicos interrompem momentaneamente a introdução da agulha para retirar
o estilete e verificar se há saída de líquido cerebrospinal (LCS). Se
não for possível avançar a agulha porque ela encontrou um osso, se o
paciente sentir dor aguda irradiada para uma das pernas, ou se não
aparecer líquido (punção seca), a agulha deverá ser retirada parcialmente e reintroduzida com um ângulo diferente. Se na segunda tentativa a agulha também encontrar um osso (indicando que não foi
introduzida exatamente entre os processos espinhosos), deverá ser
retirada por inteiro e o paciente deverá ser reposicionado. Em alguns
casos, a segunda tentativa é bem-sucedida quando o paciente retifica
completamente a coluna vertebral antes de ser reposicionado. Em seguida, a agulha poderá ser reintroduzida no mesmo nível ou em um
nível adjacente.
Quando o ESA é atingido, o manômetro deve ser fixado à agulha
para medir a pressão de abertura. O médico deve verificar se há oscilações normais da pressão do LCS com as pulsações e as respirações.
O limite superior normal da pressão de abertura dos pacientes em
posição supina é de 180 mm de H2O nos adultos, mas pode chegar a
200 a 250 mm de H2O nos indivíduos obesos.
O LCS deve ser deixado gotejar nos tubos de coleta e não deve ser
aspirado com uma seringa. Conforme a indicação clínica, o líquido
deve ser recolhido para realizar os seguintes exames: (1) contagem
diferencial das células; (2) concentrações das proteínas e glicose; (3)
cultura (bactérias, fungos, micobactérias e vírus); (4) esfregaços (p.
ex., Gram e álcool-ácido-resistente); (5) testes para antígenos (p. ex.,
aglutinação do látex); (6) reação em cadeia da polimerase (PCR) para
a amplificação do DNA ou RNA dos microrganismos (p. ex., herpesvírus simples, enterovírus); (7) dosagens dos anticorpos contra
microrganismos; (8) imunoeletroforese para a determinação do nível
das gamaglobulinas e distribuição oligoclonal; e (9) citologia. Embora 15 mL de LCS sejam suficientes para realizar todos os exames citados, a positividade das culturas para fungos e micobactérias aumenta
quando são utilizados volumes maiores. Em geral, 20 a 30 mL podem
ser retirados dos adultos sem acarretar riscos.
A punção sanguinolenta causada pela perfuração de um vaso
meníngeo (“punção traumática”) pode ser confundida com hemorragia subaracnóidea (HSA). Nesses casos, o espécime de LCS deve
ser centrifugado imediatamente depois da coleta; o sobrenadante
claro depois da centrifugação do LCS sugere o diagnóstico de punção traumática, enquanto o sobrenadante xantocrômico indica HSA.
Em geral, o LCS sanguinolento em razão da perfuração de um vaso
meníngeo clareia gradativamente nos tubos sucessivos, enquanto isto
não acontece com o sangue originado da HSA. Além da HSA, o LCS
xantocrômico também pode ser detectado nos pacientes com doença
hepática e quando a concentração proteica está acentuadamente elevada [> 1,5 a 2,0 g/L (150 a 200 mg/dL)].
Antes de retirar a agulha de PL, o estilete deve ser reintroduzido para evitar a possibilidade de aprisionamento de raiz nervosa na
dura-máter à medida que a agulha é removida; o aprisionamento
pode provocar o vazamento do LCS dural, que causa cefaleia. Alguns
médicos questionam a segurança dessa manobra, tendo em vista o
risco potencial de causar um acidente de pontada do estilete no profissional. Entretanto, esse tipo de acidente é improvável quando se
considera a flexibilidade do estilete fino, que tende a se dobrar em
vez de penetrar na pele com a qual entra em contato. Depois da PL, o
paciente geralmente deve ser colocado em uma posição confortável
de decúbito baixo por uma hora, antes de levantar-se, embora dados
recentes tenham sugerido que possa ser desnecessário ficar deitado
porque isso não parece afetar a incidência de cefaleia (ver adiante).
CEFALEIA PÓS-PL
Cefaleia é a complicação principal da PL e ocorre em 10 a 30% dos
pacientes. O risco dessa complicação aumenta nas faixas etárias mais
baixas e no sexo feminino. Em geral, a cefaleia pós-PL começa nas
primeiras 48 horas, mas pode demorar até 12 dias para iniciar. A dor
está significativamente relacionada com a posição do corpo, porque
começa quando o paciente fica sentado ou de pé e melhora quando se
deita ou aplica compressão abdominal. Quanto mais tempo o paciente ficar de pé, maior será o período de latência até que a cefaleia regrida. Em geral, a dor é difusa, mas pode ser pulsátil e sua localização
é occipitofrontal. Náuseas e rigidez da nuca frequentemente acompanham a cefaleia e, em alguns casos, os pacientes referem turvação
visual, fotofobia, tinido e vertigem. Em mais de 75% dos casos, os
sintomas regridem por completo dentro de uma semana, mas podem
persistir por semanas ou até meses em alguns poucos pacientes.
A cefaleia pós-PL é causada pela redução da pressão do LCS em
razão do extravasamento persistente pelo local onde a agulha penetrou no espaço subaracnóideo. A diminuição do volume do LCS
reduz o efeito de amortecimento e sustentação do cérebro, de forma que, quando o paciente está de pé, provavelmente há dilatação e
tensão das estruturas de ancoragem cerebral (seios durais sensíveis à
dor), que provocam dor. Embora a hipotensão intracraniana seja a
explicação habitual para a cefaleia pós-PL, esta síndrome pode ocorrer nos pacientes com pressão liquórica normal.
Como a cefaleia pós-PL geralmente regride sem tratamento específico, este consiste basicamente em medidas de sustentação como
analgésicos orais [acetaminofeno, anti-inflamatórios não esteroides,
opioides (Cap. 12)] e antieméticos. Os pacientes podem melhorar
quando são colocados em uma posição confortável (especialmente
em decúbito baixo ou na posição de Trendelenburg com a cabeça
para baixo). Alguns pacientes podem sentir alívio temporário da dor
quando ingerem cafeína.
Para os pacientes com dor persistente, o tratamento com cafeína
IV (500 mg em 500 mL de soro fisiológico administrados em 2 horas) pode ser eficaz, mas a fibrilação atrial é um efeito colateral raro.
Como alternativa, um remendo epidural de sangue pode ser aplicado por injeção de 15 mL de sangue total autólogo geralmente é
eficaz. Na maioria dos casos, esse procedimento é realizado por um
especialista em dor ou um anestesiologista. O remendo de sangue
produz efeitos imediatos e isto torna improvável que a vedação do
orifício dural pelo coágulo de sangue seja seu único mecanismo de
ação. A melhora imediata pode ser atribuída à compressão do espaço liquórico pelo coágulo, aumentando a pressão do LCS. Alguns
médicos reservam o remendo epidural de sangue para os pacientes
que não melhoram com a infusão de cafeína, enquanto outros preferem aplicá-lo como primeira medida terapêutica para os sintomas
persistentes pós-PL.
O Quadro e46.1 relaciona as estratégias indicadas para reduzir
a incidência da cefaleia pós-PL. A utilização de agulhas mais finas
está associada a um risco menor; em um estudo, o risco de cefaleia
depois da utilização da agulha convencional no 24 a 27 (Quinke) variou de 5 a 12%, em comparação com 20 a 40% quando foi utilizada
uma agulha no 20 ou 22. As agulhas mais finas geralmente exigem a
utilização de um introdutor e estão associadas à drenagem mais lenta do LCS. A utilização de uma agulha atraumática (de Sprotte, em
ponta de lápis ou não cortante) diminui a incidência das cefaleias mo-
©2013, AMGH Editora Ltda. Todos os direitos reservados.
QUADRO e46.1
Como reduzir a incidência de cefaleia pós-PL
QUADRO e46.2
Líquido cerebrospinal
Componente
Unidades do SI
Unidades convencionais
Utilizar agulha fina (no 22 ou menor)
Glicose
2,22 a 3,89 mmol/L
40 a 70 mg/dL
Utilizar agulha atraumática (de Sprotte ou outras)
Lactato
1 a 2 mmol/L
10 a 20 mg/dL
Recolocar o estilete antes de remover a agulha
Proteínas totais
Introduzir a agulha com o bisel orientado em direção cefalocaudal (quando
utilizar uma agulha convencional)
Lombar
0,15 a 0,5 g/L
15 a 50 mg/dL
Cisterna
0,15 a 0,25 g/L
15 a 25 mg/dL
Ventricular
Estratégias ineficazes
Albumina
IgG
Administração suplementar de líquidos
b
Redução do volume de LCS recolhido
Mobilização imediata depois da PL
deradas a graves, quando comparada com as agulhas convencionais
de PL (de Quinke ou traumáticas) (Fig. e46.2). Entretanto, como as
agulhas atraumáticas são mais difíceis de usar, podem ser necessárias
mais tentativas de punção eficaz, principalmente nos pacientes com
sobrepeso. Também pode ser necessário utilizar um introdutor com a
agulha atraumática, que não tem a ponta biselada cortante costumeira. Com as agulhas atraumáticas de Sprotte, há um risco pequeno de
quebra ou outros acidentes com o instrumento.
Outra estratégia usada para reduzir a incidência de cefaleia é recolocar o estilete antes de retirar a agulha de PL. Em geral, os pacientes são instruídos a permanecer na posição decúbito baixo por até
uma hora depois do procedimento. Contudo, os estudos que compararam a mobilização logo depois da PL com o repouso ao leito por
até 4 horas não mostraram diferenças significativas na incidência de
cefaleia, sugerindo que a prática rotineira de permanecer na posição
de decúbito depois da PL possa ser desnecessária.
RESULTADOS NORMAIS
(Ver Quadro e46.2.) No LCS sem infecção, a contagem normal dos
leucócitos é menor que 5 células mononucleares (linfócitos e monócitos) por L. Os leucócitos polimorfonucleares (PMN) não são
encontrados no LCS normal não centrifugado; contudo, alguns raros
PMN podem ser detectados nas amostras de LCS centrifugadas ou
concentradas, como as utilizadas para o exame citológico. As hemácias (eritrócitos) geralmente não estão presentes no LCS – mas, se
forem originadas de punção traumática, sua contagem diminui à medida que se recolhe mais LCS. As concentrações de glicose no LCS <
40 mg/dL (< 2,2 mmol/L) são anormais.
Figura e46.2 Comparação da agulha de PL tradicional (“traumática” ou
de Quinke) com a agulha “atraumática” (de Sprotte). A agulha “atraumática”
possui seu orifício na superfície, tendo este desenho o propósito de reduzir as chances de cortar as fibras da dura-máter que, depois da sua protrusão pelo orifício dural,
podem ser responsáveis pelo extravasamento subsequente do LCS e pela cefaleia
pós-PL. (Segundo SR Thomas et al.: BMJ 321:986, 2000.)
6 a 15 mg/dL
6,6 a 44,2 mg/dL
0,009 a 0,057 g/L
0,9 a 5,7 mg/dL
Índice de IgG
0,29 a 0,59
Bandas oligoclonais
< 2 bandas ausentes
na amostra de soro
pareada
Amônia
15 a 47 mol/L
Pressão do LCS
25 a 80 g/dL
50 a 180 mm de H2O
Volume do LCS
(adulto)
Cerca de 150 mL
Hemácias
0
Leucócitos Totais
0 a 5 células
mononucleares por
mm3
0
Técnica de Punção Lombar
Repouso ao leito (até 4 h) depois da PL
0,06 a 0,15 g/L
0,066 a 0,442 g/L
CAPÍTULO e46
Estratégias eficazes
Contagem
diferencial
Linfócitos
60 a 70%
Monócitos
30 a 50%
Neutrófilos
Nenhum
a
Como as concentrações no líquido cerebrospinal são valores determinados em equilíbrio, recomendam-se determinações dos mesmos parâmetros no plasma sanguíneo obtido na mesma
ocasião. Entretanto, há um intervalo até o estabelecimento do equilíbrio e os níveis cerebrospinal
dos constituintes plasmáticos, que podem oscilar rapidamente (como a glicose plasmática), podem não atingir patamares estáveis até depois de um intervalo expressivo.
b
Índice de IgG = IgG do LCS (mg/dL) X albumina sérica (g/dL)/IgG sérica (g/dL) X albumina do
LCS (mg/dL).
BIBLIOGRAFIA
Armon C, Evans RW: Addendum to assessment: Prevention of post-lumbar puncture headaches: Report of the Therapeutics and Technology
Assessment Subcommittee of the American Academy of Neurology. Neurology 65:510, 2005
Arendt K et al: Atraumatic lumbar puncture needles: After all these years, are
we still missing the point? Neurologist 15:17, 2009
Bezov D et al: Post-dural puncture headache: Part I diagnosis, epidemiology,
etiology, and pathophysiology. Headache 50:1144, 2010
Ellenby MS et al: Lumbar puncture (video). N Engl J Med 355:e12, 2006
Ferre RM, Sweeney TW: Emergency physicians can easily obtain ultrasound
images of anatomical landmarks relevant to lumbar puncture. Am J Emerg
Med 25:291, 2007
Lavi R et al: Standard vs atraumatic Whitacre needle for diagnostic lumbar
puncture: A randomized trial. Neurology 67:1492, 2006
Richman JM et al: Bevel direction and postdural puncture headache: A meta-analysis. Neurologist 12:224, 2006
Straus SE et al: How do I perform a lumbar puncture and analyze the results
to diagnose bacterial meningitis? JAMA 296:2012, 2006
Strupp M et al: Incidence of post-lumbar puncture syndrome reduced by
reinserting the stylet: A randomized prospective study of 600 patients. J
Neurol 245:589, 1998
Van Kooten F et al: Epidural blood patch in post dural puncture headache: A
randomized, observer-blind, controlled clinical trial. J Neurol Neurosurg
Psychiatry 79:553, 2008
©2013, AMGH Editora Ltda. Todos os direitos reservados.
46-3