1
Fundamentos da Termodinâmica
Objetivos:
• Definição de sistema e vizinhança
• Compreender o trabalho P-V
• Compreender processos reversíveis e irreversíveis
• Definir a primeira Lei da termodinâmica
• Cálculo de calor e trabalho
• Cálculo da energia interna
• Capacidades caloríficas a pressão constante e volume constante
• Efeito da temperatura na entalpia
2
3
Termodinâmica: Estudo a energia e
suas transformações
Sistem
a
aberto
Sistem
a
fechad
o
Sistem
a
isolado
4
Termodinâmica: Estudo a energia e
suas transformações
sistema
W, q
vizinhança
• O sistema e a vizinhança podem trocar calor e
trabalho alterando a energia interna do sistema e
da vizinhança.
•Calor e trabalho são “energia em movimento”
universo
• No entanto, a energia total do universo
permanece inalterada.
1a Lei da Termodinânica:
A energia não pode ser criada ou destruída
∆E = q + w
5
Termodinâmica
Convenção de sinais
+
Se w ou q entram no sistema, sinal
Se w ou q saem do sistema, sinal
+
+
-
6
Termodinâmica
Convenção de sinais
A energia interna do sistema irá aumentar ou diminuir nas seguintes situações?
Considere que o tamanho das setas é proporcional ao quantidade de w e/ou
calor envolvidos no processo.
w
sistema
sistema
sistema
q
w
w
q
q
7
Termodinâmica
Trabalho P-V
• Considere um gás confinado em um cilindro de pistão móvel (sem atrito);
• Forças oponentes (pressão externa e pressão interna) são iguais a P e estão
em equilíbrio;
• Se P externa é aumentada
infinitesimalmente, causará um
deslocamento do pistão em dx,
• o volume interno do gás irá
diminuir infinitesimalmente, dV.
• Como dw = F.dx
P = F/A, então
dw = PA dx
Como A.dx = -dV, então:
dw = -PdV
8
Termodinâmica
Trabalho P-V
w
Quando w entra no
sistema (compressão)
deverá ter sina positivo,
segundo a convenção de
sinais.
Vf<Vi portanto ∆V <0
Desta forma
dw = -P.(-dV)> 0
9
Termodinâmica
Trabalho P-V
w
Quando w sai no sistema
(expansão) deverá ter sinal
positivo, segundo a
convenção de sinais.
Vf>Vi portanto ∆V >0
Desta forma
dw = -P.(dV)<0
10
Termodinâmica
Trabalho P-V e reversibilidade
A variação finita do volume consiste em um número infinito de etapas
infinitesimais e leva um tempo infinito para se realizar. A diferença de pressão
interna e externa é infinitesimal, portanto muito PRÓXIMA DO EQUILÍBRIO
DURANTE TODO O PROCESSO!
A reversão do processo restaurará tanto sistema quanto vizinhanças às suas
condições iniciais.
Um processo reversível é aquele em que o sistema sempre está
infinitesimalmente próximo do equilíbrio, e uma mudança infinitesimal das
condições pode reverter o processo para restaurar tanto sistema quanto
vizinhança aos seus estados iniciais. Processo reversível é uma idealização.
11
Termodinâmica
Trabalho P-V e IRREversibilidade
Suponha que a pressão externa sobre o pistão seja subitamente reduzida
por uma quantidade finita e mantida fixa. A pressão interna então é maior
que a pressão externa e o pistão é acelerado para fora.
w
Essa aceleração do pistão para fora do sistema destruirá a pressão uniforme
no gás ali contido. A pressão do sistema será menor próximo do pistão do
que mais além dele.
A aceleração causa turbulência no gás. Assim, não podemos dar uma
descrição termodinâmica do estado do sistema.
12
Termodinâmica
Trabalho P-V e IRREversibilidade
Para saber mais..... Fonte: Levine.
13
Termodinâmica
Trabalho P-V e IRREversibilidade
2)Considere 1 mol de gás ideal a uma pressão inicial de 1,00 atm e temperatura
inicial de 273,15 K. Assuma que ele se expande adiabaticamente e
irreversivelmente contra uma pressão de 0,435 atm, até que seu volume se
duplique. Calcule o trabalho, a temperatura final e a variação de energia
interna.
Resposta: ∆E = w = -987 J. Utilizando capacidade calorífica 3/2 R, ∆T = -79,1 K
14
Termodinâmica
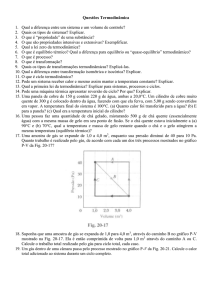
Trabalho P-V e reversibilidade
Diferentes caminhos
para sair da condição 1
à condição 2.
A resolução da integral
gera diferentes
resultados de w para as
situações a, b e c.
15
Termodinâmica
Trabalho P-V e reversibilidade
16
Termodinâmica
Trabalho P-V e reversibilidade
Processo reversível a P constante
Quando P = constante, V e T variam. Então
Processo reversível a T constante
Quando T= constante, P e V variam. Então
W = P∆V
W =-nRT ln V2/V1
ou W =+nRT ln V1/V2
q = Cp ∆T
Ou aplicando a Lei de Boyle
Processo reversível a V constante
Quando V = constante, P e T variam. Então
W = P∆V
0
qv = Cv ∆T e ∆E = qv
W =+nRT ln P2/P1
Como ∆E = 0
q = -w
17
Termodinâmica
Trabalho P-V e reversibilidade
18
Termodinâmica
Trabalho P-V e reversibilidade
Processo reversível a q constante
PROCESSO ADIABÁTICO
Quando q = constante
19
Entendendo a Natureza da Energia
Interna
Energia interna é energia a nível molecular.
Consideremos um gás. As moléculas movem-se através do
espaço:
• Energia translacional,
• Energia cinética.
Segundo a mecânica estatística, para um gás a energia
cinética translacional molecular é:
Erot= 3/2 RT para moléculas não lineares = 900 cal/mol
Erot = RT para moléculas lineares
20
Entendendo a Natureza da Energia
Interna
Também existe contribuição da energia vibracional
Evib = energia vibracional, depende das ligações químicas e
estrutura molecular
Segundo a mecânica quântica, as moléculas têm energia
restrita a certos valores chamados de níveis de energia.
Por exemplo, a distribuição de moléculas nos níveis de
energia possíveis para o CO a 298 K são:
0,93% estão no nível 0
2,7 % estão no nível 1
4,4 % no nível 2, etc.
A medida que a temperatura aumenta o nível de energia
molecular média aumenta, e a energia interna e a entalpia
aumentam.
21
Entendendo a Natureza da Energia
Interna
As moléculas também possuem energia eletrônica, εel, é a
energia da molécula com os núcleos em repouso, em
posições correspondentes à geometria molecular de
equilíbrio.
A energia eletrônica pode ser alterada por excitação de
uma molécula para nível de energia eletrônica superior. Mas,
quase todas as moléculas têm uma lacuna muito grande
entre o nível mais baixo de energia eletrônica e níveis
eletrônicos superiores.
Em uma reação química, as energias eletrônicas das
moléculas do produto diferem daquelas das moléculas do
reagente. Portanto, em uma reação química há alteração
da energia interna devido a energia eletrônica.
22
Entendendo a Natureza da Energia
Interna
Além da energia translacional, rotacional, vibracional e
eletrônica, as moléculas devido a atrações e repulsões entre
elas (forças intermoleculares). A força entre duas moléculas
depende da orientação de uma molécula em relação à
outra e da sua distância.
Diâmetros típicos de moléculas razoavelmente pequenas são
de 3 a 6 angstrom. A distância média entre as moléculas de
gás a 1 atm e 298 K é 6 a 12 vezes o diâmetro molecular.
Como as forças intermoleculares são insignificantes para
separações além de 3 vezes o diâmetro molecular, as forças
em um gás a 1 atm e 298K são bastante pequenas e
contribuem muito pouco para a energia interna.
23
Entendendo a Natureza da Energia
Interna
Para 40 atm e 298K a distância média entre moléculas de
gás é de apenas 10 angstrom e as forças intermoleculares
passam a ter contribuições significativas.
1 atm e 298 K E intermolecular = -1 a -10 call/mol
40 atm e 398 K E intermolecular = -40 a -400 cal/mol
Portanto, como em líquidos e sólidos as moléculas estão
muito mais próximas, a energia intermolecular se torna muito
relevante.
Por exemplo: energia para vaporizar um líquido encontra-se
na faixa de 3000 a 15.000 cal /mol
Resumindo:
E molecular = Etr + Erot + Evib + εel + E intermolecular + Erep
Erep é energia da massa em repouso dos elétrons e núcleo, e é constante.
24
Capacidades caloríficas a pressão
constante e volume constante
12,471 J/mol.K 20,785 J/mol.K
25
Capacidades caloríficas a pressão
constante e volume constante
CP é função de Temperatura
26
Capacidades caloríficas a pressão
constante e volume constante
27
Exercício
1)Avalie ∆E para um mol de oxigênio, O2, indo de -20,0 oC até 37oC a volume
constante, nos seguintes casos:
a) É um gás ideal com Cv,m = 20,78 J/molK
b) É um gás real com Cv,m = 21,6 + 4,18x10-3T – 1,67x105)/T2, determinado
experimentalmente.
28
Dependência entre ∆Hreação e T
29
Dependência entre ∆Hreação e T
A entalpia padrão de formação da água gasosa, a 298 K, é -241,8kJ/mol.
Estime o seu valor a 100oC, sendo dadas as seguintes capacidades
caloríficas molares, a pressão constante:
H2O (g) = 33,58 J/K.mol
H2 (g) = 28,84 J/K.mol
O2 (g) = 29,37 J/K.mol
Admita que as capacidades caloríficas seja independentes da
temperatura.
A importância das unidades....
30
31
A importância das unidades....
Fonte: Levine