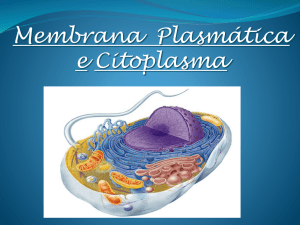
Compartimentos Celulares
Compartimentos Físicos:
Com membrana:
o Núcleo:
o Citoplasma:
o Organelos
Mitocôndria:
Compartimentos Nucleares:
o Matriz Nuclear: rede de fibras dentro do nucleoplasma;
o Nucléolo:
o Cromossomas:
Compartimento Citoplasmático:
o Organelos Citoplasmáticos
Estruturas protegidas por membrana
Retículo Endoplasmático
o Retículo Endoplasmático Liso- produção de lipídos.
o Retículo Endoplasmático Rugoso:
Complexo de Golgi
Mitocôndrias
Lisossomas
Perixossomas
o Citoesqueleto:
o Estruturas citoplasmáticas:
Ribossomas:
Proteínas
Osmose
A osmose é um tipo de transporte passivo e está relacionada com os processos de troca de
água entre as células e o ambiente intercelular. Esta é um fenómeno físico-químico que
ocorre quando duas soluções aquosas de concentrações diferentes entram em contacto
através de uma membrana semipermeável, isto é, uma membrana que deixa passar a
água, mas não deixa passar os solutos.
A passagem de água através da membrana tende a igualar a osmolaridade nos dois
compartimentos em que se está a realizar esta troca. Esta tendência de passagem de água
é combatida pela pressão osmótica, que é menor no sentido da solução hipotónica para a
hipertónica, ou seja, na direcção da solução com menor concentração de água e maior
concentração de iões e biomoléculas.
A pressão osmótica traduz-se na seguinte equação:
icRT
em que o termo ic é a osmolaridade, ou seja, o número de moles de um composto
químico que contribuem para a pressão osmótica de uma solução. A osmolaridade
depende do tipo de partículas em solução e das dimensões destas.
Soluções de igual osmolaridade são isotónicas. Quando uma célula está rodeada por uma
solução isotónica, não ganha nem perde água.
A osmolaridade de uma solução hipertónica é maior que a do citosol, há maior
concentração de água na célula. Uma célula numa solução destas perde água, e logo,
encolhe.
Uma solução hipotónica é o contrário – a osmolaridade é menor em relação ao citosol e a
célula ganha água e aumenta o seu tamanho.
As células no seu meio natural, geralmente, contêm maiores concentrações de
biomoléculas e iões do que o seu meio circundante, logo a pressão osmótica tende a levar
água para dentro das células. Contudo se este movimento de entrada de água não for, por
vezes, contrabalançado, pode levar à excessiva dilatação da membrana plasmática,
podendo eventualmente rebentar – Lise Celular.
Por outro lado, num meio hipertónico, a célula, devido ao seu encolhimento, pode deixar
de ser funcional e colapsar.
As propriedades físicas das soluções aquosas são fortemente influenciadas pelas
concentrações dos solutos, pois devido à semipermeabilidade da membrana, a água passa
quase que livremente quer para dentro quer para fora da célula ao contrário dos solutos
cuja passagem é dificultada. Deste modo as propriedades dos compartimentos celulares
mantêm-se de algum modo constantes.