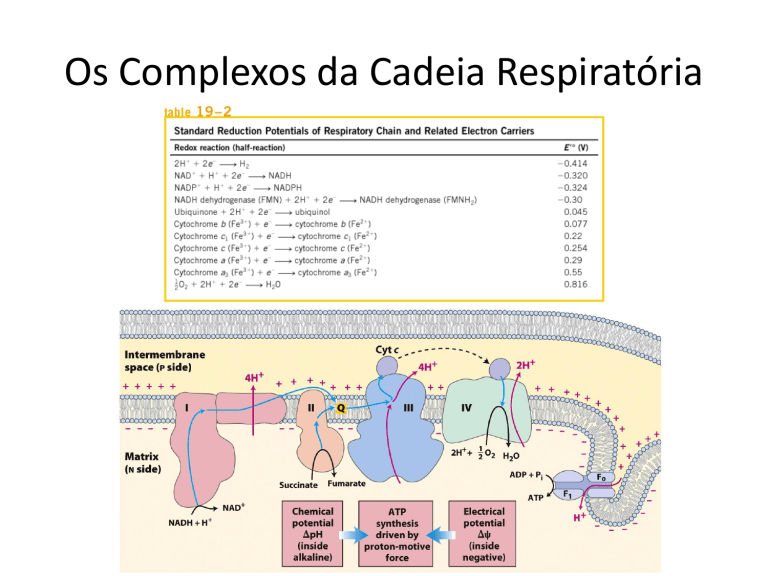
Os Complexos da Cadeia Respiratória
Complexo I
• NADH Desidrogenase
• Transferência exergônica de um
:H- (NADH) à ubiquinona
• Transferência endergônica de 4
prótons para o espaço
intermembranas
*:H- = 2 elétrons e 1 próton
Complexo II
• Succinato Desidrogenase
Complexo II
Primeira enzima que catalisa a
beta-oxidação dos ácidos geaxos
Ubiquinona ou Coenzima Q
• Quinona com uma longa cadeia lateral isoprênica
• Desempenha um papel central no transporte dos
elétrons acoplado ao movimento dos prótons
Complexo III
• Ubiquinona:citocromo c oxidorredutase
Ciclo Q
•
Uma molécula de QH2 reduz duas moléculas de citocromo
– Bifurcação do fluxo de elétrons da QH2 para os citocromos c1 e b, permitindo
o bombeamento de prótons da matriz para o espaço intermembranas.
– A QH2 transfere um dos elétrons para a proteína Fe-S liberando dois prótons
no espaço intermembranas e produzindo Q-.
– A proteína Fe-S reduz o citocromo c1, enquanto a Q- transfere os elétrons
restantes para o citocromo b, produzindo uma Q oxidada.
– Q oxidada recebe o elétron novamente do citocromo b, revertendo-se à forma
Q– No ciclo 2, outra QH2 reduzida, provinda do complexo I repete as etapas
anteriores. Esse segundo elétron reduz a Q- produzido no primeiro ciclo,
produzindo QH2
– Para cada 2 QH2 que entram no ciclo Q, uma QH2 é regenerada
Ciclo Q
•
Dois e- a partir de QH2 reduzem 2 moléculas de citocromo c e 4 H+ são
translocados para o espaço intermembranas: dois do QH2 na primeira volta do
ciclo e dois do QH2 na segunda volta
Complexo IV
• Citocromo Oxidase
Transferência dos Elétrons para o
Oxigênio
ROS - Espécies reativas de oxigênio
Doenças que podem ser vinculadas a lesão por ROS
Translocadores
e Lançadeiras
ADP
ATP
Pi
OH-
• A membrana interna da
mitocôndria é
impermeável a compostos
com carga elétrica e íons
– Coenzima NADH/NAD+ e
acetil-CoA.
Acidos dicarboxilicos
(malato, succinato e
fumarato, ...)
Pi ou Acidos
dicarboxilicos
Acidos tricarboxilicos
(Citrato ou isocitrato)
Malato
piruvato
Malato
• Sistemas transportadores
na membrana interna para
garantir o transporte e o
acesso de metabólitos
entre matriz e citosol.
glutamato
aspartato
2Na+
Ca++
Ca++
ATP/ADP translocase : a
mais abondante na mb :
represente 15% do conteudo
proteinico tatal da mb interna
da mitocôndria
Fosfato translocase :
coadjuvente da nucleotídio
translocase
Lançadeiras
Citosol
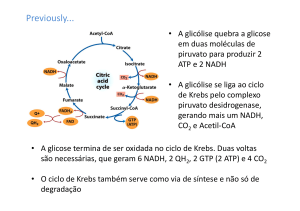
Glicose + 2NAD+ + 2ADP + 2Pi
2Piruvatos + 2NADH + H+ + 2ATP + H2O
•
Como a membrana interna da mitocôndria é impermeável a NADH e NAD+, a
oxidação destes compostos não pode ser feita diretamente pela cadeia de
transporte de elétrons.
– Existe assim um “pool” mitocondrial de NADH e um pool cistosólico de NADH
•
Elétrons transferidos para um composto citosólico, que transporta os elétrons para
a matriz mitocondrial, onde é oxidado.
•
O composto oxidado retorna ao citosol
– Sistema de Lançadeira. Existe diferente tipos de lançadeira.
• Malato-Aspartato e Glicerol-3-fosfato
Lançadeira Malato-Aspartato
•
•
•
•
•
•
NADH citosólico reduz o OAA
O malato penetra na
mitocôndria, onde é oxidado
– Enzima que utiliza o
NAD+ como coenzima.
O OAA não atravessa a
membrana interna
– Recebe o grupo amino
do glutamato
• Aspartato.
Aspartato sai da mitocôndria
No cistosol é regenerado em
OAA .
A passagem do malato e
aspartao através da
membrana interna é efetuada
via os translocadores
(glutamato-Asp e de ácidos
dicarboxílicos).
A lançadeira malato-aspartato existe nas células cardíacas e hepáticas
Lançadeira Glicerol-3-fosfato
A lançadeira glicerol 3 fosfato existe nos músculos esq. e no cérebro
O que você proporia para justificar a formação diferenciada de ATP a
partir de NADH e FADH2 como substratos?
Substratos
Inibidores
Bandas
escuras
Bandas
claras
Formação
de ATP
Q O2
NADH
CN-, CO,
NaN3
a, b, c
--
--
--
NADH
Rotenona
ou amital
--
--
--
--
NADH
Antimicina
A
b
--
--
--
FADH2
Rotenona
ou amital
a, b, c
a, b, c
2 ATP/O
Sim
NADH
--
a, b, c
a, b, c
3 ATP/O
Sim
FADH2
--
a, b, c
a, b, c
2 ATP/O
Sim
Ácido
ascórbico
--
a
a
1 ATP/O
Sim
ATP Sintase
ATP Sintase
• Localizada na membrana mitocondrial interna
Teoria Quimiosmótica
• Peter Mitchell
• Um gradiente eletroquímico impulsiona a síntese de ATP
• Transporte exergônico de H+ acoplado a síntese endergônica de ATP
Ciclo Catalítico da ATP Sintase
• Proposto por Paul Boyer
T (Tenso)
F (Frouxo)
A (Aberto)
A porção F1 sintetiza o ATP
Síntese de ATP ocorre em um
ambiente hidrofóbico
O gradiente de prótons fornece a energia necessária
para liberar o ATP sintetisado da supefície da enzima
Trabalho Mecânico
• FoF1 ATP Sintase converte parte da energia quimiosmótica em trabalho
mecânico
• Filamento de actina ligado a subunidade Fo mostrando sua rotação.
Importância do Gradiente de Prótons
•
Um gradiente eletroquímico
artificialmente imposto pode gerar a
síntese de ATP na ausência de um
substrato oxidável como doador de
elétrons
Em resumo...
Desacopladores
• Consumo de oxigênio sem associação com síntese de ATP
Desacoplamento resulta em Calor
• Ocorre principalmente no tecido
adiposo marrom
– Presente, principalmente, na região cervical
de neonatos
• Proteína desacopladora (UCP, também
conhecida como termogenina)
Regulação Integrada
•
ATP Sintase regulada pela disponibilidade de
ADP e Pi