EXERCÍCIO DA MEDICINA BASEADA EM EVIDÊNCIA
BUSCA ELETRÔNICA-RESUMINDO
Paulo R. Margotto –ESCS www.paulomargoto.com.br / [email protected]
É importante que se reconheça a necessidade da informação e a coloque em forma de
questão clínica respondível
Iniciamos a busca sempre pelo MEDLINE (www.pubmed.com);
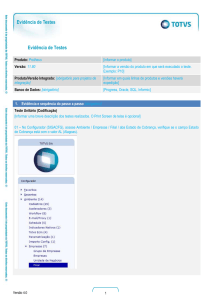
Os termos usados para a pesquisa são todos em inglês. Use o tradutor do
www.google.com do português para o inglês).
É importante lembrar quando não se encontra a questão nos sumários
baseados em evidências: buscar a pesquisa original na literatura médica, identificando o
tipo de questão clínica: Terapia ou intervenção, Diagnóstico, Prognóstico e
Etiologia/efeitos adversos Os estudos mais apropriados são: Revisão sistemática (o mais
alto nível de evidência; quando se aplica estatística, temos uma METANÁLISE),
Revisão controlada randomizada e Estudo de coorte/estudo de caso controle.
Para isto, clicar em Clinical Queries e Clinical Trials
A expressiva maioria dos artigos está em forma de Abstract. Quando estão
disponíveis, vem assinalado como Free Article
Como conseguir os artigos quando não disponibilizamos de senhas dos sites
pagos:
-solicitar diretamente ao autor, quando o seu e-mail estiver disponível no
Abstract. Use a seguinte Carta padrão:
Dear colleague, please send me a copy of your paper
-----------------(copiar o Artigo do MEDLINE e colar aqui)
Sincerely,
Seu nome e poucas referências
Exemplo: Paulo R. Margotto
ESCS/FEPECS/SES/Brasília, Distrito Federal, Brazil
Exemplo:
-solicitar a BIREME (www.bireme.br). Faça inicialmente um cadastro (é
grátis).
Vá ao Acesso a Documentos e clicar em SCAD. O artigo chega online dentro de
2-3 dias, conforme o dia da semana solicitado e posteriormente uma cobrança de 8,00
reais por artigo.
Definições importantes:
-Revisões sistemáticas: É uma forma de pesquisa na qual são sintetizados um
apanhado de relatos sobre uma questão clínica específica, ou seja, avalia e sintetiza
as informações da literatura sistematicamente. Há evidência de que são de alta
qualidade;
-Metanálise: É o método estatístico utilizado na revisão sistemática para integrar os
resultados dos estudos incluídos, aumentando a acurácia estatística; faz-se a análise da
combinação dos resultados (não combina os dados na forma de um único estudo);
utiliza conceitos como: intervalo de confiança, risco relativo, odds ratio e diferença de
risco; utiliza o Forest plot como gráfico de visualização dos resultados
-Risco Relativo: é a medida da força da associação entre a exposição e o evento
(resultado) Quando RR é igual a 1, significa que não há efeito com o tratamento, ou
seja, o efeito do tratamento é o mesmo nos dois grupos. Se o RR é < 1, significa que o
risco do evento é menor no grupo tratado que no controle. A variabilidade amostral do
estudo pode ser avaliada através de testes de significância ou via intervalo de confiança.
Para um dado nível de significância (· = 0,05), o intervalo de confiança representa o
intervalo onde deve estar o parâmetro, ou seja, o risco relativo verdadeiro. Se o valor 1,
que se refere à nulidade da associação, não estiver contido no intervalo, temos uma
confiança que na população de onde nossa amostra foi extraída, o RR é diferente de 1,
sendo, portanto significativo o achado da amostra.
-Intervalo de confiança (IC): Estima magnitude da associação informa a
variabilidade da estimativa (através da amplitude dos limites inf. e sup.).
A Redução do Risco Relativo (RRR) é 1-RR.
Exemplo (avaliação do canal arterial patente em RN com menor ou maior oferta
hídrica): RR = 0,40 (IC a 95% 0,26 – 0,63) não contém o 1. Como interpretar:
RRR = 1– 0,40 = 0,60 x 100 = 60 %%. A redução do canal arterial patente foi de
60% no grupo exposto a menor oferta hídrica e esta redução variou de 37% – 74%.
Vejam assim, que o IC estimou a magnitude da associação (reduziu em 60%) e
informou a variabilidade da estimativa (reduziu entre 37% e 74%)
É IMPORTANTE LEMBRAR QUE
QUANDO NÃO HÁ SIGNIFICÂNCIA, ou seja, o IC contém a unidade:
-se o IC for grande: o estudo é pequeno para precisar efeito no tratamento
-se o IC for pequeno, é improvável grande efeito benéfico do tratamento
Exemplo:
RR = 0,90 IC 95%%: 0,80 – 1,02
e
RR = 0,50 IC 95%%: 0,24 –
1,06
Observem que ambos RR não são significantes, pois contém no IC a unidade,
porem o primeiro, o IC é pequeno (é improvável que aumentando o n, vamos ter efeito
benéfico no tratamento). Já no segundo RR, o IC é grande, o que se conclui que o
estudo é pequeno para precisar o efeito no tratamento.
-Número necessário para tratamento (NNT): número necessário para
tratamento (expressa o beneficio do tratamento).
Exemplo:
Ex: Tratamento A (n=400)
RR = 0,80
NNT = 20
B (n=200)
0,80
100
É necessário tratar 100 RN
para evitar 1 dano
-forest plot: Mostra visualmente os resultados de uma metanálise;faz uma
estimativa visual da quantidade de variação entre os resultados.
Veja o seguinte exemplo de apresentação dos resultados de riscos relativos na
forma de forest plot, apesar de não ser uma metanálise, de um tabela que compara
individualmente desfechos de dois grupos de menores idades gestacionais com um
terceiro de maior idade gestacional. A tabela mostra os riscos relativos com os
respectivos intervalos de confianças e as significâncias (Pimentel M, Rugolo L,
Margotto PR, 2011).
Vejamos agora esta tabela representada em um forest plot
Observem que todos os riscos relativos evidenciam significantemente maior
desfecho no grupo de menor idade gestacional (15-27 semanas e 6 dias-pré-termos
extremos) em relação aos RN de maior idade gestacional (30-31 semanas 6 dias). Os
riscos relativos são significativos, pois não contém a unidade no intervalo de confiança
e visualmente vemos que NÃO tocam a linha vertical, que é a linha de nulidade.
Observem nesta metanálise sobre o uso de eritropoetina e o
desenvolvimento de retinopatia da prematuridade:
Vejam (SETA) que esta metanálise mostra que a eritropoetina aumenta
significativamente o risco de retinopatia da prematuridade (RR: 1,71; Intervalo de
confiança a 95%: 1,25-2,54).
A Biblioteca Cochrane (metanálises) integra eficientemente a informação válida,
constituindo suas informações importante base para uma tomada racional de decisão
A Neonatologia é felizarda em ter as revisões em texto completo disponível na
internet www.nichd.nih.gov/cochrane
Nota: 1) Regressão logística: A regressão logística vem sendo utilizada em diversas
áreas. Este método, tal como as regressões linear e múltipla, estuda a relação entre uma
variável resposta e uma ou mais variáveis independentes. A diferença entre estas
técnicas de regressão se deve ao fato de que na regressão logística as variáveis
dependentes estão dispostas em categorias (sim/não/alto/baixo/bom/ruim), enquanto
na regressão linear estas variáveis são contínuas. A resposta na regressão logística é
expressa por meio de uma probabilidade de ocorrência, enquanto na regressão simples,
obtém-se um valor numérico. Portanto, a regressão logística binária apresenta-se como
um método na determinação da probabilidade de ocorrência dos valores preditos de uma
variável dicotômica. Portanto, a regressão logística é uma versão da regressão múltipla
em que a saída é dicotômica (sim ou não/ alto/baixo; bom/ruim).
Exemplo; no nosso estudo sobre Corticosteróide antenatal na Maternidade do HRAS,
realizamos uma regressão logística binária; a variável resposta foi a ocorrência de
Apgar<= 3 no 5º minuto (sim ou não), caracterizando uma variável binária. As
variáveis independentes escolhidas foram aquelas que se associaram individualmente ao
Apgar <=3 no 5º minuto: corticóide, hipertensão materna, tipo de parto e pré-natal.
Resultado:
Interpretação: o corticosteróide antenatal (seta) persistiu no modelo como variável
protetora para Apgar <=3 no 5º minuto (OR-odds ratio, que é Exp (B) de 0,42)
enquanto a hipertensão materna (seta), um fator de risco (OR de 2,38). O mesmo não
ocorre com o tipo de parto e o pré-natal
Veja outro exemplo da aplicação da regressão logística: o estudo de Whelan B et
al avaliou a o sódio sérico como um fator de risco para a mortalidade intrahospitalar em
pacientes grave à admissão. A Odds ratio para a morte dentro de 30 dias da admissão
foi de 4,07 (IC a 95%%: 2,95-5,63) quando o paciente apresentava hipernatremia e
3,36 (IC a 95% de 2,59-4,36) quando apresentava hiponatremia. A regressão logística
foi usada para calcular a Odds ratio ajustada: fatores que foram incluídos neste ajuste
foram o escore de severidade da doença, permanência na UTI, efeito da idade, sexo,
transfusão de sangue e sepse. Após o ajuste, para hipernatremia, a Odds ratio (ajustada)
para a morte passou para 1,41 (Intervalo de confiança de 0,97-2,07: não alcançou a
significância, pois no intervalo de confiança contém a unidade) e a Odds ratio (ajustada)
para hiponatremia passou para 2,00 (Intervalo de confiança a 95% de 1,44-2,77, ou
seja, foi menor, porém continuou significativa, pois no intervalo de confiança não
contém a unidade). Assim, o sódio sérico é um poderoso marcador inicial para a
mortalidade, mas a mortalidade no grupo hipernatrêmico é primariamente um fator de
severidade da doença. Já para a hiponatremia o aumento da mortalidade é independente
de outras variáveis. Portanto, os dados deste estudo nos informam que o sódio sérico na
admissão é um importante determinante da mortalidade intrahospitalar em todos os
pacientes. O sódio na admissão pode ser usado para estratificar os pacientes que vão
necessitar de uma terapia mais agressiva e maior monitorização e em particular a
hiponatremia que necessita de tratamento cuidadoso para evitar um excesso de
mortalidade que é independentemente associada com anormalidade deste distúrbio.
2) Heterogeneidade:
Ao analisar os dados, a exploração de fontes de heterogeneidade (variabilidade
dos dados) corresponde a uma das etapas da metanálise. A heterogeneidade pode ser
clínica (os estudos diferem quanto às características dos participantes como idade,
severidade, intervenção (dose), variável de desfecho, duração ou estatística (variação
entre os resultados dos estudos é maior do que a esperada ao acaso). Outra fonte de
heterogeneidade pode ser diferenças na qualidade metodológica entre os estudos.
As inconsistências entre as estimativas das metanálise foram estimadas através
do teste de quiquadrado de heterogeneidade e quantificadas usando o teste I2. O I2 de
0% indica homogeneidade e o I2 maior que 50% indica heterogeneidade substancial
Exemplo: veja a figura acima da metanálise da eritropoetina e retinopatia da
prematuridade: os estudos são homogêneos, pois o teste I2 é 0%.
No entanto, outros autores usam teste Q de Cochran com nível de p<0,05
para aceitar a hipótese de heterogeneidade entre os estudos (p<0,1 quando o número de
estudos envolvidos é pequeno). Veja no estudo abaixo comparando ibuprofeno com
indometacina (Thomas, 2004): onde está a heterogeneidade? Observem (em vermelho)
que houve heterogeneidade nos estudos que avaliam o resultado uso de surfactante
quando se compara ibuprofeno (Q=5,97-p=0,05). Os demais outros resultados
apresentam Q>0.05.
E para finalizar:
Devemos lembrar que quando um paciente procura um médico para uma
consulta, ele certamente procura algo mais que a resposta cientifica ao seu problema
(Bandoher). Ser profissional de saúde exige conhecimento específico, disciplina,
responsabilidade, atenção e acima de tudo, grande capacidade de conviver com o stress,
o sofrimento, a dor e a vontade de resolver problemas alheios ((Machado MH).
O novo paradigma para a prática clínica, ou seja, base para tomar decisões tem
que incluir a evidência da pesquisa clínica. Os nossos tratamentos que usamos para os
bebês devem ter sempre mais benefícios do que prejuízos. Para isto, devemos adquirir
informação através da procura de evidências que isto seja verdadeiro na literatura. Este
é o novo paradigma da medicina: um esforço para tentar melhorar a situação do paciente
baseado na evidência das pesquisas clínicas. Medicina baseada em evidência é o uso
consciencioso da melhor evidência disponível na tomada de decisões no cuidado do
paciente. A prática da medicina baseada em evidência significa integrar experiência
clínica individual com a melhor evidência clínica disponível de pesquisas sistemáticas.
Sem a experiência clínica as práticas correm o risco de ser tiranizadas pela evidência,
podendo esta evidência ser inapropriadamente aplicada ou mesmo não aplicada ao
paciente. Sem a evidência, as práticas logo tornar-se-ão obsoletas e podem se tornar
detrimentais ao paciente. Lembre-se que as “evidências mudam em decorrer do tempo,
pois se não validarmos nossas condutas podemos causar mais mal do que bem para o
recém-nascido”.
Paulo R. Margotto
Brasília, 16/5/2012
Bons estudos!