Infecção pelo papilomavírus humano (HPV) - atualizações 2001
Dr. Charles Rosenblatt
E-mail: [email protected]
Médico urologista do Hospital São Luiz (responsável pela Urgência da Urologia do Hospital São Luiz),
especialista em Urologia pela Sociedade Brasileira de Urologia, mestrado em Urologia pela Clínica
Urológica do HCFMUSP, atualmente cursando o doutorado pela Clínica Urológica do HCFMUSP, fellow
do Departamento de Urologia da Cleveland Clinic Foundation, OHIO, USA, membro da American
Urological Association. Responsável pelas seguintes publicações na Internet:
Uronews - www.uronews.org.br
Gastronews - www.gastronews.org.br
Neuropsiconews - www.neuropsiconews.org.br
Cadastro Nacional de Saúde - www.cadastronacionaldesaúde.com.br
MedscapeBrasil - www.medscapebrasil.com
Introdução
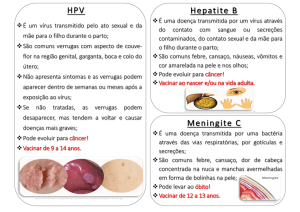
Há mais de 100 tipos conhecidos de papilomavírus humano (HPV). A infecção pelo HPV pode ocorrer
em quase qualquer parte do corpo. Alguns tipos de HPV infectam as mãos, os joelhos e os pés;
outros, a face e outros, o trato genital. Essas diretrizes enfocam a conduta para a infecção do trato
genital pelo HPV.
Mais de 20 tipos de HPV podem infectar o trato genital. A infecção pelo vírus das verrugas pode existir
sob as formas clínica, subclínica ou latente. A forma clínica de infecção pelo HPV são as verrugas
genitais. A infecção subclínica não é visível a olho nu, mas pode ser reconhecida com um microscópio,
como em um esfregaço cervical por exame ao colposcópio ou em amostras de tecido para
histopatologia. A infecção latente só pode ser detectada com o uso de técnicas moleculares. Os fatores
que influenciam a transição entre os estados clínico, subclínico e latente de infecção são mal
compreendidos, mas os mecanismos imunes são claramente importantes.
As verrugas anogenitais visíveis geralmente são causadas pelo HPV tipo 6 ou 11, e as lesões podem
aparecer na vulva, no colo uterino, na vagina, no pênis, no escroto, na uretra e no ânus. As verrugas
intra-anais são vistas predominantemente em pacientes que tiveram intercurso anal receptivo. Essas
verrugas são distintas das verrugas perianais, que podem ocorrer em homens e mulheres que não
tenham tido sexo anal receptivo. Os tipos 6 e 11 do HPV também se associam a verrugas conjuntivais,
nasais, orais e laríngeas. Esses tipos têm baixo potencial oncogênico e raramente se associam a
carcinoma espinocelular invasivo no trato genital.
Outros tipos anogenitais de HPV (16, 18, 31, 33 e 35) associam-se fortemente a neoplasias vulvares,
penianas, anais, à neoplasia intra-epitelial cervical (NIC) e ao carcinoma espinocelular. Esses tipos
oncogênicos são encontrados ocasionalmente em verrugas genitais visíveis e também se associam à
neoplasia intra-epitelial vulvar (NIV) e à neoplasia intra-epitelial peniana (PIN). As duas últimas
afecções antigamente eram conhecidas por outros nomes, como papilose bowenóide, eritroplasia de
Queyrat e doença de Bowen. Os pacientes que têm verrugas genitais visíveis podem estar infectados
simultaneamente por múltiplos tipos de HPV.
Epidemiologia da infecção genital por HPV
Embora seja difícil fazer a estimativa da prevalência total da infecção genital pelo papilomavírus
humano (HPV), os números atuais sugerem que as verrugas genitais visíveis estejam presentes em
aproximadamente 1% dos adultos sexualmente ativos, nos Estados Unidos, e que, pelo menos, 15%
tenham infecção subclínica ou latente, conforme detectado pelas provas de DNA para HPV. É provável
que, pelo menos, 75% dos adultos sexualmente ativos tenham sido infectados por 1 ou mais tipos de
HPV genital em algum momento.
As taxas mais altas de infecções genitais pelo HPV são verificadas em adultos com 18 a 28 anos de
idade. Embora os fatores de risco para infecção sejam difíceis de avaliar devido à alta freqüência de
infecção subclínica, fica claro que o principal fator de risco para adquirir infecção genital pelo HPV
envolve comportamento sexual, particularmente múltiplos parceiros sexuais.
Transmissão da infecção genital pelo HPV
O contato direto pele com pele propaga com maior eficiência a infecção pelo HPV. O vírus não é
transmitido através de sangue ou líquido corporal, como o sêmen. As formas genitais do vírus visam
às mucosas e à pele genital adjacente. Estudos entre pessoas com a infecção pelo HPV verificaram
que, pelo menos, 70% de seus parceiros também estavam infectados. A transmissão é comum por
várias razões. Em primeiro lugar, as lesões costumam passar despercebidas, particularmente em
áreas que não sejam facilmente inspecionadas na pesquisa de verrugas; acrescente-se que o HPV
genital raramente causa dor. Em segundo lugar, pode ser difícil ter certeza se as verrugas estão
presentes. Finalmente, as infecções subclínicas também podem ser infecciosas, mas parecem não ser.
O contato sexual é a forma mais comum de transmissão entre adultos, mas também pode ocorrer
raramente a transmissão vertical ou auto-inoculação. Embora raro, é possível transmitir a infecção
pelo HPV através de sexo oral, embora a boca pareça ser ambiente menos habitável para cepas
genitais do HPV que a área genital. A transmissão por fômites permanece controversa.
É extremamente variável o período de latência da infecção genital pelo HPV. Muitas vezes, as verrugas
aparecerão depois de três a seis meses, mas já foram relatados períodos de latência de muitos meses
ou até décadas. São vistas evidências de tais períodos de latência prolongados em pacientes
imunocomprometidas e normais que, apesar de estarem sexualmente inativas há muitos anos,
subitamente podem desenvolver verrugas ou anormalidades cervicais. É importante enfatizar que
desenvolver verrugas genitais durante uma relação a longo prazo não implica necessariamente
infidelidade.
Em geral, acredita-se, embora isto não tenha sido comprovado, que verrugas clinicamente visíveis
ofereçam a maior possibilidade de transmissão e que tratar as verrugas diminui essa possibilidade.
Como é difícil detectar HPV em seu estádio latente, é impossível saber se, em alguns casos, o sistema
imune pode negativar completamente o vírus no corpo ou se o vírus permanece latente em níveis
indetectáveis, capaz de reemergir se o sistema imune enfraquecer. Se as verrugas não recorrerem no
ano seguinte ao tratamento, o risco de transmissão do HPV será baixo.
Um único estudo prospectivo de acompanhamento não demonstra benefício no uso de condons para
prevenir a transmissão do papilomavírus humano. No entanto, há algumas evidências sugerindo que o
uso regular do condom aumente a taxa de curas de lesões clínicas e subclínicas e, como se pensa que
as verrugas visíveis são mais facilmente transmissíveis que a infecção subclínica, seria apropriado
aconselhar o uso de condom até que as verrugas tenham desaparecido.
Os condons proporcionam barreira física que protege os pontos mais comuns de infecção, mas não
podem prevenir todo contato genital de pele com pele. O uso de condons é, contudo, recomendado,
particularmente com novos parceiros sexuais, para proteger contra outras DSTs.
Apresentação clínica e diagnóstico
As verrugas genitais são lesões visíveis que ocorrem na área anogenital. Aparecem como lesões
distintas ou podem coalescer em placas confluentes. A inspeção, isoladam__ente, é suficiente para
diagnosticar a maioria das verrugas genitais externas, e há boa correlação entre os achados físicos e
os estudos histológicos. As verrugas genitais são freqüentemente multifocais (uma ou mais lesões em
um ponto anatômico, a vulva, por exemplo) ou multicêntricas (lesões em pontos anatômicos
separados, como períneo e colo uterino). É importante examinar o trato genital baixo inteiro para
pesquisa de verrugas visíveis multicêntricas antes do tratamento. Verrugas queratinizadas e papulares
planas tendem a ocorrer em pele inteiramente queratinizada, os condilomas acuminados ocorrem mais
comumente em superfícies úmidas e verrugas genitais externas papulares planas podem ocorrer em
qualquer das duas superfícies.
As verrugas podem ocorrer no colo uterino. A melhor prática recomenda colposcopia antes de decisões
de tratamento.
Recomenda-se a pesquisa de verrugas intra-anais por anoscopia em homens e mulheres com verrugas
perianais recorrentes e/ou história de intercso anal receptivo. A uretromeatoscopia pode ajudar a
avaliar verrugas meatais em homens.
Diagnóstico diferencial
Nas mulheres
O diagnóstico diferencial de verrugas genitais inclui lesões que causam pápulas e lesões eritematosas
planas. As pápulas genitais incluem estruturas anatômicas normais, como as pápulas penianas
perláceas, papilas vestibulares e glândulas sebáceas e de Tyson. As pápulas adquiridas incluem
molusco contagioso, líquen nítido, pólipos cutâneos, nevos melanocíticos e condilomas planos. A
neoplasia intra-epitelial vulvar (NIV) geralmente se apresenta como lesão pruriginosa papular que
pode aparecer de forma uni ou multifocal, com coloração branca, vermelha, pigmentada,
habitualmente papular, mas algumas vezes como verruga. A lesão pode ser pequena e distinta ou
pode ser extensa, cobrindo a maior parte da vulva ou a pele perianal. Algumas vezes, pode ser
clinicamente indistinguível da forma papular das verrugas genitais externas. O exame histológico
dessas lesões mostra neoplasia intra-epitelial de alto grau: NIV III geralmente se associa à infecção
pelo HPV tipo 16.
Nos homens
Em homens, lesões eritematosas planas também incluem psoríase, dermatite seborréica, balanite
circinada associada à síndrome de Reiter e PIN II e III (eritroplasia de Queyrat - doença de Bowen) da
glande do pênis.
Abordagens diagnósticas adicionais
Lentes de grande aumento podem auxiliar no diagnóstico de verrugas genitais externas. Não foi
estabelecido o valor de usar soluções de ácido acético diluído (3% a 5%) ("o teste acetobranco"),
sendo baixo o valor preditivo positivo desse teste. Alguns médicos acham que o embebimento em
ácido acético é adjunto útil no diagnóstico de lesões visíveis que se suspeita serem verrugas,
particularmente as verrugas papulares planas. No entanto, o embebimento em ácido acético não é
recomendado para triar verrugas nos indivíduos, pois a alteração acetobranca ocorre com muitas
outras afecções.
Quando houver dúvida no diagnóstico, deve-se considerar o encaminhamento a um profissional com
experiência no diagnóstico de infecção pelo HPV. O diagnóstico de verrugas genitais raramente pode
necessitar de confirmação por biópsia, como quando as lesões são desorganizadas ou endurecidas,
fixas a estruturas subjacentes ou ulceradas. Ademais, pode-se considerar uma biópsia quando houver
dúvida no diagnóstico, se as lesões não responderem a um tempo padronizado de tratamento (o que
pode ocorrer quando afecções papuloescamosas, como a NIV, o líquen plano ou a psoríase são
tratadas como verrugas) e se a doença piorar durante o tratamento. A biópsia pode estar indicada
mais freqüentemente para pacientes imunossuprimidos porque, nesses pacientes, as lesões
intra-epiteliais de células escamosas (SILs) de alto grau são mais comuns que nos pacientes
imunocompetentes, podendo ser clinicamente indistinguíveis de verrugas.
A detecção e a tipagem de HPV não têm benefício comprovado no diagnóstico ou tratamento de
verrugas genitais externas. Dessa forma, a detecção e a tipagem de rotina do HPV não são
recomendadas atualmente para o diagnóstico ou o tratamento de verrugas genitais externas.
Tratamento de verrugas genitais
O objetivo primário do tratamento é eliminar as verrugas. Fisicamente, as verrugas costumam ser
assintomáticas, mas podem ser dolorosas, friáveis ou pruriginosas. Emocionalmente, as verrugas
podem ser socialmente estigmatizantes ou esteticamente perturbadoras. O tratamento pode resultar
em estado clinicamente isento de verrugas, mas a infecção viral subjacente pode persistir ou não. A
eliminação de verrugas externas visíveis pode não diminuir a infectividade, já que as verrugas podem
não representar a carga viral inteira. Sítios internos e pele normal podem atuar como reservatórios
para infecção pelo HPV.
Se deixadas sem tratamento, as verrugas podem resolver-se espontaneamente (20% o fazem em 6
meses), ficar inalteradas ou aumentar em tamanho ou número. Raramente as verrugas evoluem para
câncer. O tratamento deve ser moldado à infecção do paciente e às suas necessidades, bem como aos
recursos disponíveis. No presente, nenhum tratamento é ideal para todos os pacientes ou todas as
verrugas.
Tratamentos feitos pelo próprio paciente
Os tratamentos auto-aplicados incluem a solução química ablativa de podofilotoxina e o creme
imunopotencializador imiquimod. Os pacientes devem ser capazes de identificar e alcançar suas
verrugas e seguir as instruções de aplicação para usar esses tratamentos com sucesso. Essas terapias
são mais eficazes em verrugas úmidas.
A podofilotoxina é antimitótica e causa necrose localizada do tecido. Pode ser vista palidez epidérmica
localizada, causada por edema intra e intercelular, até depois de 48 horas da aplicação. A solução de
podofilotoxina é dispensada em concentrações de 0,5% e contém podofilina purificada em uma forma
mais padronizada. Tem sido extensamente avaliada em ensaios clínicos randomizados e controlados
por placebo que mostram entre 45% e 82% de pacientes que atingem o desaparecimento total das
lesões em 4 a 6 semanas de tratamento e, que entre 0% e 91% dos pacientes, têm recorrências. A
podofilotoxina não é recomendada para uso interno no colo uterino ou no canal anal, para pacientes
com sabida hipersensibilidade a seus ingredientes ou para uso em áreas extensas com verrugas. A
podofilotoxina não deve ser usada durante a gravidez. Os efeitos adversos associados à podofilotoxina
incluem ulceração e erosões, eritema, irritação e cicatrizes, fimose, endurecimento, dor e queimadura
prepuciais.
Imiquimod é um creme topicamente ativo imunopotencializador que estimula a produção de interferon
e outras citocinas. Em estudos randomizados e controlados por placebo, entre 37% e 85% dos
pacientes tratados ficaram livres das verrugas depois do tratamento, e 13% a 19% tiveram
recorrências durante o período de acompanhamento. O imiquimod parece ser muito mais eficaz para
mulheres que para homens, provavelmente devido aos diferentes ambientes nos tratos genitais
feminino e masculino. Foram relatados edema localizado, irritação, queimadura, dor e ulceração como
reações adversas raras e podem estar relacionados à ação terapêutica direta do agente. Esses efeitos
colaterais causam suspensão do tratamento em apenas 2% dos pacientes. Tem havido pouco uso do
imiquimod na gravidez e há poucos dados disponíveis. Seu uso na gravidez só deve ser considerado
quando outras opções não forem adequadas e a paciente tiver sido aconselhada adequadamente.
Tratamentos aplicados pelo médico
Podofilina
A resina de podofilina geralmente é composta em suspensão a 10% a 25% em tintura de benjoim e
contém numerosos agentes antimitóticos, incluindo a podofilotoxina. A palidez epidérmica geralmente
se desenvolve em 48 horas após a aplicação devido ao edema intra e intercelular associado à necrose
nos tecidos afetados. As preparações com resina de podofilina variam grandemente em sua
concentração de componentes ativos e contaminantes, não se conhece a estabilidade da resina de
podofilina e não existem preparações bem padronizadas.
A resina de podofilina tem sido extensamente avaliada em estudos randomizados para comparação de
tratamentos que mostram que as verrugas desaparecem completamente em 19% a 80% dos
pacientes tratados e que entre 23% e 70% dos pacientes cujas verrugas desapareceram têm
recorrências. Não há evidências de que a administração de podofilina intensifique grandemente outras
intervenções terapêuticas quando feita como terapia adjuvante. Um por cento da população pode ter
severa reação de hipersensibilidade a ela.
É importante aplicar fina camada de resina de podofilina às verrugas e permitir que seque
completamente ao ar. A aplicação excessiva ou a falha em secá-la ao ar podem resultar em
disseminação do composto e reação local significativa. A tintura de benjoim localiza o tratamento nos
tecidos afetados e é insolúvel em água. Quando apropriadamente aplicada, não há necessidade de
proteger a pele em volta. Geralmente é recomendado que os pacientes sejam avisados para lavar a
área tratada quatro horas depois da aplicação.
A hipersensibilidade aos ingredientes do produto contra-indica o uso, e a podofilina não é
recomendada para mulheres grávidas. A podofilina não é recomendada para uso em áreas de verrugas
com 10cm2 ou mais, pois o uso em áreas maiores aumentará a absorção e poderá induzir toxicidade.
Os efeitos adversos locais com a podofilina incluem ulceração da pele, eritema, irritação e cicatrizes,
fimose, endurecimento, dor e queimaduras prepuciais. Não é recomendada a prescrição de podofilina
para auto-administração devido a esses efeitos colaterais em potencial.
Crioterapia
A crioterapia destrói o tecido da verruga por congelamento/descongelamento, resultando em
desprendimento e destruição da verruga. A crioterapia eficiente pode ser obtida com uma criossonda
ou aplicação de nitrogênio líquido por aerossol ou por algodão frouxo em um aplicador de madeira
(não com swabs de algodão típicos firmemente enrolados). Em geral, a crioterapia é eficaz para
verrugas secas e úmidas e pode ser usada para verrugas externas e internas. É considerado o
tratamento de escolha durante a gravidez.
Embora não haja contra-indicação relacionada ao paciente para a crioterapia, a não ser a
crioglobulinemia, é necessário treinamento, sem o qual as verrugas são freqüentemente tratadas em
excesso ou subtratadas, levando a uma eficácia pequena e ao aumento das complicações. Dor e
necrose após a aplicação do criocautério são razoavelmente universais e algumas vezes ocorre
formação de bolhas. Tratar grandes verrugas ou grandes áreas ou números de verrugas de uma só
vez pode criar problemas para cuidar dos ferimentos. Os efeitos adversos incluem balanopostite,
irritação, edema local, necrose, ulceração e dor, especialmente quando a área tratada descongela.
Embora o uso de anestesia local ou tópica injetada raramente seja necessário, pode facilitar a
crioterapia por redução da dor quando estiver presente um grande número ou uma grande área de
verrugas.
Os estudos de eficácia têm sido limitados a estudos de séries de casos e estudos randomizados que
confrontam a crioterapia com outros tratamentos padronizados e têm mostrado que entre 60% e 97%
dos pacientes tratados permaneciam livres de verrugas, 3 a 6 semanas depois do tratamento.
Relata-se a ocorrência de recorrência de verrugas em 20% a 79% dos pacientes participantes dos
estudos clínicos.
Ácido tricloroacético
O ácido tricloroacético (ATA) é um agente cáustico que destrói as verrugas por coagulação química de
proteínas. Estudos de comparação randomizados e estudos descritivos de séries de casos mostram
taxas de desaparecimento entre 50% e 100%. Somente dois relatos de estudos publicados
descreveram taxas de recorrência entre os pacientes tratados com ATA, e mostraram que entre 6% e
50% dos pacientes tratados desenvolvem verrugas recorrentes. As concentrações das soluções de
tratamento descritas na literatura não são padronizadas, tendo sido relatadas concentrações de 85% a
95%.
A solução de ATA tem viscosidade muito baixa (comparável à da água) e, se aplicada em excesso,
pode espalhar-se rapidamente e escorrer, danificando uma área significativa de tecido normal
adjacente. As soluções de ATA devem ser aplicadas com parcimônia e deve-se permitir que sequem
antes que o paciente se sente ou fique em pé e são mais eficazes para verrugas pequenas em
superfícies úmidas. Pode causar cicatriz e dor intensa, embora de curta duração, mas é segura para
usar durante a gravidez. É necessário treinamento para aplicar esse método de tratamento. Se houver
dor intensa, o ácido poderá ser neutralizado com sabão e bicarbonato de sódio. Ulceração cutânea,
erosões, eritema e irritação, bem como dor espontânea, queimaduras e dor à manipulação são efeitos
colaterais adversos associados a esse tratamento.
Eletrocauterização
A eletrocauterização ou a diatermia coagula proteínas de tecido tratado. Uma vez obtida a anestesia, o
eletrocautério pode destruir fisicamente as verrugas, não sendo necessária hemostasia adicional.
Relatos de um estudo de comparação randomizado e várias séries de casos comparativas sugeriram
que a eletrocauterização pode ser tão eficaz quanto a crioterapia. Em um estudo, 22% dos pacientes
cujas verrugas desapareceram tiveram recorrências. Dor local e possível infecção podem ser os efeitos
colaterais. Como a crioterapia, a eletrocauterização requer treinamento avançado e experiência para
prevenir subtratamento ou tratamento excessivo da área afetada.
Exérese da verruga
A curetagem e as exéreses com tesoura ou bisturi removem diretamente as verrugas genitais. Já que
a maioria das verrugas é exofítica, isso pode ser efetuado de modo que a ferida resultante se estenda
apenas até a derme superior. A hemostasia pode ser obtida com uma unidade eletrocirúrgica ou
styptic químico (bastões de nitrato de prata); raramente, são necessárias ou indicadas suturas quando
a remoção é feita apropriadamente. Estudos randomizados de comparação de tratamentos e estudos
de séries de casos descritivos têm mostrado erradicação quase completa em 1 a 6 semanas de
tratamento e taxas de recorrência de 8% a 35%, em 1 ano de tratamento. Não há contra-indicações
relatadas para exérese com tesoura/bisturi, com exceção de uma anormalidade de sangramento
conhecida. Dor localizada, para a qual podem ser necessários analgésicos fracos, e sangramento são
os efeitos colaterais associados a esse tratamento. Se for necessária cirurgia no centro cirúrgico,
aplicam-se todos os riscos associados da anestesia geral.
Laser
Algumas vezes se recomenda a terapia com laser. As taxas de recorrência variam amplamente,
conforme observado na tabela, e podem ser desviadas pelo fato de que a terapia com laser costuma
ser usada mais freqüentemente em pacientes com doença extensa. O custo relativo para esse
tratamento é muito alto.
Fluorouracila
Não se recomenda o creme de fluorouracila a 5% devido a eficácia não comprovada, toxicidade
significativa e teratogenicidade para o tratamento de rotina de verrugas e, atualmente, é medicação
de uso apenas por especialistas. Foram relatados efeitos colaterais adversos, como disúria, erosão do
meato urinário, eritema, escara, hiperpigmentação, irritação local, queimadura e prurido.
Futuras modalidades de tratamento
O desenvolvimento de vacina é área de pesquisa ativa. Várias abordagens estão sendo testadas em
modelos animais. Estão em andamento ensaios clínicos humanos na fase 1.
Escolha de tratamento(s) para pacientes individuais
A tabela 1 resume as opções de tratamento.
Muitos pacientes requerem um período de tratamento, e não um tratamento único. Os estudos não
têm avaliado sistematicamente os fatores que influenciam a seleção da terapia. Tais fatores incluem
os seguintes: tamanho, morfologia e número de verrugas; ponto anatômico; preferência do paciente;
idade e capacidade cognitiva do paciente; treinamento e experiência do médico (Quadro 1).
O paciente comum tem pequeno número de verrugas que finalmente podem ser eliminadas pela
maioria das modalidades de tratamento. Os tratamentos tópicos administrados quase nunca
funcionam prontamente naqueles com áreas grandes ou extensas de verrugas. Esses pacientes devem
ser submetidos à terapia ablativa, pelo menos para se desbastarem suas verrugas. Os pacientes com
doença limitada (1 a 5 verrugas) podem beneficiar-se mais da crioterapia, cirurgia simples em
consultório ou outros tratamentos administrados.
Para modalidades terapêuticas auto-aplicadas, não é recomendável o tratamento além das
recomendações do fabricante. Não é recomendado o uso concomitante de múltiplas modalidades
terapêuticas em uma única verruga como tratamento de rotina. Deve-se ter em mente que uma
contínua falta de resposta ao tratamento poderia indicar outra patologia e se deve considerar o
encaminhamento para avaliação em tais casos. A relação risco-benefício deve ser avaliada durante
todo o tempo de terapia para evitar tratamento em excesso e uma evolução terapêutica pior que a
própria doença. Hipo ou hiperpigmentação persistente é possível complicação das modalidades
terapêuticas ablativas. Raramente ocorrem cicatrizes afundadas ou hipertróficas. O tratamento
ablativo pode resultar em síndrome de dor crônica incapacitante (vulvodínia) ou hiperestesia no local
de tratamento.
A remoção cirúrgica de verrugas por diatermia, ablação com laser ou exérese sob anestesia local ou
geral podem tornar o paciente livre das verrugas, geralmente em uma única consulta. No entanto, as
desvantagens são a necessidade de treinamento, de uma quantidade moderada de equipamento e de
uma consulta mais longa para o paciente. Embora a cirurgia seja obviamente mais benéfica quando as
verrugas estiverem presentes em grande número ou em grandes áreas, também pode ser usada para
casos comuns. Conquanto o custo de uma consulta cirúrgica única possa ser maior, a cirurgia pode
fazer, em uma consulta, o que outras modalidades ablativas, muitas vezes, requerem múltiplas
consultas para efetuar, o que poderia resultar em melhor relação custo-benefício para alguns
pacientes. No entanto, as taxas de recorrência podem ser as mesmas que as de outras modalidades
terapêuticas.
Acompanhamento pós-tratamento
O benefício, a freqüência, o intervalo e o tipo de acompanhamento necessários depois do tratamento
das verrugas ainda não foram estudados. A avaliação de acompanhamento pode dar a oportunidade
para orientação e aconselhamento de pacientes. A necessidade de monitorizar as complicações da
terapia variarão grandemente, com base na experiência do paciente e em sua capacidade cognitiva,
no número e localização das verrugas e na modalidade de tratamento usada. Deve-se oferecer aos
pacientes preocupados com a recorrência uma avaliação três meses depois de tratamento
bem-sucedido, já que a maioria das recorrências ocorre durante esse período. Em pacientes
imunossuprimidos, as recorrências de verrugas são muito mais comuns, podendo ser necessária a
avaliação periódica de acompanhamento.
Avaliação de parceiros sexuais
O exame de parceiros sexuais não é necessário para o tratamento de verrugas genitais porque o papel
da reinfecção provavelmente é mínimo e, na ausência de tratamento curativo, o tratamento para
reduzir a transmissão não é realista. No entanto, como o auto-exame ou o exame do parceiro não foi
avaliado como método diagnóstico para verrugas genitais, os parceiros sexuais de pacientes que as
tenham podem beneficiar-se do exame para avaliar a sua presença e outras infecções sexualmente
transmissíveis. Os parceiros sexuais também podem beneficiar-se de aconselhamento sobre as
implicações de ter um parceiro com verrugas genitais. Como o tratamento das verrugas genitais
provavelmente não elimina a infecção pelo HPV, os pacientes e seus parceiros sexuais devem ser
avisados de que o paciente pode permanecer infeccioso ainda que elas desapareçam. O uso de
condons pode reduzir, mas não elimina o risco de transmissão para parceiros não infectados. As
parceiras de pacientes que tenham verrugas genitais devem ser lembradas de que se recomenda a
triagem citológica de câncer do colo uterino para todas as mulheres sexualmente ativas. No entanto, o
benefício de avaliar os parceiros sexuais de pacientes com verrugas genitais externas ainda não foi
cuidadosamente estudado.
Semelhantemente, não se conhece o benefício específico de avaliar os parceiros sexuais de mulheres
com lesões intra-epiteliais escamosas cervicais relacionadas ao HPV (SILs) para verrugas genitais
externas. Embora até metade dos parceiros sexuais masculinos das mulheres com SILs cervicais
possam ter evidências de infecção genital pelo HPV, relativamente poucos têm verrugas genitais
externas. Não está claro se o tratamento de homens com evidências de infecção genital pelo HPV
influencia a história natural de suas parceiras com doença cervical. Há poucas informações,
atualmente, sobre os efeitos de doença cervical relacionada ao HPV sobre parceiras sexuais de
mulheres com infecção pelo HPV. As mulheres que são parceiras sexuais de pacientes com verrugas
genitais externas devem ser submetidas à triagem citológica para câncer do colo uterino nos
intervalos recomendados pelas diretrizes nacionais de triagem cervical. Não se sabe qual seja o
benefício de avaliar parceiros sexuais de homens com verrugas genitais externas.
Situações especiais
Gravidez
As verrugas genitais podem proliferar e ficar friáveis durante a gravidez devido à imunidade alterada,
bem como aumento da irrigação, e alguns autores preconizam sua remoção durante a gravidez. Os
tipos 6 e 11 do HPV raramente causam papilomatose laríngea em lactentes e crianças. A via para
transmissão (transplacentária, perinatal ou pós-natal) não foi ainda completamente entendida. O
parto cesariano não deve ser realizado unicamente para prevenir a transmissão de infecção pelo HPV
ao recém-nascido. Em raras circunstâncias, o parto cesariano pode ser indicado para mulheres com
verrugas genitais, se a saída pélvica estiver obstruída ou se o parto vaginal resultar em sangramento
excessivo.
O tratamento, durante a gravidez, requer algumas considerações especiais. Imiquimod, podofilina e
podofilotoxina não devem ser usados durante a gravidez. Tratamentos apropriados para verrugas
genitais externas durante a gravidez incluem crioterapia, ATA ou remoção cirúrgica e ablação por
laser.
O HPV, na gravidez, não tem ligação com fracasso da gravidez, trabalho de parto ou outros tipos de
complicações da gravidez.
Pacientes imunossuprimidos
As pessoas imunossuprimidas pelo HIV ou por outras razões podem não responder tão bem quanto as
pessoas imunocompetentes ao tratamento para verrugas genitais, e podem ter recorrências mais
freqüentes depois do tratamento. Os carcinomas de células escamosas originados em SILs e
semelhantes a verrugas genitais ocorrem mais freqüentemente entre os imunossuprimidos.
Infecção genital pelo HPV e câncer anogenital
No mundo todo, o câncer do colo uterino vem depois, apenas, do câncer de mama como doença
maligna mais comum em incidência e em mortalidade nas mulheres. A campanha de triagem cervical
recentemente mostrou uma tendência de redução nesses números nos últimos oito anos.
As informações moleculares e epidemiológicas atuais sustentam um papel causal para o papilomavírus
humano (HPV) em cânceres cervicais, vaginais e em muitos vulvares. Pelo menos 80% dos adultos
sexualmente ativos ficarão infectados com um tipo ou mais de HPV genital em algum momento. No
entanto, somente uma pequena proporção de mulheres expostas à infecção pelo HPV desenvolverá
câncer do trato genital baixo. A infecção pelo HPV é um evento em uma via de múltiplas etapas para o
câncer, sendo improvável que, isoladamente, baste para a transformação maligna do epitélio do trato
anogenital. Outros co-fatores como o tabagismo e o sistema imune desempenham papéis importantes.
Os tipos 6 e 11 do HPV, comumente associados a verrugas genitais, têm baixo potencial oncogênico e
raramente se associam a carcinoma de células escamosas invasivo da área anogenital.
Outros tipos anogenitais de HPV (16, 18, 31 e 45) associam-se fortemente à displasia intra-epitelial
anogenital e ao carcinoma de células escamosas. O HPV 16 associa-se particularmente ao câncer
cervical e vulvar, enquanto o tipo 18 associa-se mais ao adenocarcinoma do colo uterino.
Tanto o câncer cervical invasivo quanto suas lesões precursoras (NIC) associam-se firmemente à
presença de HPV no trato anogenital. A maioria dos cânceres de células escamosas do colo uterino
avança através de uma série de anormalidades microscópicas pré-invasivas. As evidências agora
revelam que o DNA do HPV está presente em 100% das biópsias de cânceres do colo uterino. O HPV
também tem sido demonstrado em 50% a 90% dos cânceres penianos, anovaginais e vulvares.
A tipagem do DNA do HPV está passando por avaliação internacional prospectiva, mas, nessa etapa,
sua utilidade clínica parece estar limitada a mulheres com anormalidades citológicas de baixo grau.
Tem havido extraordinário aumento na incidência de neoplasia intra-epitelial vulvar (NIV), no decorrer
das duas últimas décadas. A idade mediana da apresentação agora está em meados da quarta
década. Pelo menos dois terços dessas mulheres fumam e quase metade tem história de NIC. Essas
pacientes podem apresentar prurido vulvar, um nódulo ou outras lesões visíveis. Ocasionalmente,
pode haver um aspecto verrucoso. A lesão pode ser unifocal, multifocal, plana, papular ou em placas
extensas pigmentadas de cor vermelha ou branca.
Informações para dar aos pacientes no aconselhamento de consultório
O HPV genital é vírus comum, encontrado em grande porcentagem das pessoas sexualmente ativas.
Somente casais virgens não terão HPV sexualmente adquirido. Nem todos os infectados pelo HPV
desenvolverão verrugas genitais. Isto depende de seu sistema imune. O HPV é infecção tão comum,
que as verrugas genitais também são muito comuns. Ter verrugas genitais em uma relação
monógama de longa duração não significa que o outro parceiro tenha sido infiel. É possível que um ou
até ambos tenham ficado expostos ao vírus muitos anos antes e o carregaram sob a forma latente
sem mostrar sintomas. Existem vários tratamentos para se poder estar livre dos nódulos verrucosos,
mas eles não livram necessariamente o paciente da infecção subjacente pelo vírus. Depois de
tratamento bem-sucedido, as verrugas genitais podem recorrer - isto geralmente acontece para mais
ou menos 1 em 3 pessoas. Atualmente, é impossível saber se seu sistema imune negativa
completamente o vírus de seu corpo ou se o vírus permanece em níveis indetectáveis. Depois que as
verrugas estiverem resolvidas, alguns especialistas acreditam que sua capacidade de transmitir o HPV
diminua com o tempo, mas, no presente, ninguém pode dizer se e quando o risco se torna zero. Os
condons podem reduzir o risco de transmissão e devem ser usados com novos parceiros sexuais. É
mais questionável a introdução dos condons em uma relação a longo prazo porque seu parceiro
provavelmente já está infectado. As verrugas genitais não impedem que as mulheres engravidem. As
verrugas genitais não impedem o sexo. Pode haver uma ligação entre certos tipos de infecção genital
pelo HPV e câncer cervical - citológicos cervicais regulares, como no programa de triagem cervical,
detectarão mudanças precoces que possam ser monitorizadas e/ou tratadas, assim impedindo sua
progressão para câncer. Os tipos de HPV que causam verrugas externas visíveis raramente se
associam a anormalidades no colo uterino que possam causar câncer.
Diretrizes sobre a conduta para o HPV na infância
Epidemiologia
Após um dramático aumento entre 1966 e 1984, o HPV agora é a infecção viral mais comum do trato
genital feminino de adultas e adolescentes. Não têm sido realizados estudos populacionais com
crianças. No entanto, durante o mesmo período, houve aumento paralelo do número de relatos de
casos de verrugas anogenitais em crianças, o que provavelmente reflete um aumento real da
prevalência na infância.
Comportamento clínico
A infecção por HPV na região anogenital costuma ser assintomática. As crianças, muitas vezes, se
apresentam porque alguém que toma conta delas observou as lesões, embora algumas se apresentem
com dor ou sangramento durante a evacuação ou ainda com infecção secundária. Ocorrem condilomas
acuminados semelhantes a couve-flor clássicos em crianças, mas as verrugas anogenitais podem ter
muitas aparências.
Muitos adultos têm a doença em vários níveis no trato geniturinário. Quase nunca foi descrita doença
multicêntrica em crianças, mas também quase nunca é procurada.
O período de incubação das verrugas anogenitais em adultos é da ordem de um a oito meses. O
período de incubação em crianças é incerto, em grande parte, devido às incertezas que cercam a
transmissão vertical. Há alta probabilidade de regressão espontânea com o passar do tempo. O HPV
pode ser particularmente problemático em crianças em terapia imunossupressora, devendo ser
considerada a possibilidade de imunodeficiência (inclusive HIV) em qualquer criança que tenha lesões
particularmente refratárias.
Virologia
O diagnóstico virológico depende da detecção do DNA do HPV. O uso de PCR aumentou grandemente
a sensibilidade, mas sempre há o risco de contaminação. Têm sido descritos muitos tipos de HPV, mas
nenhum tipo específico está invariavelmente associado a um aspecto clínico em particular. É comum a
infecção por múltiplos tipos, sendo tecnicamente impossível a certeza de que todos os tipos de um
dado paciente tenham sido isolados. O DNA do HPV pode ser verificado em tecido aparentemente
normal em torno das lesões clínicas, e em lavados vaginais de pacientes sem lesões detectáveis. Em
adolescentes e adultos, os tipos 1 a 4 e 7 são verificados quase exclusivamente em verrugas
cutâneas. Nas crianças, contudo, há prevalência significativa dos tipos 1 a 3, em verrugas anogenitais.
Por determinar a fonte de infecção, a virologia acrescenta pouco à história e ao exame clínico. No
presente, há pouco ou nenhum valor na tipagem com finalidades forenses.
Neoplasia
Em adolescentes e adultos sexualmente ativos, há extraordinária associação entre HPV e displasia ou
carcinoma do colo uterino, vulva, pênis e ânus. Há associação particular com os tipos 16, 18, 31, 35,
39 e 41 a 45. Tem sido relatada doença maligna em crianças com papilomatose laríngea. Não se
conhece o risco de malignidade tardia em crianças com infecção anogenital. Há relatos de casos de
displasia e carcinoma vulvares em adolescentes com verrugas na vulva desde o primeiro ano de vida,
e de papulose bowenóide (displasia potencialmente pré-maligna) em um menino de dois anos.
Métodos de transmissão na infância
Em adultos, o HPV é doença sexualmente transmissível. A transmissão sexual ocorre claramente em
crianças, mas também podem ocorrer outras formas de transmissão.
Transmissão sexual. As verrugas anogenitais, em crianças, não foram reconhecidas como DST até
1971. De 1971 a 1993, foram publicados 300 casos, dos quais 29% foram transmitidas sexualmente.
A porcentagem de abuso sexual em diversos estudos varia de 0% a 100%, refletindo diferenças na
seleção de pacientes e na qualidade da avaliação para abuso sexual. Tem sido documentado abuso
sexual já no primeiro ano de vida. Também deve ser lembrado que as verrugas orofaríngeas podem
ser transmitidas sexualmente.
Transmissão vertical. O HPV pode ser transferido de mães aos seus descendentes, provavelmente a
partir de um canal de parto infectado. É difícil quantificar o risco para esses bebês. Não há correlação
entre a presença de DNA do HPV no bebê e a presença ou ausência de infecção clínica ou virológica
conhecida na mãe. É desconhecida a duração da eliminação de partículas virais de bebês infectados.
Não foram estabelecidos os limites do período de incubação do nascimento à infecção clínica. Em
primeiro lugar, não há estudos a longo prazo publicados acompanhando um grupo de bebês
infectados. Em segundo lugar, é comum a infecção assintomática na gravidez. Não se pode, portanto,
excluir a transmissão vertical possível em qualquer criança. Em terceiro lugar, a infecção materna não
comprova transmissão vertical. Foram descritos vários casos nos quais a mãe e a criança
compartilhavam o mesmo parceiro sexual.
Na ausência de evidências científicas conclusivas, é razoável deduzir, a partir de dados publicados,
que quanto mais velha a criança, menor se torna a probabilidade de transmissão vertical. A maioria
das crianças que apresenta verrugas anogenitais pela primeira vez antes dos 12 meses provavelmente
a adquire ao nascimento. Inversamente, a transmissão vertical é improvável quando as verrugas
anogenitais aparecem pela primeira vez depois dos três anos.
Outros meios de transmissão.
A literatura dermatológica sugere que as crianças podem adquirir verrugas anogenitais por infecção a
partir de verrugas cutâneas em suas próprias mãos (auto-inoculação) ou das mãos de adultos
(heteroinoculação). Os argumentos para essa hipótese são a prevalência de HPV 2 nas verrugas
anogenitais na infância e um número de relatos de casos e séries de casos sugestivos. A transmissão
por fômites também tem sido sugerida. Essas hipóteses devem ser vistas com cautela. Em primeiro
lugar, a auto-inoculação foi uma hipótese popular em adultos até que estudos controlados
demonstraram falta de relação com as verrugas cutâneas. Nenhum dos estudos tem sido feito com
crianças. Em segundo lugar, a transmissão por fômites tem sido postulada para todas as doenças
sexualmente transmissíveis, não tendo sido comprovada em nenhuma. Em terceiro lugar, até mesmo
se fosse estabelecido que as verrugas foram pegas em contato com as mãos dos que tomam conta
das crianças, ainda ficaria para ser estabelecido se esse contato foi inocente.
Concluindo, deve ser reconhecido que ocorrem métodos de transmissão diferentes do contato sexual.
O mais comum destes provavelmente é a transmissão vertical. No entanto, jamais se pode supor que
seja esse o caso. O contato sexual deve ser incluído no diferencial sempre que uma criança ou jovem
se apresentar com verrugas anogenitais.
Avaliação
Estabeleça a idade em que as lesões apareceram pela primeira vez e quais os sintomas que causam.
Considere todos os meios de transmissão, vertical (infecção materna, incluindo colpocitológicos,
sintomas de infecção respiratória), transmissão sexual, (atividade sexual em adolescentes,
descobrimento de abuso sexual, alterações de comportamento, fatores de risco para abuso sexual,
como contato com agressor sexual conhecido ou antecedentes familiares de abuso sexual), outros
(outras verrugas na criança ou jovem, verrugas em outros parentes ou nos que cuidam da criança).
Não se esqueça de examinar o corpo inteiro (inclusive as conjuntivas, boca e garganta) para pesquisar
verrugas. Examine a genitália e o ânus com uma fonte luminosa e algum tipo de ampliação, como um
auroscópio. No sexo feminino, afaste os lábios vaginais e inspecione a vulva cuidadosamente. No sexo
masculino, não se esqueça de examinar a coroa e o frênulo do pênis (se o prepúcio for facilmente
retrátil). Nem tudo o que se apresenta como verruga é HPV. O diagnóstico alternativo mais comum é
o molusco contagioso, mas quase qualquer tipo de rash papular pode apresentar-se na região
anogenital. Se houver dúvida, a lesão pode precisar ser biopsiada, e o tecido enviado para histologia e
para análise virológica.
A menos que haja evidências claras de transmissão vertical e a auto-inoculação em uma criança ou a
atividade sexual consentida em um adolescente, encaminhe o paciente para uma avaliação
multidisciplinar para pesquisa de possível abuso sexual. Nesse caso, uma vez diagnosticadas
prováveis verrugas anogenitais, deixe outras investigações para o médico a quem você esteja
encaminhando. De maneira ideal, uma avaliação completa de abuso sexual incluirá exame por um
médico treinado na avaliação médica de abuso sexual, triagem completa de outras DST seguindo
procedimentos médico-legais aceitos, avaliação de assistente social e entrevista diagnóstica por um
entrevistador apropriadamente treinado.
Podem ser necessárias investigações mais extensas se houver lesões orais ou sintomas respiratórios
em uma criança de pouca idade ou se as lesões parecerem estender-se ao ânus, uretra ou vagina.
Elas podem incluir laringoscopia, proctoscopia, cistoscopia, vaginoscopia ou (em meninas
pós-puberdade) exame com espéculo e colpocitológico.
Tratamento
As verrugas anogenitais geralmente regredirão espontaneamente. A infecção pode ser multifocal, o
DNA do HPV quase certamente está presente no tecido "normal" adjacente. No presente, não há
evidências de que o tratamento na infância reduza o risco (não comprovado) de neoplasia
posteriormente. O tratamento "pode ser difícil, prolongado e ter eficácia apenas marginal", sendo
comum a recorrência. Por todas essas razões, o tratamento ativo geralmente não é aconselhável. O
tratamento deve ficar reservado para aqueles com sintomas significativos. Há muitas formas de
tratamento, mas, em crianças de pouca idade com lesões extensas, a diatermia sob anestesia geral
provavelmente seja a melhor opção.
Acompanhamento
Acompanhe o paciente para ter certeza de que as lesões regridam e marque retorno depois de três a
seis meses para assegurar-se de que não tenham recorrido. No caso de transmissão vertical, é
importante ter certeza de que a mãe receba acompanhamento apropriado de sua própria infecção. Se
o paciente for um adolescente sexualmente ativo, deve ser feita triagem para outras DSTs e ser
oferecida orientação para a saúde sexual. No caso de abuso sexual, o paciente deve ser acompanhado
para se ter certeza de que tenham sido seguidas as etapas apropriadas para garantir sua segurança e
providenciar apoio e aconselhamento.
Não há evidências orientando as recomendações para acompanhamento a longo prazo. É razoável
estar preocupado que as crianças e adolescentes com infecção anogenital pelo HPV possam ter maior
risco a longo prazo de doença maligna. Seria, portanto, razoável recomendar o começo precoce da
triagem cervical regular depois da puberdade no sexo feminino e, no mínimo, consulta precoce em
pacientes de qualquer sexo quando houver sintomas anogenitais ou uretrais.
Infecção pelo papilomavírus humano (HPV) - atualizações 2001 (cont.)
Formas de
Uso
tratamento
Taxa de
resposta
Taxa
de
recorr
ência
Aplicadas pelo paciente
Podofilotoxi Verrugas
45% a
0% a
na
genitais
82%
91%
(Condyline) externas.
Verrugas
Imiquimod
37% a
13% a
anogenitais
(Aldara)
85%
19%
externas.
Administrada pelo prestador de serviços
Verrugas
anogenitais
externas,
vaginais,
60% a
20% a
Crioterapia
cervicais,
97%
79%
uretrais,
anais ou
orais.
Podofilina
Verrugas
anogenitais
externas,
vaginais ou
uretrais.
19% a
80%
23% a
70%
Vantagens e desvantagens
Os resultados são dependentes da
colaboração do paciente. Não para grandes
áreas de verrugas (>=10cm2).
Imunopotencializador. Mais eficaz em
verrugas úmidas. Pode ser menos eficaz no
sexo masculino.
Uso
na
gra
vid
ez
Não
Não
Eficaz para verrugas úmidas e secas, a dor
pode ser reduzida pelo uso de anestésico,
segurança e eficácia altamente dependentes
Não
do nível de habilidade, do equipamento e da
experiência. Risco de aplicação exagerada
ou insuficiente.
Mais eficaz em verrugas úmidas,
relativamente simples de usar, pode conter
mútagenos, concentração variável dos
componentes ativos, valor limitado para
verrugas secas. Evitar grandes áreas de
verrugas e aplicações excessivas.
Não
Verrugas
anogenitais
externas,
vaginais ou
anais.
50% a
100%
0% a
50%
Verrugas
Eletrocauteri anogenitais
zação
externas ou
orais.
35% a
94%
22%
ATA
Cirurgia
Verrugas
anogenitais,
orais ou
93%
anais
extensas.
Verrugas
Terapia com
anogenitais
laser
extensas.
60% a
100%
8% a
35%
3% a
77%
Barato, eficaz para verrugas úmidas e
secas. Precisa de aplicação cuidadosa por
um profissional de saúde. Seguro durante a
gravidez, não para grandes áreas de
verrugas friáveis. Baixa viscosidade resulta
em que se espalha se aplicado em excesso.
Estado livre de verrugas imediato,
resultados dependem do nível de habilidade
e de treinamento, requer equipamento,
consultas clínicas mais longas, anestesia
local é obrigatória.
Estado livre de verrugas imediato,
resultados dependem do nível de habilidade
e do treinamento, requer equipamento,
consulta clínica mais longa, anestesia local
obrigatória.
Estado livre de verrugas imediato, pode
requerer anestesia geral, resultados e
segurança dependentes do nível de
habilidade. Cara e disponível somente em
alguns centros maiores.
Não
Não
Não
Não
Idade
Segurança e eficácia do tratamento para verrugas não foram estudadas em populações pediátricas.
Ao tratar, deve-se prestar atenção em evitar e controlar a dor associada ao tratamento. É
questionável precisar de um dos pais ou responsáveis para aplicar um tratamento que pode ser
doloroso.
Devem ser levadas em conta as variações na taxa de desenvolvimento psicossocial em adolescentes
(capacidade cognitiva de compreender e executar qualquer programa de tratamentos, particularmente
terapia aplicada pelo paciente).
Gravidez
Não se conhece a segurança da podofilina, da podofilotoxina e do imiquimod na gravidez.
O 5-fluorouracila é teratogênico.
Apresentação da doença
Tamanho e número das verrugas: em geral, os tratamentos tópicos administrados não são ideais para
grandes áreas de verrugas, embora possam ter um efeito desbastador.
Localização anatômica e circuncisão ou não (homens): Verrugas em superfícies úmidas (parcialmente
queratinizadas) e áreas intertriginosas parecem responder melhor aos tratamentos tópicos do que as
verrugas em superfícies secas (inteiramente queratinizadas) e áreas abertas. Terapia cirúrgica
agressiva deve ser evitada no clitóris, na glande do pênis, no meato urinário, no prepúcio e na
cavidade prepucial nos homens não circuncidados.
Bibliografia
1. Beutner KR, Reitano MV, Richwald GA, Wiley DJ. AMA expert panel on external genital warte, 1998.
2. McOwan AG, Broughton C, Robinson AJ. Advising patients with genital warts. A consensus approach
international journal of STD and Aids, 1999.
3. National guideline for management of anogenital warts, 1999.
4. 2000 Guidelines for the management of genital HPV in New Zealand - Dr. Ronald Jones.