Carlos Cesar Salvadori
Molécula de ácido butírico
Cada pino entre os átomos representa o
compartilhamento de um par de elétrons, ou
seja, uma ligação covalente.
Átomo carbono
O ácido butírico tem odor de (e está presente na)
manteiga rançosa.
Átomo oxigênio
46
Átomo hidrogênio
Ligações entre átomos
Uma propriedade que os átomos possuem é a capacidade de se combinar
com outros átomos para produzir substâncias.
As forças de atração que mantêm os átomos combinados são chamadas
ligações químicas.
Estudaremos aqui três tipos de ligações químicas:
• ligação iônica;
• ligação covalente;
• ligação metálica;
Gases nobres
He
Ne
Ar
Kr
Xe
Rn
Números de elétrons nas
camadas
K
2
2
2
2
2
2
L M N O P Q
8
8 8
8 18 8
8 18 18 8
8 18 32 18 8
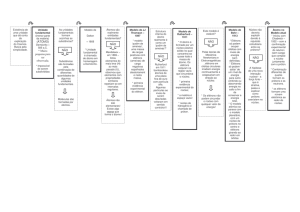
Regra do octeto
Já estudamos que:
• as propriedades de um elemento são determinadas pelo número de elétrons que o elemento apresenta na camada externa;
• Os gases nobres são elementos caracacterizados pelo fato de muito dificilmente se
combinarem com outros elementos.
O fato de os gases nobres se combinarem muito dificilmente sugere que a
presença de 2 elétrons na camada externa K e de 8 elétrons nas demais camadas externas, confere a um átomo uma configuração estável.
A regra do octeto estabelece que, ao formarem uma substância, os átomos
procuram adquirir a configuração estável de um gás nobre.
A regra do octeto aplica-se aos
elementos representativos (há algumas exceções). A regra do octeto
não se verifica para os elementos
de transição.
Configuração
estável
2 elétrons na camada externa K
ou
8 elétrons nas demais camadas
externas
Íons
Um átomo eletricamente neutro pode ceder ou receber elétrons, transformando-se em um átomo com carga elétrica positiva ou negativa, denominado Íon.
1
Um átomo neutro pode ceder elétrons transformando-se em um íon com
carga positiva, denominado cátion.
A formação de íons positivos ou cátions é característica dos metais.
Considere um átomo do metal sódio.
Prótons no núcleo
Na
11
Elétrons nas camadas
K
L
M
2
8
1
camada externa
A carga positiva dos 11 prótons é igualada pela carga negativa dos 11 elétrons. O átomo de sódio é eletricamente neutro.
Para adquirir configuração estável, o átomo de sódio perde o elétron da
camada externa. Ao perder o elétron da camada externa o átomo de sódio fica
com 11 prótons no núcleo e 10 elétrons nas camadas K e L . A carga negativa
destes 10 elétrons iguala a carga positiva de apenas 10 prótons. O átomo de
sódio deixa de ser neutro e transforma-se em um íon com uma carga positiva (a
carga do próton que não é igualada pela carga dos elétrons).
O íon sódio resultante é representado pela fórmula Na+.
Prótons no núcleo
Na+
11
Elétrons nas camadas
K
L
2
8
configuração estável
Carlos Cesar Salvadori
Comparando com o átomo Na, observe que no íon Na+ um número menor
de elétrons é atraído pelo mesmo número de prótons. Os elétrons são mais
fortemente atraídos pelo núcleo. Resulta que o raio do íon Na+ é menor que o
raio do átomo Na.
Na
Raio do átomo de sódio
1,57 . 10–8cm
Na+
Raio do íon sódio
0,95 . 10–8cm
47
2
Um átomo neutro pode receber elétrons, transformando-se em um íon com
carga negativa, denominado ânion.
A formação de íons negativos ou ânions é característica dos não-metais.
Considere um átomo do não-metal oxigênio.
Prótons no núcleo
O
8
Elétrons nas camadas
K
L
2
6
camada externa
A carga positiva dos 8 prótons é igualada pela carga negativa dos 8 elétrons. O átomo de oxigênio é eletricamente neutro.
Para adquirir configuração estável, o átomo de oxigênio recebe dois elétrons na camada externa. Ao receber dois elétrons na camada externa, o átomo
de oxigênio fica com 8 prótons no núcleo e 10 elétrons nas camadas K e L . A
carga positiva dos 8 prótons iguala a carga negativa de apenas 8 elétrons. O
átomo de oxigênio deixa de ser neutro e transforma-se em um íon com duas
cargas negativas (as cargas dos dois elétrons que não são igualadas pela carga
dos prótons).
O íon oxigênio resultante é representado pela fórmula O2–.
Prótons no núcleo
O2–
8
Elétrons nas camadas
K
L
2
8
configuração estável
48
O
Raio do átomo de
oxigênio
0,66 . 10–8 cm
O2–
Carlos Cesar Salvadori
Comparando com o átomo O, observe que no íon O2– um número maior
de elétrons é atraído pelo mesmo número de prótons. Os elétrons são mais
fracamente atraídos pelo núcleo. Resulta que o raio do íon O2– é maior que o
raio do átomo O.
Raio do íon oxigênio
0,95 . 10–8 cm
Agora somos capazes de interpretar as cargas elétricas que aparecem nas
fórmulas de íons.
+
11
Na
Cátion
Na formação do cátion houve perda de um elétron
O cátion tem 10 elétrons nas camadas
O
8
2–
Ânion
Na formação do ânion houve recebimento de dois elétrons
O ânion tem 10 elétrons nas camadas