Zoonoses Virais
Raiva
Definição
Zoonoses são doenças transmitidas de animais ao homem, direta ou
indiretamente (através de vetores).
Quando um inseto vetor está envolvido, a doença também é conhecida
como uma “arbovirose” (de arthorpod borne virus”).
Nem todas as arboviroses são zoonoses. Ex.: quando o ciclo de
transmissão se desenvolve entre o vetor e os humanos. ex: dengue
e febre amarela urbana.
Zoonoses: raiva,
hantaviroses,
hemorrágicas argentina e boliviana.
febre de lassa, ebola, febres
Raiva
Zoonose;
Todos animais de sangue quente;
Amplamente distribuída;
Geralmente fatal;
Atinge SNC;
Transmissão
MORDIDAS
Aérea ?
Transplantes !!
Família Rhabdoviridae
• vírion em forma de bala de revólver
• Simetria helicoidal
• RNA fs negativa
Gêneros:
Lyssavirus:
Raiva, Lagos Bat, Mokola,
Obodhiang, Kotonkan
Vesiculovírus: Estomatite Vesicular
Efemerovirus: Febre efêmera bovina
EPIDEMIOLOGIA
Ciclo urbano;
MORCEGOS NÃO
HEMATÓFAGOS
Diversas espécies
Humanos
Raiva - o vírus
Membro do gênero Lyssavirus, família Rhabdoviridae.
RNA fs envelopado; forma de bala de revólver característica
com espículas de 6-7 nm (glicoproteína, ou “G”).
vírion 130-240nm * 80nm
RNA de polaridade neg., codifica 5 proteínas: G, M, N, L, S
Muito ampla gama de hospedeiros .
Outros Lyssavirus : Mokola, Lagos bat, Duvenhage, EBL-1, e
EBL-2.
Duvenhage e EBL-2 já foram associados a encefalites em
humanos.
REPLICAÇÃO VÍRUS RNA FITA SIMPLES (fs), NEGATIVA
Adsorção
Brotamento/
envelopamento
Receptores
Penetração
Membrana
Desmontagem
RNA (-)
Replicação
Montagem
RNA (+)
(inclusão? )
RNA (+)
Síntese
Proteínas
Núcleo
Patogenia
Após inoculação, o vírus se multiplica no músculo
estriado ou tecido conjuntivo no sítio de inoculação e
penetra nos nervos periféricos através da junção
neuro-muscular.
Segue ao CNS via movimento axonal retrógrado.
Terminalmente, o vírus se dissemina de forma
centrífuga para os órgãos do corpo. O vírus causa
pouca destruição neuronal.
Diagnóstico laboratorial de raiva
Imunofluorescência direta IFD
ou “direct fluorescent antibody test (DFAT)
Isolamento viral em camundongos
Diagnóstico de Raiva
IFD
Corpúsculo de Negri em neurônio
(fonte: CDC)
Diagnóstico de raiva
Presentemente, para determinação da
origem da amostras de vírus isoladas:
Exames complementares: Análises com
anticorpos monoclonais;
Amplificação genômica por RT-PCR:
Análise com enzimas de restrição, ou:
Sequenciamento e análise filogenética
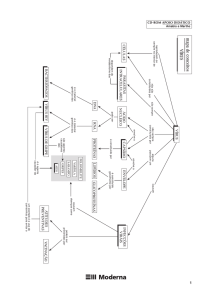
Análise de grau de relacionamento de amostras
do vírus da raiva
AF070450Tb
BRct97.1
BRbt576
AF070449Dr
BRbv189
BRfx2217
BRfx2263
BRdg585
rvu22862dg
U22477
BRbt686
14.3
14
12
10
8
6
4
Nucleotide Substitutions (x100)
2
0
Tratamento e prevenção
Profilaxia pré-exposição - vacinas inativadas
Profilaxia pós-exposiçãos - observação de animais suspeitos por 10
dias. Se surgirem sinais, devem ser sacrificados e remetidos ao
laboratório para diagnóstico.
Animais selvagens: devem ser sacrificados e examinados.
A profilaxia pós-exposição baseia-se na desinfecção local, na
administração de vacina ou, em casos graves, soro + vacina.
Uma vez estabelecida a doença => tratamento de suporte.
Profilaxia pós-exposição
Ferida - lavagem intensa com agua e detergente, e debridação
Imunização passiva - imunoglobulina anti-rábica humana, 50% em
torno da área da ferida, 50% IM.
Imunização ativa - Vacina tipo Fuenzalida, preparadas em cérebro de
camundongos lactentes (1-4dias). Hoje disponível: vacinas preparadas
em cultivos celulares de células diplóides humanas ou céulas Vero.
Regime de doses pode atingir até 7 inoculações.
O tratamento combinado de soro com vacina é mais eficaz do que
somente um ou outro. Disponível também imunoglobulina de origem
equina, mais barata do que a de origem humana.
Vacinas contra Raiva
No Brasil , atualmente: Cultivo celular ( células Vero)
Human Diploid Cell Vaccine (HDCV) em células diplódes WI 38
Vacina em células Vero
No passado:
Tecido nervoso ( Fuenzalida)
Embrião de pato
Na Europa:
Vacinas em iscas para animais selvagens
Controle da Raiva
Urbana- raiva canina causa a grande maioria dos casos de raiva
humana.
Na região Sul do Brasil: não ocorre raiva canina há mais de 20 anos !!
Para o controle:
Controle de cães vadios.
Vacinação de cães
Quarentena
Animais selvagens - mais difícil.
- morcegos hematófagos, não hematófagos:
em grande centros urbanos, como São Paulo e Porto Alegre.
Os Hantavírus
Formam um gênero distinto dentro
da família Bunyaviridae.
Diferente dos demais bunyavírus,
não é transmitido por artrópodos.
Vírus de fita simples, envelopado,
com três fitas de RNA (L, M, and
S).
Vírions 98 nm em diâmetro.
Hantavirose-
A síndrome pulmonar por Hantavírus
Em SC:
O brotamento da Taquara
No MS:
O plantio de soja
Todos:
O desmatamento
História
Febre Hemorrágica com Sídrome Renal (HFRS: mais tarde
denominada Hantavirose) surgiu inicialmente durante a guerra
da Coréia quando cerca de 3000 soldados da ONU foram
infectados.
A doença, entretanto já havia sido descrita pelos chineses há
1000 anos.
Em 1974, o vírus foi isolado de um camundongo do campo
coreano (striped field mouse) e foi chamado vírus Hantaan.
Em 1995, uma nova doença chamada síndrome pulmonarpor
hantavírus foi descrita na região de “four corners”nos EUA.
Alguns subtipos de hantavírus
associados a doenças em humanos
Hantaan, Porogia e vírus relacionados - Causa a forma clássica de HFRS.
China, Leste da Rússia,e partes da Europa. Transmissor: Apodemus
agrarius
Seul - causam doença moderada. Tansmissor: ratos. Distribuição mundial
China, Japão, Rússia, USA e América do Sul.
Puumala - Causa doença leve (nefropatia epidêmica) principalmente em
países escandinavos. Transmissor: Clethrionomys glareolus.
Sin Nombre - Causa a síndrome pulmonar, que corresponde aos casos
identificados aqui no Brasil. em muitas partes do mundo, USA, México,
América do Sul. Transmissor: Peromyscus maniculatus e outros.
A síndrome pulmonar por Hantavírus (HPS)
Sintomas:
Febre alta
Dores abdominais,
Dor de cabeça,
Dores generalizadas
Tosse
Taquicardia
Dificuldade respiratória.
Características clínicas das
hantaviroses
Patologia (forma hemorrágica) caracterizada por danos aos capilares
pequenos vasos, resultando em vasodilatação e consequentes hemorragias.
Classicamente, as hantaviroses apresentam
desapercebidas em casos mais leves.
e
5 fases. Estas podem passar
Fase Febril - surgimento abrupto de uma doença gripal
eritematoso após um período de incubação de 2-3 dias.
severa,
com um rash
Fase hipotensiva - começa pelo quinto dia da doença
Fase oligúrica - começa pelo nono dia de doença. O paciente pode desenvolver falha
renal aguda e choque. Hemorragiass são usualmente do tipo petéquias. A maioria das
mortes ocorre durante as fases hipotensiva e oligúrica.
Fase Diurética - ocorre entre os dias 12-14 .
Fase convalescente - pode levar até 4 meses.
Roedores envolvidos na
transmissão de hantavírus
striped field mouse (Apodemus agrarius)
Bank vole (Clethrionomys glareolus)
Deer Mouse (Peromyscus maniculatus)
Rat (Rattus)
Síndrome Pulmonar por Hantavírus
(HPS)
Mais de 250 casos de HPS tem sido reportados nas Américas do Norte e Sul,
com mortalidade de aprox. 50%
Em comum com as hantaviroses da Ásia, a HPS tem uma fase febril similar.
Entretanto, os danos aos capilares ocorrem predominantemente nos pulmões, ao
invés dos rins.
Edema pulmonar, choque e complicações cardíacas podem levar à morte.
A maioria dos casos de HPS são causados por vírus do grupo do vírus Sin
Nombre. Outros são associados a uma variedade de outros hantavírus, como: New
York e Black Creek Canal.
Diagnóstico
Diagnóstico sorológico - uma variedade de testes tais como IF, HAI, SRH,
ELISAs tem sido desenvolvidos para o diagnóstico sorológico.
Detecção direta do antígeno- mais sensível do que a sorologia e detectável mais
cedo. Antígenos virais podem ser demonstrados no sangue ou urina.
RT-PCR - muito útil no diagnóstico da HPS.
Isolamento viral - da urina, logo ao início da infecção, apresenta grande chance
de sucesso. Do sangue é menos consistente. O vírus Sin Nombre nunca foi
isoladode pacientes com HPS.
Immunohistoquímica - útil no diagnóstico de HPS.
Tratamento e Prevenção
Depende de terapias de suporte.
Ribavirina - reportes indicam ser útil no tratamento de doença
por hantavírus quando administrada no início. Sua eficácia na
HPS é ainda desconhecida.
Vacinação - uma vacina inativada esta em testes na China.
Outras vacinas candidatas vem sendo preparadas.
Controle de roedores- medidas de controle devem
diminuir o contato entre humanos e roedores.
visar
Prevenção
- Eliminar fontes de alimento para roedores
- Evitar contato com roedores silvestres
- Consciência do risco frente a roedores silvestres
- Cuidados com passeios em zonas rurais/florestas
Viroses emergentes
Gênero Henipavirus
- Nipah
- Hendra
Família Paramyxoviridae
Henipavirus
(Proposta)
Hendra
Nipah
human
parainfluenza-2
Sendai
human parainfluenza-3
Respirovirus
simian
virus-41
simian
virus-5
mumps
Rubulavirus
Measles
Newcastle
disease
rinderpest
Morbillivirus
phocid distemper
canine distemper
Outros vírus de morcêgos
O vírus denominado “Australian bat lyssavirus identificado em 1996. é
um rhabdovírus. Um morcegófilo morreu da infecção em 1996 e outro
em 1998.
Outro vírus denominado Menangle foi isolado 1997 de suínos,
causando doença e abortos, assim como uma enfermidade respiratória
em humanos. O vírus Menangle é também um paramixovírus, da
mesma família mas não relacionado ao vírus Hendra. Também é
transmitido por morcêgos frugívoros.
Em 1999, surgiu o vírus Nipah, na Malaysia. Hoje classificado
juntamente com o vírus Hendra, no gênero Henipavirus da família
Paramyxoviridae.
E muitos outros estão por vir!!
Aguarde!!!!