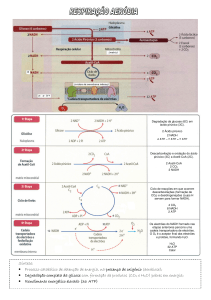
BIOENERGÉTICA
Na célula milhares de compostos estão a ser
sintetizados e degradados em simultâneo.
Metabolismo: é o conjunto de todas as reacções
envolvidas na manutenção deste estado dinâmico.
No geral as reacções metabólicas podem ser
divididas em dois grupos: reacções catabólicas e
reacções anabólicas.
O nosso organismo utiliza uma via catabólica
diferente para cada família de macromoléculas,
porém todas elas convergem para uma única via.
O principal propósito das diferentes vias catabólicas
é converter a energia química dos alimentos em
moléculas de ATP e obter ainda percursores para
síntese de determinados metabolitos.
1
A célula e a Mitocôndria
A célula animal típica possui inúmeros componentes
os quais servem para diferentes funções.
2
A
mitocôndria
é
o
organelo
dos
organismos
superiores onde ocorre a via catabólica comum.
3
Membrana interna
Cristas
Matriz Membrana externa
As
enzimas
do
ciclo
do
ácido
cítrico
estão
essencialmente localizadas na matriz mitocondrial.
Os principais componentes da via catabólica comum
Existem duas partes comuns à via catabólica: 1ª ciclo do
ácido cítrico, 2ª fosforilação oxidativa.
É importante compreender a molécula de ATP.
As ligações P-O-P do anidrido fosfórico contém mais
energia química (7,3 kcal/mol) do que as ligações
C-O-P dum fosfoéster (3,4 kcal/mol).
Pi
ATP
Pi
ADP
7,3 kcal/mol
Pi
AMP
7,3 kcal/mol
4
A
3,4 kcal/mol
O ATP e o ADP cotem ligações fosfato de elevada
energia.
O ATP é uma forma de armazenamento de energia
por um curto tempo de vida.
A molécula de ATP permanece na célula durante,
aproximadamente, 1 minuto.
Estimativas sugerem que durante um exercício
violento o corpo humano produz e degrada mais de
0,5 Kg de ATP por minuto (≃9.000.000 €/min).
Para além do ATP, outras moléculas podem também
ser utilizadas como moléculas armazenadoras de
energia, são elas as coenzimas NAD+ e FAD.
5
O
C
NH2
Nicotinamida
N+
O
H
H2C
H
H
OH
H
NH2
O
-
P
O
O
N
O
-
P
O
O
Ribose
H
N
ADP
O
CH2
H
N
O
H
H
OH
H
N
H
NAD+
H3C
NH2
CH3
N
H OH OH OH H
N
N C C
H H
O
O
O
C
C
C O
P O P
H
H
H
O
-
N
H2
O C
-
O
O
N
N
H
Flavina
H
O
Ribitol
H
H
OH
H
ADP
Riboflavina
FAD
6
H
N
N
As coenzimas NAD+ e FAD são muitas vezes vistas como
moléculas transportadoras de electrões.
Outra molécula importante nesta via catabólica comum é a
coenzima A (Co A), a qual é uma molécula transportadora
de um grupo acetilo.
A coenzima A também contém ADP, o qual está
ligado ao ácido pantoténico (uma das formulas
estruturais da vitamina B)
Ligação de elevada
energia
CoA S
C
O
7
CH3
CO2
COOC O
CH3
HS CoA
S CoA
Piruvato desidrogenase
NAD+
C O
CH3
NADH
8
Bioenergética: conversão dos
alimentos em energia
CO2
COOC
HS-CoA
Piruvato
desidrogenase
NAD+
NADH
O
CH3
S CoA
C O
CH3
Piruvato
Acetil CoA
Reacções do ciclo do ácido cítrico
O ciclo do ácido cítrico também conhecido por ciclo
de Krebbs ou dos ácidos tricarboxílicos é constituído
por 8 passos:
1ª reacção: enzima citrato sintase
S CoA
C O
CH3
Acetil CoA
+
COOC O
CH2
COO-
Oxaloacetato
COOCH2
HS-CoA
H2O
Citrato sintase
HO
C COOCH2
COOCitrato
∆G’º=-32,2 kJ/mol
Esta é a única reacção do ciclo do ácido cítrico na
qual há formação de uma ligação C-C.
S CoA
C O
C
H H H
S CoA
C O
C
C
C
H
O-
S CoA
H
H
O
H
carbanião
AsP C
O
2ª reacção: enzima aconitase
H2C
HO C
H C
H
COOCH2
H2O
COOCOO- aconitase
COO-
Citrato
H2O
C COOC
H2O
H
COO
COOCH2
-
aconitase
H2O
Cis-Aconitato
H C COOHO CH
COO-
2R-3S-Isocitrato
∆G’º=13,3 kJ/mol
3ª reacção: enzima isocitrato desidrogenase
COOCH2
NAD(P)H+H+
COOCH2
COOCH2
CO2
+
NAD(P)
C COO- Isocitrato
HC COO- Isocitrato CH2
desidrogenase
desidrogenase
H
HO CH
COO-
2R-3S-Isocitrato
C O
COOOxalo
succinato
H+
C O
COO-
α-cetoglutarato
∆G’º=-20,9 kJ/mol
4ª reacção: enzima α-cetoglutarato desidrogenase
COOCH2
CH2
C O
COO-
NADH
+
NAD
α-cetoglutarato
desidrogenase
HS-CoA
CO2
COOCH2
CH2
C O
S-CoA
Succinil CoA
α-cetoglutarato
∆G’º=-33,5 kJ/mol
5ª reacção: enzima succinil-CoA sintase
COOCH2
CH2
GTP HS-CoA
GDP+Pi
C O
S-CoA
Succinil CoA
Succinil CoA
sintase
COOCH2
H2C
COOSuccinato
∆G’º=-2,9 kJ/mol
COOCH2
CH2
1
C O
O-
N
S-CoA
O-
His
NH
P O
OH
HS-CoA
COOCH2
CH2
HS-CoA
+
H
COOCH2
CH2
H+
-
O
+
P N
His
-
O
NH
O
GDP+H+
O
O-
O-
C
C O
2
3
O
GDP+H+
P O
N
O-
His
GTP
GTP
NH
4
N
His
NH
6ª reacção: enzima succinato desidrogenase
COOCH2
H2C
COOSuccinato
FADH2
FAD
Succinato
desidrogenase
COOCH
HC
COOFumarato
∆G’º=0 kJ/mol
7ª reacção: enzima fumarase
COOCH
HC
H2O
Fumarase
COO-
COOHO CH
HC H
COO-
L-Malato
Fumarato
∆G’º=-3,8 kJ/mol
8ª reacção: enzima L-Malato desidrogenase
COOHO C H
HC H
COOL-Malato
NADH + H+
NAD+
Malato
desidrogenase
COOO C
H2C
COOOxaloacetato
∆G’º=29,7 kJ/mol
Como é que o ciclo do ácido cítrico leva à
produção de energia?
Numa das etapas há formação de uma molécula de
elevada energia (GTP) e noutras duas há conversão
de NAD+ em NADH e FAD em FADH2.
Estas
coenzimas
(potencial
redutor)
transportam
que
podem
H+
e
electrões
num
processo
subsequente ser utilizadas para a síntese de ATP.
O ciclo para oxidação do acetato para além de
maximizar a conservação da energia obtida,
proporciona ainda materiais de partida para a
síntese
de
aminoácidos
e
proporciona
um
excelente método para regulação da velocidade
das reacções catalíticas.
Reacção representativa da totalidade das reacções
do ciclo do ácido cítrico:
CH3COOH + 2H2O + 3NAD+ + FAD
⇌
2CO2 +
3NADH + FADH2 + 3H+
O ciclo do ácido cítrico é controlado por um
mecanismo de feedback
Quando alguns dos produtos formados (ATP e
NADH) são acumulados, observa-se a inibição de
algumas enzimas do ciclo: citrato sintase, isocitrato
desidrogenase, α-cetoglutarato desidrogenase.
Quando a acetil-CoA é abundante, a velocidade do
ciclo é aumentada, sendo a enzima isocitrato
desidrogenase estimulada por ADP e NAD+.
Fosforilação oxidativa
As coenzimas reduzidas (NADH e FADH2) são
produtos finais do ciclo do ácido cítrico, que podem
reduzir o oxigénio a água:
4H+ + 4e- + O2 → 2H2O
Esta reacção altamente exotérmica é realizada em
diversas
etapas,
de
forma
a
maximizar-se
a
conservação da energia libertada.
A transferência dos electrões até ao oxigénio faz-se
através de várias enzimas de acordo com uma
determinada sequência.
São bombeados 6H+ por cada NADH oxidado e 4H+
por cada FADH2 oxidado.
Fosforilação e a bomba quimiosmótica
Peter Mitchell em 1961 formulou a teoria
quimiosmotica: a energia obtida da transferência de
electrões é conservada na formação de um
gradiente de protões.
A força motora que leva a que ocorra um
movimento espontâneo de iões das regiões de
maior concentração para as de menor concentração
leva a que os iões retornem à matriz através de
uma enzima transmembranar denominada por
ATPase/ATPsintase (complexo V).
Esta enzima catalisa a conversão de ADP em ATP:
ADP + Pi ⇄ ATP + H2O
Equações globais da fosforilação oxidativa
NADH+3ADP+½O2+3Pi+H+→NAD++3ATP+H2O
FADH2+2ADP+½O2+2Pi→FAD+2ATP+H2O
Rendimento energético
A energia libertada na cadeia transportadora de
electrões é conservada na molécula de ATP.
Por
cada
2
protões
que
entram
na
matriz
mitocondrial ocorre a produção de uma molécula de
ATP.
Por cada grupo acetilo que entra no ciclo do ácido
cítrico são obtidos 3 NADH e 1 FADH2 mais 1 GTP.
3NADH x 3ATP/NADH = 9 ATP
1FADH2 x 2ATP/FADH2 = 2 ATP
1GTP
= 1 ATP
12 ATP
C2+2O2+12ADP+12Pi → 12ATP + 2CO2