DISCIPLINA: Física
DATA: 12/04/2017
Atividades de Calor Sensível
01 - A quantidade de calor para elevar de um grau
centígrado a temperatura de um grama de uma
substância pura é uma grandeza denominada:
(A) capacidade térmica.
(B) equivalente térmico.
(C) calor de fusão.
(D) calor latente.
(E) calor específico.
02 - O calor específico de uma substância é 0,5 cal/g.°C.
Se a temperatura de 4 g dessa substância se eleva de
10°C, pode-se afirmar que ela absorveu uma quantidade
de calor, em calorias, de:
(A) 0,5
(B) 2
(C) 5
(D) 10
(E) 20
03 - Fornecendo-se a um corpo de massa 0,2 kg a
quantidade de calor de 0,2 kcal, sua temperatura passa
de 5°C a 15°C, sem que ocorra mudança de estado.
Pode-se afirmar que o calor específico do corpo em
cal/g.°C é:
(A) 100
(B) 50
(C) 10
(D) 1
(E) 0,1
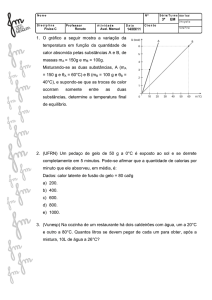
04 - Duas substâncias, J e K, de mesma massa, variam
suas temperaturas em função do calor recebido, de
acordo com o gráfico abaixo. A razão entre os calores
específicos das substâncias J e K é igual a:
(A) 1/2
(B) 1/4
(C) 1
(D) 2
(E) 4
05 - Um coletor solar absorve 300 kcal/minuto e seu
rendimento é 20%. Em 10 minutos de funcionamento o
coletor pode elevar a temperatura de 50 litros de água
em:
(A) 6°C
(B) 15°C
(C) 5°C
(D) 20°C
(E) 12°C
06 - Um corpo de 250 g de massa e temperatura inicial
de 10°C é aquecido durante 5 minutos por uma fonte de
potência constante que lhe fornece 700 cal/min. Ao final
desse tempo, a temperatura do corpo é de 80°C. Podese concluir que o calor específico da substância que
constitui o corpo é, em cal/g.°C, igual a:
(A) 2,0
(B) 0,175
(C) 0,04
(D) 0,2
(E) 0,02
07 - Atualmente, encontra-se no comércio determinada
panela de "vidro" que traz a recomendação a seus
usuários para que "desliguem o fogo" um pouco antes do
cozimento total do alimento, pois esta panela, mesmo
com o fogo desligado, continua com o cozimento do
alimento. Este fato ocorre devido ao material que
constitui a panela ter:
(A) uma fonte térmica intermolecular.
(B) elevada massa molecular.
(C) transparência ao calor.
(D) grande capacidade térmica.
(E) pequeno calor específico.
Página | 1
08 -Um corpo recebe calor na razão de 35 calorias por
minuto. A temperatura desse corpo, em função do
tempo, está representada no gráfico abaixo,
A capacidade térmica desse corpo, em cal/°C , é igual a:
(A) 1,4
(B) 2,5.10
(C) 3,0.10
(D) 3,0.10³
(E) 3,5.10³
09 -Uma fonte fornece a 600 g de uma substância um
fluxo calorífico constante de 600 cal/min, fazendo com
que a temperatura (T) da substância varie com o tempo
(t) segundo o diagrama dado. Nessas condições,
podemos afirmar que o calor específico da substância
em cal/g.°C
11 - A tabela fornece os valores de massa, calor
específico e temperatura de três corpos A, B e C,
respectivamente. Supondo que estes corpos são
colocados num sistema isolado, qual é a temperatura de
equilíbrio?
(A) 15°C
(B) 25°C
(C) 40°C
(D) 50°C
(E) 70°C
12 - A capacidade calorífera (térmica) de uma amostra
de água é cinco vezes maior do que a de um bloco de
ferro. Considere tal amostra de água na temperatura de
20 °C e tal bloco de ferro na temperatura de 50 °C.
Colocando-os num recipiente termicamente isolado e de
capacidade térmica desprezível, a temperatura final de
equilibro, em °C, será igual a:
(A) 12,5
(B) 25
(C) 35
(D) 45
(E) 70
13 - Um calorímetro de capacidade térmica 100 cal/°C
contém 800 g de água a 80 °C. A quantidade de água a
20 °C que deve ser adicionada afim de que a mistura
tenha uma temperatura de equilíbrio de 40 °C é igual a:
(A) 1 800 g
(B) 2 000 g
(C) 1 600 g
(D) 1 000 g
(E) 800 g
(A) 0,10
(B) 0,25
(C) 0,50
(D) 0,75
(E) 1,00
10- Dentro de um calorímetro ideal (isolação perfeita)
encontra-se um bl°Co de alumínio de 100 g à
temperatura ambiente: 25°C. O calor específico do
alumínio é 2,15.10-1 cal/g.K. São colocados 200 g de
água no calorímetro à temperatura de 0°C. O equivalente
em água do calorímetro é de 50 g. Depois de algum
tempo qual será, aproximadamente, a temperatura no
interior do calorímetro? Suponha que os calores
específicos da água e do alumínio não dependem da
temperatura.
(A) 2,0°C
(B) 23°C
(C) 9,0°C
(D) 16°C
(E) 6,6°C
14 - Com 336 kJ de energia pode-se, aproximadamente,
I - fundir ______ kg de gelo a 0 °C;
II - elevar a temperatura de 1 kg de água de 20 °C para
______°C;
III - evaporar ______ kg de água a 100 °C.
Dados: calor de fusão do gelo: 335 J/g; calor específico
da água: 4,19 J/g.°C; calor de vaporização da água: 2
268 J/g.
Assinale a alternativa que preenche de forma correta as
três lacunas, respectivamente:
(A) 1; 100; 6,75
(B) 1000; 80; 0,15
(C) 1; 80; 0,15
(D) 1000; 100; 6,75
(E) 1; 100; 0,15
Página | 2
15 - Misturando um litro de água a 70 °C e dois litros de
água a 10 °C, obtemos três litros de água a:
(A) 70 °C
(B) 40 °C
(C) 35 °C
(D) 30 °C
(E) 20 °C
16 - Em um dia ensolarado, 4200 cal/s de energia solar
incidem sobre um coletor solar residencial. O coletor
aquece de 5 °C um fluxo de água de 420 g/s. A eficiência
do coletor é de:
(A) 20%
(B) 40%
(C) 50%
(D) 80%
(E) 100%
17 - Um bloco de massa 2,0 kg, ao receber toda a
energia térmica liberada por 1000 gramas de água que
diminuem a sua temperatura de 1 °C, sofre um
acréscimo de temperatura de 10 °C.
Considere o calor específico da água igual a 1 cal/g.°C.
O calor específico do bl°Co em cal/g.°C
(A) 0,2
(B) 0,1
(C) 0,15
(D) 0,05
(E) 0,01
18 - O calor específico de uma substância é 0,5 cal/g. °C.
Se a temperatura de 4 g dessa substância se eleva de
10 °C, pode-se afirmar que ela absorveu uma quantidade
de calor, em calorias, de:
(A) 0,5
(B) 2
(C) 5
(D) 10
(E) 20
19 - Cedem-se 684 cal a 200 g de ferro que estão a uma
temperatura de 100 °C. Sabendo que o calor específico
do ferro vale 0,114 cal/g.°C, concluímos que a
temperatura final do ferro será:
(A) 10 °C
(B) 20 °C
(C) 30 °C
(D) 40 °C
20 - Na termologia são estudados os conceitos de calor
específico e capacidade térmica. Em relação à
capacidade térmica, pode-se afirmar que:
(A) é uma propriedade da substância.
(B) é uma propriedade de determinado corpo.
(C) independe da massa do corpo.
(D) independe do calor específico da substância.
(E) é inversamente proporcional à massa do corpo.
Página | 3
Gabarito – Física (12-04)
Física
1
2
3
4
5
6
7
8
9
10
E
E
E
A
E
D
D
B
D
E
11
12
13
14
15
16
17
18
19
20
D
A
A
E
D
C
D
E
D
A
Página | 4